近年来,重组蛋白类药物研究在找新药用蛋白的同时,作重改变已上市的重组蛋白药物结构。使其活性更强,在体内半衰期延长。从而达到减小剂量和减少注射次数的目的。目前已批准几种新的改变结构的重组蛋白类药物上市,市场前景很好。在研的改构重组蛋白类药物更多。现综述如下:
1. 重组蛋白类药物结构中活性强的片段相联
美国Amgen公司详细分析了a干扰素结构中活性强的氨基酸片段,再用蛋白工程的方法把这些片段反复相联,正好也是165个氨基酸组成结构全新的复合干扰素,取名“干复津”,其活性比原a干扰素强了10 倍,这样注射剂量减小10 倍,付反应减少。在临床应用上很受欢迎。并已进入我国市场。
我国也有多家单位正在研制复合干扰素,如四川生物工程中心,三元基因,双鹭,辽宁卫星,海王生物等。大都进入中试申报阶段,双鹭的复合干扰素已进入II 期临床,还没有一家获准生产。国内干扰素市场已经供大于求。
2. 重组蛋白类药物的PEG 修饰
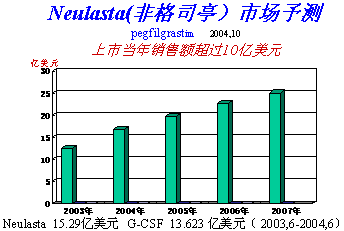
PEG 是一种无毒性,无抗原性和强生物相容性的蛋白修饰好材料。经修饰过的蛋白质稳定性提高,在人体的保留时间延长;免疫原性降低,减少抗体产生。而且蛋白溶解度增加。被PEG 掩盖后,酶解机会减少,药物半衰期延长,注射次数减少。使重组蛋白类药物变成长效制剂。美国首先批准了PEGIFNa2a 上市,其后又批准PEG-G-CSF,PEG-Somatropin antagonist 等。PEG-G-CSF 商品名Peg-Filgrastim,中文名“非格司亭”,上 |
|
市当年销售额超过10 亿美元,这种业绩是其它生物技术药物所达不到的。而且据最新统计其销售额已超过
原型,其市场预测见图1。
我国也开展了PEG修饰重组蛋白类药物的研究,如PEG-IFN-a2a,PEG-G-CSF,PEG-GM-CSF 等,但处于研发阶段,格兰伯克公司的PEG-GCSF 已申报,均未获准上市。
3. 重组蛋白类药物的改构化研究
改变重组蛋白类药物的结构,如将单链变成双链和增加结构中活性基团的数量,使其抗酶能力增强或本身活性增加,在体内的半衰期延长。达到减小剂量和减少注射次数的目的。美国已上市的tPA改变成TNK-tPA,将EPO变成ARANESP,这些新型重组蛋白类药物的市场均很好。我国改构的重组TNF已批准生产,主要对TNF 的N端进行了改变,这样毒性降低。长春博泰生物技术公司将两个EPO分子联在一起,注 |