这篇综述总结了最近发表的多篇文献中提及的应用Biacore的SPR技术在免疫原性测定中的一些独到的优势。我公司将完全忠实于原文,并感到很荣幸能展示其最精华的部分。
免疫原性是指一种物质引发抵抗它的免疫反应的能力。是目前评价内服药越来越关注的课题,它不仅是众多药物生产/生物技术企业主要的关注点,也是管理机构如美国FDA的主要关注点。免疫原性对药物的临床应用非常重要,因为药物所引发的病人的抗该药物的免疫反应可能会导致该药物的有效性被大大地削弱,甚至药效完全消失。
随着包括基因治疗以及抗体治疗在内的更多的复杂治疗方案被开发,同时也增加了与免疫原性相关联的复杂问题产生的可能性。因此,对新药将会产生的免疫原性影响进行评估就尤为重要,同时也就对既能够提供高质量的分子结合信息而且操作简单、检测快速又灵敏的技术产生了很大的需求。显而易见的是对低亲和力免疫反应的测定也变得越来越重要,因为这些反应将对长期临床实验产生重大的影响。以下的几个例子将说明,Biacore的SPR技术所能提供的免疫原性研究的鉴定数据与其他的技术相比较具有明显的优势。

Abad等用SPR技术开发了一种用来识别和测定抗腺病毒基因治疗载体的抗体的方法1。这种方法被用来研究一种非复制的5型腺病毒(rAd),该腺病毒被用作野生型人p53基因的传递载体而进行抗癌症治疗。
Abad等发展出了一套快速检测方法,用于检测在rAd/p53注射后的免疫反应,包括检测针对所有可能的病毒表面抗原的抗体,并能够分型免疫反应。
固定rAd/p53达到8000RU后,用稀释到人血清水平的多克隆抗rAd/p53抗体对传感器表面进行测试。经过35轮分析检测,显示剂量效应,高特异性和稳定的抗体与已固定的病毒结合。为确证固定的病毒的完整性,芯片取下后用电子扫描显微镜分析,电镜下清晰显示所固定病毒的二十面外壳是完整的。
然后对治疗病人们在给药前后取10ul血清,检测抗腺病毒抗体。给药前,都显示出较低的,但是可检测的抗体水平,在第一次给药后,抗体水平有显著地增加。持续观察三周,抗体反应在病人个体间有差异(多数都在三周内达到峰值后并衰减),但都被观察到,在第二次给药后,引起的较强的持续的免疫反应,超过了第一次给药后的效果。这种情况符合典型的免疫记忆反应,就是第一次免疫刺激产生的B-记忆细胞,在第二次同样的免疫刺激时,更快和更持续地产生抗体。当用SPR方法的结果和原先用ELISA方法的结果对比时,发现结果是有很大可比性的,但ELISA的结果相比之下稳定性较差。 |
|
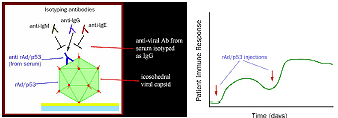
图1:左面的图显示,一个二十面的病毒蛋白外壳固定到了芯片(右旋糖苷包被的金色外壳用黄色表示,玻璃载体用蓝色表示)。抗各种病毒表面抗原的抗体都被检测到,并随后用特异的抗Lg抗体同形化。右面的图显示一个标准的免疫记忆反应,在给药中持续取血清,跟踪免疫反应变化。第二次给药引起了持续的免疫反应,超过了第一次给药。
免疫反应的分型,可以用一简单的SPR“夹心”法检测,在注入血清样品后,马上注入免疫球蛋白分型抗体(抗IgG,IgA,IgM,IgE)。正如预期,IgG是观察到的最多的类型,而在后期取的腹水样品中IgA的贡献更大。
这一SPR技术运用研究,采用新的全病毒固定方法,检测、观察和分型抗肿瘤P53基因治疗中对腺病毒载体的免疫反应。研究表明,这一方法与现有的ELISA的方法相比更为简便快捷,结果更可靠。这一SPR分析方法为基于病毒载体的基因治疗提供了重要的免疫反应数据,有助于建立更有效的治疗方案和给药安排。

Gonzales 等用Biacore来筛查人源化抗体的免疫原性,取已给过鼠源抗肿瘤抗体的病人血清2。
人源化抗体的变种由鼠源的抗体mCC49 而来,mCC49能识别与肿瘤相关的TAG-72蛋白。以往研究表明,mCC49可以成为诊断和治疗抗体,但它的临床作用由于病人会发生 HAMA反应而打了折扣。HuCC49由转移mCC49的CDR区到人源抗体的框架上而构成,然后HuCC49的变种由在其重组位点进行遗传操作而成。HuCC49和其两个变种V5和V10,作为实验对象。芯片上分别固定HuCC49和兔免疫球蛋白(对照)。免疫应答分析用在临床I期实验时已注射3mCC49的病人血清,和三种抗体变种混合,作竞争结合分析。TAG-72抗原和鼠抗Fc抗体已经用免疫吸附从血清中移去。血清稀释后使用。
初始实验显示病人血清中有HuCC49特异结合活性,滴度在病人间变化15-20倍。竞争结合实验中,血清和不同量的HuCC49、V10和V5混合并平衡。以结合比例(比较加抗体和不加抗体的SPR信号)和抗体浓度作图显示每种抗体的竞争结合情况。并计算IC50值(半抑制的抗体浓度)。
1) 鼠单克隆抗体mCC49(含抗TAG-72 的CDRs)注射入临床试 |