
-

…ķőÔÕ®ĻŔőĘ
Ň„ń„◊•◊°…ķ√ŁŅ∆ľľ
ŐÝ∂ĮĶń¬Ų≤ę
STRaM£ļ“Ľ÷÷ŐŠ…żŌłįŻ≤ķ∆∑ň›‘ī–‘Ķń“Ňīę—ßŅÚľ‹°™°™ő™—–ĺŅļÕŃŔī≤◊™ĽĮŐŠĻ©ĺę◊ľĶńĽý“Ú÷łő∆ľľ ű
°ĺ◊÷ŐŚ£ļ īů ÷– –° °Ņ Īľš£ļ2025ńÍ08‘¬17»’ ņī‘ī£ļCommunications Biology 5.1
Īŗľ≠Õ∆ľŲ£ļ
°°°°Īĺ—–ĺŅ’Ž∂‘ŌłįŻ÷őŃ∆≤ķ∆∑ň›‘ī÷–Ķń…ķőÔį≤»ę–‘ļÕ”––ß–‘ŐŰ’Ĺ£¨Ņ™∑ĘŃňSTRaM£®∂ŐīģŃ™÷ōłīļÕÕĽĪš∑÷őŲ£©…ķőÔ–ŇŌĘ—ßŃų≥Ő°£ł√ľľ űÕ®Ļż’ŻļŌSTR∑÷őŲ°ĘSTR≤ŗ“Ū∑÷őŲļÕEMS£®Īŗľ≠/ÕĽĪš–ÚŃ–£©∑÷őŲ»żīůń£Ņť£¨ĻĻĹ®ŃňįŁļ¨Ōŗň∆–‘÷ł ż£®SI£©°ĘīŅ∂»÷ł ż£®PI£©ļÕĪŗľ≠ÕĽĪš÷ł ż£®EMI£©Ķń∆ņĻņŐŚŌĶ£¨Ņ…ĺę◊ľ ∂ĪūÕ¨‘īĪŗľ≠/Ļ§≥ŐĽĮŌłįŻ°£—–ĺŅ÷§ ĶSTRaMń‹ľž≤‚ĶÕ÷Ń1%ĶńĹĽ≤śőŘ»ĺ£¨≤Ę≥…Ļ¶”¶”√”ŕCAR-TŌłįŻ÷őŃ∆ľŗ≤‚£¨ő™Ō÷īķŌłįŻ≤ķ∆∑Ļ‹ņŪŐŠĻ©ŃňłŖ–‘ľŘĪ»Ĺ‚ĺŲ∑Ĺįł°£
‘ŕŌłįŻ÷őŃ∆ļÕ…ķőÔ“Ĺ—ß—–ĺŅŃž”Ú£¨ŌłįŻŌĶĹĽ≤śőŘ»ĺļÕ…Ū∑›ĽžŌżő Ő‚≥§∆ŕņß»Ň◊ŇŅ∆—–»ň‘Ī°£īęÕ≥√ęŌłĻ‹ĶÁ”ĺ£®CE£©ő™Ľýī°Ķń∂ŐīģŃ™÷ōłī£®STR£©∑÷–Õľľ űňšĪĽ∑Óő™ĹūĪÍ◊ľ£¨»īīś‘ŕŃĹīů÷¬√Ł»ĪŌ›£ļőř∑® ∂ĪūSTR÷ōłīĶ•‘™ńŕĶńĶ•ļň‹’ňŠ∂ŗŐ¨–‘£®SNP£©£¨«“∂‘ĶÕňģ∆ĹĹĽ≤śőŘ»ĺ£®<10%£©ľž≤‚∑¶Ń¶°£ňś◊ŇCRISPR-Cas9Ľý“ÚĪŗľ≠ľľ űļÕłŲ–‘ĽĮŌłįŻŃ∆∑®ĶńŇÓ≤™∑Ę’Ļ£¨Ĺ®ŃĘłŁĺę◊ľĶńŌłįŻň›‘īŐŚŌĶ“—≥…ő™∆»‘ŕ√ľĹřĶńŅ∆—ßŐŰ’Ĺ°£
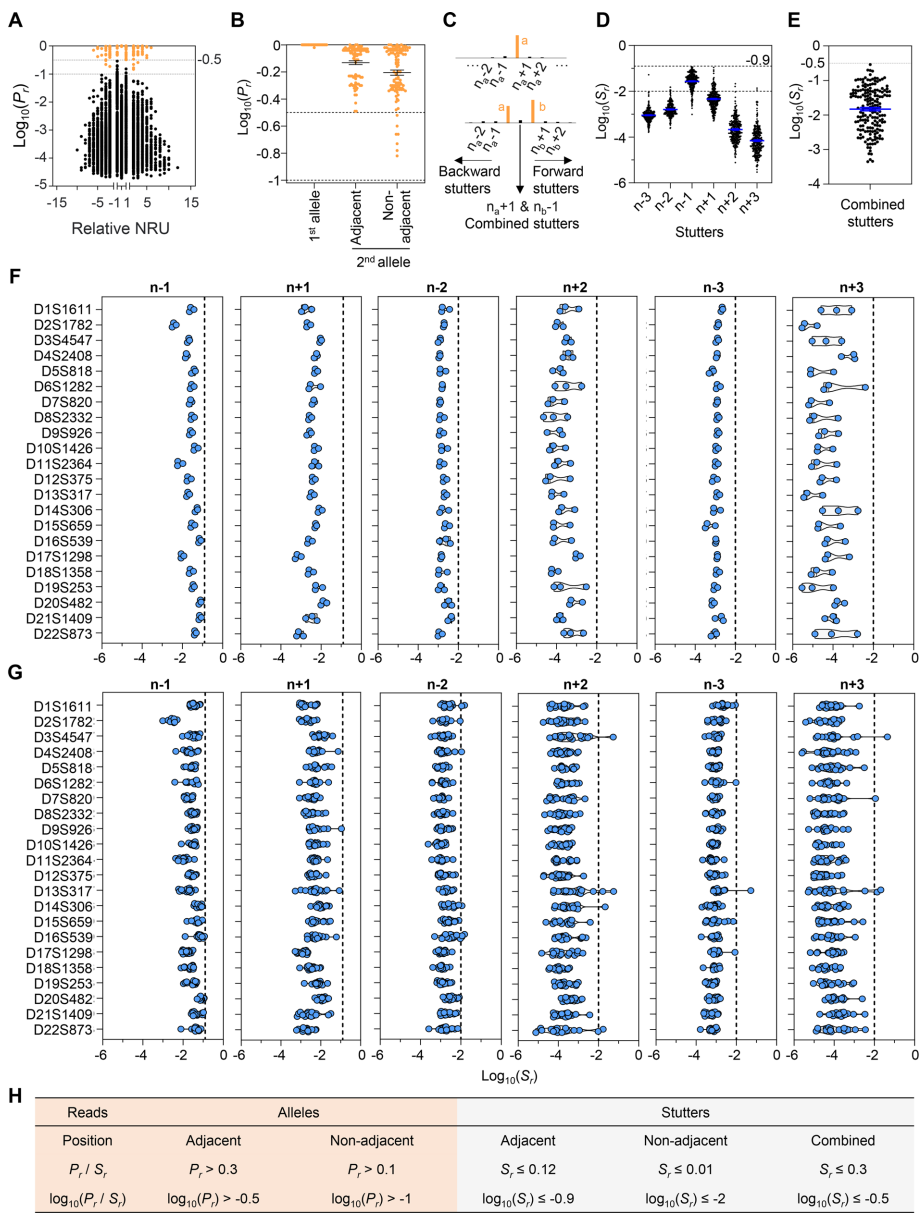
’Ž∂‘’‚“Ľń—Ő‚£¨’„Ĺ≠īů—ß…ķ√ŁŅ∆—ß—–ĺŅ‘ļ”ŽĹ≠őų÷–“Ĺ“©īů—ßĶń—–ĺŅÕŇ∂”‘ŕ°∂Communications Biology°∑∑ĘĪŪŃňÕĽ∆∆–‘—–ĺŅ≥…ĻŻ°£ňŻ√«Ņ™∑ĘĶńSTRaM“Ňīę—ßŅÚľ‹£¨Õ®Ļżīī–¬–‘Ķō’ŻļŌŌ¬“Ľīķ≤‚–Ú£®NGS£©ľľ ű”Ž»ż÷ō…ķőÔ–ŇŌĘ—ß∑÷őŲń£Ņť£¨ĻĻĹ®ŃňŅ…Õ¨ Ī∆ņĻņŌłįŻ…Ū∑›°ĘīŅ∂»ļÕĽý“Ú–ř ő◊īŐ¨Ķń"»żőĽ“ĽŐŚ"ľž≤‚ŐŚŌĶ°£—–ĺŅ≤…”√į–ŌÚņ©‘Ų◊”≤‚–Ú£®TAS£©ľľ ű∂‘22łŲĺę—°STRőĽĶ„ĹÝ––…Ó∂»≤‚–Ú£¨ĹŠļŌ◊‘÷ų—–∑ĘĶńProminence-cutoffń£–Õ ĶŌ÷Ķ»őĽĽý“Ú”Žstutter≤ķőÔĶńĺę◊ľ«Ý∑÷£¨≤Ęīī–¬–‘ĶōĹ®ŃĘŃňŅ…ŃŅĽĮ∆ņĻņĶńPI÷ł żŌĶÕ≥°£
ĻōľŁľľ ű∑Ĺ∑®įŁņ®£ļ£®1£©Ľý”ŕGalaxy∑ĢőŮ∆ųĻĻĹ®Ķń◊‘∂ĮĽĮ∑÷őŲŃų≥Ő£¨≤Ę––‘ň––STR-FM ∂ĪūļÕNucmer≤ŗ“Ū–ÚŃ–Ī»∂‘£Ľ£®2£©…Ťľ∆įŁļ¨22łŲłŖ‘”ļŌ∂»£®Hobs>0.6£©STRőĽĶ„Ķńľž≤‚panel£Ľ£®3£©Ĺ®ŃĘProminence ratio£®Pr£©ļÕStutter ratio£®Sr£© ż—ßń£–Õ£Ľ£®4£©”¶”√į–ŌÚņ©‘Ų◊”≤‚–Ú ĶŌ÷Ķ•ľÓĽý∑÷Īś¬ ľž≤‚£Ľ£®5£©ŃŔī≤—ýĪĺ—ť÷§ļ≠ł«Ľľ’Ŗņī‘īņŗ∆ųĻŔ£®PDO£©°Ę“ž÷÷“∆÷≤ń£–Õ£®PDX£©ļÕCAR-T÷őŃ∆ľŗ≤‚°£
—–ĺŅĹŠĻŻ≤Ņ∑÷£ļ
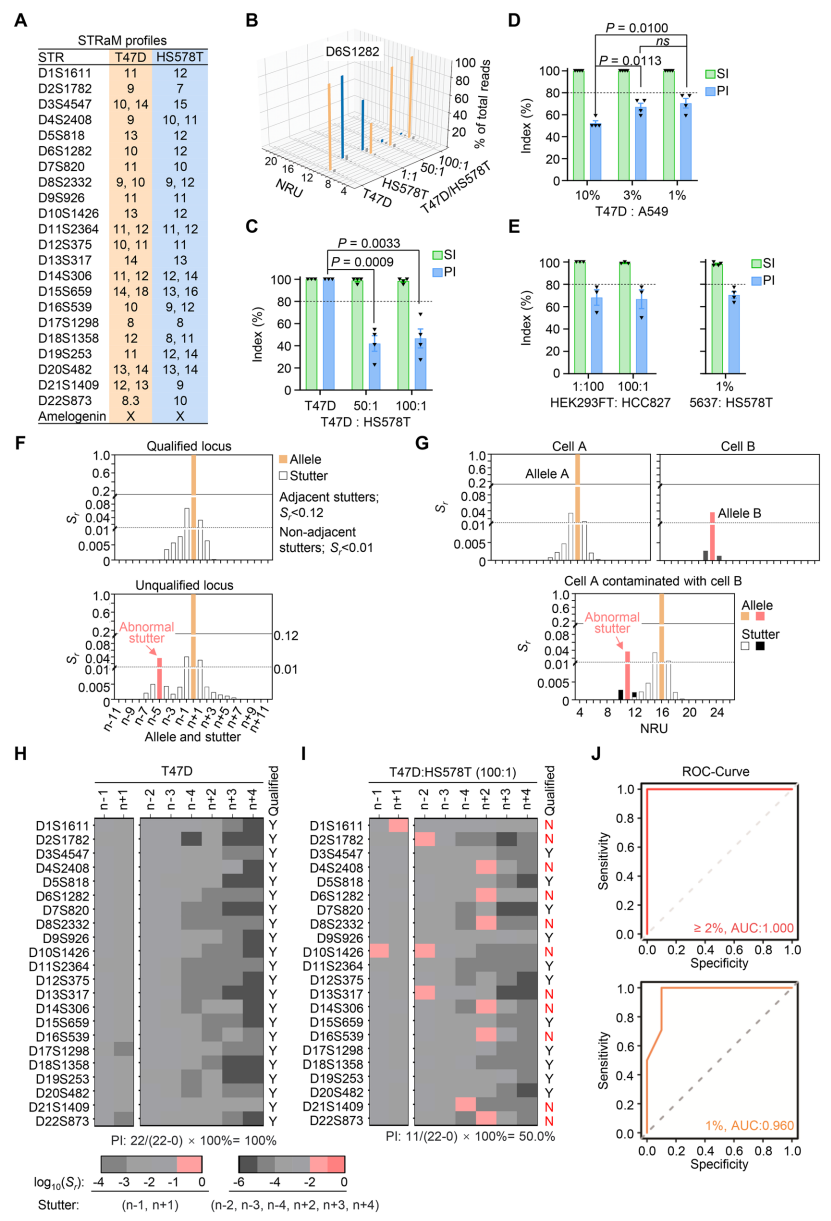
"STRaM∑÷őŲ–¬Ļś‘Ú"Ĺ“ ĺīęÕ≥CE∑Ĺ∑®‘ŕD5S818ļÕD13S317Ķ»őĽĶ„“ÚļŲ¬‘ĪŖľ SNPĶľ÷¬÷ōłīĶ•‘™ľ∆ ż£®NRU£©īŪőů£¨∂ÝSTRaMÕ®ĻżįŁ»›–‘Ļś‘Ú–£’żŃň’‚–©ņķ ∑–‘īŪőů£®Õľ2C,D£©°£
"PIŐŠ…żĹĽ≤śőػ從≤‚Ńť√Ű∂»"≤Ņ∑÷÷§ Ķ£¨STRaMń‹ ∂Īū1%ňģ∆ĹĶńHS578TŌłįŻ∂‘T47DŌłįŻĶńőŘ»ĺ£®PI=46.6°ņ8.6%£©£¨∂ÝīęÕ≥SI÷ł ż£®98.4°ņ1.1%£©ÕÍ»ę ߖߣ®Õľ4C£©°£
"EMI◊∑◊ŔĻ§≥ŐĽĮŌłįŻ"≤Ņ∑÷Ō‘ ĺ£¨SW480/SW620’‚∂‘Õ¨‘īŌłįŻŌĶ‘ŕSTR∆◊Ōŗň∆£®SI°÷100%£©«ťŅŲŌ¬£¨Õ®ĻżBRMS1c.708_709delĶ»ÕĽĪšőĽĶ„ĶńEMI∑÷őŲ£®0% vs 33.1%£© ĶŌ÷√ų»∑«Ý∑÷£®Õľ5D£©°£‘ŕCRISPRĪŗľ≠ĶńHEK293ŌłįŻ÷–£¨PTEN-7SM£®∆ŖőĽĶ„≥Ńń¨ÕĽĪš£©ĶńEMIīÔ98.7°ņ0.2%£¨ő™Ľý“ÚĪŗľ≠÷ ŃŅŅō÷∆ŐŠĻ©–¬Ļ§ĺŖ°£
—–ĺŅĹŠ¬Ř÷ł≥Ų£¨STRaMŅÚľ‹Õ®Ļż»żīůīī–¬ÕĽ∆∆Ō÷”–ľľ ű∆ŅĺĪ£ļ£®1£©ĹęCEĶńĶ•“Ľ…Ū∑›ľž≤‚ņ©’Ļő™SI-PI-EMI∂ŗ≤ő ż∆ņĻņŌĶÕ≥£Ľ£®2£© ĻĹĽ≤śőػ從≤‚Ńť√Ű∂»ŐŠ…ż10Ī∂£Ľ£®3£© ◊īő ĶŌ÷Õ¨‘īĻ§≥ŐĽĮŌłįŻĶńĺę◊ľ◊∑◊Ŕ°£‘ŕCAR-T÷őŃ∆ľŗ≤‚÷–£¨STRaM≥…Ļ¶Õ¨≤Ĺ◊∑◊ŔŃň◊™Ľý“Ú‘ōŐŚĶń∂ĮŐ¨ĪšĽĮ£®Õľ7G£©ļÕ ‹ŐŚŌłįŻīŅ∂»£®PI=97.7°ņ0.9%£©£¨ő™ŌłįŻ÷őŃ∆≤ķ∆∑»ęŃų≥Ő÷ Ņō ųŃĘ–¬ĪÍ◊ľ°£’‚ŌÓľľ ű≤ĽĹŲľś»›Ō÷”–STR żĺ›Ņ‚£¨∆š»ňĺý300-400‘™»ň√ŮĪ“Ķń≥…Ī峣ő™īůĻśń£ŃŔī≤”¶”√∆Ő∆ĹĶņ¬∑£¨ĪÍ÷ĺ◊ŇŌłįŻ≤ķ∆∑ň›‘īĹÝ»Ž"∂ŗő¨∂»°Ę ż◊÷ĽĮ"Ķń–¬ Īīķ°£
 …ķőÔÕ®őĘ–ŇĻę÷ŕļŇ
…ķőÔÕ®őĘ–ŇĻę÷ŕļŇ
÷™√Ż∆ů“Ķ’–∆ł
ĹŮ»’∂ĮŐ¨ | »ň≤Ň –≥° | –¬ľľ ű◊®ņł | ÷–ĻķŅ∆—ß»ň | ‘∆’ĻŐ® | BioHot | ‘∆Ĺ≤Ő√÷Ī≤• | ĽŠ’Ļ÷––ń | ŐōľŘ◊®ņł | ľľ űŅž—∂ | √‚∑— ‘”√
įś»®ňý”– …ķőÔÕ®
Copyright© eBiotrade.com, All Rights Reserved
Ń™ŌĶ–ŇŌš£ļ
‘ŃICPĪł09063491ļŇ