
-

生物通官微
陪你抓住生命科技
跳动的脉搏
益生菌Bifidobacterium animalis通过吲哚-3-乙酸调控AHR/METTL3/STAT3轴抑制非小细胞肺癌进展
【字体: 大 中 小 】 时间:2025年08月14日 来源:Cell Reports 6.9
编辑推荐:
本研究针对非小细胞肺癌(NSCLC)防治需求,揭示了肠道菌群Bifidobacterium animalis及其代谢产物吲哚-3-乙酸(IAA)通过调控AHR/METTL3/STAT3轴和肿瘤免疫微环境抑制NSCLC进展的分子机制。研究人员通过临床队列分析、动物模型和m6A测序等技术,证实IAA通过激活芳烃受体(AHR)抑制METTL3介导的STAT3 m6A甲基化,同时降低IL-6表达改善CD8+ T细胞功能,为NSCLC防治提供了新的微生物-代谢物干预策略。
肺癌长期占据全球癌症死亡率首位,其中非小细胞肺癌(NSCLC)占比高达85%。尽管靶向治疗和免疫治疗取得进展,但耐药性和高复发率仍是临床面临的重大挑战。近年来,肠道菌群与癌症的"肠-器官轴"调控机制成为研究热点,但特定菌种在NSCLC中的作用机制尚不明确。山东第一医科大学附属山东省肿瘤医院的研究团队在《Cell Reports》发表的研究,首次揭示了益生菌Bifidobacterium animalis通过代谢产物吲哚-3-乙酸(IAA)调控"肠-肺轴"抑制NSCLC的全新机制。
研究采用多组学技术联用策略,包括:27例NSCLC患者和29例健康对照的粪便宏基因组测序;构建皮下移植瘤和原位肺癌小鼠模型;非靶向代谢组学分析细菌上清液;m6A甲基化测序分析表观遗传调控;流式细胞术检测肿瘤免疫微环境变化。
B. animalis在NSCLC患者粪便中显著减少
通过宏基因组测序发现,NSCLC患者肠道菌群中B. animalis丰度显著降低,且与肿瘤标志物CEA、CYFR21-1呈负相关。从健康人粪便分离的B. animalis新菌株(基因组1,944,701 bp)在动物实验中显示出显著抑瘤效果。
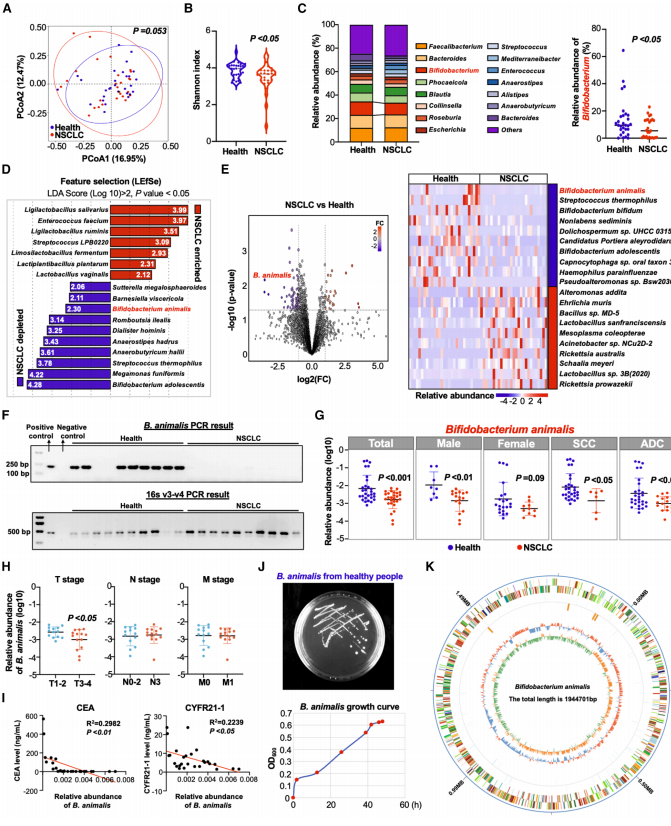
IAA是B. animalis的关键抑瘤代谢物
代谢组学分析锁定IAA为B. animalis的特征性代谢物。在无菌小鼠中证实IAA可经血液循环到达肺部。动物实验显示IAA处理使肿瘤体积缩小50%以上,并诱导肿瘤细胞G1-S期阻滞和凋亡。
AHR/METTL3/STAT3轴调控机制
分子对接和表面等离子共振证实IAA与芳烃受体(AHR)结合(KD=130 μM)。RNA-seq和m6A-seq揭示IAA通过激活AHR抑制甲基转移酶METTL3,降低STAT3 mRNA的m6A修饰水平,从而抑制STAT3信号通路。AHR抑制剂CH-223191可部分逆转这种抑瘤效应。
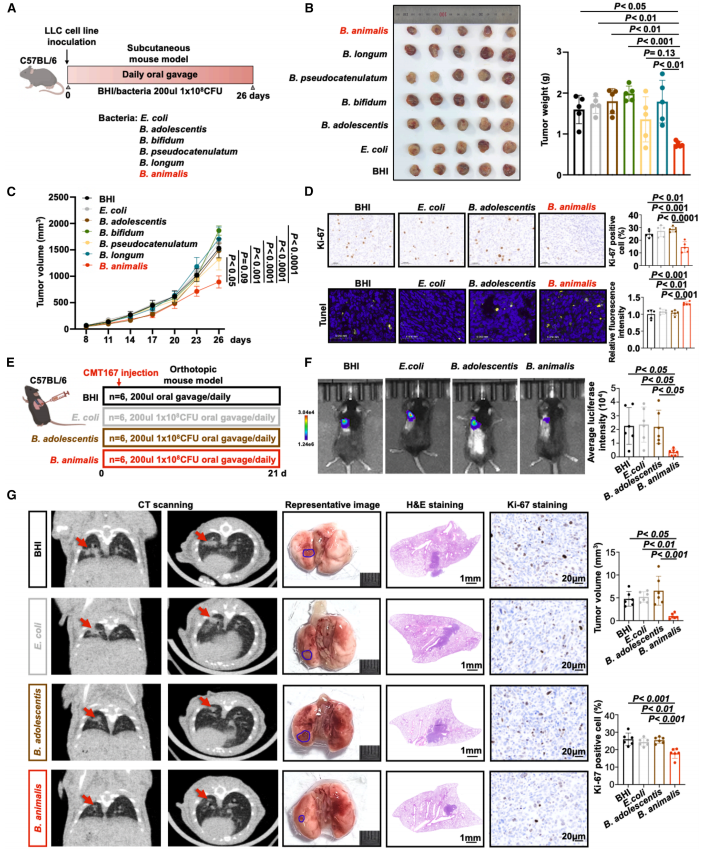
肿瘤免疫微环境重塑
B. animalis和IAA使M2型肿瘤相关巨噬细胞减少40%,同时增加CD8+ T细胞浸润和IFN-γ分泌。机制上,IAA通过抑制IL-6的m6A修饰降低其表达,从而改善免疫抑制微环境。CD8+ T细胞清除实验证实免疫调节是抑瘤的重要机制。
该研究首次系统阐明了肠道益生菌B. animalis通过"代谢物-受体-表观遗传"三级调控网络抑制NSCLC的机制:IAA→AHR→METTL3→STAT3/IL-6→肿瘤增殖/免疫微环境。这不仅为NSCLC防治提供了新的微生物疗法思路,也为"肠-肺轴"理论提供了直接分子证据。研究提出的菌株补充和代谢物干预策略,具有临床转化潜力且副作用小,为克服当前NSCLC治疗瓶颈提供了新方向。
 生物通微信公众号
生物通微信公众号
知名企业招聘