
-

生物通官微
陪你抓住生命科技
跳动的脉搏
靶向LAG-3的PET成像监测PD-1/STING/LAG-3三重免疫疗法协同抑制肝癌的机制研究
【字体: 大 中 小 】 时间:2025年08月14日 来源:Biomarker Research 11.5
编辑推荐:
本研究针对肝癌抗PD-1单抗(mAb)响应率低的问题,通过开发LAG-3靶向PET探针[68]GaGa-NOTA-C25,首次实现对抗PD-1 mAb、STING激动剂和抗LAG-3 mAb三重免疫疗法的动态监测。研究发现STING激动剂与抗PD-1 mAb联用可显著上调TILs中LAG-3表达,而三重疗法较双疗法进一步延长生存期(55天 vs 32天对照),为肝癌免疫联合治疗提供新策略。
肝癌作为全球第六大常见恶性肿瘤,其治疗面临严峻挑战。尽管免疫检查点抑制剂(ICIs)如PD-1/PD-L1抑制剂为晚期肝癌患者带来希望,但客观缓解率仅15%且易产生耐药性。肿瘤免疫表型中的"非热肿瘤"特征――特别是免疫抑制型肿瘤中T细胞浸润不足的问题,成为制约疗效的关键瓶颈。如何突破PD-1单药治疗局限,实现肿瘤免疫表型从"冷"向"热"的转化,同时建立疗效预测的动态监测方法,成为肝癌免疫治疗领域的重大科学问题。
华中科技大学同济医学院附属协和医院放射科的研究团队创新性地将分子影像技术与免疫治疗监测相结合,在《Biomarker Research》发表的研究中,开发了靶向LAG-3的PET探针[68]GaGa-NOTA-C25,系统评估了PD-1/STING/LAG-3三重免疫疗法在肝癌模型中的协同效应。研究采用放射性标记技术合成探针,通过荷瘤小鼠模型进行体内外验证,结合流式细胞术和免疫荧光分析免疫细胞亚群变化,最终通过生存分析评估不同治疗方案的效果。
研究结果部分,首先证实了[68]GaGa-NOTA-C25 PET可特异性检测LAG-3+ TILs,阻断实验显示肿瘤摄取从0.874±0.121%ID/g降至0.402±0.017%ID/g。在治疗监测方面,双免疫治疗组(STING激动剂+抗PD-1 mAb)第13天摄取达1.35±0.191%ID/g,显著高于单药组(抗PD-1 mAb 0.647±0.037%ID/g)。流式结果显示该组LAG-3+ CD8+ T细胞增加3倍,且与PET信号呈正相关(r=0.82)。
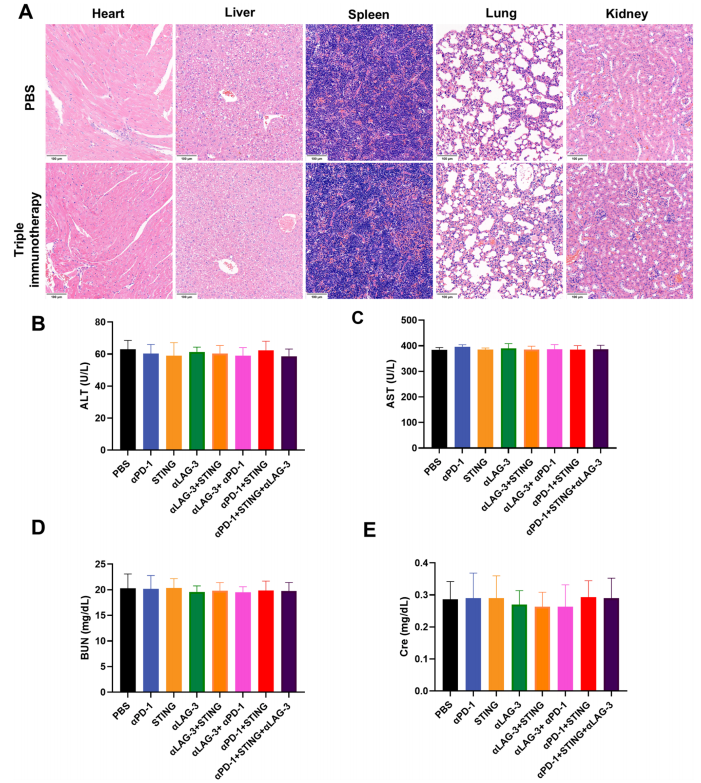
三重免疫治疗展现出显著优势:肿瘤体积从双疗法的208±23 mm3进一步降至53±5 mm3,生存期延长至55天(对照组32天)。机制研究表明,该方案使CD8+/Treg比值提高4倍,IFN-γ分泌增加2.3倍,同时H&E染色显示广泛坏死区域。安全性评估显示主要器官无病理损伤,肝肾功能指标(ALT/AST/BUN/Cre)均在正常范围。
该研究首次证实STING激动剂可协同PD-1阻断上调LAG-3表达,为"免疫治疗诱导的检查点代偿上调"理论提供直接证据。临床转化方面,口服STING激动剂MSA-2的应用方案突破了现有瘤内注射限制,而LAG-3靶向PET成像为免疫治疗动态监测提供了新工具。研究提出的三重免疫治疗策略,通过同时靶向先天免疫(STING)、适应性免疫(PD-1)和代偿性检查点(LAG-3),为克服肝癌免疫治疗耐药性提供了创新解决方案,其转化价值值得期待。
 生物通微信公众号
生物通微信公众号
知名企业招聘