
-

…˙ŒÔÕ®πŸŒ¢
≈„ƒ„◊•◊°…˙√¸ø∆ºº
ï∂صƒ¬ˆ≤´
≥¶µ¿æ˙»∫Œ»∂®–‘”Î∑≈¡∆œ‡πÿ–‘∑Œ—◊µƒπÿ¡™—–æø£∫∑«–°œ∏∞˚∑Œ∞©ªº’flªØ¡∆∑≈¡∆∆⁄º‰Œ¢…˙ŒÔŒ»Ã¨µƒ¡Ÿ¥≤“‚“Â
°æ◊÷ã∫ ¥Û ÷– –° °ø ±º‰£∫2025ƒÍ08‘¬02»’ ¿¥‘¥£∫iScience 4.1
±‡º≠Õ∆ºˆ£∫
°°°°±æ—–æø’Î∂‘∑«–°œ∏∞˚∑Œ∞©(NSCLC)ªº’flªØ¡∆∑≈¡∆(CCRT)∆⁄º‰≥¶µ¿æ˙»∫Œ»∂®–‘”Î∑≈¡∆œ‡πÿ–‘∑Œ—◊(RP)µƒπÿ¡™’πø™…Ó»ÎÃΩÀ˜°£—–æø»À‘±Õ®π˝¶ÃSTASISÀ„∑®¡øªØ◊›œÚ—˘±æµƒŒ¢…˙ŒÔŒ»∂®–‘(mS∆¿∑÷)£¨∑¢œ÷∏flŒ»∂®–‘æ˙»∫ªº’flRP∑Áœ’œ‘÷¯ΩµµÕ(p=0.035)£¨≤¢º¯∂®FaecalibacteriumŒ™πÿº¸‘§≤‚æ˙ Ù(p=0.040)°£∏√—–æøŒ™Õ®π˝Œ¢…˙ŒÔ∏…‘§ΩµµÕ∑≈¡∆∂斑÷π©¡À–¬∞–µ„°£
‘⁄÷◊¡ˆ÷Œ¡∆¡Ï”Ú£¨∑≈¡∆◊˜Œ™∑«–°œ∏∞˚∑Œ∞©(NSCLC)µƒ÷ÿ“™÷Œ¡∆ ÷∂Œ£¨»¥√Ê¡Ÿ◊≈“ª∏ˆº¨ ÷µƒ≤¢∑¢÷¢°™°™‘º30%-40%ªº’flª·≥ˆœ÷∑≈¡∆œ‡πÿ–‘∑Œ—◊(Radiation Pneumonitis, RP)£¨’‚÷÷—◊÷¢∑¥”¶—œ÷ÿ”∞œÏ÷Œ¡∆–ßπ˚∫Õ…˙ªÓ÷ ¡ø°£¥´Õ≥—–æø∂‡æ€Ωπ”⁄ŒÔ¿Ìº¡¡ø≤Œ ˝”≈ªØ£¨µ´Ω¸ƒÍ¿¥£¨»ÀÃÂ"µ⁄∂˛ª˘“Ú◊È"≥¶µ¿æ˙»∫”Î∑≈…‰À…Àµƒπÿ¡™÷Ω•∏°≥ˆÀÆ√Ê°£∂ØŒÔ µ—È“—÷§ µ≥¶µ¿Œ¢…˙ŒÔƒ‹µ˜øÿ∑Œ≤ø∑≈…‰À…À£¨µ´¡Ÿ¥≤÷§æ›¡¥ º÷’¥Ê‘⁄»±ø⁄£¨Ãÿ± «÷Œ¡∆∆⁄º‰æ˙»∫∂Ø豉ªØ”ÎRPµƒπÿ¡™ª˙÷∆…–Œ¥≤˚√˜°£
’Î∂‘’‚“ªø∆—ߌ £¨π„∂´ °ø∆—ß‘∫Œ¢…˙ŒÔ—–æøÀ˘¡™∫œ÷–…Ω¥Û—ß÷◊¡ˆ∑¿÷Œ÷––ƒµƒ—–æøÕ≈∂”ø™’π¡À“ªœÓ¥¥–¬–‘¡Ÿ¥≤—–æø°£À˚√« ’ºØ¡À17¿˝Ω” ‹Õ¨≤Ω∑≈ªØ¡∆(CCRT)µƒNSCLCªº’flÀƒ∏ˆ ±º‰µ„(T0-T3)µƒ∑‡±„—˘±æ£¨≤…”√shotgun∫ͪ˘“Ú◊È≤‚–ÚΩ·∫œ–¬–Õ¶ÃSTASISÀ„∑®£¨ ◊¥Œ¡øªØ¡À÷Œ¡∆∆⁄º‰≥¶µ¿æ˙»∫µƒ∂Ø茻∂®–‘£¨≤¢∑¢œ÷Œ¢…˙ŒÔŒ»Ã¨”ÎRP∑¢…˙∑Áœ’¥Ê‘⁄œ‘÷¯∏∫œ‡πÿ°£’‚œÓÕª∆∆–‘≥…π˚∑¢±Ì”⁄°∂iScience°∑‘”÷棨Œ™÷◊¡ˆ∑≈…‰÷Œ¡∆µƒ∂æ–‘π‹¿Ì÷π©¡À»´–¬ ”Ω«°£
—–æøÕ≈∂”‘À”√»˝œÓπÿº¸ºº ı£∫1) ◊›œÚ∂”¡–…˺∆£¨≤…ºØCCRT÷Œ¡∆«∞(T0)°¢ ◊≥Ã÷Œ¡∆∫Û(T1)°¢‘ˆ¡ø∑≈¡∆«∞(T2)∫Õ÷Œ¡∆∫Û(T3)µƒ∑‡±„—˘±æ£ª2) shotgun∫ͪ˘“Ú◊È≤‚–ÚΩ·∫œ¶ÃSTASISÀ„∑®º∆À„Œ¢…˙ŒÔŒ»∂®–‘∆¿∑÷(mS score)£ª3) LEfSe∑÷Œˆº¯∂®”ÎŒ»∂®–‘œ‡πÿµƒÃÿ’˜æ˙÷÷°£Õ®π˝±»Ωœ10¿˝G2+RPªº’fl”Î7¿˝G0RPªº’flµƒŒ¢…˙ŒÔÃÿ’˜£¨Ω“ æ¡Àæ˙»∫Œ»Ã¨µƒ¡Ÿ¥≤‘§≤‚º€÷µ°£
NSCLCªº’fl undergoing CCRT ∆⁄º‰≥¶µ¿æ˙»∫Œ»∂®–‘∂Ø豉ªØ
—–æø∑¢œ÷≥¶µ¿æ˙»∫‘⁄T1_T2Ω◊∂Œ( ◊≥Ã∑≈¡∆∫Û)Œ»∂®–‘œ‘÷¯ΩµµÕ(mS=0.10)£¨∑¥”≥40Gyº¡¡ø¿€ª˝∂‘Œ¢…˙ŒÔ»∫µƒ»≈∂Ø–ß”¶°£”–»§µƒ «£¨≤ø∑÷ªº’flƒ‹‘⁄‘ˆ¡ø∑≈¡∆Ω◊∂Œ(T2_T3)ª÷∏¥Œ»Ã¨(mS=0.38)£¨’‚÷÷ª÷∏¥ƒ‹¡¶”ÎRP∑Áœ’√‹«–œ‡πÿ°£PCoA∑÷Œˆ÷±π€œ‘ 棨∏flŒ»∂®–‘(HS)ªº’flµƒ—˘±æµ„≥ 怺Ø∑÷≤º£¨∂¯µÕŒ»∂®–‘(LS)ªº’fl‘Ú≥ œ÷¿Î…¢ƒ£ Ω°£
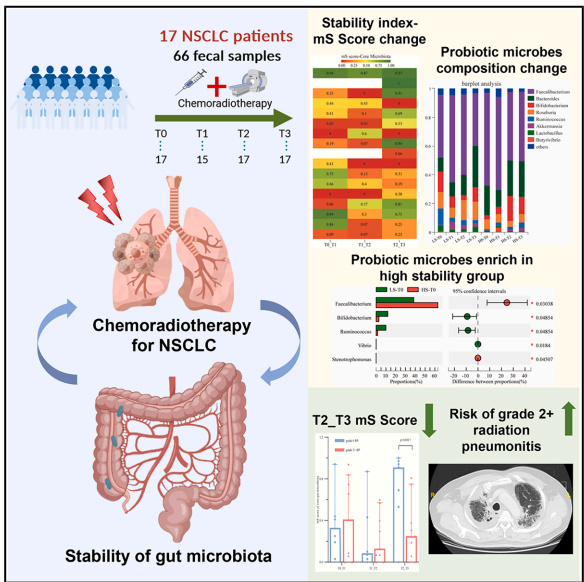
Œ¢…˙ŒÔŒ»Ã¨”ÎRP∑Áœ’µƒ∏∫œ‡πÿ–‘
∂‡“ÚÀÿ∑÷Œˆ÷§ µ£¨T2_T3Ω◊∂ŒµƒmS∆¿∑÷ «G2+RPµƒ∂¿¡¢‘§≤‚“Ú◊”(OR=0.014,p=0.048)°£HS◊È(9¿˝)RP∑¢…˙¬ œ‘÷¯µÕ”⁄LS◊È(8¿˝)(33.3% vs 87.5%,p=0.050)°£Ãÿ±÷µµ√◊¢“‚µƒ «£¨ƒ‹ª÷∏¥T2_T3Œ»∂®–‘µƒªº’flmS∆¿∑÷÷–Œª ˝¥Ô0.91£¨∂¯≥÷–¯–‘Œ…¬“ªº’flΩˆ0.25(p=0.033)£¨Ã· æ÷Œ¡∆÷–∫Û∆⁄æ˙»∫ª÷∏¥ƒ‹¡¶µƒπÿº¸◊˜”√°£
Faecalibacterium prausnitzii µƒŒ»Ã¨µ˜øÿ◊˜”√
Õ®π˝“Ê…˙æ˙Ãÿ’˜∑÷Œˆ∑¢œ÷£¨HS◊Èœ‘÷¯∏ªºØ≤˙∂°À·—ŒµƒFaecalibacterium(p=0.030)∫ÕStenotrophomonas(p=0.045)°£ª˘œfl∆⁄Faecalibacterium∑·∂»°›6.115(log÷µ)µƒªº’fl£¨ªÒµ√∏flŒ»∂®–‘µƒº∏¬ ‘ˆº”10.5±∂(p=0.040)°£∏√æ˙Õ®π˝Œ¨≥÷…œ∆§∆¡’œÕÍ’˚–‘∫Õøπ—◊◊˜”√£¨ø…ƒ‹∞Ô÷˙Àfi÷˜µ÷øπ∑≈¡∆“˝∆µƒŒ¢…˙ŒÔŒ…¬“°£
’‚œÓ—–æøø™¥¥–‘µÿΩ®¡¢¡À≥¶µ¿æ˙»∫Œ»∂®–‘”ÎRP∑Áœ’µƒ¡Ÿ¥≤πÿ¡™£¨Ã·≥ˆ¡À"Œ¢…˙ŒÔŒ»Ã¨"◊˜Œ™–¬–Õ…˙ŒÔ±Í÷æŒÔµƒ∏≈ƒÓ°£—–æø∑¢œ÷CCRT÷Œ¡∆π˝≥Ã÷–¥Ê‘⁄πÿº¸µƒ"Œ¢…˙ŒÔ¥‡»ı¥∞ø⁄∆⁄"(T1_T2)£¨∂¯∫Û–¯ª÷∏¥ƒ‹¡¶æˆ∂®RP∑Áœ’°£∏¸æfl”–÷ÿ“™“‚“µƒ «£¨º¯∂®≥ˆFaecalibacterium prausnitzii◊˜Œ™«±‘⁄µƒ“Ê…˙æ˙∏…‘§∞–µ„£¨Œ™Õ®π˝Œ¢…˙ŒÔµ˜øÿΩµµÕ∑≈¡∆∂斑÷π©¡À÷±Ω”“¿æ›°£µ±«∞—–æøæ÷œfi–‘‘⁄”⁄—˘±æ¡øΩœ–°£¨Œ¥¿¥–Ë“™¿©¥Û∂”¡–—È÷§£¨≤¢ÃΩÀ˜æ˙»∫-¥˙–ªŒÔ-√‚“fl÷·µƒæflÃÂ◊˜”√ª˙÷∆°£¥”¡Ÿ¥≤◊™ªØΩ«∂»ø¥£¨∏√≥…π˚÷ æ‘⁄∑≈¡∆πÿº¸ ±º‰¥∞Ω¯––Œ¢…˙ŒÔº‡≤‚∫Õ∏…‘§£®»ÁÃÿ∂®“Ê…˙æ˙≤π≥‰£©ø…ƒ‹≥…Œ™∏ˆ–‘ªØ÷ß≥÷÷Œ¡∆µƒ–¬≤fl¬‘°£
 …˙ŒÔÕ®Œ¢–≈π´÷⁄∫≈
…˙ŒÔÕ®Œ¢–≈π´÷⁄∫≈
÷™√˚∆Û“µ’–∆∏
ΩÒ»’∂Øè | »À≤≈ –≥° | –¬ºº ı◊®¿∏ | ÷–π˙ø∆—ß»À | ‘∆’πî | BioHot | ‘∆Ω≤Ã√÷±≤• | ª·’π÷––ƒ | Ãÿº€◊®¿∏ | ºº ıøÏ—∂ | √‚∑— ‘”√
∞Ê»®À˘”– …˙ŒÔÕ®
Copyright© eBiotrade.com, All Rights Reserved
¡™œµ–≈œ‰£∫
‘¡ICP±∏09063491∫≈