
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:靶向自噬在功能失调的肿瘤血管系统中的作用
《iScience》:Targeting autophagy in dysfunctional tumor vasculature
【字体: 大 中 小 】 时间:2025年12月03日 来源:iScience 4.1
编辑推荐:
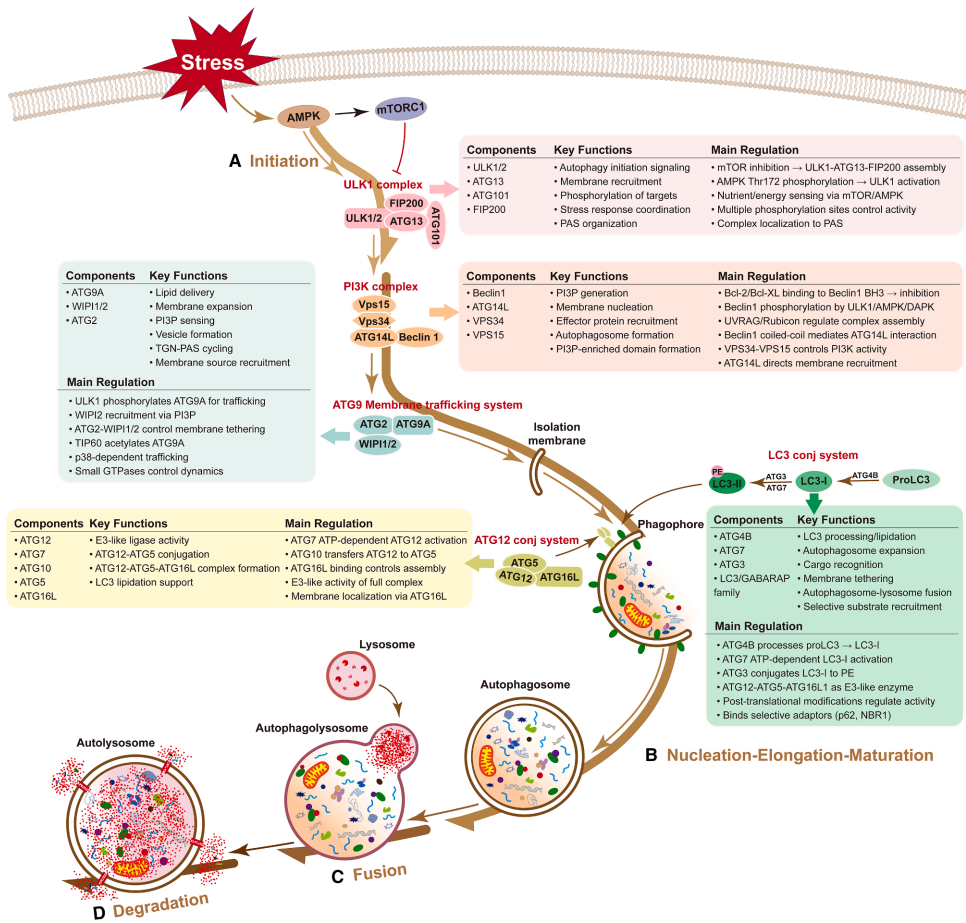
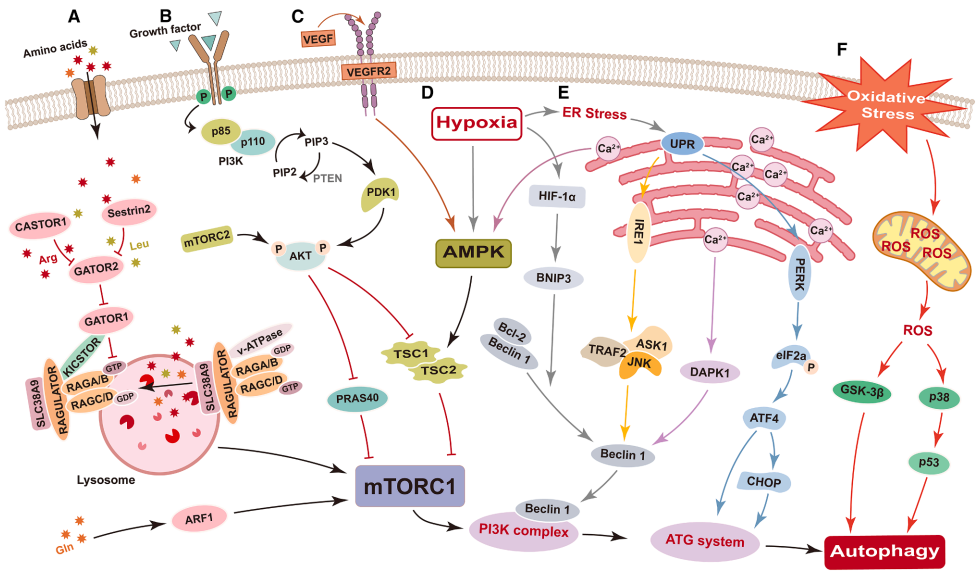
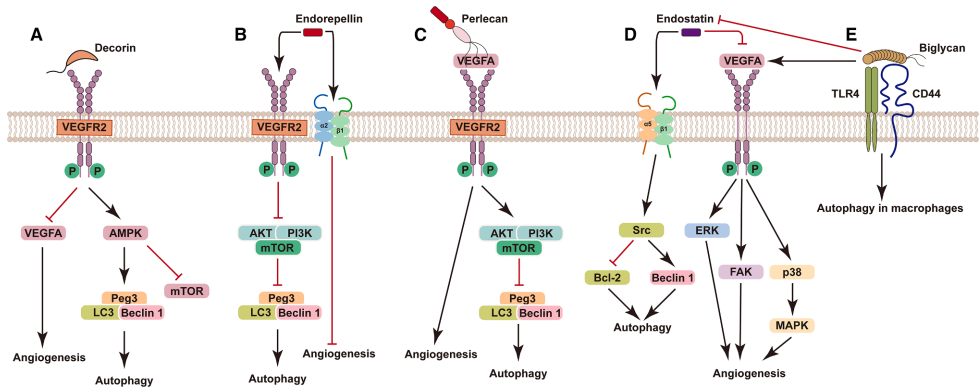
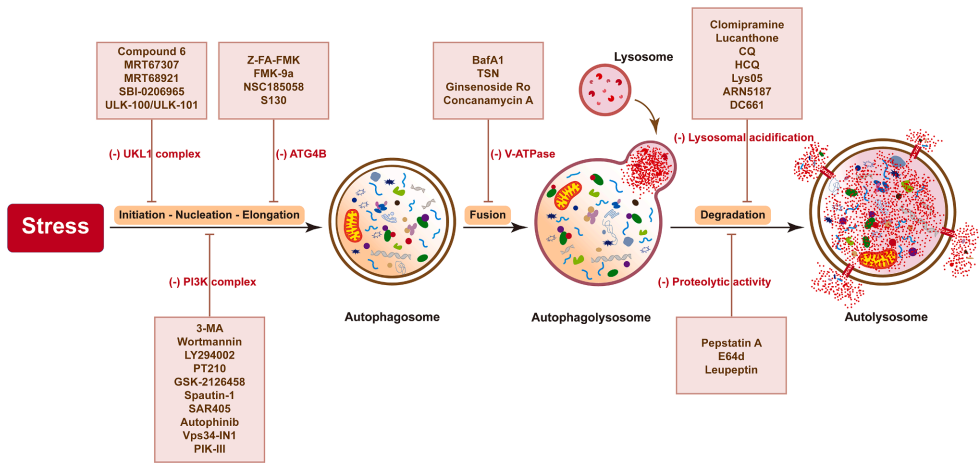
本综述系统阐述了自噬在肿瘤血管系统中的核心调控作用,深入探讨了其分子机制(如mTOR/AMPK信号通路、VEGF介导的调节)、细胞相互作用(如周细胞与蛋白聚糖的调控)及治疗应用(如自噬抑制剂与抗血管生成药物、免疫检查点抑制剂的联合策略),为开发靶向肿瘤血管的新型癌症疗法提供了关键理论基础和转化视角。
 生物通微信公众号
生物通微信公众号
知名企业招聘