靶向TBK1/IKKε介导的RIPK1磷酸化抑制增强肿瘤对免疫细胞杀伤的敏感性
《Cell Death Discovery》:Inhibition of TBK1/IKKε mediated RIPK1 phosphorylation sensitizes tumors to immune cell killing
【字体:
大
中
小
】
时间:2025年11月30日
来源:Cell Death Discovery 7
编辑推荐:
本研究针对肿瘤对免疫细胞介导的细胞毒性(如免疫检查点阻断疗法)的耐药性问题,通过多组学分析与功能实验,揭示了TBK1/IKKε激酶通过磷酸化RIPK1第25位丝氨酸(S25)维持肿瘤存活的关键机制。研究发现,抑制TBK1/IKKε可阻断RIPK1的生存磷酸化,促进其激活(S166磷酸化),从而增强CD8+ T细胞和NK细胞对黑色素瘤的杀伤效果。该工作为克服肿瘤免疫耐受提供了新靶点,有望提升现有免疫疗法的疗效。
在癌症治疗领域,免疫检查点阻断(ICB)疗法通过激活患者自身的免疫系统来攻击肿瘤,已成为革命性的突破。然而,大多数患者因肿瘤对免疫细胞杀伤的固有抵抗而疗效有限。尤其令人困扰的是,即使免疫细胞(如CD8+ T细胞)能浸润肿瘤并释放肿瘤坏死因子(TNF)等细胞因子,肿瘤仍可通过激活内部生存信号逃脱死亡。这种耐药性背后的分子机制尚不明确,成为提升免疫疗法效果的关键瓶颈。
为解决这一难题,Anastasia Piskopou等研究团队在《Cell Death Discovery》上发表了一项研究,聚焦于TNF信号通路中的核心调控蛋白RIPK1。RIPK1如同一个“分子开关”,其活性状态决定细胞在TNF刺激下走向生存或死亡。此前研究发现,某些肿瘤突变可通过依赖RIPK1的方式增强T细胞杀伤,但RIPK1的精准调控机制及其在免疫细胞攻击下的动态变化仍待揭示。本研究通过整合磷酸化蛋白质组学、CRISPR筛选和功能性验证,首次阐明TBK1/IKKε激酶通过磷酸化RIPK1第25位丝氨酸(S25)维持肿瘤存活,而靶向这一机制可显著增强免疫细胞的杀伤效力。
研究利用健康捐赠者来源的PBMC(外周血单核细胞)分离CD8+ T细胞和NK细胞,通过抗原受体工程化构建共培养系统;采用CRISPR-Cas9技术构建基因敲除细胞系(如TRAF2、CYLD、TBK1/IKKε等);通过生物素标记的TNF刺激与链霉亲和素磁珠富集TNFR1复合物,结合质谱(AP-MS)分析其组成和磷酸化修饰;开发靶向质谱(SRM)方法定量RIPK1磷酸化位点;利用竞争性细胞存活实验和流式细胞术评估免疫细胞杀伤效果。
1. 敏感化肿瘤细胞在T细胞攻击下丧失促生存磷酸化事件
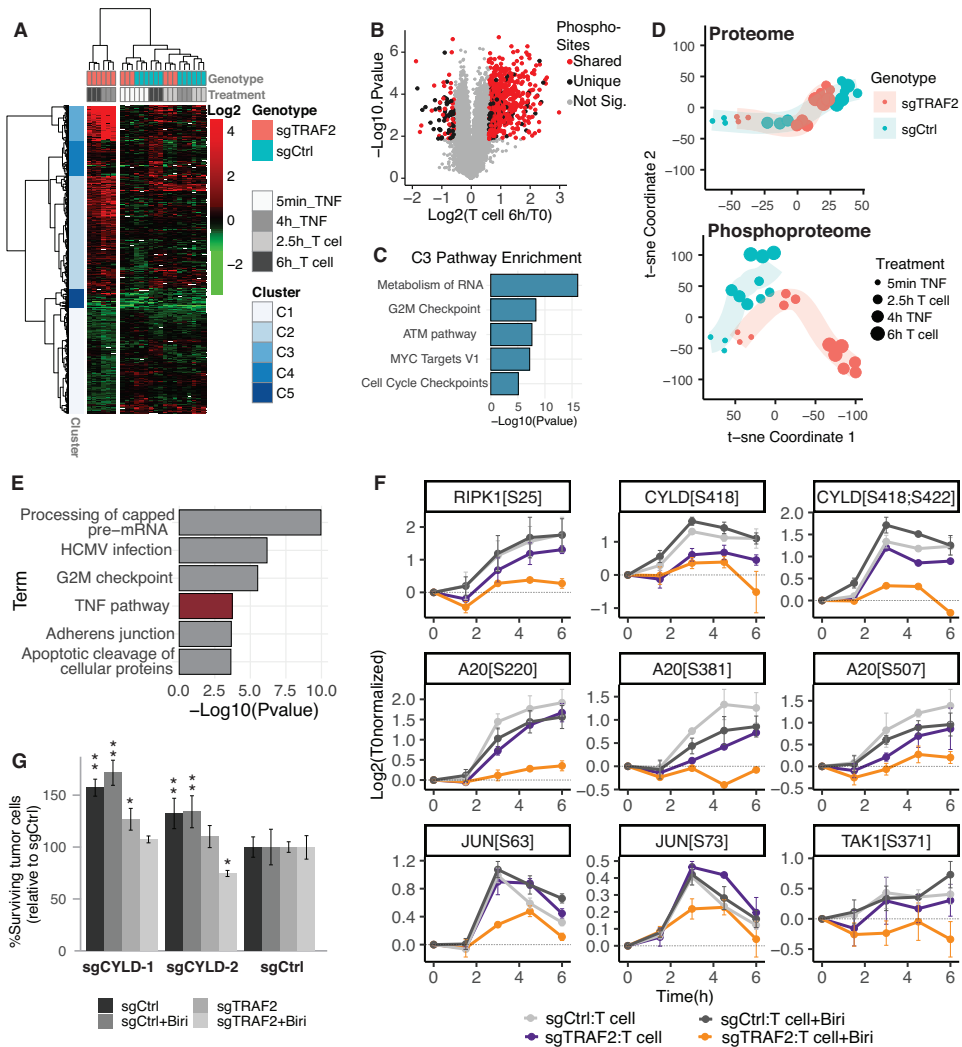
通过对比野生型与TRAF2敲除(KO)黑色素瘤细胞在TNF或T细胞共培养下的磷酸化蛋白质组,发现敏感化肿瘤细胞中近90%的磷酸化位点变化与TNF处理高度重叠,且DNA损伤响应通路(如ATM、ATR)被快速激活。进一步时间序列分析显示,耐药细胞在T细胞攻击下能诱导RIPK1 S25和CYLD S418/S422等位点的磷酸化(抑制细胞死亡),而敏感细胞(TRAF2 KO联合Birinapant处理)则丧失该响应。CYLD敲除实验证实其失活可增强肿瘤抵抗性,验证了磷酸化修饰在免疫逃逸中的核心作用。
2. 敏感化肿瘤细胞的TNFR1复合物缺乏非经典IKK激酶
通过TNF刺激后TNFR1复合物的亲和纯化与质谱分析,发现敏感细胞中LUBAC线性泛素化复合物及IKK激酶(包括IKKα/β和TBK1/IKKε)的招募显著减少。相关性分析显示,复合物中蛋白丰度降低与CRISPR筛选中的肿瘤敏感化基因高度相关。值得注意的是,在多种敏感化模型(如RNF31 KO或HOPIN-8抑制剂处理)中,TBK1/IKKε的缺失是共同特征,表明其招募是维持肿瘤抵抗的关键。
3. 敏感化肿瘤细胞无法抑制TNFR1复合物内RIPK1激活
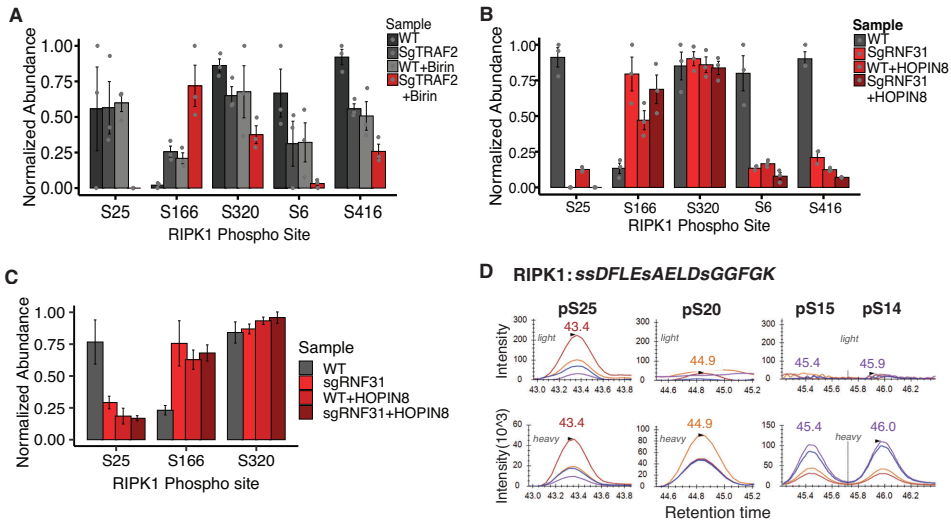
靶向质谱分析揭示,敏感细胞中RIPK1 S25磷酸化水平显著降低,而代表激活状态的S166磷酸化升高。这种磷酸化失衡在TBK1/IKKε缺失的细胞中尤为明显,且不受经典IKK激酶(IKKα/β)影响,证实TBK1/IKKε是RIPK1 S25磷酸化的主要激酶。
4. 非经典IKK检查点激酶的缺失增强肿瘤对免疫细胞杀伤的敏感性
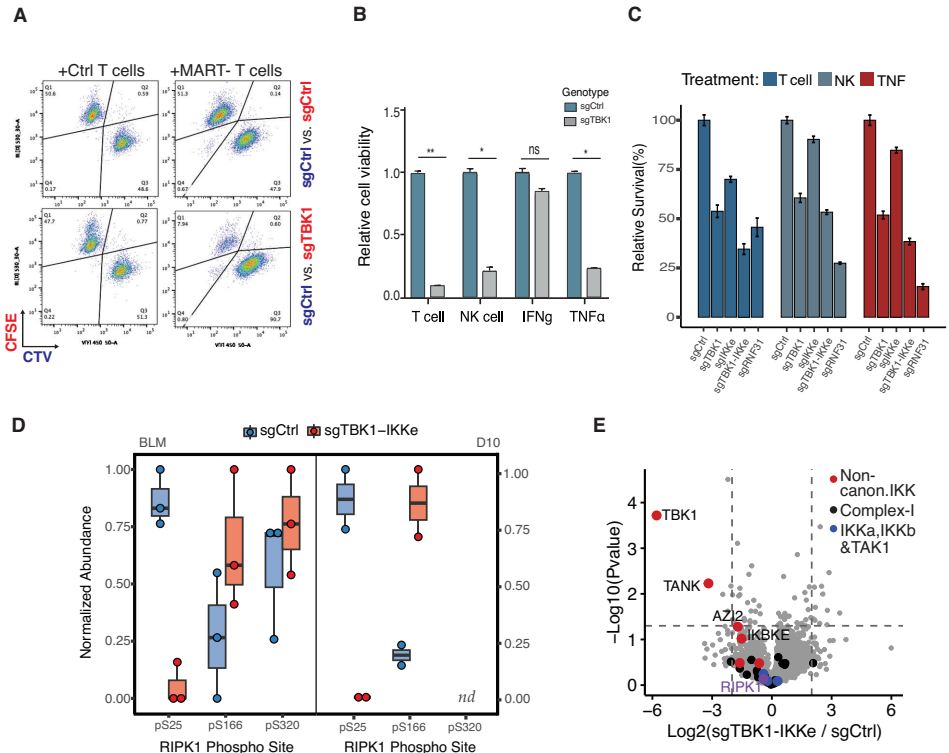
功能实验表明,TBK1单独敲除或TBK1/IKKε双敲除可显著增强黑色素瘤细胞对CD8+ T细胞和NK细胞的敏感性,且该效应特异于TNF通路(对IFN-γ无响应)。TNFR1复合物质谱进一步验证敲除细胞中RIPK1 S25磷酸化缺失及S166磷酸化升高,证实TBK1/IKKε通过直接调控RIPK1磷酸化平衡决定免疫杀伤结局。
本研究系统阐明了肿瘤抵抗T细胞杀伤的一种新机制:TBK1/IKKε激酶通过磷酸化RIPK1 S25维持其非活性状态,从而抑制TNF介导的细胞死亡。干扰这一检查点可促进RIPK1激活,将TNF信号导向凋亡方向。与直接敲除RIPK1的策略相比,靶向TBK1/IKKε不仅能解除生存信号,还保留了RIPK1的促死亡功能,具有更好的治疗潜力。该发现为联合ICB疗法提供了新思路,例如通过开发TBK1/IKKε抑制剂增强免疫细胞杀伤效率。未来需在体内模型中验证其安全性,并深入探索经典与非经典IKK激酶的交互作用。这一研究从分子层面揭示了肿瘤免疫耐受的可塑性机制,为克服临床耐药性提供了理论依据。
 生物通微信公众号
生物通微信公众号
 生物通新浪微博
生物通新浪微博
今日动态 |
人才市场 |
新技术专栏 |
中国科学人 |
云展台 |
BioHot |
云讲堂直播 |
会展中心 |
特价专栏 |
技术快讯 |
免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号


 生物通微信公众号
生物通微信公众号