可靶向基因组CRISPR筛选揭示KEAP1/NRF2轴调控PD-L1表达的新机制
《Communications Biology》:Druggable genome CRISPR screening identifies the KEAP1/NRF2 axis as a mediator of PD-L1 expression
【字体:
大
中
小
】
时间:2025年11月21日
来源:Communications Biology 5.1
编辑推荐:
本研究通过靶向“可靶向基因组”的CRISPR筛选,在胰腺癌和卵巢癌细胞中发现KEAP1/NRF2轴是IFNγ诱导PD-L1表达的关键调控通路。KEAP1缺失或抑制剂激活NRF2可转录抑制PD-L1,增强抗肿瘤免疫。该研究为免疫检查点调控提供了新靶点,对改善免疫治疗耐药性具有重要意义。
在肿瘤免疫治疗领域,程序性死亡配体1(PD-L1)在癌细胞表面的表达是帮助肿瘤逃避免疫清除的关键机制。当细胞毒性T细胞释放干扰素γ(IFNγ)等炎症因子时,癌细胞会快速上调PD-L1,进而通过结合T细胞上的PD-1受体抑制其活性。尽管PD-1/PD-L1抑制剂在部分癌症中取得显著疗效,但多数患者仍存在原发性或获得性耐药。因此,揭示PD-L1表达的深层调控机制,尤其是寻找可药物靶向的通路,已成为当前研究的焦点。
为系统筛选调控PD-L1表达的关键基因,美国西北大学Feinberg医学院的Fidan Seker-Polat、Mazhar Adli团队在《Communications Biology》上发表研究,通过定制化的CRISPR基因敲除文库,对6种胰腺癌和卵巢癌细胞系进行功能筛选。研究不仅验证了已知的PD-L1调控因子(如JAK1/2、IFNGR1/2),还首次发现KEAP1/NRF2轴在所有测试细胞系中均能负向调控PD-L1转录。机制研究表明,KEAP1缺失会解除对转录因子NRF2的抑制,活化的NRF2进入细胞核后直接结合PD-L1增强子区域,抑制其mRNA和蛋白表达。在动物模型中,药物激活NRF2可降低肿瘤PD-L1水平,促进细胞毒性T细胞浸润,减少耗竭T细胞,从而抑制肿瘤生长。
该研究创新性地将氧化应激应答关键通路KEAP1/NRF2与免疫检查点调控联系起来,为通过代谢-免疫交叉对话增强抗肿瘤免疫提供了新策略。
研究采用定制化sgRNA文库(靶向约1400个可药物化基因)在6种癌细胞系中进行CRISPR筛选,通过流式细胞术分选PD-L1高/低表达群体,并利用Beta-binomial模型分析基因富集。验证实验包括基因敲除、药物抑制(如Bardoxolone、CDDO-me)、蛋白质印迹、实时定量PCR、染色质免疫沉淀(ChIP)及活细胞成像。体内实验采用免疫健全小鼠模型,通过高维流式细胞术分析肿瘤免疫细胞浸润。
可靶向基因组CRISPR筛选鉴定PD-L1调控因子
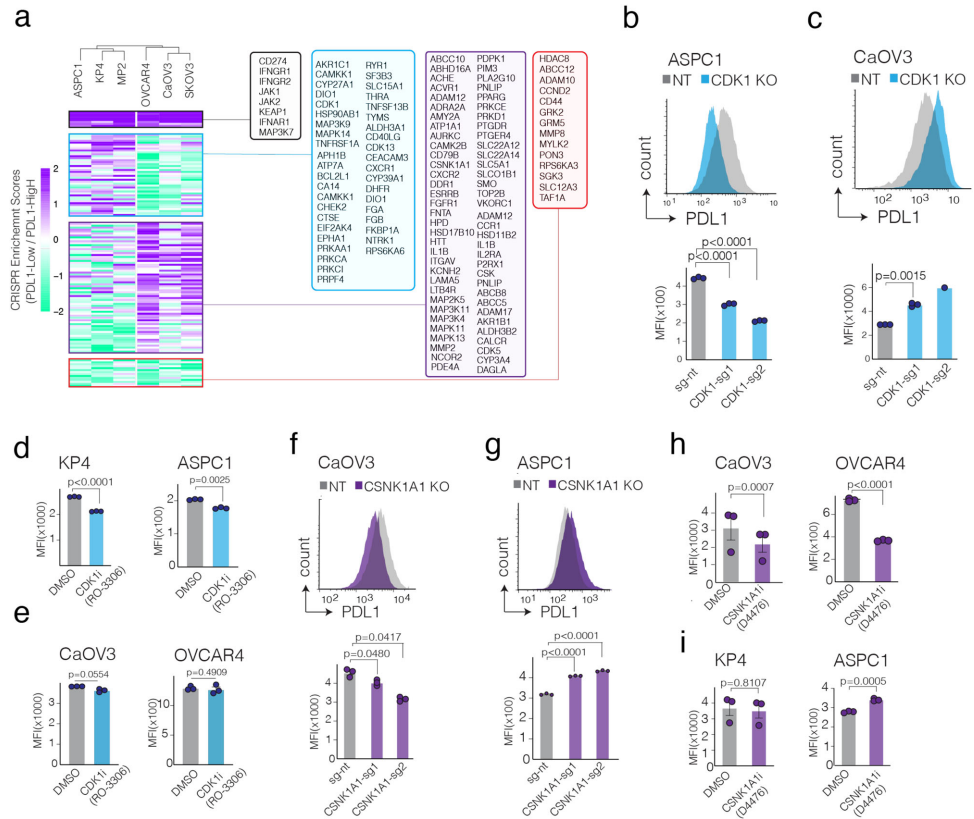
筛选成功富集了已知的PD-L1调控基因(如CD274、JAK1/2),并发现KEAP1是新型正向调控因子。
胰腺癌与卵巢癌细胞的调控网络具显著异质性。CDK1特异性调控胰腺癌PD-L1,而CSNK1A1仅影响卵巢癌。
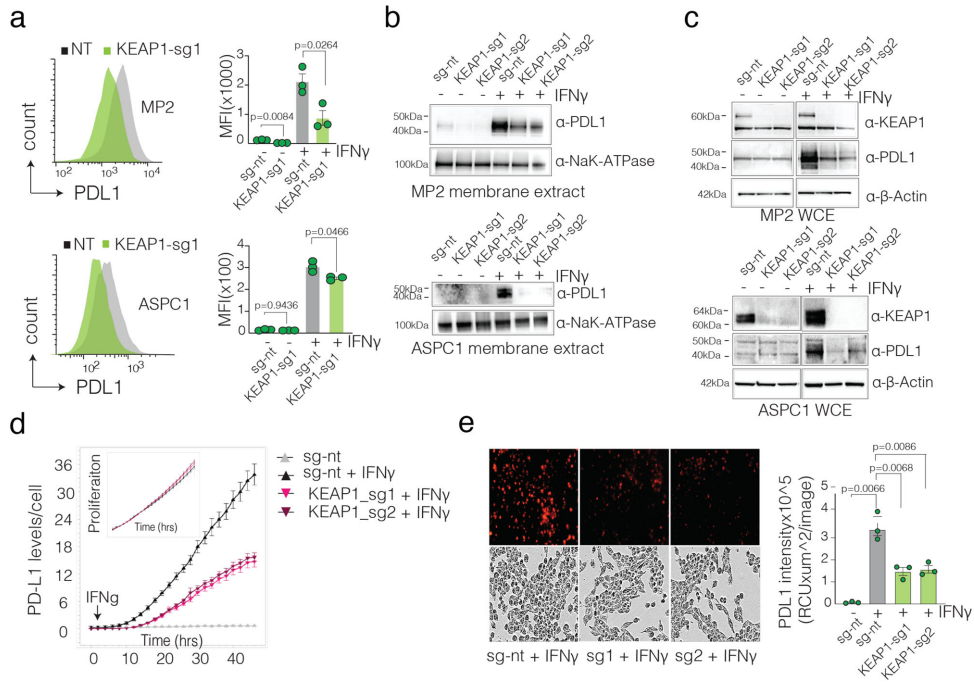
KEAP1敲除或抑制剂处理均显著降低膜结合与总PD-L1蛋白,且不影响细胞活力。
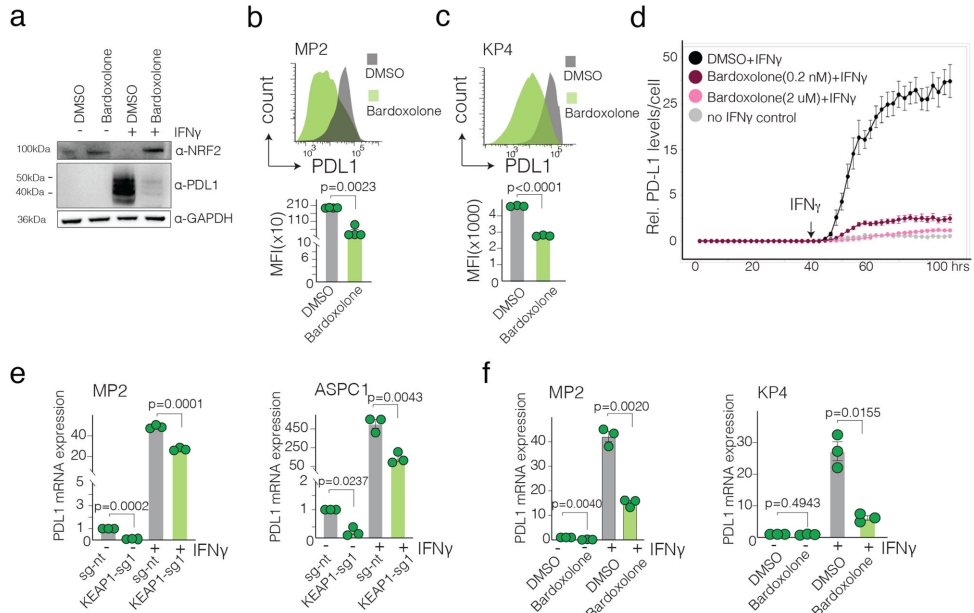
Bardoxolone处理抑制KEAP1后,PD-L1的mRNA水平显著下降,且NRF2激活是关键中介。
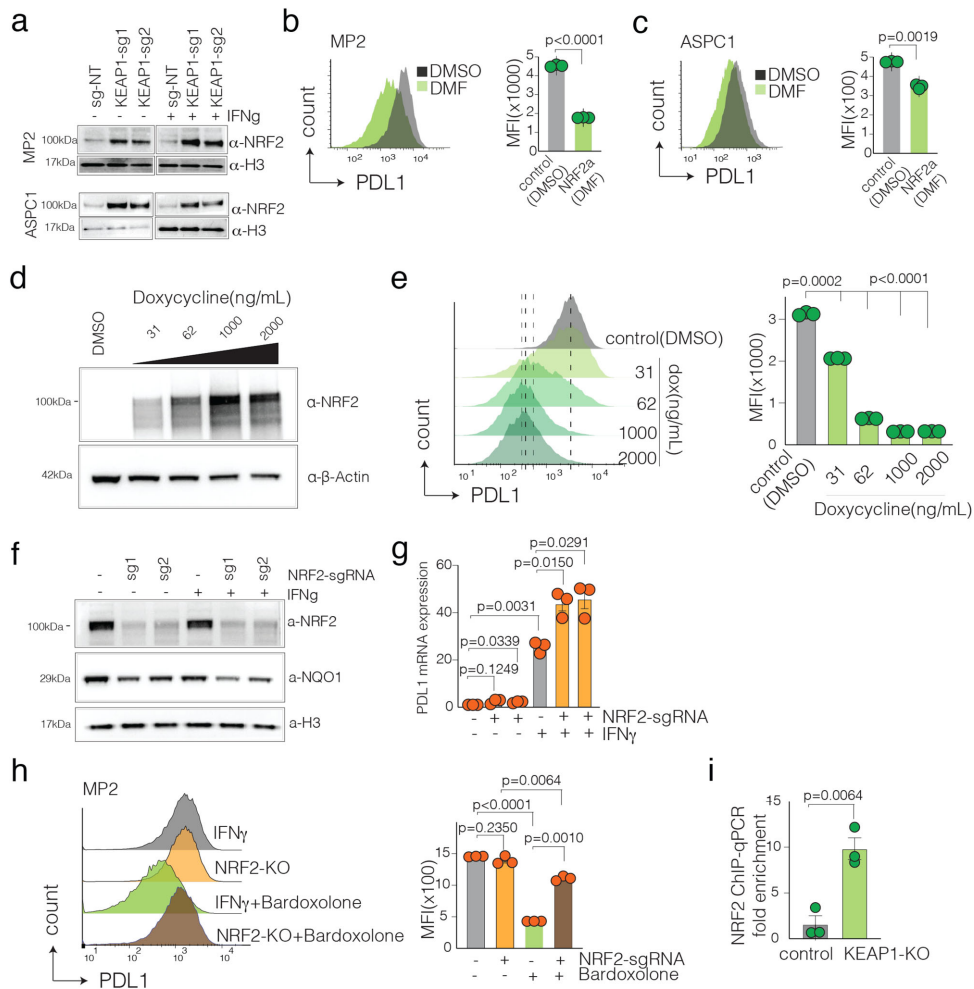
NRF2过表达直接抑制PD-L1转录,其缺失则逆转该效应。ChIP实验证实NRF2结合PD-L1增强子。
在免疫健全小鼠模型中,CDDO-me处理激活NRF2可降低肿瘤PD-L1表达,减少耗竭T细胞,增强CD8+ T细胞功能,抑制肿瘤生长。
本研究通过多维度功能筛选,揭示了KEAP1/NRF2轴作为PD-L1转录调控的核心通路,突破了既往仅关注蛋白稳定性或膜定位的局限。值得注意的是,NRF2在PD-L1调控中表现出语境依赖性功能:在应激应答中通常激活抗氧化基因,而在本模型中却作为转录抑制因子发挥作用。这一发现为理解代谢-免疫交叉对话提供了新视角,尤其对PD-L1高表达且免疫治疗应答差的癌症(如胰腺癌、卵巢癌)具有转化价值。研究提示,靶向KEAP1/NRF2可能通过双重机制――降低肿瘤细胞PD-L1表达与重塑免疫微环境――增强抗肿瘤免疫,为联合治疗策略开发奠定基础。
 生物通微信公众号
生物通微信公众号
 生物通新浪微博
生物通新浪微博
今日动态 |
人才市场 |
新技术专栏 |
中国科学人 |
云展台 |
BioHot |
云讲堂直播 |
会展中心 |
特价专栏 |
技术快讯 |
免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号



 生物通微信公众号
生物通微信公众号