UHRF1通过表观遗传沉默病毒受体APN限制HCoV-229E感染:一种与年龄相关的宿主防御机制
《Nature Communications》:UHRF1 restricts HCoV-229E infection through epigenetic silencing of the viral receptor APN
【字体:
大
中
小
】
时间:2025年11月19日
来源:Nature Communications 15.7
编辑推荐:
本研究针对常见冠状病毒HCoV-229E在老年人群中引发严重疾病的问题,通过全基因组CRISPR敲除筛选,发现表观遗传调控因子UHRF1是关键的宿主防御因子。机制研究表明,UHRF1通过维持病毒受体APN启动子的高甲基化抑制其表达,从而限制病毒入侵。单细胞测序和原代肺泡巨噬细胞实验证实,UHRF1表达随年龄增长而下降,导致老年人对HCoV-229E易感性增加。该研究揭示了宿主通过表观遗传调控病毒受体的新型防御机制,为开发针对冠状病毒的年龄特异性治疗策略提供了新视角。
当SARS-CoV-2疫情逐渐平息,人们可能忽视了那些常年在我们身边存在的普通冠状病毒。像HCoV-229E这样的病毒,通常只引起普通感冒症状,却在老年人和免疫功能低下者中可能引发严重肺炎甚至急性呼吸窘迫综合征。这种年龄相关的易感性差异背后隐藏着怎样的分子机制?这正是复旦大学张荣团队在《Nature Communications》上发表的最新研究试图解答的问题。
研究人员采用全基因组CRISPR敲除筛选这一前沿技术,意外发现了一个名为UHRF1的表观遗传调控因子。这个蛋白以往主要在研究DNA甲基化和肿瘤发生中被关注,而在这项工作中,它展现出了全新的抗病毒功能。更为有趣的是,UHRF1的表达水平与年龄呈现负相关,这为解释老年人对冠状病毒更易感提供了重要线索。
研究团队采用的关键技术方法包括:全基因组CRISPR敲除筛选鉴定宿主限制因子;聚焦CRISPR激活筛选验证UHRF1下调基因的功能;假病毒系统分析病毒入侵机制;转录组和单细胞RNA测序分析基因表达与年龄相关性;原代肺泡巨噬细胞感染实验(样本来源于年轻和老年捐赠者的支气管肺泡灌洗液);DNA甲基化状态分析(亚硫酸氢盐测序)和染色质免疫沉淀等技术。
基因组CRISPR敲除筛选鉴定UHRF1为HCoV-229E感染的宿主限制因子
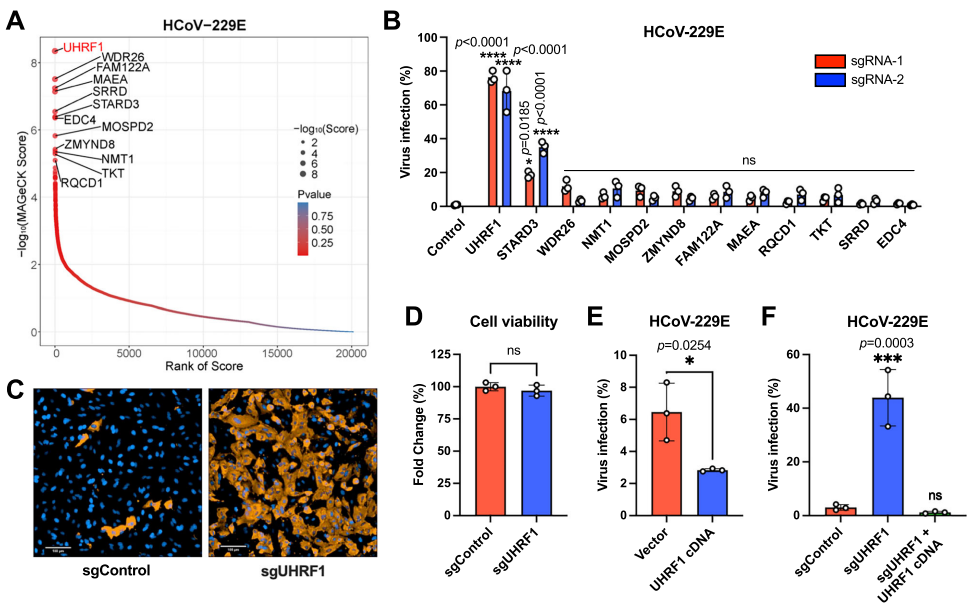
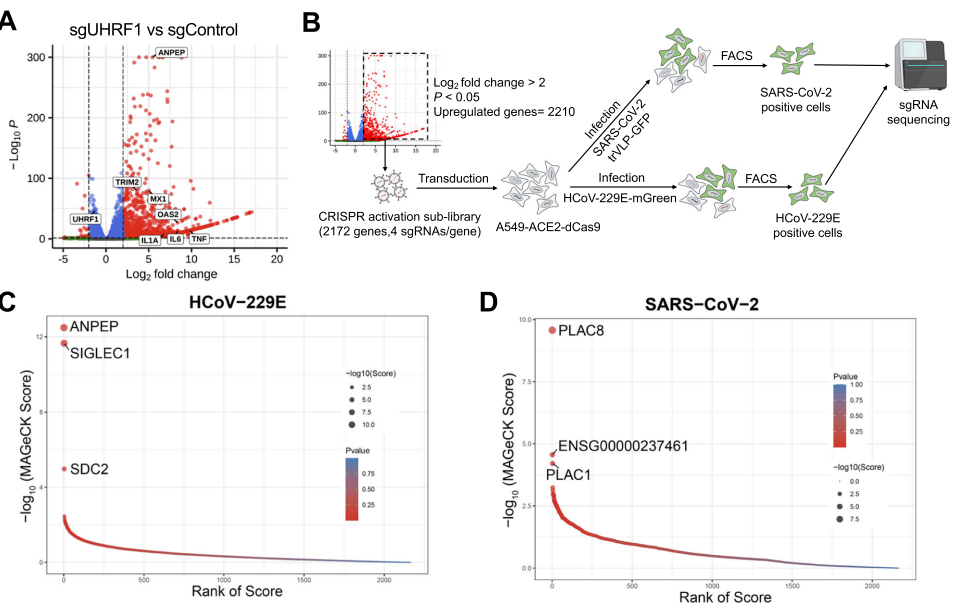
研究团队首先利用表达mGreenLantern报告基因的HCoV-229E病毒,在A549细胞中进行了全基因组CRISPR敲除筛选。通过感染24小时后分选报告基因阳性细胞并分析sgRNA富集情况,发现UHRF1(Ubiquitin-like with PHD and RING finger domains 1)得分最高。验证实验表明,敲除UHRF1可使HCoV-229E感染率从约1%大幅提升至近80%,而UHRF1过表达则抑制病毒感染,证明其在冠状病毒感染中发挥关键限制作用。
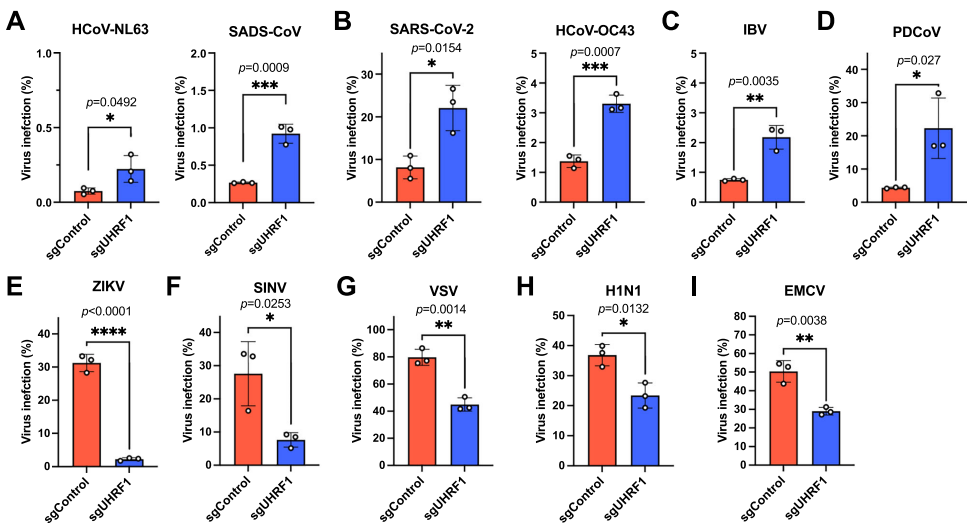
研究人员进一步测试了UHRF1对不同冠状病毒属的代表毒株的影响。结果显示,UHRF1敲除对α属(HCoV-229E)、β属(SARS-CoV-2、HCoV-OC43)、γ属(传染性支气管炎病毒)和δ属(猪德尔塔冠状病毒)均有一定程度的感染增强作用,但对HCoV-229E的效果最为显著。有趣的是,对于其他RNA病毒如寨卡病毒、辛德比斯病毒、水泡性口炎病毒、流感病毒和脑心肌炎病毒,UHRF1敲除反而抑制感染,表明其抗病毒作用具有冠状病毒特异性。
UHRF1通过抑制APN表达抑制HCoV-229E入侵
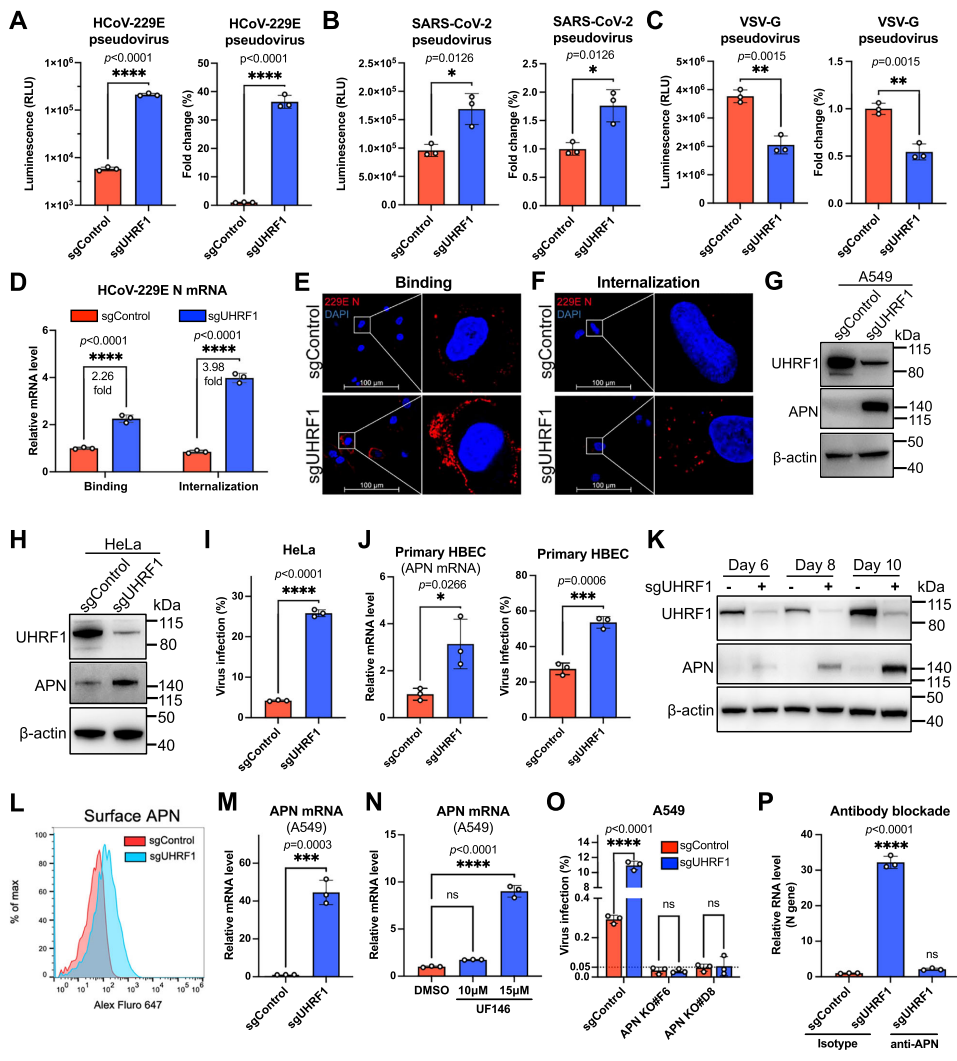
机制研究发现,UHRF1主要影响病毒的入侵阶段。假病毒实验显示,UHRF1敲除特异性增强带有HCoV-229E刺突蛋白的假病毒感染,而不影响VSV-G假病毒。病毒结合和内化实验证实,UHRF1缺失同时增强了病毒与细胞的结合和内化过程。进一步研究揭示,UHRF1通过表观遗传调控下调HCoV-229E的细胞进入受体APN(氨肽酶N)的表达。Western blot和流式细胞术分析表明,UHRF1敲除显著提升APN的mRNA和蛋白水平,尤其是细胞表面表达。
UHRF1通过维持APN启动子甲基化抑制HCoV-229E感染
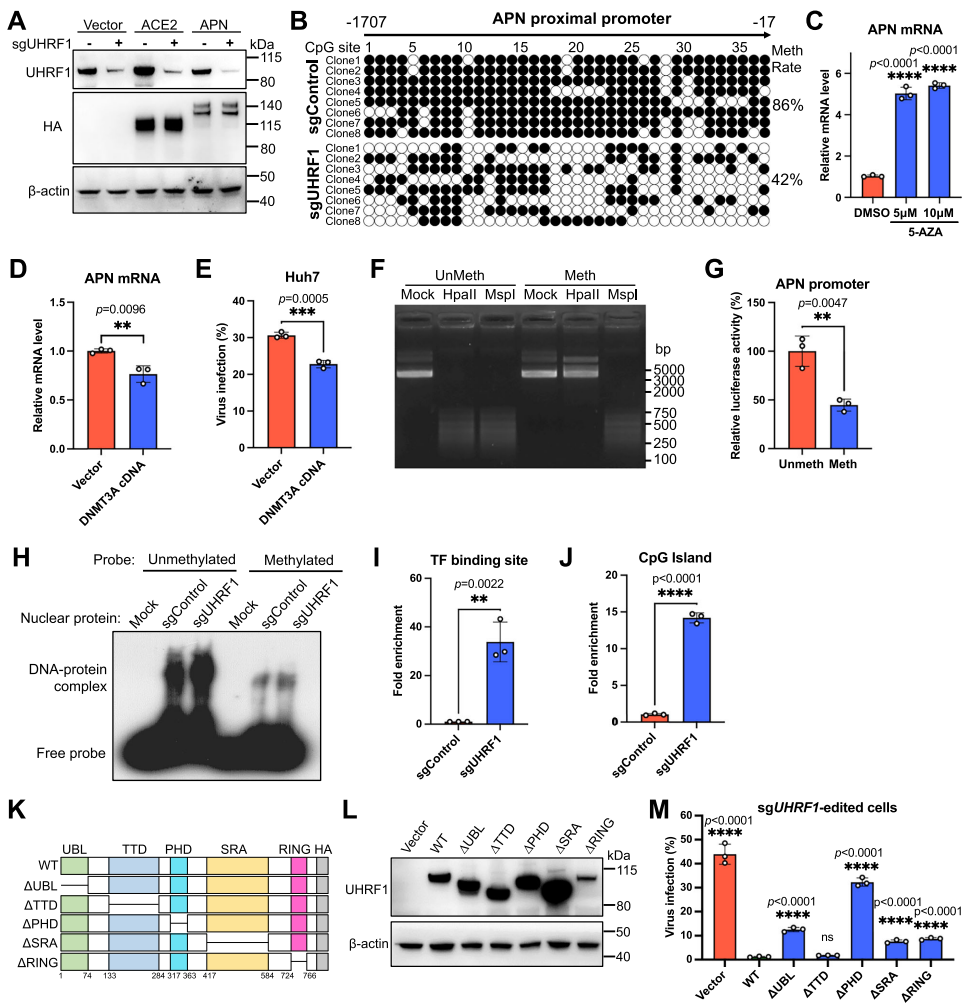
为阐明UHRF1调控APN表达的具体机制,研究人员进行了深入的分子研究。蛋白质稳定性实验排除了UHRF1通过促进APN降解的可能性。亚硫酸氢盐测序分析发现,UHRF1敲除导致APN启动子区CpG位点的甲基化率从86.15%显著下降至42.23%。使用DNA甲基化抑制剂5-氮杂胞苷处理可模拟UHRF1敲除效应,上调APN表达。双荧光素酶报告基因实验进一步证实,APN启动子的甲基化直接抑制其转录活性。电泳迁移率变动分析显示,甲基化降低了转录因子c-Maf与APN启动子的结合,染色质免疫沉淀实验验证了这一发现。
APN是UHRF1抑制HCoV-229E感染的最主要靶基因
RNA-seq分析显示,UHRF1敲除导致2210个基因上调和51个基因下调,其中APN mRNA表达上调约40倍。为系统鉴定UHRF1抑制的促病毒感染基因,研究团队构建了针对2172个上调基因的聚焦CRISPR激活筛选文库。结果显示,在HCoV-229E感染筛选中,APN得分最高,其次是SIGLEC1和SDC2等已知的冠状病毒感染促进因子。在SARS-CoV-2筛选中,PLAC8得分最高。此外,研究还发现UHRF1调控硫酸肝素的生物合成基因,表明其抗病毒作用具有多因子参与的特点。
UHRF1表观遗传调控驱动年龄相关的HCoV-229E易感性
转录组数据分析发现,UHRF1在肺组织中的表达随年龄增长而下降,而APN表达则随年龄上升。单细胞RNA测序数据显示,UHRF1在胎儿肺中高表达,而在老年人中表达降低;相反,APN在老年人肺组织中高表达,尤其在巨噬细胞和单核细胞中。对原代肺泡巨噬细胞的研究证实,老年捐赠者(53-80岁)的UHRF1 mRNA水平比年轻捐赠者(20-25岁)低50%,而APN表达高约4倍。相应地,老年捐赠者的肺泡巨噬细胞对HCoV-229E更易感,病毒载量和细胞因子(如IL6和TNFα)产生更高。APN启动子甲基化分析显示,老年个体甲基化程度降低。
这项研究首次揭示了UHRF1作为年龄相关的宿主防御因子,通过表观遗传沉默病毒受体APN限制冠状病毒感染的机制。研究不仅阐明了普通冠状病毒在老年人中引起严重疾病的分子基础,还为开发针对冠状病毒的年龄特异性治疗策略提供了新靶点。UHRF1-APN轴可能成为预测和干预年龄相关病毒感染易感性的重要靶标,具有重要的临床转化价值。
 生物通微信公众号
生物通微信公众号
 生物通新浪微博
生物通新浪微博
今日动态 |
人才市场 |
新技术专栏 |
中国科学人 |
云展台 |
BioHot |
云讲堂直播 |
会展中心 |
特价专栏 |
技术快讯 |
免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号


 生物通微信公众号
生物通微信公众号