靶向CDK7:头颈癌治疗新策略――有效阻断细胞周期与致癌信号传导
《Signal Transduction and Targeted Therapy》:CDK7-targeted therapy effectively disrupts cell cycle progression and oncogenic signaling in head and neck cancer
【字体:
大
中
小
】
时间:2025年11月07日
来源:Signal Transduction and Targeted Therapy 52.7
编辑推荐:
本研究针对头颈鳞状细胞癌(HNSCC)缺乏有效靶向治疗的临床困境,通过全基因组CRISPR筛选发现CDK7是关键治疗靶点。研究人员采用基因敲除和选择性抑制剂(YKL-5-124/samuraciclib)证实CDK7抑制能显著抑制HNSCC细胞增殖,诱导细胞周期阻滞和凋亡,并在患者来源类器官(PDO)和异种移植(PDX)模型中验证其抗肿瘤活性。该研究为HNSCC提供了新的治疗策略,支持CDK7抑制剂进入临床转化。
头颈鳞状细胞癌(HNSCC)是全球第六大常见恶性肿瘤,尽管手术、放疗和化疗等多模式治疗策略不断进步,但患者五年生存率仍徘徊在40%-50%之间。对于复发或转移性患者,预后尤其不容乐观。当前HNSCC的精准医疗主要局限于EGFR特异性抑制剂西妥昔单抗以及免疫治疗药物纳武利尤单抗和帕博利珠单抗,但这些治疗方案受益人群有限,且易产生耐药性。因此,识别新的治疗靶点成为改善HNSCC治疗效果的迫切需求。
在这项发表于《Signal Transduction and Targeted Therapy》的研究中,研究人员通过全基因组CRISPR筛选技术,在五种HNSCC细胞系中系统性地探索了遗传脆弱性,最终将目光聚焦于细胞周期蛋白依赖性激酶7(CDK7)。CDK7作为CDK激活激酶(CAK),不仅调控细胞周期进程,还参与转录起始和延伸,在癌症中异常高表达。研究团队通过遗传学和药理学方法深入阐述了靶向CDK7在HNSCC治疗中的潜力。
研究采用的主要关键技术方法包括:全基因组CRISPR-Cas9敲除筛选以识别HNSCC细胞系中的必需基因;体外细胞活力测定、集落形成实验、细胞周期和凋亡分析以验证CDK7抑制的表型;RNA测序(RNA-seq)进行转录组分析;以及利用细胞系来源异种移植(CDX)、患者来源异种移植(PDX)和患者来源类器官(PDO)模型进行体内药效评估。患者样本来源于阿斯图里亚斯亲王医院生物样本库。
全基因组功能性CRISPR-Cas9筛选揭示CDK7是HNSCC细胞的脆弱性靶点
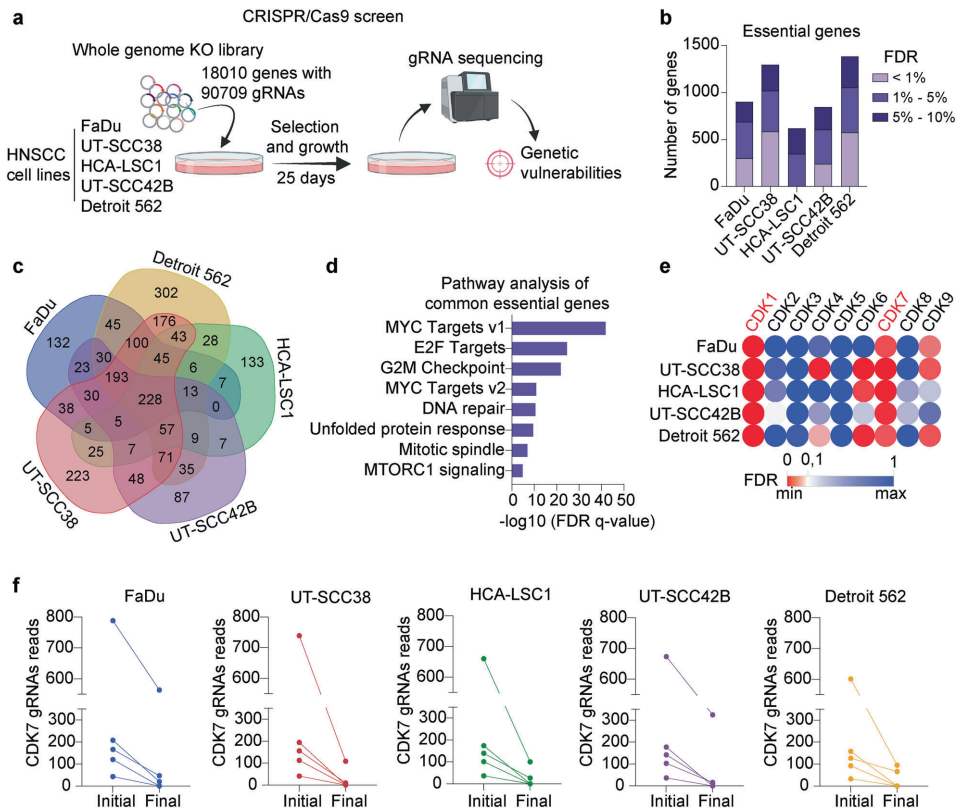
研究人员在五种HNSCC细胞系(FaDu, UT-SCC38, HCA-LSC1, UT-SCC42B, Detroit 562)中进行了CRISPR-Cas9敲除筛选,识别出228个在所有细胞系中共同必需的基因。通路分析显示这些基因显著富集于MYC和E2F靶点以及细胞周期检查点相关通路。在CDK家族中,CDK1和CDK7被确定为 across all cell lines 最关键的基因,鉴于CDK7抑制剂已有临床开发,研究选择CDK7进行深入探究。
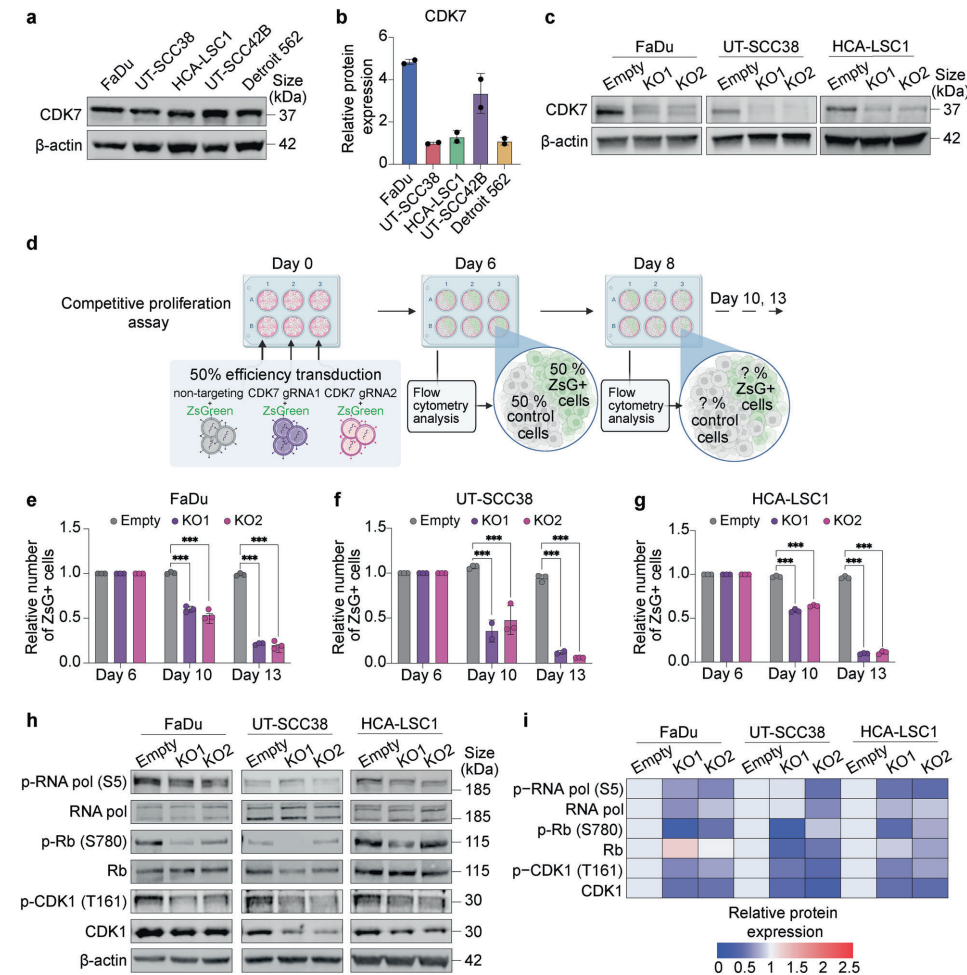
通过特异性gRNA敲除CDK7,研究人员证实CDK7蛋白水平显著降低,并且CDK7敲除细胞在竞争性共培养实验中生长劣势明显。救援实验进一步排除了脱靶效应,支持CDK7对HNSCC细胞存活的关键作用。机制上,CDK7缺失导致RNA聚合酶II羧基末端结构域(CTD)磷酸化(Ser5)、视网膜母细胞瘤蛋白(Rb)(Ser780)磷酸化以及CDK1 T-loop磷酸化(Thr161)水平降低,表明其通过影响关键下游效应器破坏细胞周期控制和转录。
两种选择性CDK7抑制剂YKL-5-124(共价抑制剂)和samuraciclib(口服ATP竞争性抑制剂)在HNSCC细胞系中均表现出强效抗增殖活性,IC50值显著低于CDK4/6抑制剂palbociclib。它们引起细胞周期S/G2/M期阻滞、凋亡诱导以及DNA损伤标志物γH2AX水平升高。蛋白质印迹分析证实了其对CDK7下游靶点的抑制。
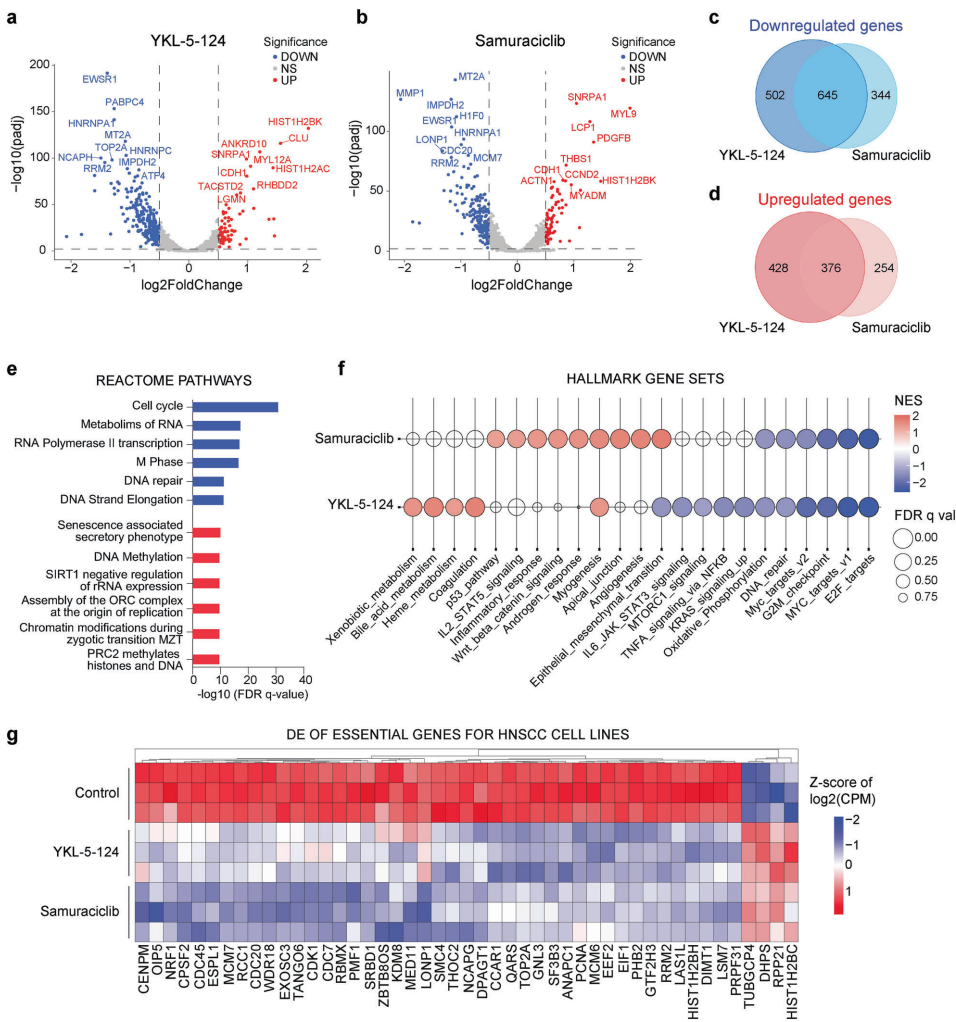
RNA测序分析显示,CDK7抑制导致大量基因表达改变,特别是细胞周期、DNA修复、MYC和E2F靶点等相关基因集的下调。值得注意的是,CRISPR筛选识别出的许多必需(且通常不可成药)基因也被CDK7抑制下调,提示CDK7抑制可广泛靶向HNSCC的遗传脆弱性。
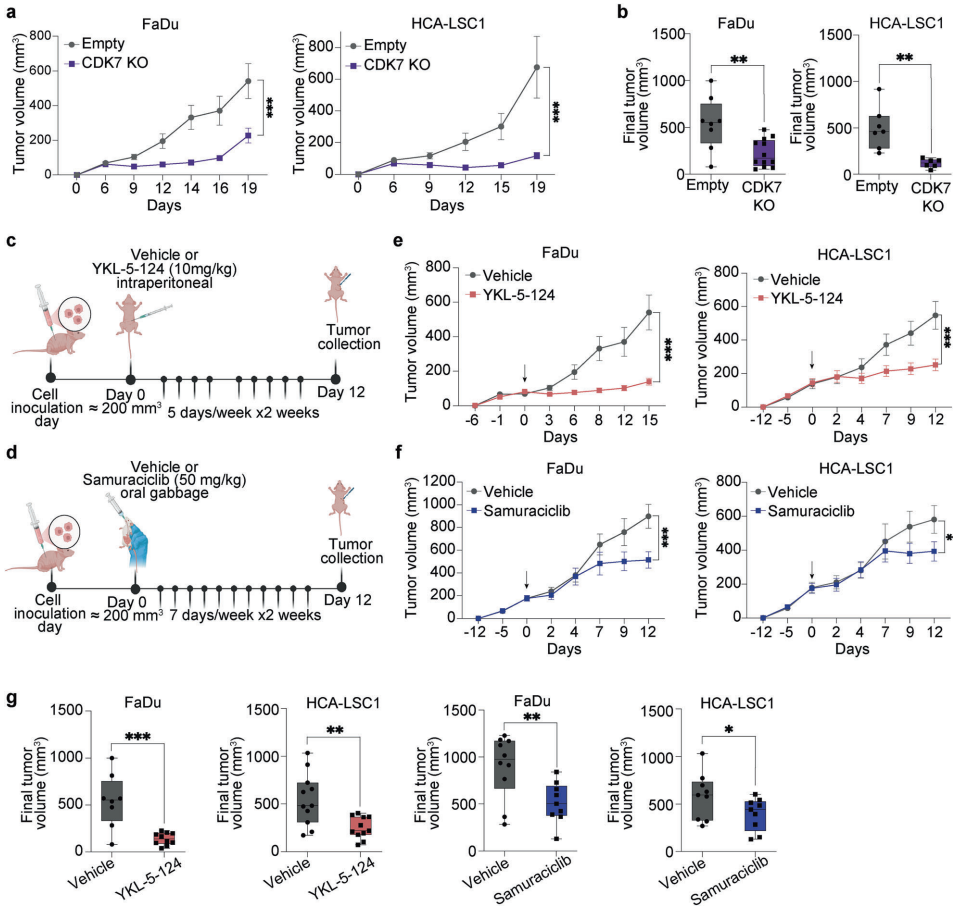
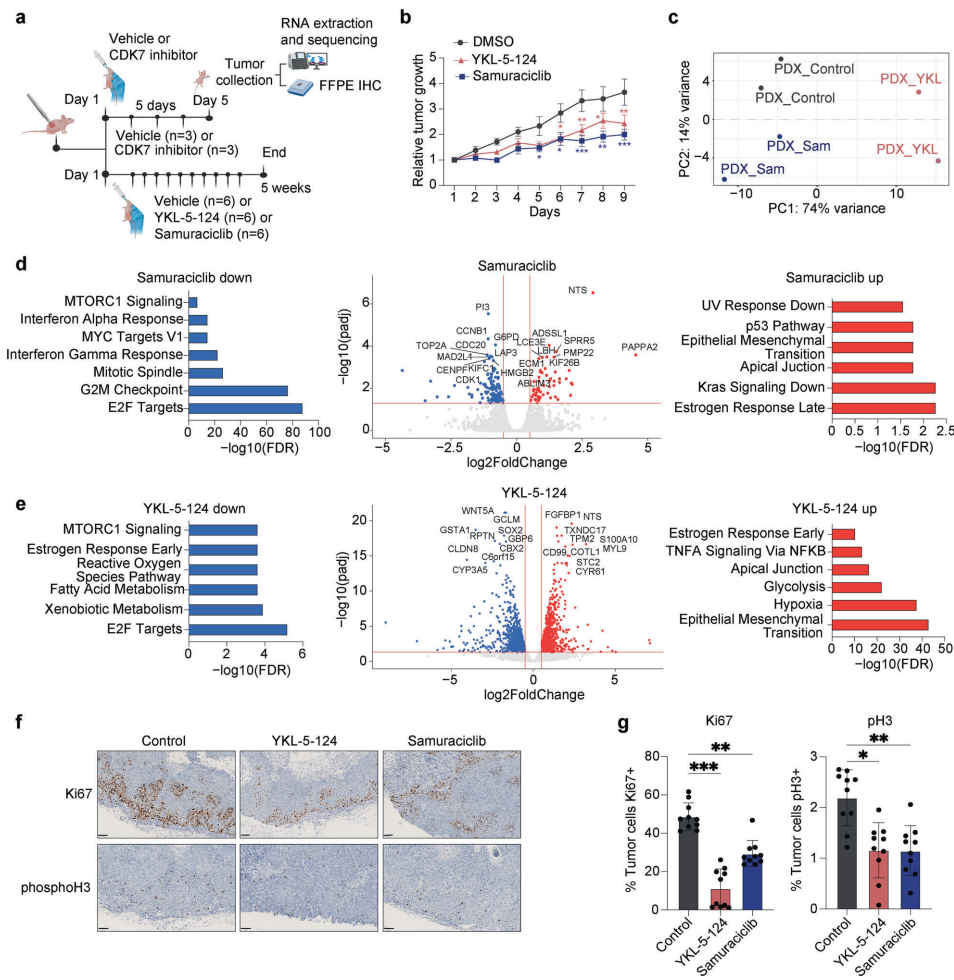
体内实验表明,CDK7基因敲除以及YKL-5-124和samuraciclib治疗均能显著抑制FaDu和HCA-LSC1细胞来源的异种移植瘤生长,且未观察到明显毒性。
选择性CDK7抑制对患者来源异种移植(PDX)的影响
在HNSCC PDX模型中,两种CDK7抑制剂均表现出显著的抗肿瘤活性,并下调增殖标志物Ki67和磷酸化组蛋白H3(pH3)。转录组分析再次确认了细胞周期相关通路的下调。
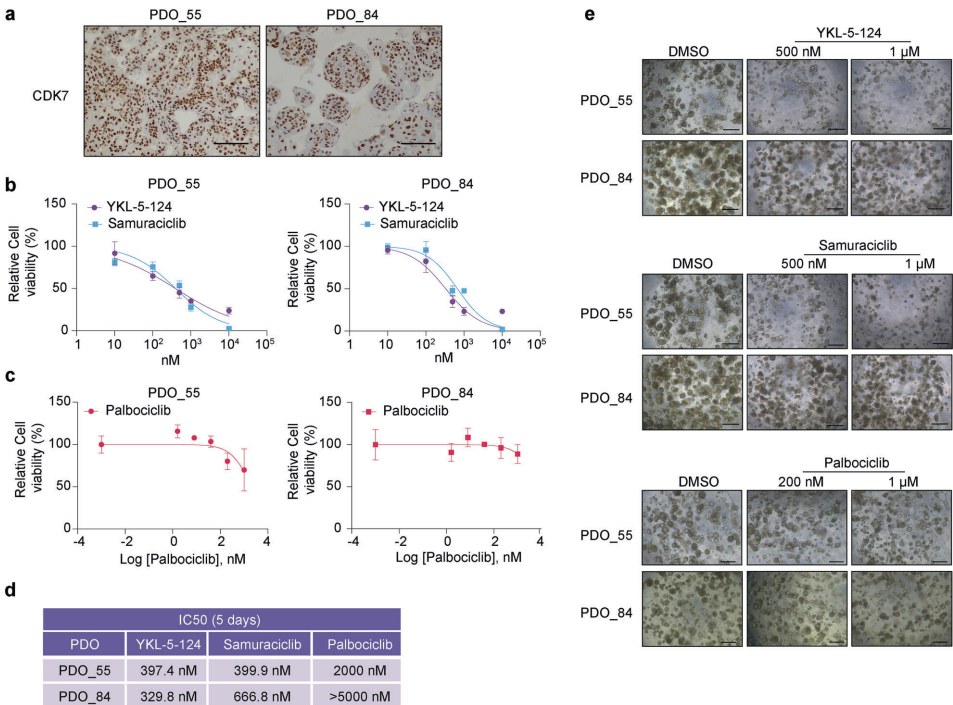
选择性CDK7抑制对患者来源类器官(PDO)的影响
CDK7抑制剂在两种HNSCC PDO模型中有效抑制了类器官生长,且效果优于palbociclib,甚至在palbociclib耐药的PDO中依然有效。此外,CDK7抑制还能减少癌症干细胞(CSC)富集的肿瘤球形成。
本研究通过系统性的功能基因组学筛选,确立了CDK7作为HNSCC的一个新的、关键的治疗靶点。遗传学和药理学抑制CDK7均能有效破坏细胞周期进程、诱导凋亡和DNA损伤,并通过广泛下调致癌转录程序发挥抗肿瘤作用。重要的是,CDK7抑制在包括PDO和PDX在内的多种临床前模型中均显示出强大的疗效和良好的安全性。该研究不仅为HNSCC提供了一种有前景的治疗新策略,也为克服现有CDK4/6抑制剂耐药性问题提供了潜在解决方案,有力地支持了CDK7选择性抑制剂进入HNSCC的临床评估。
 生物通微信公众号
生物通微信公众号
 生物通新浪微博
生物通新浪微博
今日动态 |
人才市场 |
新技术专栏 |
中国科学人 |
云展台 |
BioHot |
云讲堂直播 |
会展中心 |
特价专栏 |
技术快讯 |
免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号


 生物通微信公众号
生物通微信公众号