
-

����ͨ��
����ץס�����Ƽ�
����������
Daratumumab�������ǶȰ�ά�����Ƹ�����ֲ������϶�Թ���������MRDת���ʼ�����Ԥ��AURIGA�о��������
�����壺 �� �� С �� ʱ�䣺2025��10��08�� ��Դ��Blood Cancer Journal 11.6
�༭�Ƽ���
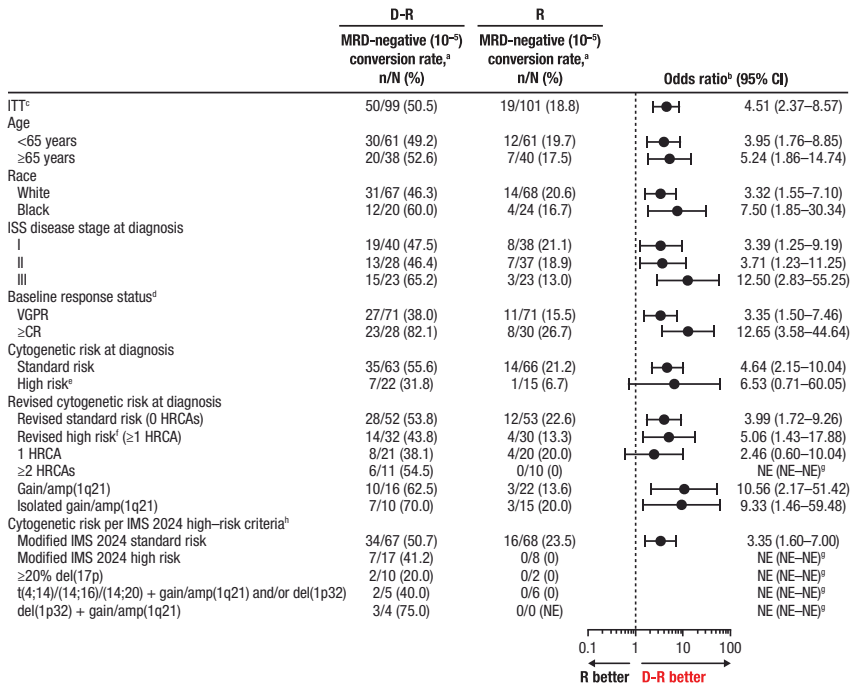
���������Ƽ�AURIGA�о�����������ɹ������о������ֲ��MRD���ԡ���CD38����δ�ù�������϶�Թ�������NDMM�����ߣ�̽����Daratumumab�������ǶȰ���D-R��ά�����ƶԱȵ������ǶȰ���R������Ч�밲ȫ�ԡ��о���ʾD-R�������������MRDת���ʣ�10-5�������ͼ�����չ���������մ�47%�����ڲ�ͬ���䡢���弰ϸ���Ŵ�ѧ���������о����ֳ�һ�»��棬Ϊ��Σ�����ṩ���µ����Ʋ��ԡ�

 ����ͨ�Ź��ں�
����ͨ�Ź��ں�
֪����ҵ��Ƹ