
-

生物通官微
陪你抓住生命科技
跳动的脉搏
富含生育三烯酚组分(TRF)对高脂血症动物模型血脂谱影响的系统评价与荟萃分析:机制探索与模型适用性评估
【字体: 大 中 小 】 时间:2025年10月02日 来源:Scientific Reports 3.9
编辑推荐:
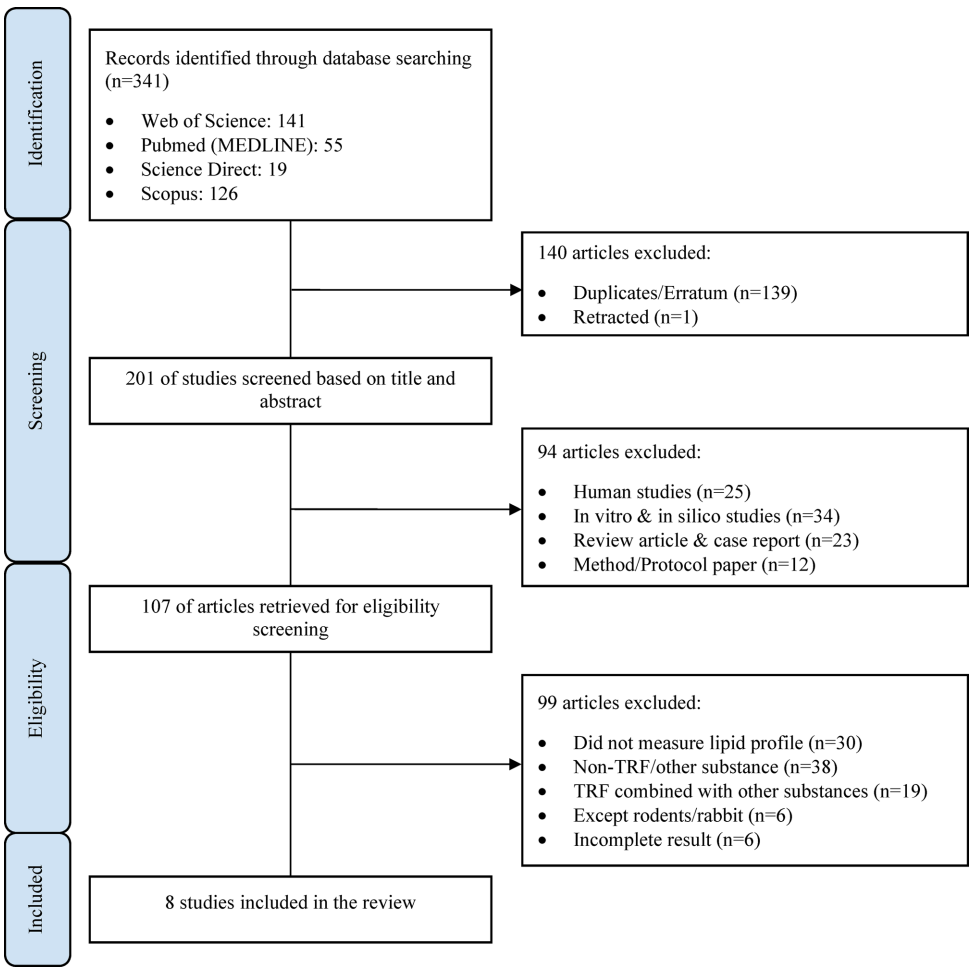
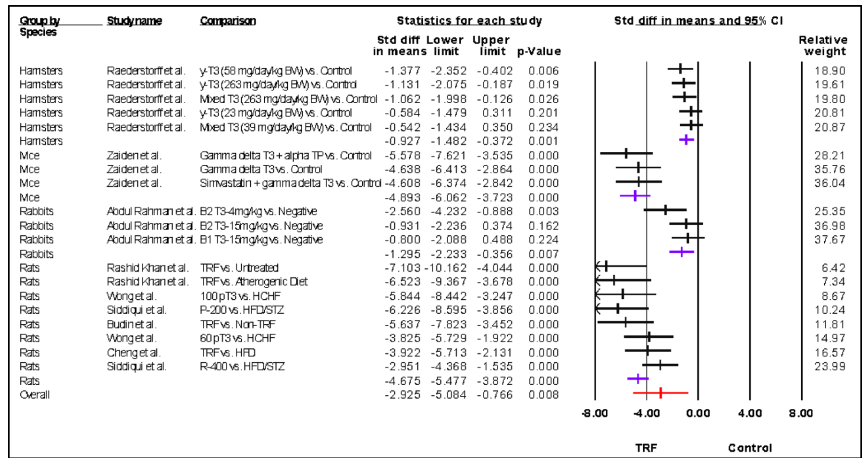
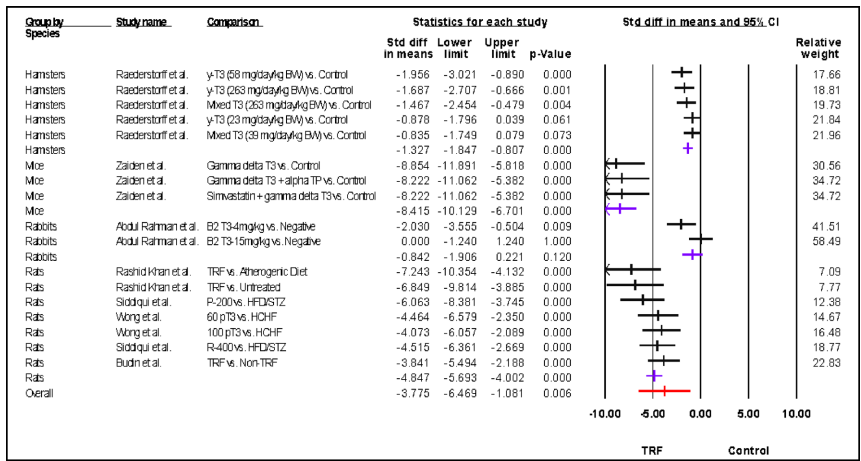
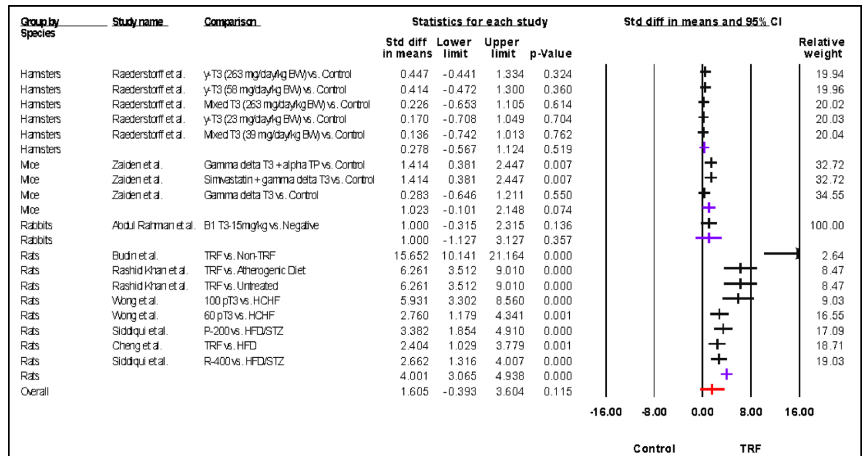
为解决高脂血症这一心血管疾病关键风险因素的治疗难题,研究人员系统评价了富含生育三烯酚组分(TRF)在动物模型中的降脂效应。通过荟萃分析8项研究,发现TRF显著降低总胆固醇(TC)(效应值=-4.675, p<0.0001)、低密度脂蛋白(LDL)(-4.847, p<0.0001)和甘油三酯(TG)(-4.736, p<0.0001),同时升高高密度脂蛋白(HDL)(4.001, p<0.0001)。研究还揭示兔类和仓鼠等模型对较低剂量TRF更敏感,为临床前研究模型选择提供了重要依据。


 生物通微信公众号
生物通微信公众号
知名企业招聘