
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Biomaterials | 台万一课题组在构建抗体片段偶联物方面取得新进展
【字体: 大 中 小 】 时间:2024年09月14日 来源:武汉大学药学院
编辑推荐:
武汉大学药学院研究生徐若琳为论文第一作者, 台万一教授为本论文通讯作者,武汉大学为论文唯一完成单位,于 2024 年 9 月 2 日,在线发表在 Elsevier 旗下知名国际期刊 Biomaterials 上
抗体偶联药物(Antibody-drug conjugate, ADC)由单克隆抗体(monoclonal antibody, mAb)、连接子以及毒性药物组成,它们通过结合单克隆抗体的特异性与高毒性药物的杀伤力,实现了对肿瘤细胞的精确打击,显著提升了肿瘤治疗的效率和安全性。虽然ADCs在临床应用中取得了显著成效,并有多种产品获得FDA批准,但它们仍面临一系列挑战,包括肿瘤组织穿透能力不足、体内长时间暴露、清除速度缓慢,以及由Fc片段介导的副作用等问题。基于抗体Fab片段的药物偶联物被认为是具有潜力的改进方案。Fab片段在保留与抗原特异性结合能力的同时,避免了Fc介导的副作用,在安全性、体内清除率及肿瘤组织渗透性方面展现出独特优势,有望提升抗体偶联药物的疗效和安全性。然而,目前制备Fab药物偶联物的方法仍面临诸多挑战,其中Fab蛋白的双链错配和不稳定性是主要难点。
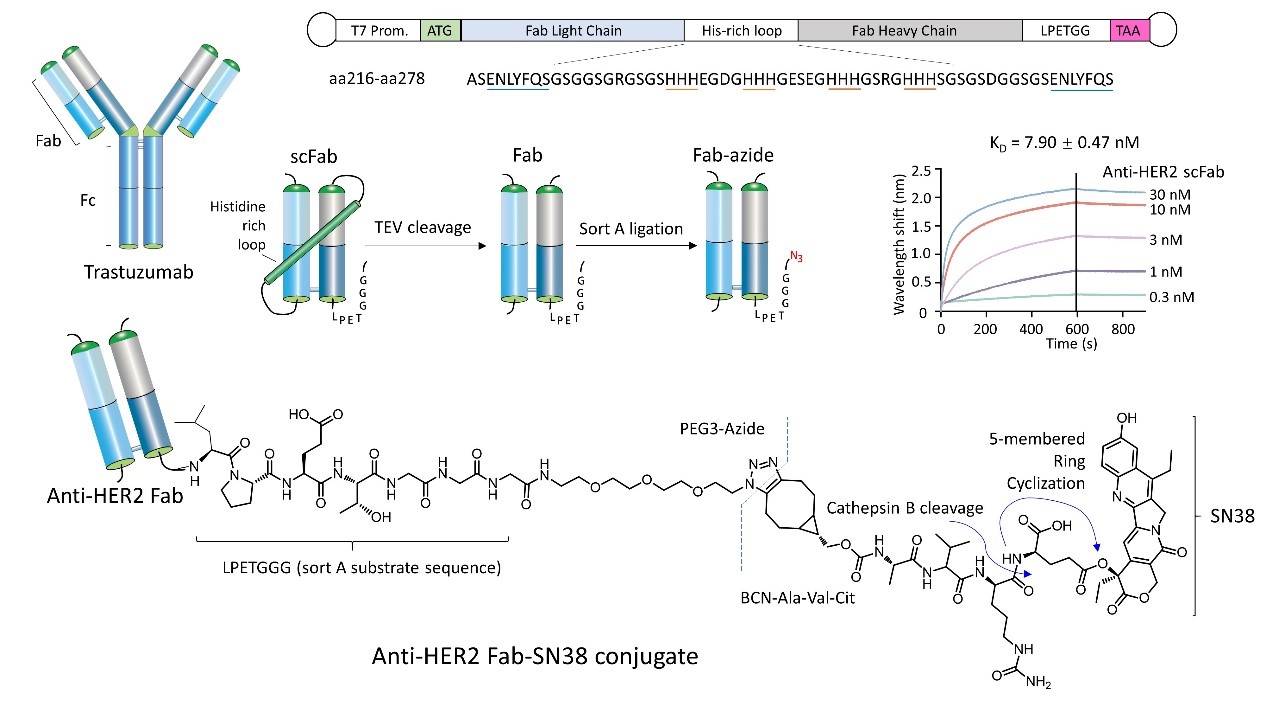
在本研究中,作者通过串联Fab双链得到一种scFab结构,证实了其在细菌细胞质中能高效表达。通过在细菌中应用经过优化的多肽连接子,成功以单链形式生产出高品质的曲妥珠单抗Fab片段。此外,我们利用分选酶A将抗肿瘤药物SN38连接至C端,从而制备出药抗比(DAR)为1的均质Fab偶联物。所得的HER2靶向Fab-SN38偶联物,在其特有的组织蛋白酶触发的环化释放机制的辅助下,在体外和体内均对HER2阳性肿瘤细胞显示出卓越的特异性和治疗效果。Fab-SN38偶联物不仅继承了传统抗体偶联药物的高度靶向性和抗肿瘤活性,而且其展现出的高剂量耐受性和渗透优势,也有效地弥补了现有ADCs的诸多局限性。本研究进一步证实了基于抗体片段的药物偶联物在靶向癌症治疗中的巨大潜力,并为Fab新型药物偶联物的开发提供了一种新思路。
武汉大学药学院研究生徐若琳为论文第一作者,台万一教授为本论文通讯作者,武汉大学为论文唯一完成单位,于2024年9月2日,在线发表在Elsevier旗下知名国际期刊Biomaterials上。
本项工作得到了国家重点研发计划和国家自然科学基金的支持。
文章链接:https://doi.org/10.1016/j.biomaterials.2024.122798