
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Theranostics丨北京大学基础医学院郑瑞茂团队揭示βAR-mTOR-Lipin1轴...
【字体: 大 中 小 】 时间:2024年08月29日 来源:北京大学基础医学院
编辑推荐:
北京大学郑瑞茂研究员团队研究发现了调控脂肪组织褐变的新机制,该研究以βAR-mTOR-lipin1 pathway mediates PKA-RIIβ deficiency-induced adipose browning为题,于2024年8月26日,在线发表于一线国际期刊Theranostics,为PKA调控脂肪组织褐变的分子基础提供了新的理论参考
白色脂肪组织褐变(browning of white adipose tissue, WAT browning)可加速脂肪分解代谢,增强机体产热量与能量消耗,降低体内脂肪蓄积量,继而优化脂代谢稳态。因此,激活白色脂肪组织褐变,是一种治疗肥胖及代谢性疾病的潜在新方法。脂肪组织褐变经中枢及外周途径共同调控,其机制仍待研究。
北京大学郑瑞茂研究员团队研究发现了调控脂肪组织褐变的新机制,该研究以βAR-mTOR-lipin1 pathway mediates PKA-RIIβ deficiency-induced adipose browning为题,于2024年8月26日,在线发表于一线国际期刊Theranostics,为PKA调控脂肪组织褐变的分子基础提供了新的理论参考。

该新发现,也是该团队2023年发表在Advanced Science论文的姊妹篇,两篇论文共同揭示了下丘脑背内侧核γ-氨基丁酸(GABA)能神经元RIIβ-PKA信号对脂肪组织褐变的中枢调控机制及外周分子机制,系统的阐述了PKA发挥脂代谢稳态调控作用的中枢特异脑神经结构与相关分子机理。
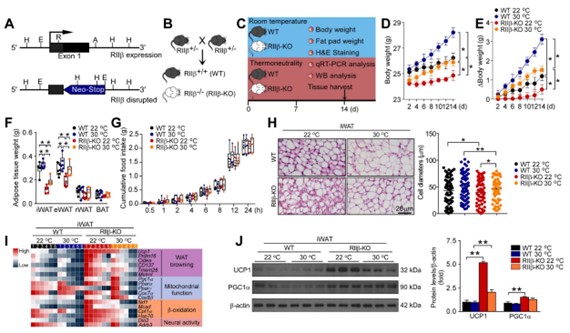
图1 PKA-RIIβ亚基敲除可引起热中性条件下白色脂肪褐变
(图源:Bingwei Wang, et al. Theranostics, 2024)
该团队的前期研究发现,白色脂肪组织褐变是PKA的RIIβ亚基敲除小鼠(RIIβ-KO)小鼠低体脂表型的主要贡献因素,下丘脑背内侧核GABA能神经元是PKA调控脂肪褐变的关键神经元。激活下丘脑背内侧核GABA能神经元,或抑制这些神经元PKA活性,均可诱导白色脂肪组织褐变,降低小鼠肥胖度(Adv Sci. 2023;10(5):e2205173.)。
在本研究,研究人员首先用热中性实验策略,去除环境温度(基础的交感神经兴奋)对褐变的影响,以评价在体情况下RIIβ敲除对诱导褐变的作用。该团队发现,即使在热中性条件,RIIβ-KO小鼠仍表现出褐变表型,其体重和脂肪组织重量仍然显著低于野生型(图1)。
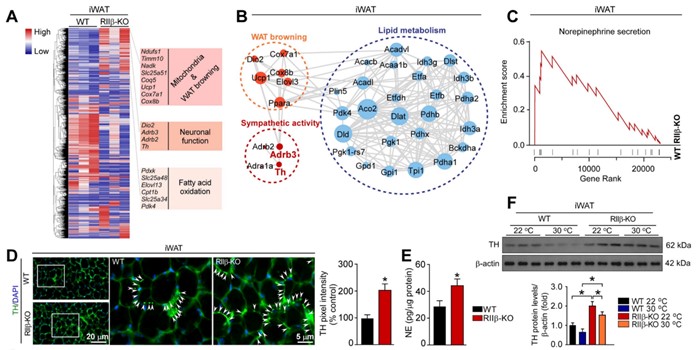
图2 PKA-RIIβ亚基敲除可增强脂肪组织内交感神经活性
(图源:Bingwei Wang, et al. Theranostics, 2024)
该团队进一步评估了交感神经活性以及脂肪细胞主要交感神经递质(去甲肾上腺素)β受体信号强度的标志性分子在RIIβ-KO小鼠腹股沟脂肪组织(iWAT)的表达水平。研究发现,交感神经标记物TH以及β受体ADRB3表达水平在RIIβ-KO均升高。GSEA分析表明,RIIβ-KO小鼠去甲肾上腺素分泌(regulation of norepinephrine secretion)信号通路增强。这些结果表明RIIB-KO小鼠脂肪组织内的交感神经呈高度激活状态(图2)。
为进一步验证RIIβ-KO褐变是否依赖于β3信号,该研究团队通过基因小鼠杂交策略,得到Adrb3和RIIβ双敲除小鼠(DKO)。敲除RIIβ-KO小鼠的β3受体,可恢复RIIβ-KO小鼠的褐变以及消瘦表型,而不改变摄食。用化学微量注射法去交感神经支配,亦显著抑制RIIβ-KO小鼠褐变水平,并削弱其抵抗高脂饮食诱导脂肪组织褐变的能力。
借助于转录组测序分析技术,该团队发现mTOR和Lipin1可能是RIIβ-KO小鼠褐变的关键脂肪组织内介导因子。mTORC1可经磷酸化Lipin1 S106和S472位点,抑制Lipin1核转移,从而促进脂肪酸和胆固醇合成基因SREBP1表达。然而,mTOR、Lipin1与褐变的关系,尚不明确。为了确认mTOR与Lipin1是否介导RIIβ-KO小鼠交感神经激活诱导的脂肪组织褐变,该团队利用Cre-LoxP再表达系统,在体情况下特异性抑制mTOR与Lipin1与在iWAT内表达,以评估这两个靶点对脂肪组织内交感神经激活情况下对褐变的介导作用。与对照组相比,当敲低RIIβ-KO小鼠iWAT的mTOR和Lipin1,可导致其体重与脂肪垫重量增加,褐变水平降低。该结果证实,交感神经通过mTOR-Lipin1介导白色脂肪组织褐变。
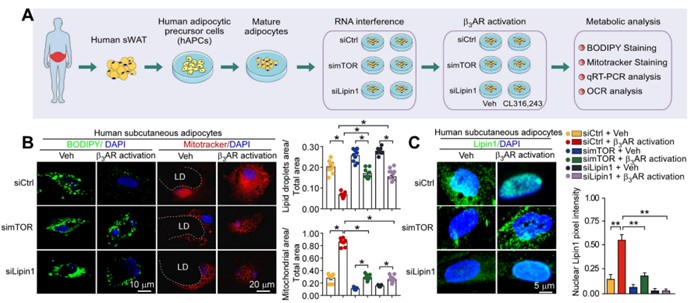
图3 mTOR-Lipin1轴介导人类脂肪脂肪细胞褐变相关代谢过程
(图源:Bingwei Wang, et al. Theranostics, 2024)
利用人类原代脂肪细胞、结合药理学及基因工程方法(基因敲低技术),研究人员检测β3AR特异性激动剂是否作用于人类脂肪细胞对褐变相关指标。结果显示,该激动剂促进mTOR、Lipin1及UCP1、Prdm16、PGC1α、CD137等褐变、脂解与线粒体氧化相关基因表达;而敲低mTOR和Lipin1则削弱其诱导褐变相关指标变化的能力,说明在人类脂肪细胞,βAR信号诱导脂解依赖于Lipin1和mTOR(图3)。
通过人类临床相关数据、以及公共医学转录组测序大数据、进行人类医学数据挖掘分析,该团队发现脂肪组织内mTOR和Lipin1表达水平与体重指数(BMI)呈负相关,并与Adrb3,Cidea,Pparα及Cox7α呈显著正相关,证实了mTOR和Lipin1与人类肥胖及减肥防治的潜在重要关联。
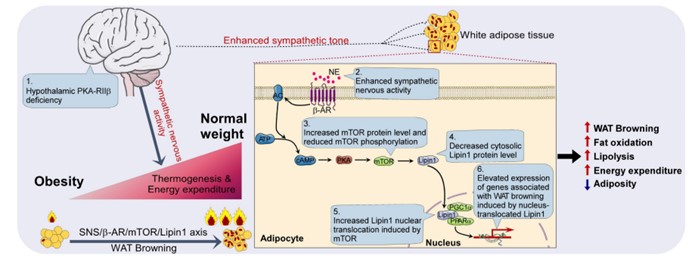
图4 SNS/βAR/mTOR/Lipin1轴介导白色脂肪脂肪细胞褐变发挥减肥作用的机理
(图源:Bingwei Wang, et al. Theranostics, 2024)
综上,该研究发现脂肪细胞βAR-mTOR-Lipin1轴介导交感神经兴奋引起的脂肪组织褐变,为机体能量平衡及代谢稳态调控机制,及肥胖及相关代谢性疾病的预防和治疗提供了新思路和新参考(图4)。
北京大学基础医学院王炳蔚博士及北京大学人民医院胡志平副教授为该论文第一作者,北京大学郑瑞茂研究员为通讯作者。该研究是在人体解剖与组织胚胎学系、北京大学神经科学研究所、教育部神经科学重点实验室、国家卫生健康委员会神经科学重点实验室平台上完成的,同时也得到国家自然科学基金、北京市自然科学基金、中国博士后科学基金、北京生命科技研究院重点项目、北京大学科研启动基金的等资金支持。
原文链接:https://www.thno.org/v14p5316.htm