
-

生物通官微
陪你抓住生命科技
跳动的脉搏
化学学院陈鹏、樊新元团队开发生物正交光催化的细胞互作定量标记技术CAT-Cell
【字体: 大 中 小 】 时间:2024年07月21日 来源:北京大学新闻网
编辑推荐:
CAT-Cell技术的出现,标志着生物正交光催化邻近标记体系从胞内到胞膜、再到胞际的以细胞为基–单元的生物空间全覆盖,实现了生命体系中不同空间尺度的时空标记与原位解析,充分体现了生物正交光催化这类新型策略的潜力和优势。
肿瘤的发生发展与复杂的细胞-细胞相互作用(cell-cell interactions,CCIs)密切相关。有效的抗肿瘤细胞免疫取决于肿瘤与细胞毒性免疫细胞,特别是细胞毒性T细胞之间的特异性相互作用。这些相互作用直接影响肿瘤的抑制和根除,因此,研究这些状态特异的细胞互作对表征免疫反应和指导免疫治疗应用至关重要。但由于这类相互作用高度动态、强度复杂多样并且受到肿瘤特有的免疫逃逸机制的影响,使得在活细胞背景下直接定量检测他们十分具有挑战性。近期,邻近标记策略被逐渐应用于细胞互作表征领域,其利用原位标记,集检测、分离和下游分析于一体,具有独特的优势。部分基于生物酶或是化学分子的邻近标记策略已在检测特定CCIs方面有了进展。但是这些方法的应用受限于基因层面操作、复杂的偶联物的合成、额外的细胞刺激损伤或是专职抗原提呈细胞相关的应用范围。由于肿瘤-免疫细胞互作的特殊性和复杂性,新的邻近标记策略亟待发展。
北京大学化学与分子工程学院陈鹏和樊新元课题组前期利用光催化反应的特点和优势,提出开发生物正交光催化反应,并基于这类新型反应进行了生物体系中蛋白质邻近标记的系统研究。例如,他们基于光催化产生亚甲基醌标记探针的反应,分别开发了靶向细胞内线粒体的CAT-Prox技术(J. Am. Chem. Soc. 2021, 18714),靶向胞膜的CAT-Ex技术(Chem. 2022,2179)。同时,他们积极探索生物正交光催化的应用边界,分别从标记靶标拓展(PhotoCAX技术,Angew. Chem. Int. Ed. 2022, e202202008)、光源波长优化(CAT-NIR技术,Angew. Chem. Int. Ed. 2023,e202310920)、标记探针迭代(CAT-S技术,Nat. Commun.2024, 2712)等多个方面开展了系统性的探索与研究,充分展示了这类新型化学反应在生命科学研究中的应用和价值。
近日,针对上述CCIs研究面临的问题,他们利用化学改造调控亚甲基醌探针的标记半径使其适用于细胞间的化学标记,进而开发了靶向胞际的CAT-Cell技术。该研究以“Bioorthogonal quinone methide decaging enables live-cell quantification of tumor-specific immune interactions”为题发表在近期上线的JACS期刊(J. Am. Chem. Soc.2024, DOI: 10.1021/jacs.4c02052)。CAT-Cell技术利用铱(III)配合物光催化剂和叠氮苯基PAB保护的亚甲基醌探针,其具有灵敏、通用、无创和灵活的化学调控性等优势,实现了在细胞系样品和原代组织样品中肿瘤-免疫细胞的活细胞互作标记和定量表征,证明了该策略于原代样品中解码肿瘤细胞与免疫细胞之间多种相互作用状态以及解析肿瘤微环境中浸润性淋巴细胞组成的巨大潜力(图1)。CAT-Cell技术的出现,标志着生物正交光催化邻近标记体系从胞内到胞膜、再到胞际的以细胞为基–单元的生物空间全覆盖,实现了生命体系中不同空间尺度的时空标记与原位解析,充分体现了生物正交光催化这类新型策略的潜力和优势。
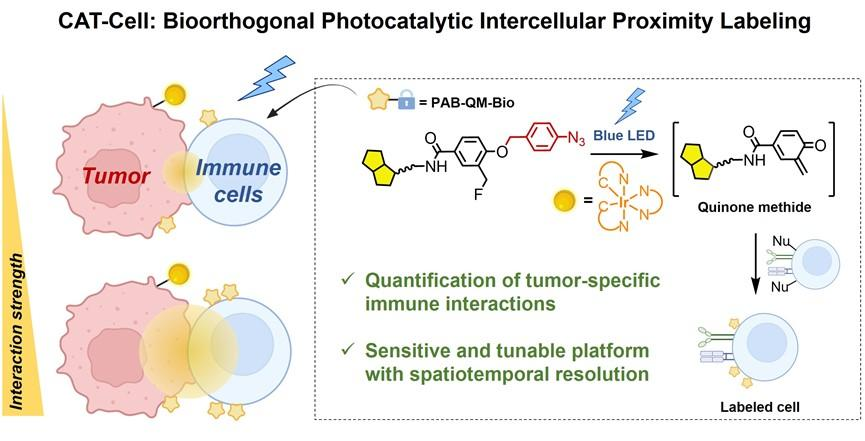
图1. 基于生物正交光催化的细胞间相互作用标记方法(CAT-Cell)示意图
首先,作者合理设计和优化了亚甲基醌探针的结构,通过调整探针中间体的活性和扩散半径,使其适配于细胞间标记的环境与空间距离。之后,他们分别在小分子、蛋白质层面对该标记反应进行表征,并在CD40-CD40L介导的HEK293T细胞互作体系中进行了细胞间标记的验证。此外,作者们还将CAT-Cell策略与抗体靶向平台相结合,通过制备纳米抗体—光催化剂偶联物成功实现了特定肿瘤细胞的互作细胞鉴定与分析,展示了该策略应用于多种场景的潜力(图2)。
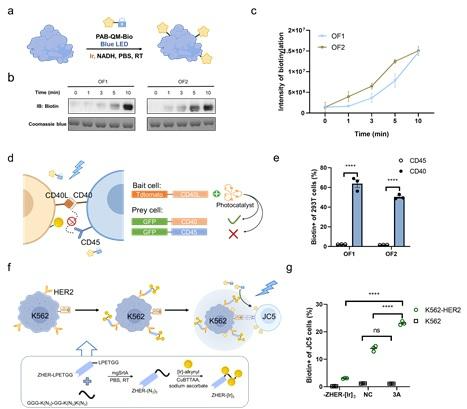
图2. CAT-Cell策略在蛋白质层面、互作细胞体系及串联抗体靶向系统中的标记效率
进一步,他们又拓展了CAT-Cell策略在pMHC-TCR互作体系以及原代样品中的应用。在肿瘤微环境中存在多种肿瘤—免疫细胞相互作用,其中pMHC-TCR介导的细胞间相互作用对研究杀伤性免疫细胞特别是抗原特异性T细胞对肿瘤细胞的识别具有重要意义。然而,由于TCR具有高度多样性和亲和力低的特点,解析pMHC-TCR介导的互作细胞信息十分具有挑战。作者们成功将CAT-Cell策略用于pMHC-TCR互作体系中,证明了该方法的高效性、灵敏性、特异性和定量性,证明了该策略综合反映细胞互作强度以及免疫细胞响应状态的能力。之后,他们也成功将CAT-Cell应用于表征肿瘤组织中浸润性的CD8+ T细胞对肿瘤细胞的特异性识别情况,并灵敏定量地反映了两者间相互作用的强度和CD8+ T细胞的抗肿瘤活性。此外,CAT-Cell策略还成功在小鼠原代脾脏组织中鉴定了重要的固有免疫细胞-自然杀伤细胞对肿瘤细胞的识别情况,证明了该生物正交光催化策略对多种细胞互作表征的灵敏性和普适性(图3)。
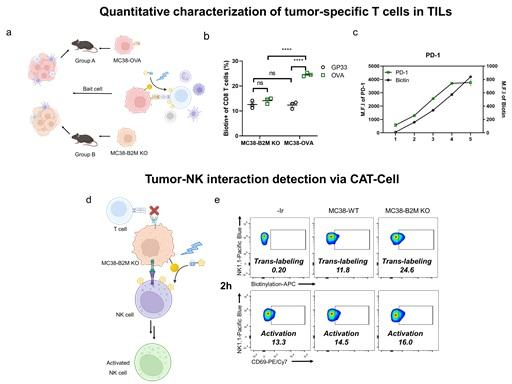
图3. CAT-Cell技术用于肿瘤-T细胞互作的定量表征
总而言之,该研究利用亚甲基醌类探针反应底物的广泛性、化学可控性和生物相容性,结合具有时空分辨率的光催化生物正交剪切反应,发展了表征细胞间相互作用的CAT-Cell策略。该策略高效、灵敏、通用、温和且无需基因操作,可以帮助研究者们在没有预先了解介导细胞互作的分子信息的情况下,对多种细胞—细胞相互作用进行分析,为研究肿瘤细胞特异性识别进而深入解析免疫应答机制提供了有力工具。同时,该策略进一步将生物正交光催化这类新型化学生物学技术从胞内和胞膜拓展到胞际空间,充分体现了新型技术在生命科学研究中的巨大潜力和优势。
樊新元和陈鹏为该文的通讯作者,博士研究生张妍与博士后刘士博与为该文的共同第一作者。该研究工作得到了中国科学技术部、国家自然科学基金委员会、北京市科学技术委员会、新基石基金会和北京分子科学国家研究中心等项目资金的支持。