
-

ЩњЮяЭЈЙйЮЂ
ХуФузЅзЁЩњУќПЦММ
ЬјЖЏЕФТіВЋ
ЩњУќПЦбЇбЇдКЖХХєПЮЬтзщЗЂЯжгЩDGCR8/FLII/JUNНщЕМЕФЫВЪБзЊТММЄЛюЪТМўЕїПизХДВЦкХпЬЅЕФаЮЬЌзЊБф
ЁОзжЬхЃК Дѓ жа аЁ ЁП ЪБМфЃК2024Фъ07дТ12Ше РДдДЃКББОЉДѓбЇаТЮХЭј
БрМЭЦМіЃК
ЁЁЁЁдкБОбаОПжаЃЌбаОПепдЫгУna?ve-poised-formative/PrimedЕШИЩЯИАћФЃаЭЃЌНсКЯЪЕбщЪвЯШЧАдкmiRNAЕїПиЗНУцЕФбаОПЛљДЁЃЌНтЪЭСЫЧ§ЖЏзХДВЦкХпЬЅаЮзДНЈГЩЕФЗжзгЧ§ЖЏСІЁЃ
дкдчЦкХпЬЅЗЂг§Й§ГЬжаЃЌХпЬЅзХДВЪЧвЛИіМЋЮЊЙиМќЕФЩњЮябЇЪТМўЁЃЦфМфХпЬЅжВШыФИЬхзгЙЌЃЌНЈСЂФИЬЅНЛСїНчУцЃЌетЪЧКѓајЗЂг§ЕФЛљДЁЁЃШЛЖјетвЛЙ§ГЬГфТњЗчЯеЃЌСйДВЩЯГЃГЃГіЯжвђзХДВЪЇАмЕМжТЕФЩњг§ЮЪЬтЁЃгЩгкИУЙ§ГЬМЋЮЊЫВЪБКЭЖЏЬЌЃЌХпЬЅзХДВЗНУцЕФбаОПШдЪЧвЛИіЁАКкЯЛзгЁБЁЃ
miRNAЪЧецКЫЩњЮяжаБЃЪиЕФзЊТМКѓЕїПиЛњжЦЃЌВЂдкзХДВЙ§ГЬжаЦ№ЕНживЊзїгУЁЃDGCR8ЪЧmiRNAКЯГЩЭЈТЗЕФКЫаФЕААзЃЌЫќгыDROSHAвЛЦ№зщГЩMicroprocessorИДКЯЬхЃЌЧаИюpri-miRNAЩЯЕФОЅЛЗНсЙЙаЮГЩpre-miRNAЃЌpre-miRNAдйНјвЛВНБЛМгЙЄЮЊГЩЪьЕФmiRNAЁЃ1 DCGR8ЧУГ§КѓЃЌХпЬЅЮоЗЈЗЂг§жСзХДВКѓНзЖЮЃЌАЕЪОзХDGCR8дкзХДВЙ§ГЬжаЦ№ЕНживЊзїгУЃЌШЛЖјИУжТЫРБэаЭШДВЛФмЭъШЋгУmiRNAЕФШБЯнРДНтЪЭЁЃ2,3
гыЩаВЛЧхГўЕФзХДВЦкЙ§ГЬЯрБШЃЌШЫУЧЖдгкзХДВЧАХпЬЅКЭзХДВКѓЕФХпЬЅвбгаЙуЗКЕФбаОПЃЌетжївЊЕУвцгкЬхЭтИЩЯИАћФЃаЭЕФНЈСЂЁЃгЩзХДВЧАХпЬЅЗжРыЕУЕНЕФИЩЯИАћБЛГЦЮЊna?ve mESCsЃЈаЁЪѓХпЬЅИЩЯИАћЃЉЃЌЖјзХДВКѓХпЬЅЗжРыЕУЕНЕФИЩЯИАћБЛГЦЮЊFormative/Primed mESCsЃЌетМИжжЯИАћвбБЛЙуЗКгІгУИїжжЗЂг§ЮЪЬтЕФбаОПЁЃ4,5 ББОЉДѓбЇЩњУќПЦбЇбЇдК/ББДѓ-ЧхЛЊЩњУќПЦбЇСЊКЯжааФ/ББОЉДѓбЇКЫЬЧКЫЫсББОЉбаОПжааФЕФЖХХєНЬЪкПЮЬтзщдк2018ФъВЖзНЕНСЫвЛжжНщгкnaiveКЭFormative/primedЖрФмадЕФжаМфЬЌЖрФмадИЩЯИАћЃЌГЦЮЊPoised mESCsЁЃ6,7 ИУзДЬЌДњБэСЫДІгкзХДВЦкЕФХпЬЅЃЌЧвгЩвЛзщЬивьЕФmiRNAЫљЕїПиЁЃ
2024Фъ7дТ1ШеЃЌЖХХєПЮЬтзщдкMolecular cellдгжОдкЯпЗЂБэСЫЬтЮЊЁАA transient transcriptional activation governs unpolarized-to-polarized morphogenesis during embryo implantationЁБЕФбаОПТлЮФЁЃдкБОбаОПжаЃЌбаОПепдЫгУna?ve-poised-formative/PrimedЕШИЩЯИАћФЃаЭЃЌНсКЯЪЕбщЪвЯШЧАдкmiRNAЕїПиЗНУцЕФбаОПЛљДЁЃЌНтЪЭСЫЧ§ЖЏзХДВЦкХпЬЅаЮзДНЈГЩЕФЗжзгЧ§ЖЏСІЃЌжївЊФкШнИХРЈШчЯТЃК
1. DGCR8зїЮЊmiRNAКЯГЩЭЈТЗЕФКЫаФЕААзЃЌПЩвдЗЂЛгВЛвРРЕгкmiRNAЕФзЊТМвжжЦЕФЗЧОЕфЙІФмЁЃдкna?ve mESCsжаЃЈДњБэзХДВЧАХпЬЅЃЉЃЌDGCR8ПЩвдНсКЯЮЛгкmRNAЩЯЖЬЕФОЅЛЗНсЙЙЃЌеаФМВЂИєРызЊТММЄЛюзгFLIIЃЌвжжЦзЊТМНјааЁЃдкPoised mESCsжаЃЈДњБэзХДВжаХпЬЅЃЉЃЌERKЭЈТЗЫВЪБМЄЛюЃЌЪЙЕУFLIIЪмЕНСзЫсЛЏаоЪЮВЂгыDGCR8НтРыЃЌНјЖјгызЊТМвђзгJUNНсКЯВЂМЄЛюЯИАћЧЈвЦЛљвђЕФзЊТМЁЃзХДВКѓERKЭЈТЗбИЫйЪЇЛюЃЈFormative mESCsЃЉЃЌDGCR8жиаТНсКЯВЂвжжЦFLIIЁЃвђДЫDGCR8/FLII/JUNдкERKЭЈТЗЕФНщЕМЯТЃЌдкзХДВЦкЬивьЕиНщЕМСЫвЛИіЫВЪБзЊТММЄЛюЪТМўЕФЗЂЩњЃЈЭМ1ЃЉЁЃ
2. ИУзЊТММЄЛюЪТМўПижЦСЫХпЬЅзХДВЦкгЩЮоађзДЬЌЕНМЋЛЏзДЬЌЕФаЮЬЌзЊБфЃЌЧвИУЪТМўдкШЫКЭаЁЪѓЪЧБЃЪиЕФЃЈЭМ1ЃЉЁЃ
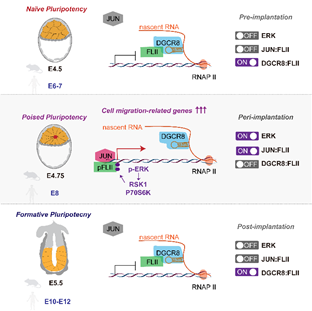
ЭМ1. дкзХДВЧАЃЈnaiveЃЉ-зХДВжаЃЈPoisedЃЉ-зХДВКѓЃЈFormativeЃЉЗЂг§Й§ГЬжаЃЌDGCR8/FLII/JUNдкERKЭЈТЗЕїПиЯТНщЕМЫВЪБзЊТММЄЛюЪТМўЕФЗЂЩњЃЌНјЖјЕїПизХДВЦкХпЬЅаЮЬЌзЊБф
БОбаОПОпЬхНсТлШчЯТЃК
вЛЁЂдкna?ve mESCsжаЃЌDGCR8ЭЈЙ§НсКЯmRNAЩЯЕФОЅЛЗНсЙЙЃЌеаФМВЂвжжЦзЊТММЄЛюзгFLIIЁЃ
ЛљгкЧАЦкЕФna?veаЁЪѓХпЬЅИЩЯИАћжаDGCR8ЛЅзїЕААзЪ§Он/Co-IP/Pull downЃЌзїепЗЂЯжЃЌDGCR8гызЊТММЄЛюзгFLIIДцдкжБНгЕФЕААзЯрЛЅзїгУЁЃШЛЖјFLIIВЂВЛВЮгыmiRNAКЯГЩЭЈТЗЁЃНјвЛВНЕФЭЈЙ§вХДЋбЇЪжЖЮЃЌзїепЗЂЯжЃКDGCR8КЭFLIIЙВЭЌдкзЊТМЫЎЦНЩЯПижЦСЫвЛзщВЛЪмmiRNAЕїПиЕФЛљвђЃЌИУРрЛљвђжївЊВЮгыЯИАћЧЈвЦЕШЛюЖЏЃЌГЦЮЊЗЧmiRNAАаЯђЛљвђЁЃDGCR8ПЩвдвжжЦЃЌЕЋFLIIПЩвдМЄЛюДЫРрЛљвђЕФзЊТМЁЃ
ЮЊСЫНјвЛВНбаОПDGCR8ШчКЮвжжЦетРрЛљвђЕФзЊТМЃЌдкna?veаЁЪѓХпЬЅИЩЯИАћжаЃЌзїепЭЈЙ§eCLIPЪЕбщМјЖЈСЫDGCR8/FLIIЕФRNAНсКЯАаЕуЃЌЭЌЪБдкeCLIPЪЕбщжаЛЙВєШыСЫS4UЃЌПЩвдЭЌЪБМјЖЈГіаТЩњЕФRNAЃЈnascent RNAЃЉЁЃзїепЗЂЯжDGCR8КЭFLIIЭЌЪБНсКЯСЫДѓСПЕФАаЛљвђЕФаТЩњmRNAЃЌЧвDGCR8НсКЯЧјгђЧуЯђгкаЮГЩОЅЛЗНсЙЙЁЃИУОЅЛЗНсЙЙЯджјЖЬгкpri-miRNAЩЯЕФОЅЛЗНсЙЙЃЌВЂВЛФмБЛDGCR8КЭDROSHAаЮГЩЕФИДКЯЬхНсКЯВЂЧаИюЁЃЭЈЙ§ЧУГ§DGCR8ЫљНсКЯЕФЮЛгкАаЛљвђmRNAЩЯЕФОЅЛЗНсЙЙЃЌАаЛљвђЕФзЊТМвжжЦзДЬЌБЛНтГ§ЁЃетжЄУїDGCR8ШЗЪЕЭЈЙ§НсКЯmRNAЩЯЕФОЅЛЗНсЙЙРДвжжЦзЊТМЁЃ
злЩЯЃЌетЫЕУїDGCR8вЛЗНУцКЭDROSHAНсКЯИКд№pri-miRNAЕФЧаИюЃЌвЛЗНУцНсКЯдкАаЛљвђmRNAЩЯЕФОЅЛЗНсЙЙЃЌеаФМВЂвжжЦзЊТММЄЛюзгFLIIЃЌДгЖјвжжЦзЊТМЕФНјааЃЈЭМ2ЃЉЁЃ
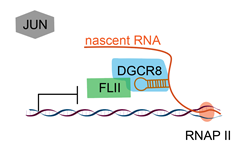
ЭМ2. дкna?veЃЈДњБэзХДВЧАХпЬЅЃЉаЁЪѓХпЬЅИЩЯИАћжаЃЌDGCR8НсКЯАаЛљвђmRNAЩЯЕФОЅЛЗНсЙЙЃЌеаФМВЂИєРызЊТММЄЛюзгFLIIЃЌвжжЦзЊТМНјаа
ЖўЁЂFLIIдкPoised mESCsЃЈДњБэзХДВЦкХпЬЅЃЉжагыDGCR8НтРыЃЌВЂгызЊТМвђзгJUNНсКЯЃЌМЄЛюЛљвђзЊТМЁЃ
ЭЈЙ§na?ve-poisedЃЈзХДВЧАЁњзХДВжаЃЉзЊБфЬхЯЕЃЌзїепЗЂЯжЃКFLIIдкжЛгадкPoisedЪБЦкЃЈзХДВжаЃЉВХОпгазЊТММЄЛюЛюадЃЌЖјдкna?veЪБЦкЃЈзХДВЧАЃЉдђУЛгаЁЃгыДЫЖдгІЕФЪЧFLIIдкPoisedЪБЦкНтГ§СЫгыDGCR8ЕФЛЅзїЃЌЭЌЪБвВВЛдйНсКЯАаЛљвђЕФmRNAЁЃетЫЕУїFLIIгыDGCR8ЕФНтРыЪЧFLIIОпгазЊТММЄЛюЛюадЕФЙиМќЬѕМўЁЃЭЈЙ§вЛЯЕСаЩњЛЏЪЕбщЃЌзїепжЄУїna?ve-poisedзЊБфЙ§ГЬжаЃЌERKЭЈТЗЫВЪБМЄЛюЃЌСзЫсЛЏFLIIЃЌЪЙЕУFLIIгыDGCR8ВЛдйНсКЯЁЃЭЌЪБСзЫсЛЏЕФFLIIЛсгызЊТМвђзгJUNЛЅзїдіЧПЃЈЭМ3ЃЉЁЃНјвЛВНЕФЭЈЙ§JUNЕФCUT&TagЪЕбщЗЂЯжЃЌJUNПЩвдЙуЗКНсКЯдкFLIIМЄЛюЕФАаЛљвђЩЯЃЌЧвJUNдкFliiЧУГ§жаЕФЯИАћжаЮоЗЈНсКЯАаЛљвђЁЃетЫЕУїJUNжЛгагыFLIIНсКЯВХФмЙЛНсКЯАаЛљвђЃЌМЄЛюЦфзЊТМЃЈЭМ3ЃЉЁЃ
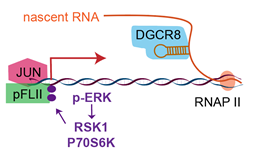
ЭМ3. дкPoisedЃЈДњБэзХДВжаЕФХпЬЅЃЉаЁЪѓХпЬЅИЩЯИАћжаЃЌERKМЄЛюгеЕМDGCR8гыFLIIЕФНтРыЃЌДйНјFLIIгыJUNаЮГЩаТЕФИДКЯЬхМЄЛюЛљвђзЊТМ
Ш§ЁЂPoised mESCsДњБэаЁЪѓКЭШЫЕФзХДВЦкХпЬЅЃЌетвЛЪБЦкЕФХпЬЅе§ОРњЮоађЕНМЋЛЏЕФаЮЬЌзЊБфЁЃ
ЭЈЙ§гыЬхФкХпЬЅЕФзЊТМзщБШНЯЃЌзїепЗЂЯжPoised ESCsЕФзЊТМзщгыаЁЪѓгыШЫЕФзХДВЦкХпЬЅзЊТМзщзюЮЊЯрЫЦЃЈаЁЪѓЮЊE4.75ЬьЃЌШЫЮЊE8ЬьЃЉЁЃетвЛЪБЦкХпЬЅЕФЩЯХпВуЯИАћж№НЅДгЮоађзДЬЌБфГЩУЕЙхЛЈЛЗбљЕФМЋЛЏНсЙЙЁЃЧвдкЬхЭтХрбјЕФзХДВЦкаЁЪѓХпЬЅжаЃЌФмЙЛЙлВьЕНJUNКЭЦфЫћОВЯЂЬЌЖрФмадБъМЧЛљвђЕФБэДяЃЌНјвЛВНжЄУїСЫвбгаНсТлЁЃЭЈЙ§ЬхЭтЕФФЃФтЮоађЕНМЋЛЏЕФаЮЬЌзЊБфЬхЯЕЃЌзїепЗЂЯжвжжЦИУзЊТММЄЛюЪТМўЖМЛсЕМжТЮоађЕНМЋЛЏНсЙЙаЮЬЌзЊБфЕФЪЇАмЁЃвђДЫЃЌБОЮФжаМјЖЈЕНЕФзЊТММЄЛюЪТМўЖдгІгкзХДВЦкХпЬЅЃЌЖјМЄЛюЛљвђвдЯИАћЧЈвЦЯрЙиЛљвђЮЊжїЃЌдђЖдгІзХетвЛЪБЦкЯИАћЕФаЮЬЌзЊБфЃЈЭМ4ЃЉЁЃ
злЩЯЃЌИУбаОПЗЂЯжСЫDGCR8ЖРСЂгкmiRNAжЎЭтЕФзЊТМвжжЦЙІФмЃЌВЂгыFLII/JUNвЛЦ№ЃЌдкERKЭЈТЗЕФПижЦЯТЃЌПижЦСЫзХДВЦкЕФЫВЪБзЊТММЄЛюЪТМўЃЌНјЖјПижЦетвЛЪБЦкЕФаЮЬЌНЈГЩЁЃ
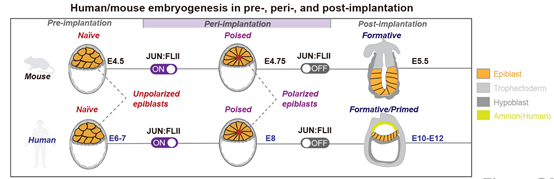
ЭМ4. Poised ESCsЃЈОВЯЂЬЌЖрФмадИЩЯИАћЃЉДњБэзХДВЦкЕФаЁЪѓ/ШЫХпЬЅЃЌЦфepiblastе§ОРњЮоађЕНМЋЛЏЕФаЮЬЌзЊБфЁЃБОЮФМјЖЈЕФзЊТММЄЛюЪТМўЖдгІгкетвЛаЮЬЌзЊБфЙ§ГЬ
ЖХХєЮЊИУТлЮФЕФЭЈбЖзїепЁЃББОЉДѓбЇЩњУќПЦбЇбЇдКВЉЪПКѓТРбЇъЭЁЂДогЂзЫЃЌЧАбиНЛВцбЇПЦбаОПдКВЉЪПКѓПзвњЗЩЮЊБОЮФЕФВЂСаЕквЛзїепЁЃББОЉДѓбЇВЉЪПБЯвЕЩњбюУєЁЂВЉЪПКѓЩъЛдЁЂВЉЪПКѓРюЪЋгъЁЂвбГіеОВЉЪПКѓЮЬНЈРђЃЌББОЉДѓбЇеХембаОПдБМАЦфВЉЪПЩњСЮЪіѓоЃЌжаЙњПЦбЇдКЖЏЮябаОПЫљЭѕ№ЉвубаОПдБМАЦфВЉЪПБЯвЕЩњАВГНШ№ЃЌЩНЖЋДѓбЇРюбобаОПдБЖдБОЮФгаживЊЙБЯзЁЃИУЯюЙЄзїЕУЕНСЫЙњМвжиЕубаЗЂМЦЛЎЃЌЙњМвздШЛПЦбЇЛљН№ЕФжЇГжЁЃ
ВЮПМЮФЯзЃК
1. DeVeale, B., Swindlehurst-Chan, J., and Blelloch, R. (2021). The roles of microRNAs in mouse development. Nat Rev Genet 22 , 307ЁЊ323. 10.1038/s41576-020-00309-5.
2. Greve, T.S., Judson, R.L., and Blelloch, R. (2013). microRNA control of mouse and human pluripotent stem cell behavior. Annu Rev Cell Dev Biol 29 , 213-239. 10.1146/annurev-cellbio-101512ЁЊ122343.
3. Wu, Q., Song, R., Ortogero, N., Zheng, H., Evanoff, R., Small, C.L., Griswold, M.D., Namekawa, S.H., Royo, H., Turner, J.M., and Yan, W. (2012). The RNase III enzyme DROSHA is essential for microRNA production and spermatogenesis. J Biol Chem 287 , 25173ЁЊ25190. 10.1074/jbc.M112.362053.
4. Kinoshita, M., Barber, M., Mansfield, W., Cui, Y., Spindlow, D., Stirparo, G.G., Dietmann, S., Nichols, J., and Smith, A. (2021). Capture of Mouse and Human Stem Cells with Features of Formative Pluripotency. Cell Stem Cell 28 , 2180. 10.1016/j.stem.2021.11.002.
5. Wang, X., Xiang, Y., Yu, Y., Wang, R., Zhang, Y., Xu, Q., Sun, H., Zhao, Z.A., Jiang, X., Wang, X., et al. (2021). Formative pluripotent stem cells show features of epiblast cells poised for gastrulation. Cell Res 31 , 526ЁЊ541. 10.1038/s41422-021-00477-x.
6. Du, P., Pirouz, M., Choi, J., Huebner, A.J., Clement, K., Meissner, A., Hochedlinger, K., and Gregory, R.I. (2018). An Intermediate Pluripotent State Controlled by MicroRNAs Is Required for the Naive-to-Primed Stem Cell Transition. Cell Stem Cell 22 , 851ЁЊ864 e855. 10.1016/j.stem.2018.04.021.
7. Du, P., Wang, L., Sliz, P., and Gregory, R.I. (2015). A Biogenesis Step Upstream of Microprocessor Controls miR-17ЁЋ92 Expression. Cell 162 , 885ЁЊ899. 10.1016/j.cell.2015.07.008.
 ЩњЮяЭЈЮЂаХЙЋжкКХ
ЩњЮяЭЈЮЂаХЙЋжкКХ
жЊУћЦѓвЕеаЦИ
НёШеЖЏЬЌ | ШЫВХЪаГЁ | аТММЪѕзЈРИ | жаЙњПЦбЇШЫ | дЦеЙЬЈ | BioHot | дЦНВЬУжБВЅ | ЛсеЙжааФ | ЬиМлзЈРИ | ММЪѕПьбЖ | УтЗбЪдгУ
АцШЈЫљга ЩњЮяЭЈ
Copyright© eBiotrade.com, All Rights Reserved
СЊЯЕаХЯфЃК
дСICPБИ09063491КХ