
-

生物通官微
陪你抓住生命科技
跳动的脉搏
季红斌组、陈洛南组和朱学良组合作发现EML4-ALK融合基因通过激活JAK-STAT通路介导肺腺鳞癌转分化及其耐药
【字体: 大 中 小 】 时间:2024年02月01日 来源:中国科学院生物化学与细胞生物学研究所
编辑推荐:
1月29日,国际学术期刊Journal of Experimental Medicine在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)季红斌研究组、陈洛南研究组、朱学良研究组与同济大学附属肺科医院任胜祥团队、暨南大学陈良研究组的合作研究成果:“EML4-ALK fusions drive lung adeno-to-squamous transition through JAK-STAT activation”
1月29日,国际学术期刊Journal of Experimental Medicine在线发表了中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)季红斌研究组、陈洛南研究组、朱学良研究组与同济大学附属肺科医院任胜祥团队、暨南大学陈良研究组的合作研究成果:“EML4-ALK fusions drive lung adeno-to-squamous transition through JAK-STAT activation”。该研究通过整合性分析小鼠模型和临床数据,发现EML4-ALK融合基因可以通过激活JAK-STAT信号通路来驱动肺腺鳞癌转分化,从而介导肺癌ALK靶向治疗的耐药。
肺癌是一类发病率高、可塑性强的恶性肿瘤,约0.7-11.4%的非小细胞肺癌在一个样本中同时包含腺癌和鳞癌两种组织病理学类型,临床上称之为肺腺鳞癌。研究表明肺腺鳞癌样本中的腺癌和鳞癌部分往往存在相同的基因突变,提示两种病理亚型之间存在着谱系转变。季红斌研究组长期致力于肺腺鳞癌转分化及其分子机制的研究。前期工作发现LKB1基因失活会导致肺腺鳞癌转分化(Ji et al., Nature 2007; Han et al., Nat Commun 2014)。肺腺癌在氧化应激压力过度累积下会发生向肺鳞癌的转分化(Li et al., Cancer Cell 2015)。Hippo通路成员YAP在腺鳞癌转分化过程中起着非常重要的开关作用(Gao et al., Nat Commun 2014)。动态网络标志物分析发现,Wnt通路在腺鳞癌转分化临界点的瞬时失活对于腺鳞癌转分化是非常重要的(Fang et al., STTT 2023)。大规模的临床肺腺鳞癌样本分析揭示了肺腺癌和肺鳞癌的谱系特异性转录因子及其靶基因调控网络之间存在的阴阳关系(Tang et al., NSR 2023)。最近的工作进一步发现肺腺鳞癌转分化与临床KRASG12C靶向药物Adagrasib的耐药密切相关,并提出KRT6A是一个新的指导临床Adagrasib 用药的分子标志物(Tong et al., bioRxiv 2023)。
随着近年来对肺癌靶向治疗的长期监测,临床上出现了越来越多的耐药伴随肺腺鳞癌转分化的病例。研究发现几乎所有转变的鳞癌都与腺癌具有相同的驱动基因,比如同样的EGFR突变或者ALK融合。病理学的转变使得癌症进程不可控,大大增加了肿瘤耐药的可能,为临床治疗造成很大困难。然而,目前对于这些肺癌驱动基因是否可以直接导致肺腺鳞癌转分化的发生还很不清楚。
在该项工作中,研究团队利用109例中国人肺腺鳞癌的全基因组和转录组测序数据发现,ALK融合事件在肺腺鳞癌中的频率显著高于腺癌,提示其可能是驱动腺鳞癌转分化的潜在分子事件。为了进一步探究ALK融合基因的功能,研究人员构建了EML4-ALK融合基因驱动的肺癌小鼠模型,并分析了超过1000例ALK阳性的临床肺癌样本。通过病理学和单细胞转录组整合性分析,研究人员发现EML4-ALK阳性的肺腺癌可以通过肺腺鳞癌转变成肺鳞癌;细胞谱系研究进一步发现,club细胞是EML4-ALK驱动的肺腺鳞癌转分化事件的主要起源细胞。利用类器官培养体系对肺腺鳞癌转分化过程进行了重构,研究人员还发现EML4-ALK在肿瘤细胞内会发生相分离,激活下游PI3K-AKT、MAPK和 JAK-STAT通路,而JAK-STAT通路是调控肺腺鳞转分化的关键信号通路。更重要的是,转变后的鳞癌和具有鳞癌特征基因表达的肺腺癌都表现出对ALK抑制剂的耐受性。临床样本的分析进一步验证了这一发现,与肺腺癌患者相比,接受ALK抑制剂治疗的鳞癌患者往往呈现出显著缩短的无进展生存期;复发患者的再活检样本也显示鳞癌生物学标志物的显著升高。进一步研究表明,在小鼠模型中联合使用 JAK1/2 抑制剂与 ALK 抑制剂可以有效克服肺腺鳞癌转分化介导的药物耐受。该工作为EML4-ALK阳性肺癌的临床治疗提供了新的思路和策略。
分子细胞卓越中心博士后秦榛、博士研究生岳美廷、博士后唐诗婕、孙鸿华和同济大学附属肺科医院吴凤英副教授为该论文的共同第一作者。分子细胞卓越中心季红斌研究员、陈洛南研究员、朱学良研究员及同济大学附属肺科医院任胜祥教授、暨南大学陈良研究员为该论文共同通讯作者。该研究得到国家重点研发计划、国家自然科学基金、中国科学院基础前沿科学研究计划、上海市自然科学基金等项目的资助,以及分子细胞卓越中心分子生物学技术平台、细胞分析技术平台、化学生物学技术平台和动物实验技术平台的帮助与支持。
文章链接:https://rupress.org/jem/article-abstract/221/3/e20232028/276527
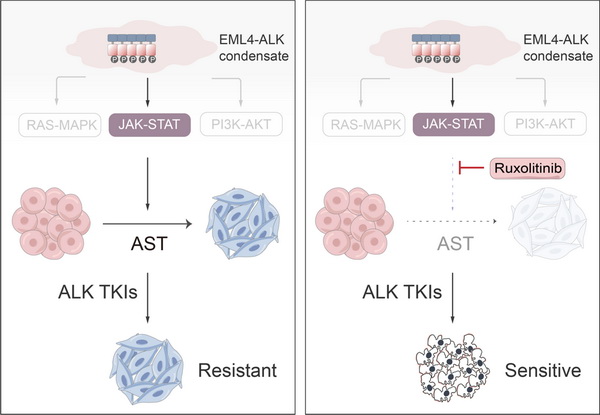
EML4-ALK 驱动肺腺鳞癌转分化及ALK抑制剂耐药的模式图