
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Nature Biomedical Engineering | 通过生物力学机制促进造血干细胞移植的新理论和新策略
【字体: 大 中 小 】 时间:2024年12月27日 来源:中国科学技术大学 | 生命科学与医学部
编辑推荐:
2024 年 12 月 23 日,中国科学技术大学生命科学与医学部、免疫应答与免疫治疗重点实验室倪芳团队与中国科学技术大学工程科学学院近代力学系姜洪源团队及中国科学技术大学生命科学与医学部程临钊 / 刘森泉团队合作,在 Nature Biomedical Engineering 在线发表题为“ Enhanced engraftment of human haematopoietic stem cells via mechanical remodelling mediated by the corticotropin-releasing hormone” 的研究论文,率先提出了基于生物力学机制促进 HSCT 的新理论和新策略,研究表明通过促肾上腺皮质激素释放激素( CRH )介导的机械重塑机制,可以显著促进人脐血 HSC 的归巢和植入
造血干细胞移植(HSCT)是治疗恶性血液病等重大疾病的有效方法,移植后的造血与免疫系统重建是治疗成功的关键。然而,植入延缓或失败仍是HSCT面临的主要挑战,尤其是在脐血移植中,由于单份脐血中造血干细胞(HSC)数量有限,植入延缓问题尤为突出。HSC归巢是HSCT成功的关键过程,除了生化因素的调控,HSC的生物力学特性,如粘附、迁移和变形能力,也在这一过程中发挥重要作用。然而,目前对于HSC归巢及植入过程中生物力学调节机制的了解仍然十分有限。
2024年12月23日,中国科学技术大学生命科学与医学部、免疫应答与免疫治疗重点实验室倪芳团队与中国科学技术大学工程科学学院近代力学系姜洪源团队及中国科学技术大学生命科学与医学部程临钊/刘森泉团队合作,在Nature Biomedical Engineering在线发表题为“Enhanced engraftment of human haematopoietic stem cells via mechanical remodelling mediated by the corticotropin-releasing hormone”的研究论文,率先提出了基于生物力学机制促进HSCT的新理论和新策略,研究表明通过促肾上腺皮质激素释放激素(CRH)介导的机械重塑机制,可以显著促进人脐血HSC的归巢和植入。
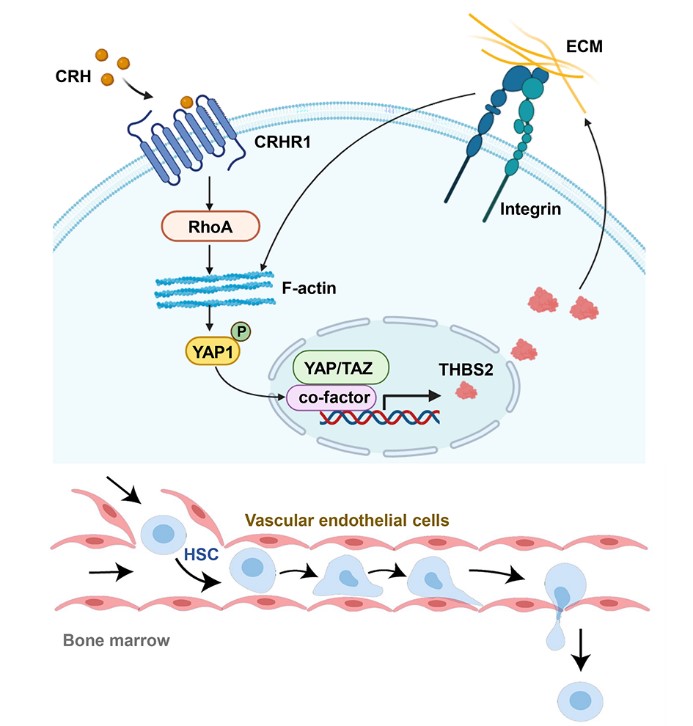
图1 CRH通过生物力学调剂机制促进造血干细胞归巢和植入
研究人员首先发现人类HSC表面表达CRH受体CRHR1,并通过细胞粘附、3D凝胶迁移以及微流控实验等验证了CRH通过该受体显著改变HSC的生物力学特性,增强了其粘附、迁移和主动变形能力。进一步的双光子活体成像和长期植入实验表明,CRH显著提升了HSC在免疫缺陷小鼠骨髓中的归巢和植入效率。
机制研究进一步揭示,CRH通过RhoA依赖的YAP核转位机制,促进HSC细胞外基质蛋白(尤其是THBS2)的表达。HSC产生并释放的THBS2与细胞表面整合素αvβ3结合,增强了HSC的粘附、运动和机械重塑能力。此外,THBS2通过与整合素αvβ3相互作用,促进F-actin聚合,进一步增强YAP的核转位,形成机械反馈回路,调控HSC的生物力学行为,并显著促进其归巢和植入(图1)。
综上,该研究揭示了CRH/CRHR1/RhoA/YAP/THBS2/αvβ3信号通路在HSC机械重塑及其归巢和植入中的重要作用,为干细胞生物力学研究提供了新的视角。该发现为优化HSCT、提升脐血移植效率提供了新思路,有望为恶性血液病等重大疾病的治疗带来新突破。
中国科学技术大学博士研究生吴明明、博士后杨皓翔、副研究员刘森泉为本文的共同第一作者,中国科学技术大学生命科学与医学部、免疫应答与免疫治疗重点实验室倪芳教授为最后通讯作者,中国科学技术大学近代力学系姜洪源教授和生命科学与医学部程临钊教授为本文的共同通讯作者。该研究还得到中国科学技术大学第一附属医院血液科朱小玉主任、妇产科周颖主任、蒋来医生、上海交通大学基础医学院郭滨教授的大力支持,该成果得到了科技部、基金委、中科院、中国科学技术大学等项目资助。
原文链接:https://www.nature.com/articles/s41551-024-01316-1
 生物通微信公众号
生物通微信公众号
知名企业招聘