
-

生物通官微
陪你抓住生命科技
跳动的脉搏
广州健康院揭示VL6-57轻链编码人群抗体促使新冠病毒奥密克戎变异株产生的分子机制
【字体: 大 中 小 】 时间:2024年12月19日 来源:中国科学院广州生物医药与健康研究院
编辑推荐:
近日,中国科学院广州生物医药与健康研究院(以下简称“广州健康院”)、广州医科大学和广州国家实验室等单位合作在Nature Communications上发表了题为“Antibodies utilizing VL6-57 light chains target a convergent cryptic epitope on SARS-CoV-2 spike protein and potentially drive the genesis of Omicron variants”的研究论文
近日,中国科学院广州生物医药与健康研究院(以下简称“广州健康院”)、广州医科大学和广州国家实验室等单位合作在Nature Communications上发表了题为“Antibodies utilizing VL6-57 light chains target a convergent cryptic epitope on SARS-CoV-2 spike protein and potentially drive the genesis of Omicron variants”的研究论文。该研究鉴定了一类由VL6-57轻链基因编码的人群共享抗体,揭示其介导的群体免疫压力驱动新冠病毒371-373-375位点抗原进化并潜在导致Omicron变异株产生的分子机制。
自新冠疫情爆发以来,新的变异株不断出现,病毒的刺突蛋白(S)也呈现明显的抗原漂移。Omicron BA.1变异株及其后续衍生株在S蛋白上携有30余个突变,其中S371F/L、S373P、S375F突变是这些变异株的特征突变。这3个位点的突变被证明影响S蛋白的功能,扰乱抗原呈递并导致Omicron变异株的鼻腔组织嗜性,但371-373-375位点突变的驱动因素尚不明确。
研究人员从新冠病毒野生株感染者中分离到6个靶向S蛋白受体结合域(RBD)的中和抗体,除R1-32外,以R1-26为代表的另外5个抗体的轻链均由VL6-57基因编码,且HCDR3含有相似的疏水性基序。研究发现,R1-26仅能结合并中和OmicronBA.1之前的变异株。结构分析显示,R1-26通过HCDR3的“LGPWV”疏水性基序和LCDR1的“NY”基序结合S蛋白371-373-375位点定义的隐藏表位,属于“4类抗体”(结合RBD内表面的一类抗体)。不同于大部分4类抗体,R1-26与ACE2存在竞争并能诱导S蛋白发生构象变化,从而抑制病毒入侵。
比对R1-26的结构,蛋白数据库(PDB)分析发现,近10个结构已解析的4类抗体的轻链均由VL6-57编码。这些VL6-57抗体通过相似的HCDR3疏水性基序和LCDR1的“NY”基序与RBD上371-373-375位点定义的趋同表位相互作用。冠状病毒抗体数据库(CoV-AbDab)分析显示,VL6-57抗体的HCDR3富含“WLRG”基序,LCDR3富含“QSYDSS”基序。进一步的抗体组库分析发现,含“WLRG”基序的IgH序列在新冠感染和健康人群中均存在,但在感染后显著扩增并发生类别转换,而含“QSYDSS”基序的VL6-57轻链在两组中的表达水平相当。这些结果表明,在新冠病毒刺激下,表达VL6-57抗体的na?veB细胞被激活并发生克隆扩增和类别转换,在近90%的新冠感染者中诱导了VL6-57类人群抗体。
最后,研究人员发现,OmicronRBD中S371L-S373P-S375F突变同时回复至野生型后,R1-26等VL6-57人群抗体的结合能力完全恢复,表明371-373-375位点的突变是Omicron变异株逃逸VL6-57人群抗体的关键因素。
广州健康院熊晓犁研究员、广州医科大学赵金存教授、广州国家实验室陈凌研究员和广州健康院何俊研究员为本论文的共同通讯作者。广州医科大学博士后颜奇鸿、实习研究员高夕杰和广州健康院助理研究员刘邦慧为本论文的共同第一作者。该研究得到了国家自然科学基金、国家重点研发计划、广州实验室应急攻关项目、广东省自然科学基金和中国博士后科学基金等的支持。
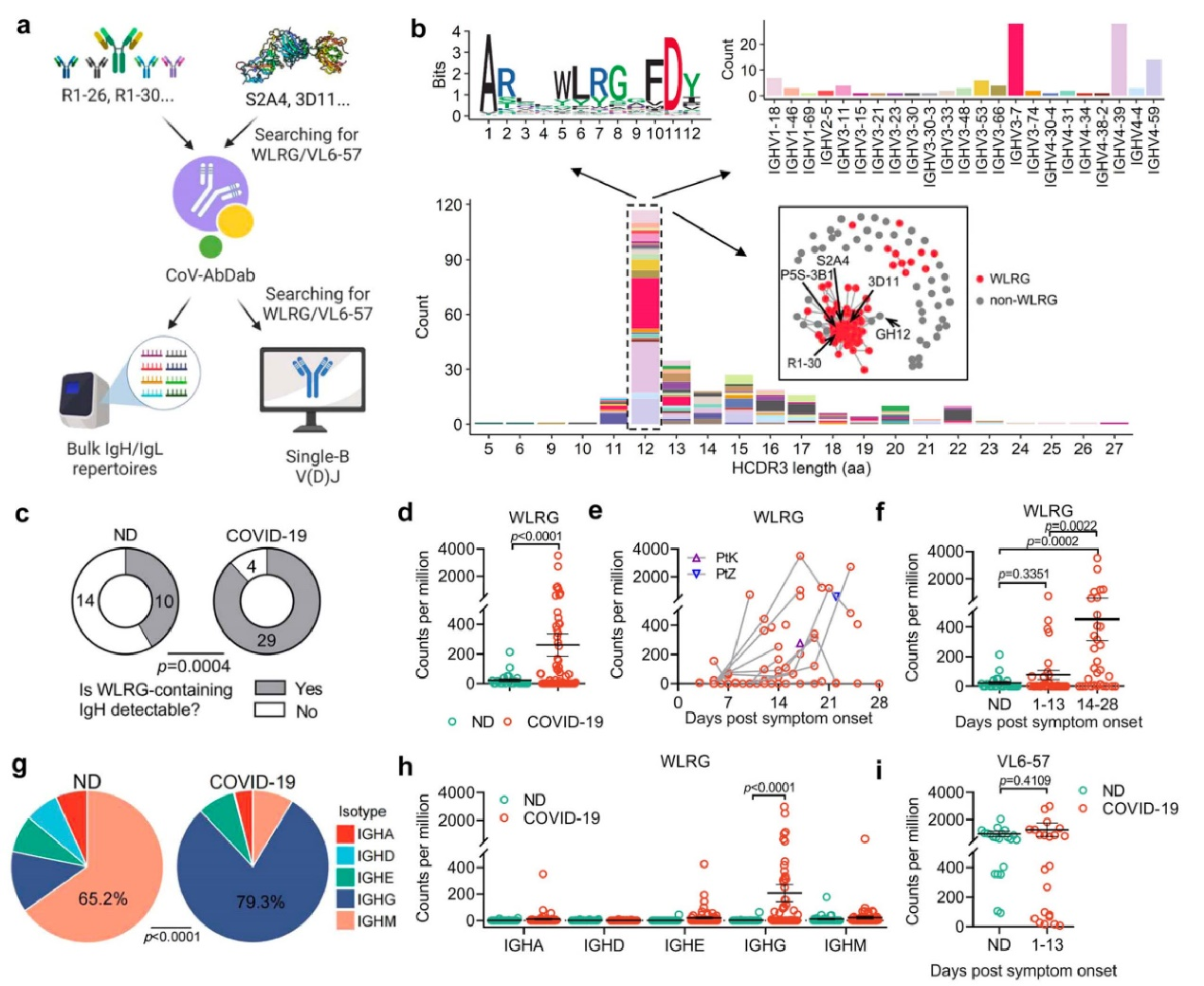
VL6-57抗体的序列特征分析