
-

生物通官微
陪你抓住生命科技
跳动的脉搏
【科研动态】“自古逢秋悲寂寥”的原因找到了:华中科技大学生命学院张珞颖教授课题组揭示冬季抑郁的机制
【字体: 大 中 小 】 时间:2024年11月30日 来源:华中科技大学生命与科学技术学院
编辑推荐:
2024年11月11日,华中科技大学生命科学与技术学院张珞颖教授团队在Nature Metabolism杂志上发表了题为“ Human PERIOD3 variants lead to winter depression-like behaviours via glucocorticoid signalling ”的文章, 该团队利用遗传学、神经生物学和分子生物学等方法发现人的生物钟基因 PERIOD3 的天然变异( PER3-P415A/H417R )在模拟冬季的短光照下通过增强糖皮质激素合成从而导致抑郁样行为,并进一步阐明了糖皮质激素导致抑郁的机理
季节性情感障碍,俗称“悲秋综合症”、“冬季抑郁”,是抑郁的一种特殊类型。该疾病主要特征为患者在秋冬季节抑郁反复发作,而到春夏季节则自发缓解,在世界范围内发病率约1-10%。目前认为冬季抑郁由秋冬季节白昼长度过短、日照过少所诱导,强光暴露治疗则有助于抑郁症状的缓解。然而,自从该疾病在四十年前被提出和定义以来,关于其发生发展的机理仍不清楚,明确这一问题有助于理解季节变化影响情绪的机制。

2024年11月11日,华中科技大学生命科学与技术学院张珞颖教授团队在Nature Metabolism杂志上发表了题为“Human PERIOD3 variants lead to winter depression-like behaviours via glucocorticoid signalling”的文章,该团队利用遗传学、神经生物学和分子生物学等方法发现人的生物钟基因PERIOD3的天然变异(PER3-P415A/H417R)在模拟冬季的短光照下通过增强糖皮质激素合成从而导致抑郁样行为,并进一步阐明了糖皮质激素导致抑郁的机理。此研究揭示了冬季抑郁的发病机制,为理解情绪的季节性调控机理提供了基础。
该团队前期在一个遗传家系中发现携带生物钟基因PER3的两个变异(PER3-P415A/H417R)的个体罹患有冬季抑郁。在本研究中,研究人员首先检测了PER3-P415A/H417R是否是导致冬季抑郁的致病变异。他们构建了全身表达野生型或突变型人类PER3基因的转基因小鼠,并检测了这些小鼠在模拟冬季的短光照条件(每天4小时光照-20小时黑暗)和正常光照条件(每天12小时光照-12小时黑暗)下的类抑郁行为,发现突变组小鼠在短光照下表现出更明显的抑郁样表型。运用临床上冬季抑郁治疗常用的清晨光暴露治疗以及经典的抗抑郁药物氟西汀(选择性5-羟色胺再摄取抑制剂)都能够显著缓解突变组小鼠的抑郁样表型。这一系列结果表明PER3-P415A/H417R极有可能是冬季抑郁的致病变异。
研究人员接下来探究PER3-P415A/H417R如何导致冬季抑郁。他们发现突变型小鼠对慢性社交挫败应激更为敏感,提示PER3-P415A/H417R增强了对应激的敏感性。下丘脑-垂体-肾上腺轴(HPA轴)的激活以及最终肾上腺中糖皮质激素的合成和释放是机体响应应激的重要通路。因此,研究人员检测了糖皮质激素皮质酮(corticosterone)的丰度,发现在短光照下突变组小鼠呈现出比野生型组更高的血浆皮质酮水平,过量的皮质酮使得动物的抑郁样行为增加。皮质酮增高是因为突变型肾上腺对垂体释放的促肾上腺皮质激素(ACTH)更敏感,ACTH能诱导突变型肾上腺合成更多的皮质酮。研究人员进一步构建转基因小鼠实现仅在肾上腺表达野生型或突变型人类PER3基因,发现仅在此一个组织表达突变型PER3就能导致冬季抑郁样表型以及血浆皮质酮水平的升高,说明PER3-P415A/H417R在肾上腺中起效导致冬季抑郁。为了解析PER3-P415A/H417R在肾上腺中促进皮质酮合成的机制,研究人员运用了多种分子生物学、生物化学手段,发现PER3-P415A/H417R蛋白通过抑制皮质酮合成的关键蛋白StAR的降解,促进肾上腺合成皮质酮,继而导致抑郁样表型。
为了回答皮质酮的增加以及抑郁样表型为何仅发生在短光照下,研究人员比较了突变组小鼠和对照组小鼠在不同光照下的血浆皮质酮水平,发现对照组小鼠在短光照下呈现出皮质酮水平的下调,而突变型小鼠未能呈现出此下调现象,从而使得在短光照下突变型小鼠的皮质酮水平比对照组高。通过一系列药理学及神经生物学手段,研究人员发现HPA轴响应光照长度改变,在短光照下ACTH会下调。然而PER3-P415A/H417R增强了肾上腺对ACTH的敏感性,即便短光照下ACTH变少了,肾上腺仍然合成了大量皮质酮,使得突变型小鼠的皮质酮水平仅在短光照下比对照组高。
最后,研究人员阐明了过量皮质酮导致抑郁的机理。既往研究发现糖皮质激素信号会抑制脑内中缝背核(DRN)内色氨酸羟化酶-2(Tph2)的转录。此蛋白是5-羟色胺(5-HT)合成途径的关键限速酶,上文中也提到了使用5-HT再摄取抑制剂氟西汀能缓解突变组小鼠的抑郁样表型,提示突变组小鼠可能存在5-HT信号的缺陷。因此,研究人员检测了中缝背核Tph2的表达情况,发现短光照下突变组小鼠的Tph2的转录显著下调,使得Tph2的mRNA与蛋白均显著减少。进一步利用遗传学、神经生物学、药理学、分子生物学的多种手段,研究人员证实了突变型小鼠中过量的皮质酮抑制DRN中Tph2的转录,从而导致抑郁样行为。研究人员还发现TPH2蛋白水平随光照长度而变化,在短光照下会下调。而短光照下突变型小鼠中过量的皮质酮则使得TPH2进一步减少,继而诱发了抑郁样行为。
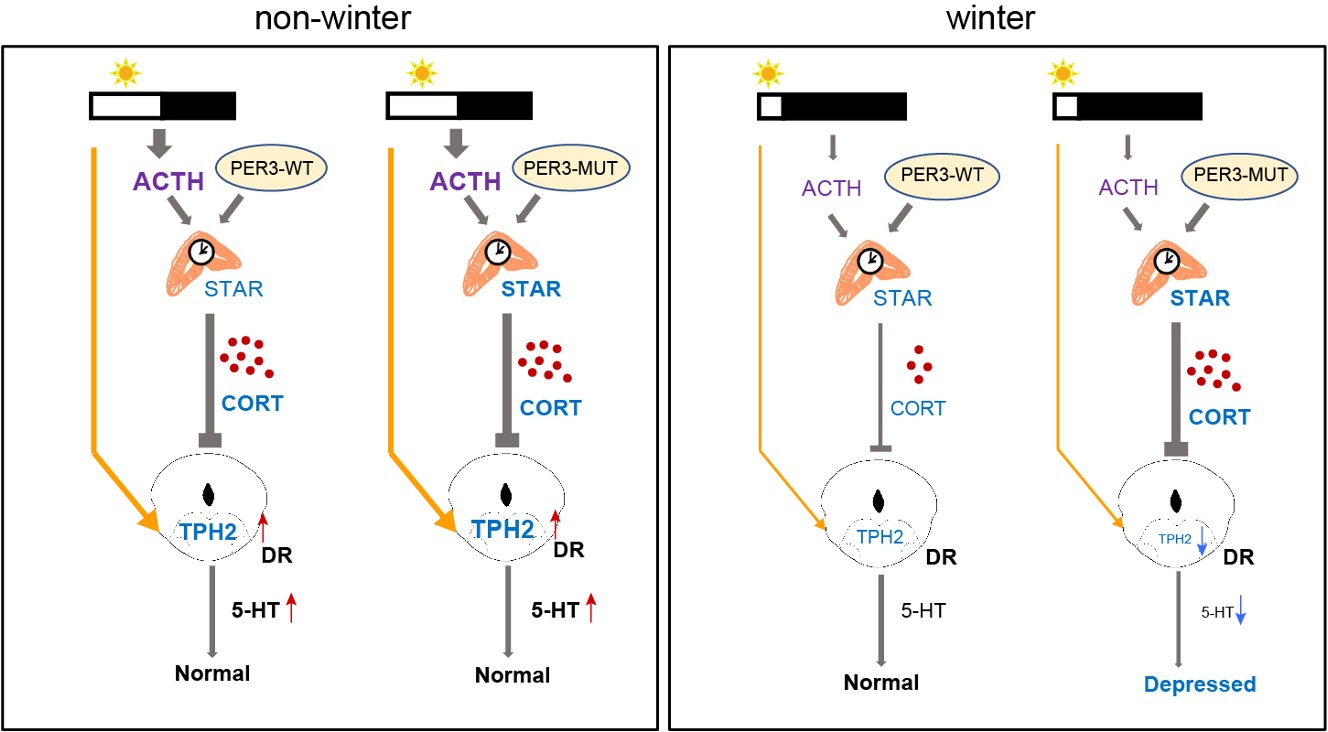
总而言之,本研究发现人的PER3-P415A/H417R变异增加肾上腺中皮质酮合成的关键蛋白StAR的丰度,使得肾上腺对ACTH更易感,在模拟冬季的短光照下产生过量皮质酮,抑制脑内DRN中Tph2的表达从而导致冬季抑郁样表型的产生。
华中科技大学生命科学与技术学院博士后高倩、博士研究生唐志炜和王海莉为本文的共同第一作者,华中科技大学生命科学与技术学院张珞颖教授为本文的通讯作者。对本研究感兴趣的读者可以阅读论文作者受邀撰写的“Behind the paper”博客,了解有关此研究的“内情”(https://communities.springernature.com/posts/light-circadian-clock-and-mood-linked-together-by-human-genetic-variants)。
专家点评:
中国科技大学薛天教授:
张珞颖团队的这项研究工作,揭示了季节性情感障碍(SAD)背后可能的分子机制,为理解情绪与季节变化的深层关联提供了全新的生物学视角。SAD,也称“冬季抑郁症”,长期以来被认为与日照时间缩短有关。日照的减少不仅影响生物钟,还改变了体内激素的平衡,导致情绪和行为的波动。尽管光疗法是目前较常用的治疗方法,但情绪变化如何产生、及其背后的调控机制仍未明晰。
在此背景下,张珞颖团队创新性地发现了PER3基因的两个变体(P415A和H417R)在短光周期下显著增加了小鼠的抑郁样行为,揭示出SAD的分子机制。研究构建的PER3变异转基因小鼠在模拟冬季白昼的短光周期(4小时光照-20小时黑暗)下,表现出显著的抑郁样行为,同时血浆皮质酮水平显著升高。值得注意的是,糖皮质激素受体拮抗剂米非司酮可逆转这些抑郁症状,暗示了糖皮质激素在SAD中的关键作用。进一步实验表明,这种现象并非通过交感神经通路,而是直接通过肾上腺促进皮质酮合成,进而抑制中缝背核的Tph2表达,从而触发抑郁样行为。这一发现揭示了基因、光周期、内分泌系统和情绪之间复杂的跨层次调控网络,深化了我们对环境适应和情绪调节的认识。
本研究为理解SAD的机制带来了深远影响,使我们认识到个体在自然季节变化下的适应能力。这一成果不仅为SAD的防治提供了新靶点,更在广义上启示我们,季节性环境因子或许在心理健康、内分泌调控乃至行为适应中扮演重要角色。这一研究为理解光照在调控情绪中的多层次影响提供了新思路,激励未来研究进一步探讨环境与情绪的复杂关系。
浙江大学胡海岚教授:
许多情绪障碍,例如抑郁症,其症状多存在季节性波动现象,秋冬的抑郁症状较春夏更严重。既往研究多认为这种情绪变化多与体内激素以及影响情绪的单胺递质水平随光周期变化形成的季节性变化有关,但导致季节性情绪障碍(SAD)发生的分子和环路机制一直没有系统的研究和解读。
继前期通过在家族性睡眠障碍并伴有抑郁量表高分人群中发现了生物钟基因PER3的两个变异P415A/H417R,2024年11年11月,华中科技大学张珞颖团队又在前期的研究基础上深入解析了“P415A/H417R突变能够通过糖皮质激素信号通路诱导冬季抑郁样行为”,这项研究发现携带P415A/H417R的突变动物能够稳定类固醇急性调节蛋白(StAR), 阻断了短光周期下的肾上腺皮质酮下调,引起小鼠中缝背核色氨酸羟化酶(Tph2)以及下游血清素水平下降,最终诱发了动物抑郁样表型,完成了从遗传因素到激素水平到单胺递质以及动物行为的多脑区和多层面精细分析。
这篇文章深入探讨了SAD的潜在机制,特别是通过PER3基因变体的视角。研究的重要发现在于:首次将SAD的病理机制从传统认知的大脑中心论转向了肾上腺皮质的作用。文章揭示了一个复杂的调节网络:光周期变化→肾上腺对ACTH的敏感性(受PER3变体影响)→皮质酮分泌→血清素合成的调控。这一发现不仅解释了SAD的季节性特征,也为疾病的异质性提供了新的解释框架,对未来个性化治疗策略的制定具有重要意义。
斯坦福大学陈晓科教授:
季节性情感障碍(SAD),也叫做“冬季忧郁症”,是一种普遍的情绪障碍,通常在秋冬季节出现抑郁情绪,而在春夏季节有所缓解。随着对SAD及其生物学机制研究的深入,越来越多的研究开始探讨如何将遗传因素与环境因素结合来理解这一复杂的心理健康问题。最近,发表在《Nature Metabolism》上名为Human PERIOD3 variants lead to winter depression-like behaviours via glucocorticoid signalling的研究揭示了人类周期基因PERIOD3(PER3)中的两个变异(P415A和H417R)如何通过糖皮质激素信号通路导致冬季抑郁样行为。
在这项研究中,研究人员使用了携带PER3基因两种变异(P415A和H417R)的人源化小鼠模型。这些小鼠在短日照的环境下表现出明显的抑郁样行为。这种抑郁情绪与它们体内皮质酮(压力激素)水平的上升密切相关。具体而言,这些变异使小鼠的肾上腺对促肾上腺皮质激素(ACTH)的反应更加敏感,从而导致皮质酮的合成增加。与此同时,这种变异还抑制了色氨酸羟化酶2(Tph2)的表达,而Tph2是合成5-羟色胺的重要酶。5-羟色胺的减少可能直接导致抑郁情绪的加重。此外,研究还发现,糖皮质激素在情绪调节中扮演了复杂的角色。通过使用糖皮质激素受体拮抗剂,研究人员能够成功缓解小鼠的抑郁样行为,这表明糖皮质激素在冬季抑郁症的发病机制中起着关键作用。
这项研究不仅为理解冬季抑郁症的生物学基础提供了新的视角,还强调了基因与环境之间的相互作用。总的来说,这项研究为我们提供了新的认识,显示出遗传因素如何影响情绪和行为,进而影响心理健康。这些发现也为未来的治疗和干预策略提供了新的方向,帮助我们更好地理解和应对冬季抑郁症,改善患者的生活质量。