
-

生物通官微
陪你抓住生命科技
跳动的脉搏
STTT|北京大学张强/汪贻广团队提出了PROTACs智能纳米递送新策略
【字体: 大 中 小 】 时间:2024年10月23日 来源:北京大学药学院
编辑推荐:
2024 年 10 月 18 日,我院天然药物及仿生药物全国重点实验室张强院士 / 汪贻广教授团队在国际著名期刊 Signal Transduction and Targeted Therapy 上在线发表了题为 “Sequential responsive nano-PROTACs for precise intracellular delivery and enhanced degradation efficacy in colorectal cancer therapy (实现精准胞内递送和蛋白降解效果增强的程序响应纳米 PROTACs 用于结直肠癌治疗) ” 的研究论文,介绍了团队在 PROTACs 纳米递送领域的最新研究成果
2024年10月18日,我院天然药物及仿生药物全国重点实验室张强院士/汪贻广教授团队在国际著名期刊Signal Transduction and Targeted Therapy上在线发表了题为“Sequential responsive nano-PROTACs for precise intracellular delivery and enhanced degradation efficacy in colorectal cancer therapy(实现精准胞内递送和蛋白降解效果增强的程序响应纳米PROTACs用于结直肠癌治疗)”的研究论文,介绍了团队在PROTACs纳米递送领域的最新研究成果。

蛋白降解靶向嵌合体(PROteolysis TArgeting Chimeras, PROTACs)是一种双功能分子,由目标蛋白结合配体、E3连接酶配体和连接子构成。PROTACs通过招募细胞内泛素-蛋白酶体系统实现目标蛋白降解,为肿瘤治疗提供了一种创新的选择性降解肿瘤相关蛋白的策略。与传统的小分子抑制剂相比,PROTACs具有作用靶点多、催化效率高、选择性强、耐药性低等明显优势。然而,小分子PROTACs的疗效常因肿瘤组织靶向性差、瘤内渗透有限以及细胞内化不足等而受到限制。实现更有效的肿瘤递送和良好的抗肿瘤功效,是PROTACs面临的重大挑战。理想的递送系统应当可以精准地将活性药物递送至肿瘤细胞内的靶点,从而有效发挥抗肿瘤活性。由于PROTACs主要在肿瘤细胞质中起作用,为了使PROTACs在作用部位的暴露最大化,需要设计一个合理的递送系统以同时实现PROTACs的长循环、肿瘤渗透、细胞内化和胞内释放。
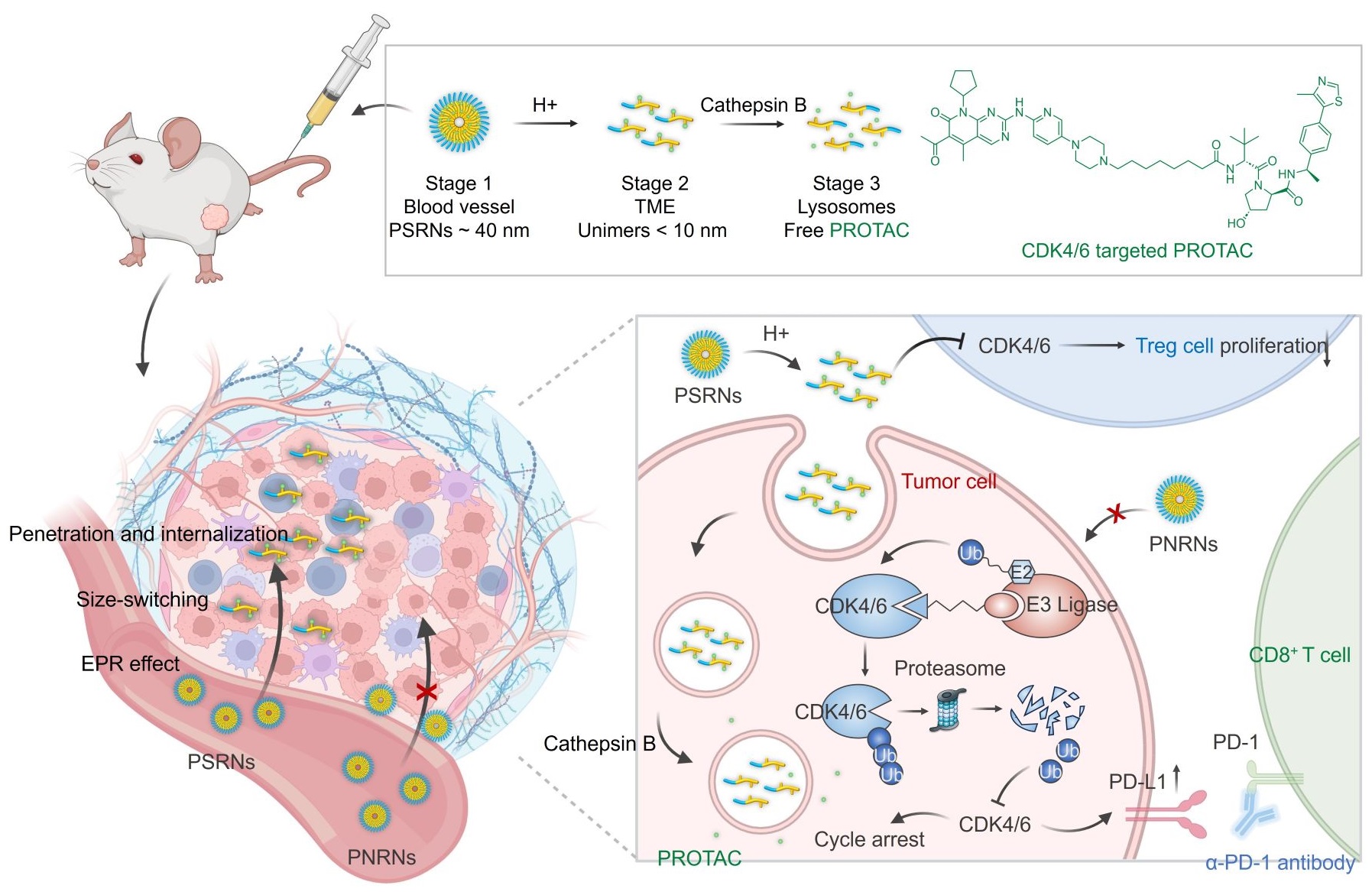
针对上述问题,张强/汪贻广团队利用pH超敏感(Ultra-pH-sensitive, UPS)技术,设计和制备了基于PROTACs的pH和组织蛋白酶B顺序响应纳米粒(PROTAC-conjugated pH/cathepsin B sequential responsive nanoparticles, PSRNs),以结直肠癌为治疗模型,细胞周期依赖性激酶4和6(Cyclin-dependent kinases 4 and 6, CDK4/6)为目标蛋白,系统地探究了PSRNs的PROTACs抗肿瘤疗效和高效递送机制。
研究发现,PSRNs在血液循环中能保持其纳米结构(40 nm),并通过增强的渗透和滞留效应在肿瘤中有效积累。在酸性肿瘤微环境下,PSRNs迅速解离,粒径减小(<10 nm),实现了良好的肿瘤渗透和细胞内化。经细胞内吞的PSRNs在溶酶体中的组织蛋白酶B作用下,将PROTACs释放到细胞内,实现了PROTACs的胞内递送和高效的蛋白降解。结果显示,与PROTACs原药相比,PSRNs的CDK4/6蛋白的降解效率分别提高了2.6和3.0倍。此外,PSRNs通过降解CDK4/6蛋白,上调癌细胞表面PD-L1的表达,并抑制肿瘤微环境中调节性T细胞的增殖,从而增强了免疫检查点阻断剂的敏感性。在小鼠结直肠癌模型中,PSRNs与α-PD-1联用显著增强了抗肿瘤疗效。综上,该研究通过设计顺序响应纳米递送系统验证并实现了PROTACs在细胞内精确递送,解决了PROTACs的递送难题,并为结直肠癌的靶向联合治疗提供了一种有希望的治疗策略。
北京大学药学院张强院士、汪贻广教授和代文兵副教授为本研究论文的共同通讯作者。北京大学药学院2020级博士生杨柳青和2019级直博生杨晔为该论文的共同第一作者。团队成员张静、李明慧、杨龙、王兴、陈梅芳、张华副教授、何冰研究员以及王学清研究员为该研究做出了重要贡献。北京大学药学院天然药物及仿生药物全国重点实验室为第一单位,该项研究得到国家自然科学基金、北京市自然科学基金和国家重点研发计划等项目的支持。
论文链接:https://www.nature.com/articles/s41392-024-01983-1
通讯作者简介:

张强,北京大学博雅讲席教授,中国医学科学院学部委员,中国工程院院士,973首席科学家,北京市重点实验室主任,教育部创新团队负责人,中国药学会常务理事、纳米药物专委会副主委,国家药典会制剂专委会副主任,Acta Pharm Sinica B副主编,ADDR和JCR等国际杂志编委,国际控释协会中国分会首任主席,第6/7届药剂专委会主委。主要从事创新药物制剂研究,包括难溶药物、抗肿瘤药和生物大分药物递释系统的基础与转化研究。先后承担国家973计划、国家重大专项、863项目、国家自然科学基金重点项目等。获多项国家或省部级奖励。在国际权威杂志等发表SCI论文300多篇。开发多种新型高端制剂上市,产生显著的社会经济效益。

汪贻广,教授、博士生导师、北京大学药学院副院长、药剂学系主任、天然药物及仿生药物全国重点实验室PI。主要从事智能纳米药物递送及疾病诊疗研究,取得了一系列创新性研究成果,以第一作者或通讯作者在Nat. Mater.、Nat. Nanotechnol.、Nat. Commun.、J. Am. Chem. Soc.、Angew. Chem. Int. Ed.等国际著名期刊上发表高水平学术论文60余篇。获得国家级人才计划青年项目、国家杰出青年科学基金、国家优秀青年科学基金、北京杰出青年科学基金等。

代文兵,北京大学药学院副教授,博士生导师,研究方向包括:1)多肽自组装调控及其生物医学应用;2)难溶性药物纳米化新策略的研究与转化。承担国家重点研发计划课题和国家新药重大专项等课题;在Sig Transduct Target Ther、Adv Funct Mater、ACS Nano等期刊上发表研究论文,H-index为42;获得1项国家科技进步二等奖(第5完成人);获得2项创新纳米制剂的临床批件;执笔《纳米药物质量控制研究技术指导原则》、《脂质体药物质量控制研究技术指导原则》等国家新药研发指导原则。
天然药物及仿生药物全国重点实验室 供稿