
-

生物通官微
陪你抓住生命科技
跳动的脉搏
【科研动态】Nature Metabolism|华中科技大学生命学院薛宇/贾大团队合作揭示生酮饮食发挥作用的新机制
【字体: 大 中 小 】 时间:2024年10月13日 来源:华中科技大学生命与科学技术学院
编辑推荐:
近日,华中科技大学薛宇教授团队和四川大学贾大教授团队在 Nature Metabolism 杂志上合作发表了题为“Ketogenic diet reshapes cancer metabolism through lysine β-hydroxybutyrylation”的研究论文
生酮饮食(Ketogenic Diet, KD)是一种以高脂肪、极低碳水化合物和适量蛋白质为比例的饮食方式,自20世纪20年代初以来一直被临床用来治疗癫痫等疾病。生酮饮食减少了葡萄糖的利用,导致游离脂肪酸在肝脏中转化为酮体,包括乙酰乙酸、β-羟基丁酸(β-OHB)和丙酮,其中β-羟基丁酸是最丰富的形式。迄今为止,生酮饮食已在多种人类疾病中显示出一定的治疗效果,包括癫痫、肥胖、癌症等。然而。生酮饮食由于特殊的食物比例配置,较难坚持,还可能会引起高脂血症、肾结石等一系列并发症。进一步理解生酮饮食发挥作用的机制,有助于开发更为健康的饮食方式或疾病治疗手段。

近日,华中科技大学薛宇教授团队和四川大学贾大教授团队在Nature Metabolism杂志上合作发表了题为“Ketogenic diet reshapes cancer metabolism through lysine β-hydroxybutyrylation”的研究论文。生酮饮食可提高一种新型的蛋白质翻译后修饰――赖氨酸β-羟基丁酰化(lysine β-hydroxybutyrylation, Kbhb)的修饰水平,该修饰基团来源于β-羟基丁酸的活化形式β-羟基丁酰辅酶A(β-hydroxybutyryl-CoA)。在该工作中,通过对生酮饮食小鼠肝脏开展转录组学、蛋白质组学、代谢组学、赖氨酸β-羟基丁酰化组学的多组学定量,发现小鼠肝脏转录组、蛋白质组和赖氨酸β-羟基丁酰化组差异性地发生变化。生酮饮食通过赖氨酸β-羟基丁酰化修饰调控多种细胞过程,包括糖酵解和三羧酸循环等。为了找到发挥重要功能的赖氨酸β-羟基丁酰化修饰位点,基于前沿人工智能技术,设计了新的分层学习框架(Hierarchical learning framework)pFunK,是首个预测蛋白质修饰功能的语言模型。该框架采用分层思维,巧妙利用Transformer模型捕捉序列之间的上下文依赖关系,并结合十种蛋白质序列和结构特征,逐层学习赖氨酸修饰特征、赖氨酸β-羟基丁酰化修饰特征,再学习赖氨酸β-羟基丁酰化的功能特征,仅使用9个已知功能的赖氨酸β-羟基丁酰化位点,即实现了赖氨酸β-羟基丁酰化功能的精准预测。
针对该修饰,使用pFunK-Kbhb预测潜在具有重要功能的赖氨酸β-羟基丁酰化位点。通过算法预测、细胞实验、动物实验等发现生酮饮食或添加β-羟基丁酸可增加缩醛酶B(Aldolase B, Aldob)的K108位赖氨酸β-羟基丁酰化修饰水平,抑制mTOR信号通路和糖酵解过程,削弱癌细胞增殖,从而揭示了生酮饮食重塑代谢的新机制。综上所述,此研究不仅发现了生酮饮食发挥作用的新机制,还为预测功能重要的赖氨酸修饰位点提供了普遍适用的语言模型。
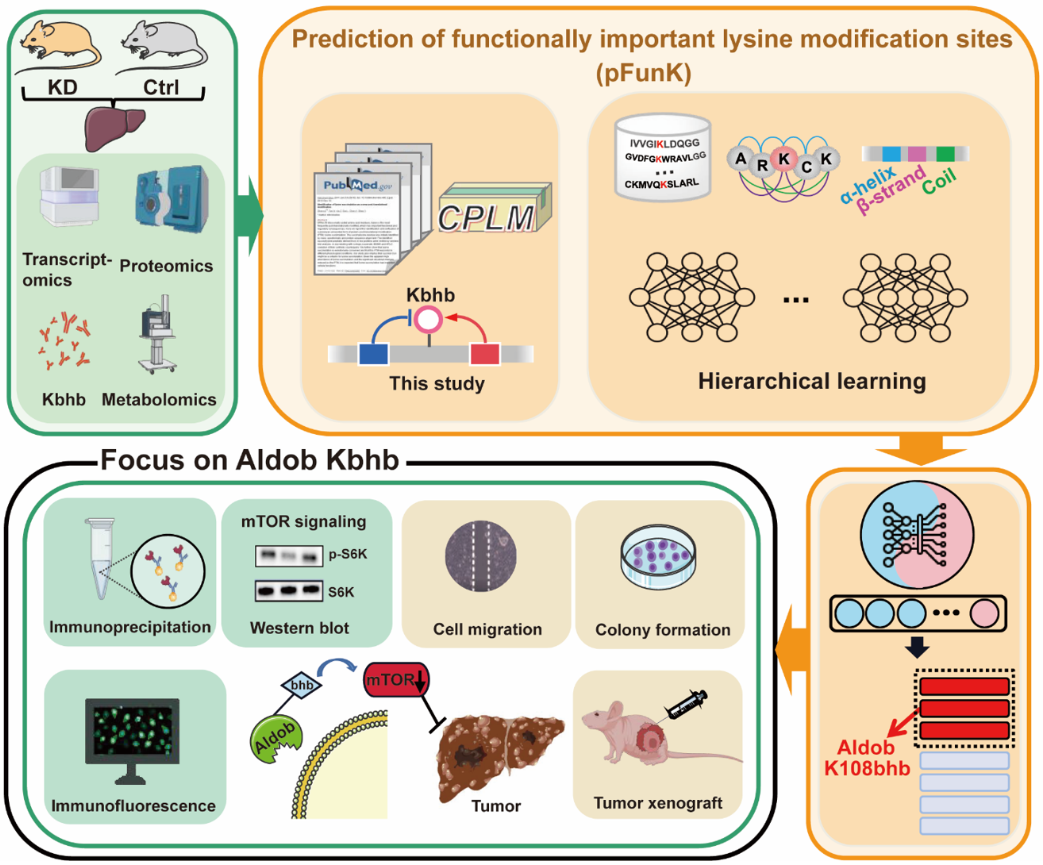
图1. 实验流程。利用喂养生酮或对照饮食的小鼠肝脏,开展转录组、蛋白质组、β-羟基丁酰化组和代谢组的多组学分析。构建了分层学习框架pFunK,可预测功能重要的赖氨酸修饰位点。使用pFunK分析β-羟基丁酰化组数据,预测ALDOB的K108为潜在重要的β-羟基丁酰化位点。后续实验揭示ALDOB的β-羟基丁酰化调控其酶活、mTOR信号通路及肿瘤增殖。
四川大学秦俊红、华中科技大学黄新荷、四川大学苟圣松、四川大学张思韬为该论文的共同第一作者。薛宇教授和贾大教授为该论文的通讯作者。四川大学戴伦治教授、张燕教授、杜丹研究员、胡以国教授、魏强教授、刘振华教授、天津大学轩维民教授、华中科技大学彭迪博士、中山大学刘泽先研究员、芝加哥大学赵英明教授、中国科学院上海药物研究所黄河教授、上海交通大学程金科教授、重庆医科大学谭帅教授、成都中医药大学沈晓飞副研究员等也为课题提供了大力支持。杭州景杰生物科技股份有限公司在赖氨酸β-羟基丁酰化修饰组学分析、多种修饰性泛抗体、修饰性抗体定制方面提供了原创性的蛋白质组学技术与抗体产品支持。本项目得到国家重点研发计划、国家自然科学基金(杰出青年、重点项目和“生命过程分子语言逻辑结构的AI解析专项项目”)等项目资助。
原文链接:https://www.nature.com/articles/s42255-024-01093-w