
-

生物通官微
陪你抓住生命科技
跳动的脉搏
我国学者在放射性药物领域取得进展
【字体: 大 中 小 】 时间:2024年10月11日 来源:国家自然科学基金委员会
编辑推荐:
最新研究成果以“共价靶向放射配体增强放射性核素治疗(Covalent Targeted Radioligands Potentiate Radionuclide Therapy)”为题,于2024年5月22日在线发表于《自然》(Nature),论文链接为:https://www.nature.com/articles/s41586-024-07461-6
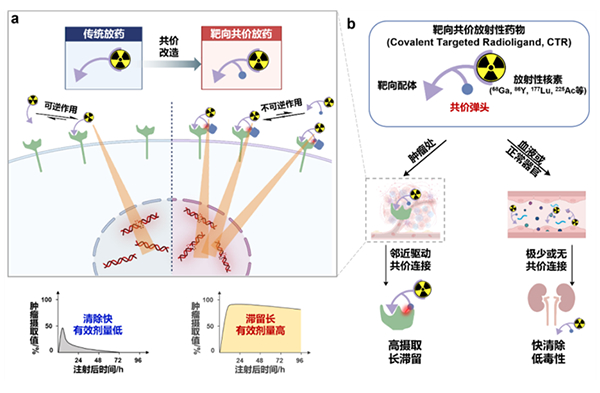
图 靶向共价放射性药物工作原理及其优势
在国家自然科学基金项目(批准号:22225603)等资助下,北京大学、昌平实验室刘志博团队基于现代共价药物分子工程发展了一类新型药物形式,即靶向共价放射性药物(Covalent Targeted Radioligand, CTR),突破了传统放射性药物“快清除”与“长滞留”不可兼得的难题。最新研究成果以“共价靶向放射配体增强放射性核素治疗(Covalent Targeted Radioligands Potentiate Radionuclide Therapy)”为题,于2024年5月22日在线发表于《自然》(Nature),论文链接为:https://www.nature.com/articles/s41586-024-07461-6。
CTR是一个三功能配体,通过在适宜位置和取向上安装基于二代“点击化学”硫(Ⅵ)-氟交换反应(SuFEx)的“潜弹头”(latent warhead),当CTR到达肿瘤时,先非共价地结合靶标,后通过邻近效应加速不可逆的共价连接,将肿瘤清除率降至最低,而其他未结合靶标的自由CTR则被快速排出体外。这一技术已从分子、细胞、小鼠及患者层面验证了有效性,突破了成纤维细胞活化蛋白(FAP,为泛癌种靶点)靶向放射性药物因肿瘤摄取、滞留不足导致疗效不佳的瓶颈(如图)。在一项初步的肿瘤成像临床研究中,这一策略比其他方法(包括传统FAPI-PET/CT)识别出了更多的甲状腺髓样癌病灶,并通过手术和病理研究确认了这些病灶为真阳性。研究还分别采用β-(Lu-177)和α-放射性核素(Ac-225)标记CTR-FAPI(及FAPI-mFS),在后续治疗中几乎完全抑制了小鼠的FAP高表达皮下肿瘤生长。在另一种靶向前列腺特异性膜抗原(PSMA)的SuFEx工程化放射配体也显示出更强的治疗效果。
肿瘤成像临床研究表明CTR-FAPI有潜力成为下一代更高灵敏度的FAPI-PET探针。由于可连接SuFEx弹头的蛋白质较为广泛,这一策略或可用于靶向其他靶点的放射性药物,并为调控其他低分子量偶联类药物的药代动力学提供了新途径。