
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Immunity:南方医科大学团队解析妊娠期的脓毒症易感机制
【字体: 大 中 小 】 时间:2023年05月17日 来源:赛业生物
编辑推荐:
近日,南方医科大学中医药学院的龚神海团队在妊娠期脓毒症易感机制研究方面取得进展。研究者发现,妊娠引起的肠道菌群变化会驱动巨噬细胞焦亡,并加剧化脓性炎症。
每年,全球大约有5000万人患上脓毒症,其中死亡人数超过20%。脓毒症是一种由感染引发的疾病,严重时可导致一个或多个器官功能衰竭。孕产妇脓毒症可导致严重的并发症,包括先兆子痫和早产,在英国被认为是孕产妇死亡的主要原因之一。
妊娠期间发生的生理变化容易导致脓毒症恶化,并带来较高的死亡风险。然而,造成死亡率增加的机制尚不清楚,也缺乏相关的治疗方法。若能深入了解脓毒症妇女全身免疫紊乱的机制,也许能揭示一些治疗方法,改善孕产妇及新生儿的健康。
近日,南方医科大学中医药学院的龚神海团队在妊娠期脓毒症易感机制研究方面取得进展。研究者发现,妊娠引起的肠道菌群变化会驱动巨噬细胞焦亡,并加剧化脓性炎症。这项研究成果发表在《Immunity》杂志上,中医药学院龚神海副教授、肖炜研究员和基础医学院姜勇教授为本文通讯作者。

图片来源:《Immunity》
(https://doi.org/10.1016/j.immuni.2023.01.015)
研究材料与方法
在这项研究中,研究人员使用了两种脓毒症小鼠模型:盲肠结扎穿刺(CLP)和脂多糖(LPS)诱导模型,其中使用的无菌雌性小鼠是由赛业生物提供的。研究者用广谱抗生素ABX来清除小鼠的肠道菌群,然后开展肠道菌群移植。在分析肠道菌群变化时研究者采用了多组学分析,还通过免疫沉淀等分析确定了FMN的互作对象和作用机制。
技术路线
01 通过肠道菌群移植确定脓毒症的易感性增加与肠道菌群有关
02 通过综合多组学分析确定粪副拟杆菌及其产物FMN对脓毒症小鼠有保护作用
03 FMN可抑制脓毒症小鼠的巨噬细胞焦亡
04 FMN直接与hnRNPUL2相互作用,阻止其与Nlrp3启动子序列结合
研究结果
脓毒症的易感性增加与肠道菌群有关
为了分析妊娠是否会增加对脓毒症的易感性,研究人员采用了多种模型。在盲肠结扎穿刺(CLP)小鼠模型中,与非怀孕组相比,怀孕组在CLP后的死亡率大幅增加。LPS处理的小鼠也出现了类似的结果。组织病理学检查显示,接受CLP的怀孕小鼠出现更严重的多器官损伤和细胞死亡。同时,妊娠会增加CLP诱导的局部炎症反应,并抑制病原体清除能力,从而增加对脓毒症诱导的多器官衰竭的易感性。
肠道菌群参与了脓毒症的发病机制,其组成在妊娠期间被重塑。因此,研究人员假设孕产妇脓毒症的高死亡率与肠道菌群失调有关。通过抗生素处理和肠道菌群移植 FMT。研究者发现接受怀孕供体肠道菌群的小鼠有更高的血清ALT活性,且CLP后血浆中的细胞因子浓度也高于对照小鼠。怀孕供体的肠道菌群移植增加了脓毒症小鼠血液和腹腔灌洗液中的细菌载量。这些结果表明,妊娠期间肠道微生物组的变化足以驱动脓毒症进展。
粪副拟杆菌或FMN对脓毒症小鼠有保护作用
接下来,研究者便深入剖析了妊娠期间肠道菌群的变化如何导致脓毒症的易感性增加。16S rRNA基因测序的结果显示,怀孕组和非怀孕组的肠道菌群存在明显的组间分离。线性判别分析表明,怀孕妇女和小鼠的共同点是肠道副拟杆菌属(Parabacteroides merdae)丰度下降。同时,与非怀孕小鼠相比,怀孕小鼠体内的芒柄花素(FMN)水平较低(图1),FMN属于异黄酮类化合物,具有抗炎作用。通过综合多组学分析,研究者进一步证实了副拟杆菌与FMN丰度之间的相关性。而且在怀孕妇女和小鼠中,下降的是粪副拟杆菌,而不是其他物种。
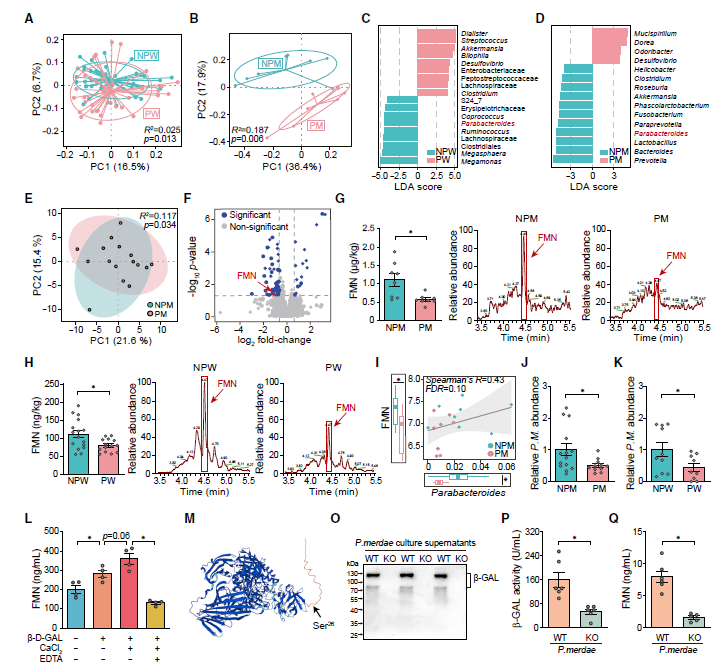
图1 副拟杆菌(P. merdae) 丰度和芒柄花素(FMN)在妊娠期间下降[1]
对粪副拟杆菌进行全基因组测序后,研究者发现这种细菌的基因组包含13个开放阅读框,编码不同的β-半乳糖苷酶家族成员。肠道中的β-半乳糖苷酶可水解食物中的活性化合物,生成高活性的异黄酮类化合物(包括FMN)。研究者发现,利用粪副拟杆菌预处理脓毒症小鼠后,小鼠腹腔灌洗液中的FMN浓度增加。妊娠期间随着粪副拟杆菌的减少,脓毒症小鼠腹腔内的FMN浓度也下降,表明粪副拟杆菌通过减少FMN的生成而参与脓毒症的进展。
为了明确粪副拟杆菌在脓毒症中的作用,研究人员用粪副拟杆菌对脓毒症小鼠进行预处理,发现小鼠血浆和腹腔灌洗液中的TNF-α和IL-1β等细胞因子下降,且小鼠生存率提高。同样地,FMN处理也减少了脓毒症小鼠腹腔和血液中的细菌量,提高了小鼠的生存率。这些数据表明,粪副拟杆菌或FMN的注射可以减少炎症反应,对脓毒症小鼠有保护作用。
FMN抑制了巨噬细胞焦亡
研究人员猜测,妊娠通过破坏正常的免疫功能而加重了脓毒症。为了验证这一假设,研究者对脓毒症小鼠腹腔灌洗液中的免疫细胞进行定量。怀孕小鼠接受CLP或LPS处理后,巨噬细胞和中性粒细胞数量减少。后续分析发现,巨噬细胞的耗竭会加剧脓毒症小鼠的多器官功能衰竭,而粪副拟杆菌和FMN注射都能增加小鼠的腹膜巨噬细胞数量。因此,FMN通过抑制免疫功能失调来促进细菌清除,从而降低脓毒症小鼠的死亡率。
不过,这背后的具体机制是什么?以往的研究发现,在脓毒症发生时腹膜巨噬细胞会发生焦亡。因此,研究者提出,怀孕脓毒症小鼠腹膜巨噬细胞的减少是因为焦亡。FMN的注射抑制了LPS加ATP诱导的巨噬细胞焦亡,伴随着caspase-1 p20和GSDMD-N产生和LDH释放的减少。在经过LPS加ATP处理的BMDM中,FMN还减少了Nlrp3 mRNA转录本以及IL-1β和IL-18的释放(图2)。
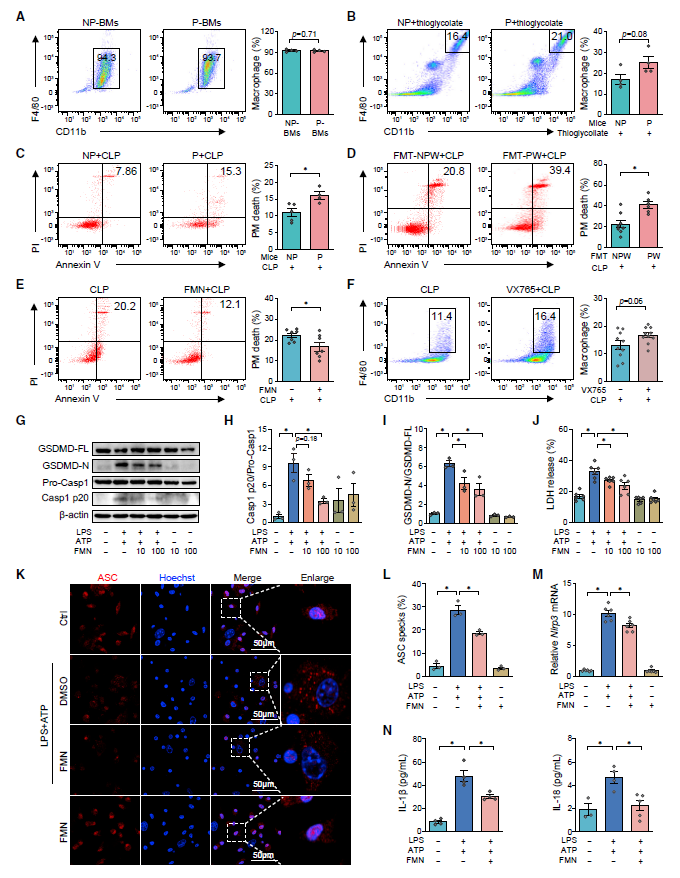
图2 FMN抑制了巨噬细胞焦亡[1]
蛋白质组学分析显示,在LPS加ATP处理的BMDM中,RNA结合蛋白hnRNPUL2是FMN注射后降幅最大的蛋白质。通过RNA干扰分析,研究者发现hnRNPUL2的沉默可以减少BMDM的细胞焦亡。在hnRNPUL2-siRNA处理的BMDM中,FMN对焦亡的抑制作用减弱,表明FMN以hnRNPUL2依赖性的方式阻止巨噬细胞焦亡。通过免疫沉淀等分析,研究者发现FMN直接与hnRNPUL2相互作用,引发BMDM的溶酶体降解,从而导致hnRNPUL2在细胞核的积累减少,最终阻止其与Nlrp3启动子序列的结合,进而抑制巨噬细胞焦亡。
最后,研究人员评估了hnRNPUL2在CLP诱导的脓毒症中的作用。hnRNPUL2的基因沉默改善了CLP小鼠的存活率并减弱了多器官功能衰竭。此外,脓毒症患者肠道内的粪副拟杆菌和FMN丰度与病情发展呈负相关。至此,研究者揭示了FMN-hnRNPUL2-NLRP3轴在妊娠期脓毒症中的重要性。
研究结论
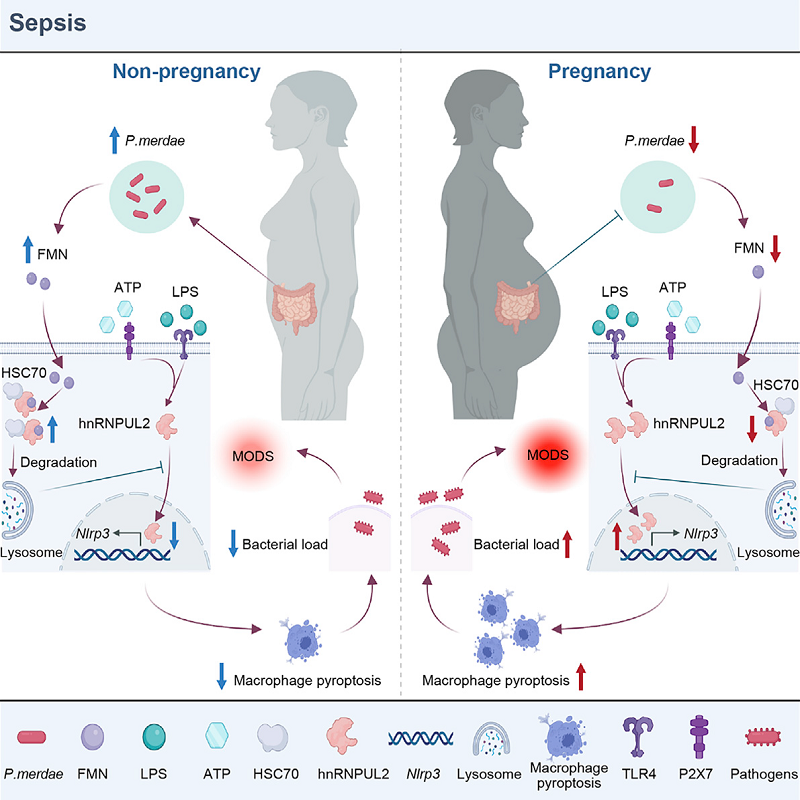
图3 妊娠期肠道微生物紊乱驱动脓毒症期间巨噬细胞死亡的分子机制[1]
总的来说,这项研究显示了妊娠期间的肠道菌群失调如何通过促进hnRNPUL2与Nlrp3启动子区域的相互作用来引发caspase-1介导的细胞焦亡,从而增加了脓毒症易感性(图3),这为开发脓毒症的新型治疗策略提供了思路。
原文检索:
[1] Chen X, Wu R, Li L, et al. Pregnancy-induced changes to the gut microbiota drive macrophage pyroptosis and exacerbate septic inflammation. Immunity. 2023 Feb 14;56(2):336-352.e9. doi: 10.1016/j.immuni.2023.01.015. PMID: 36792573.