
-

生物通官微
陪你抓住生命科技
跳动的脉搏
马明团队在多环倍半萜形成机制和结构多样性扩展方面取得新进展
【字体: 大 中 小 】 时间:2023年04月21日 来源:北京大学医学部
编辑推荐:
近日,北京大学药学院马明团队在JACS 上发表了题为“Structural Insights into Three Sesquiterpene Synthases for the Biosynthesis of Tricyclic Sesquiterpenes and Chemical Space Expansion by Structure-Based Mutagenesis” 的研究论文
近日,北京大学药学院马明团队在JACS上发表了题为“Structural Insights into Three Sesquiterpene Synthases for the Biosynthesis of Tricyclic Sesquiterpenes and Chemical Space Expansion by Structure-Based Mutagenesis”的研究论文。该研究阐明了三种三环倍半萜环化酶的晶体结构和催化机制,并通过环化酶的理性改造扩展倍半萜结构多样性。
倍半萜是一类极具化学结构和生物活性多样性的天然产物,在药物研发和香料工业领域具有重要的应用价值。倍半萜化学骨架的生物合成由倍半萜环化酶催化链状前体FPP形成,而FPP的不饱和度决定了其形成的碳氢骨架最多只有四个环,若形成醇类骨架则最多只有三个环。相对于二萜前体GGPP(C20)、二倍半萜前体GFPP(C25)和三萜前体FFPP(C30),较短的FPP(C15)形成多环产物更具挑战性并且需要精准的控制。目前对于多环倍半萜的骨架形成机制探究较少,准确理解这一复杂过程需要酶三维结构、定点突变、能量计算、同位素标记等手段的综合运用。
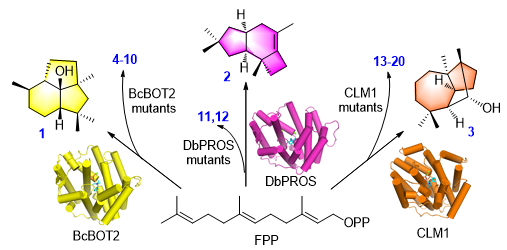
图1. 三环倍半萜1–3的化学结构和三个环化酶的晶体结构
基于此,研究团队针对三种骨架各异的三环倍半萜presilphiperfolan-8β-ol (1)、Δ6-protoilludene (2)、longiborneol (3)开展了研究,解析了这三个倍半萜环化酶BcBOT2、DbPROS、CLM1的晶体结构。这些环化酶晶体结构中均含有底物类似物BTAC和镁离子,揭示了活性口袋中参与催化反应的关键氨基酸残基。基于上述三个酶的复合物晶体结构,研究团队通过量子力学/分子力学(QM/MM)分析,分别探究了三种环化酶催化FPP到化合物1–3的环化过程,揭示了从FPP到最终产物之间各个碳正离子中间体与酶的相互作用细节。虽然三个酶都是催化FPP首先产生1, 11位的碳-碳键连接,但它们活性口袋中不同类型氨基酸通过π-cation、dipole-cation等相互作用稳定不同碳正离子,使它们通过不同的环化路径产生各自的单一终产物1–3。为了进一步确证1–3的环化过程,研究团队开展了FPP中多个位置的2H和13C同位素标记实验,对环化过程中氢负离子迁移、烷基迁移、脱质子等过程进行了准确的锚定。
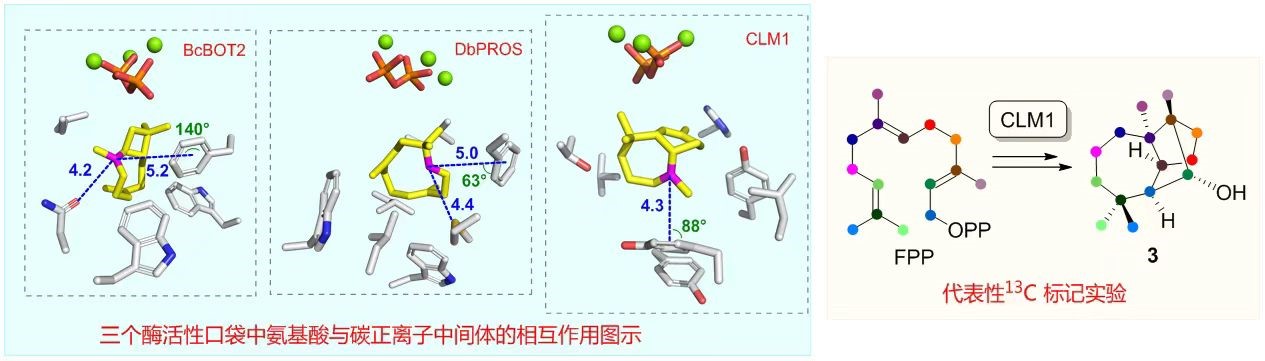
图2. 活性口袋关键氨基酸与碳正离子中间体的相互作用和同位素标记实验
基于上述揭示的环化机制,研究团队开展了三种环化酶BcBOT2、DbPROS、CLM1的理性改造,针对环化过程中对碳正离子中间体起稳定作用的氨基酸、或者参与形成紧密活性口袋形状的氨基酸进行定点突变,可以打开特定碳正离子中间体衍生的旁路路径,产生了一系列不同骨架的倍半萜旁路产物(4–20)。这些与原产物1–3不同环系的旁路产物扩展了结构多样性,并且它们是一些重要活性倍半萜的生物合成前体或化学合成原料。
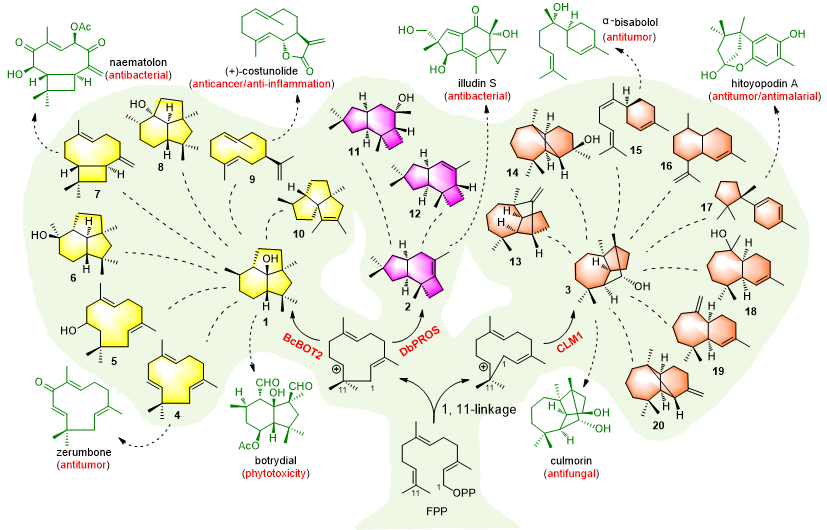
图3. 三个环化酶的原产物1–3以及酶工程改造后产生的不同骨架产物4–20,以及可以进一步制备的活性倍半萜化合物(绿色显示)
该研究揭示了多环倍半萜环化酶催化的一些普遍性规律,比如环化酶在长期的进化中已经能够跟环化过程中的每个中间体或者过渡态完美结合,并且这种结合非常紧密,避免了旁路产物的产生,使环化路径流向单一的倍半萜终产物;而通过对特定氨基酸的突变可以打开旁路路径,将单一产物的酶改造成多个产物的酶,这种单一产物和多个产物之间的切换对于倍半萜环化酶的从头设计和理性改造提供了依据。另一方面,该研究通过酶工程改造得到的倍半萜化合物在野生资源中含量低微,有的以挥发油混合物形式存在,难以高效地提取和分离,而它们的化学全合成大多步骤繁琐;因此通过特定环化酶突变体的催化可以实现这些化合物的定向制备,为更多药用倍半萜衍生物的合成生物学研究奠定基础。
北京大学药学院硕士生娄婷婷、李安南(晶体结构解析、突变改造和化合物制备),德国波恩大学Houchao Xu(同位素标记),中山大学药学院硕士生潘井峰(能量计算)为本论文第一作者。北京大学药学院马明研究员、杨东辉研究员,波恩大学Jeroen S. Dickschat教授,中山大学药学院巫瑞波教授为共同通讯作者。
原文链接:https://doi.org/10.1021/jacs.3c00278
第一作者:
?
娄婷婷 硕士生 ?李安南 硕士生
通讯作者简介:

马明,北京大学药学院、天然药物及仿生药物国家重点实验室研究员,博士生导师。研究领域为天然药用分子的生物合成、酶的三维结构及其催化机制、天然产物合成生物学。近5年以通讯作者在JACS、Angew. Chem. Int. Ed.、ACS Catal.、Chem. Sci.、Acta Pharm. Sin. B.等国际学术期刊发表SCI论文19篇。任中国药学会海洋药物专业委员会委员、中华中医药学会青年委员会委员、北京药学会天然药物专业委员会委员。

杨东辉,北京大学药学院研究员,研究方向为天然药源分子的发现与生物合成。以通讯作者在JACS、Angew. Chem. Int. Ed.、Commun. Chem.、Org. Lett.、J. Org. Chem.、J. Nat. Prod.、等本领域权威期刊发表学术论文28篇。担任世中联中药化学专业委员会常务理事、中西医结合学会分子生药学专业委员会委员、中国民族医药学会药用资源委员会理事。
(北京大学药学院)