
-

生物通官微
陪你抓住生命科技
跳动的脉搏
南京医科大学,中科院Nature发文:精子发生中的新型核糖体能够产生精子特异蛋白组
【字体: 大 中 小 】 时间:2023年01月04日 来源:中科院
编辑推荐:
南京医科大学沙家豪、郭雪江团队与中科院生物物理所秦燕团队合作在Nature上发表了文章 “A male germ-cell-specific ribosome controls male fertility”,发现精子发生中的新型核糖体(RibosomeST)能够产生精子特异蛋白组。
核糖体是最重要的聚合酶之一,以信使RNA(mRNA)为模板,氨酰化tRNA(aa-tRNA)为底物,合成蛋白质的工厂。核糖体在每个哺乳动物的细胞中有百万至千万的拷贝【1,2】。核糖体本身也占有细胞的大量物质占比,核糖体RNA(ribosomal RNA, rRNA)占所有细胞类型中总RNA的80-85%,核糖体蛋白(ribosomal protein, rProtein)在哺乳动物中占总蛋白量的5-10%,总蛋白拷贝数的10-20%【1】(图1)。
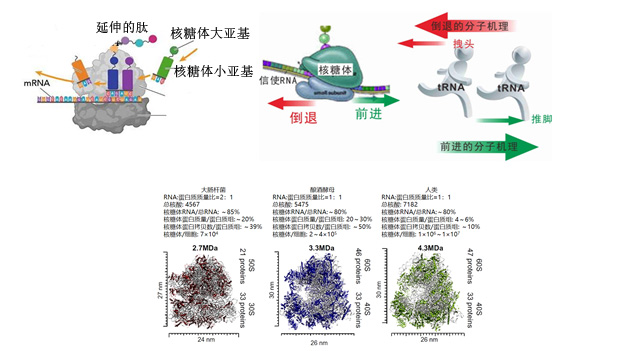
图1.核糖体结构图与核糖体参与蛋白质合成工作原理图
(A) 核糖体以信使RNA(mRNA)为模板,氨酰化转运RNA(aa-tRNA)为底物,合成蛋白质的工厂。(B)tRNA在核糖体内移动,是蛋白质合成工厂中生产线上的物流【3,4】 (C)核糖体的基本结构与细胞内拷贝数、占有物质的比例【1】
2022年12月14日,南京医科大学沙家豪、郭雪江团队与中科院生物物理所秦燕团队合作在Nature上发表了文章 “A male germ-cell-specific ribosome controls male fertility”,发现精子发生中的新型核糖体(RibosomeST)能够产生精子特异蛋白组。

核糖体为直接20~30nm的近球体,在细胞的高分辨成像中,可以看到核糖体的广泛分别(图2)。在快速增殖的细胞中,核糖体占有的物质、能量比例更高,组织细胞发生发展、决定细胞命运 (秦燕课题组2022年7月在Science Bulletin综述【5】)。特殊的核糖体能够产生特殊的蛋白组,从而决定细胞的功能和命运,是近年来的重要命题,对理解细胞功能的主要载体-蛋白质的产生,是追根溯源的问题:核糖体如何决定蛋白组。
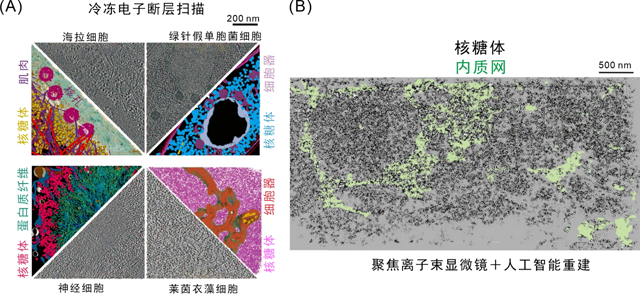
图2.(A)冷冻电子显微镜呈现的不同细胞原位状态下的核糖体。(B)聚焦离子束显微镜结合人工智能技术重塑细胞成分。【3】
在雄性生殖细胞中,核糖体大亚基蛋白L39,在精子发生的减数分裂后会发生转移并使用L39L的形式在核糖体上。该研究发现L39是核糖体大亚基新生肽链通道上的重要成分,L39L替换L39后,这个通道可以变宽很多,有利于精子成熟中大量正电蛋白的产生。那么核糖体L39如何决定精子生殖蛋白组?
研究人员通过L39L型核糖体(RibosomeST)和普通L39型核糖体(Ribosome)的超分辨cryo-EM结构解析(分辨率在L39的2.82埃,L39L的3.03埃),发现核糖体大亚基新生肽链通道上的重要成分,L39L替换L39后,这个通道可以变宽很多,有利于精子成熟中大量正电蛋白的产生。
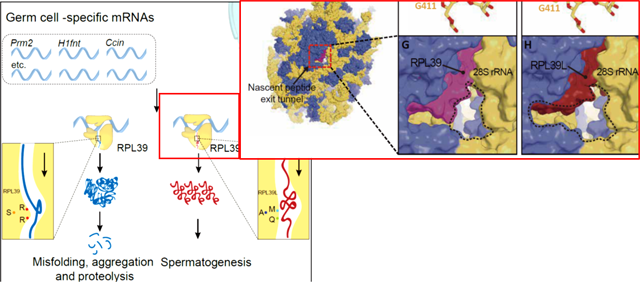
图3 精子发生中的特殊核糖体-ribosomeST, 由L39L(右图,红色蛋白)替换普通的L39(右图,紫色蛋白),导致核糖体新生肽链通道变宽,有助于精子发生中大量带正电新生肽链的产生。
精子发生是物种繁衍的核心功能,少弱精症是近年来的重要国民健康问题,该研究将会为相关疾病提供重要标记物和治疗靶点。
文章链接:https://www.nature.com/articles/s41586-022-05508-0
参考文献:
1. An, H., and Harper, J. W. (2020) Ribosome Abundance Control Via the Ubiquitin-Proteasome System and Autophagy. J Mol Biol 432, 170-184
2. An, H., Ordureau, A., Korner, M., Paulo, J. A., and Harper, J. W. (2020) Systematic quantitative analysis of ribosome inventory during nutrient stress. Nature 583, 303-309
3. Wang, Q., Wang, Y. B., Li, S. G., Zhou, A. Q., and Qin, Y. (2022) Organelle biogenesis: ribosomes as organizer and performer. Science Bulletin 67, 1614-1617
4. Liu, G., Song, G., Zhang, D., Zhang, D., Li, Z., Lyu, Z., Dong, J., Achenbach, J., Gong, W., Zhao, X. S., Nierhaus, K. H., and Qin, Y. (2014) EF-G catalyzes tRNA translocation by disrupting interactions between decoding center and codon-anticodon duplex. Nat Struct Mol Biol 21, 817-824
5. Zhang, D., Yan, K., Liu, G., Song, G., Luo, J., Shi, Y., Cheng, E., Wu, S., Jiang, T., Lou, J., Gao, N., and Qin, Y. (2016) EF4 disengages the peptidyl-tRNA CCA end and facilitates back-translocation on the 70S ribosome. Nat Struct Mol Biol 23, 125-131