
-

生物通官微
陪你抓住生命科技
跳动的脉搏
Nature子刊:推翻旧理论,直指新一代阿尔兹海默症研究方向
【字体: 大 中 小 】 时间:2022年06月22日 来源:精准医学
淀粉样蛋白不是阿尔茨海默病的原因。
长期以来,阿尔茨海默病是神经细胞外β-淀粉样蛋白沉积所致的概念深入人心,关于降低β-淀粉样蛋白的药物研究也很多。
但纽约大学格罗斯曼医学院和内森克莱恩研究所最近的一项研究推翻了这一观点。
他们在《自然神经科学》(Nature Neuroscience)上发表的一篇文章认为,神经细胞内溶酶体的“酸化”紊乱是导致细胞外β淀粉样蛋白增加的罪魁祸首,从而导致阿尔茨海默病(AD)。

有研究发现,阿尔茨海默病的发生是由神经细胞内自噬溶酶体功能障碍引起的,更准确地说,是“酸化”障碍,而这一切都始于自噬溶酶体功能障碍。
自噬溶酶体是由自噬体和溶酶体融合形成的。像一个自动的细胞垃圾处理系统,自噬小体运输细胞内受损的蛋白质,核酸,细胞器等,酶降解这些物质。
通常情况下,溶酶体内部为酸性(pH值4.2-5.3),内部的酶只有在这种酸性环境下才能正常工作。
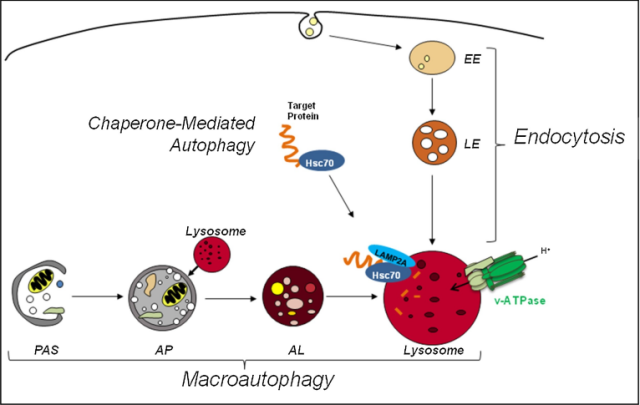
溶酶体自噬和内吞途径。
一旦溶酶体酸化受阻,包括β淀粉样蛋白和β淀粉样前体蛋白(APP)代谢物APP-βCTF在内的蛋白质就难以清除,只能在溶酶体中积累,而自噬泡也会源源不断地将细胞废物输送到溶酶体中。
随着溶酶体中细胞废物的积累,当它无法承受时就会破裂,进一步导致细胞解体,释放β -淀粉样蛋白到组织环境中,造成阿尔茨海默病的典型特征“细胞外斑块”"
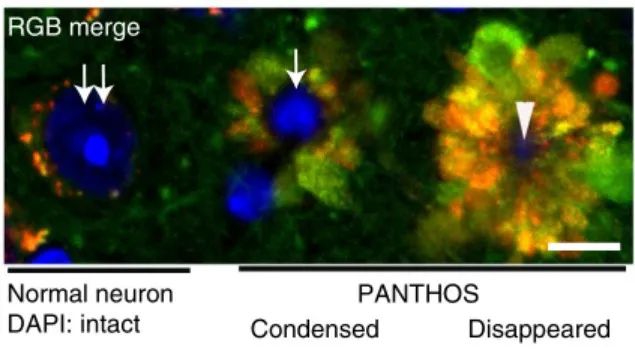
这一理论已经在阿尔茨海默病模型小鼠中得到验证。出生后5个月,大脑新皮层中90%的自噬溶酶体已酸化,高于脑淀粉样斑块。时间(10-12个月),至少提前5个月。
早发性阿尔茨海默病模型5xFAD小鼠的时间更早,在2月龄的5xFAD小鼠的大脑中可以发现酸化受损的自噬溶酶体和神经元变性现象。
溶酶体的酸化调控主要依赖于质子泵v-ATPase以及离子转运体介导的溶酶体膜内阴离子和阳离子的运动。
质子泵v-ATPase是一种依赖于ATP的质子泵,它能将H+离子从细胞质泵入溶酶体,维持酸性环境。
但是v-ATPase是一个电泵,它产生的梯度必须通过阳离子流出和/或阴离子输入来消散,以保持H+的连续输入。
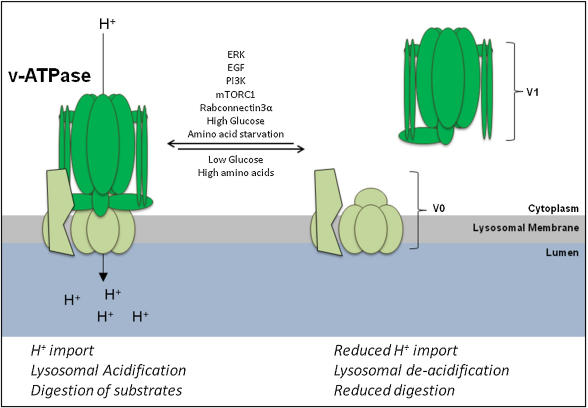
v-ATPase通过ATP依赖的质子转运跨溶酶体膜促进溶酶体酸化。
相应的,早发性阿尔茨海默病模型5xFAD小鼠神经元溶酶体的质子泵vATPase活性在6个月时显著低于同年龄野生型小鼠(65.6±4.1%),到12个月时则不到野生型小鼠的一半(45.3±3.7%)。
根据上述研究,只要恢复神经细胞内溶酶体的酸化功能,就有可能治疗阿尔茨海默病。
一些研究人员在果蝇实验中发现,果蝇v-ATPase亚基的功能丧失突变会导致蛋白质降解失败和衰老依赖性神经退行性变。
也许这就是下一代阿尔茨海默病药物的研究方向。
中国也有一些团队做出了不同的选择。
南开大学的研究团队开发了一种改良的溶酶体,用于制备治疗性蛋白质错误折叠或处理疾病。将脑小胶质细胞来源的溶酶体注射到小鼠的尾静脉。
溶酶体可以促进阿尔茨海默病小鼠大脑中表达的有毒蛋白的降解,而不存在失活或神经毒性,也是一种治疗选择。