
-

����ͨ��
����ץס�����Ƽ�
����������
�ɶ�������������1, 4-������वIJ��Գƺϳ��о��л���½�չ
�����壺 �� �� С �� ʱ�䣺2022��04��09�� ��Դ���й���ѧԺ�ɶ������о���
�༭�Ƽ���
���� ���о��ԡ� Chiral Phosphoric Acid Catalyzed Enantioselective Desymmetrization of 1,4-Dihydropyridines by C(sp3)-H Bromination ��Ϊ�ⷢ���� Angewandte Chemie International Edition �ڿ��ϣ�ͬʱ��Ӧ�ɹ�Ҳ����ר��
1��4-�����������й㷺��������ԣ���������Ҫ������Ч��Ca2+ͨ����������ĿǰΪֹ���г����ж���1��4-���������ṹ��ҩ��ɹ����ѡ����������ƽ����Ⱥ��ƽ��������ƽ��������ƽ�������ƽ�����ȵ�ƽ�ȡ�����Щ���㷺ʹ�õ�ҩ���У����ȵ�ƽ��������ƽ��ʮ����һֱ�������������ҩ������������öȻ���֯ѡ���ԵȲ�ͬ���ʣ��Ѿ���������������ҩ��ı���Щҩ�����ʵļ������Ǹı�ȡ������ͬʱ����ͬ�Ķ�ӳ����ֳ���ͬ�������෴�Ļ��ԡ���ϸ������Щҩ����ӽṹ���֣���Щҩ����Ӵ־���Hantzsch-type�ṹ���ͣ���3��5λ������ȡ����2��6λ�����ȡ����N-H���룬Ŀǰȱ����Ч���Ʊ�������
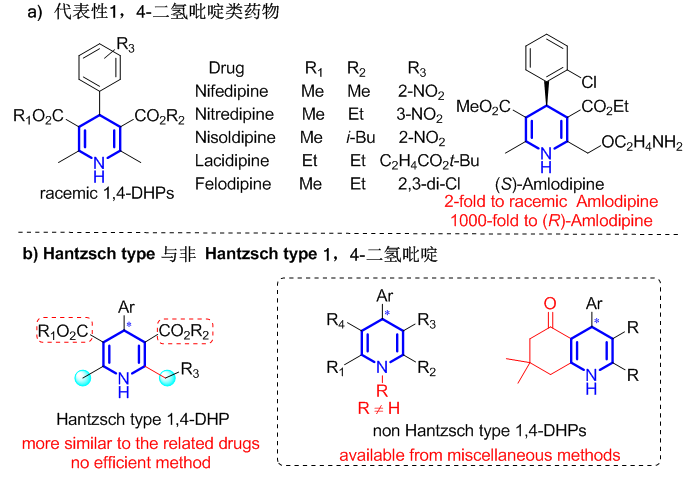
������������ѧ���Ե�1��4-������������
���գ��й���ѧԺ�ɶ������о����������ѫ�Ŷӷ�չ��һ�������������C(sp3)�CH��ӳѡ����ȥ�Գ������Ӧ���������õĶԳ�1��4-��������������2��6λ��ȥ�ԳƵ�����������Ӧ������1��4-������ड�
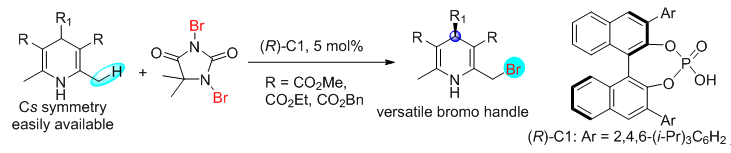
����ȥ�Գ�����ϳɲ����Ʊ�����1��4-�������
�����������£����߶�4-λ��ȡ��������ϵͳ���죬���ָ���ȡ�����������ӻ���ȡ��ϩ����������ܺܺõķ�Ӧ�õ���Ӧ�����Բ��ͬʱ������Ҳ������3��5-λ������������λ��ϴ���л�Ҳ�ܼ��ݵķ�Ӧ�õ���Ӧ�����Բ��
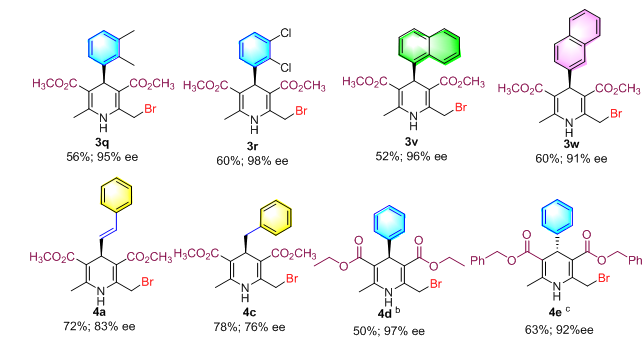
����1��4-������व����������о�
���⣬���������ò����������ϵͳ�о������ȣ����������Է���������ȡ����Ӧ�õ���Ӧ������1��4-������ण������ǿ����������������ͨ��Clik��Ӧ���뵪����Σ������������Ե�1��4-��������ܺܺõ������������ϳɾ��������ԵĶ�ȡ��4-������ड��÷�������Ч�ϳ�DPP4���Ƽ������߶Է�Ӧ�������г���̽���������漰1��4-�������ϩ��˫���Ķ�ӳѡ����������Լ�������[1-3]-BrǨ�ơ�
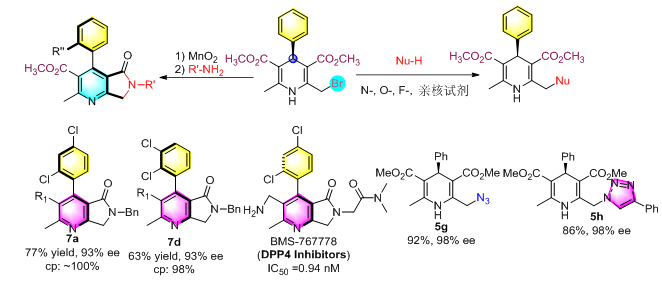
�����������ϳ�Ӧ���о�
�Գ��Ե�Hantzsch type 1,4-������ि���ͨ��Hantzsch��Ӧ��Ч��á��ڸ��о��ԶԳ���1��4-�������Ϊ���ͨ��C(sp3)�CH��ӳѡ����ȥ�Գ�������ԣ�������C-H��ת��Ϊ�������ε�C-Br�����ϳɶ�������1��4-������ड�ͬʱ�������������ܺܺõ�ת��Ϊ�����ԡ��÷���Ϊ���й㷺����ѧ���Ե�1��4-������व��о����Ʊ��춨�����õĻ�����
���о��ԡ�Chiral Phosphoric Acid Catalyzed Enantioselective Desymmetrization of 1,4-Dihydropyridines by C(sp3)-H Bromination��Ϊ�ⷢ����Angewandte Chemie International Edition�ڿ��ϣ�ͬʱ��Ӧ�ɹ�Ҳ����ר�������о��õ��й���ѧԺ���괴�´ٽ��ᡢ�й���ѧԺ����֮���˲�A�ࡢ�Լ��Ĵ�ʡ�Ƽ������������ط���Ŀ��2021ZYD0061����֧�֡�
 ����ͨ�Ź��ں�
����ͨ�Ź��ں�
֪����ҵ��Ƹ