
-

生物通官微
陪你抓住生命科技
跳动的脉搏
清华大学《Nature》揭示PIEZO1在脂膜上的张力感受机制
【字体: 大 中 小 】 时间:2022年04月08日 来源:清华大学药学院
编辑推荐:
近期,清华大学药学院肖百龙团队与生命学院李雪明团队合作首次解析了机械力受体PIEZO1在脂膜环境中的受力形变过程,定量了其皮牛尺度的机械敏感性,建立了其曲率感知理论学说,从根本上解答了其将物理机械刺激转化成生物电信号这一核心科学问题
近期,清华大学药学院肖百龙团队与生命学院李雪明团队合作首次解析了机械力受体PIEZO1在脂膜环境中的受力形变过程,定量了其皮牛尺度的机械敏感性,建立了其曲率感知理论学说,从根本上解答了其将物理机械刺激转化成生物电信号这一核心科学问题。

机械力感知决定我们的日常行为,例如握手、拥抱、亲吻、行走、刷手机、血压飙升等。力是无形的,那我们人体如何感知?直到2010年,Ardem Patapoutian教授团队报道了一类介导人体机械力感知的分子受体—PIEZO蛋白,为我们认识了解这一基本的生物学问题带来了突破。因为发现PIEZO并证明其触觉受体的功能,Ardem Patapition与David Julius教授(温度受体发现者)分享了2021年诺贝尔生理学或医学奖(图1)。
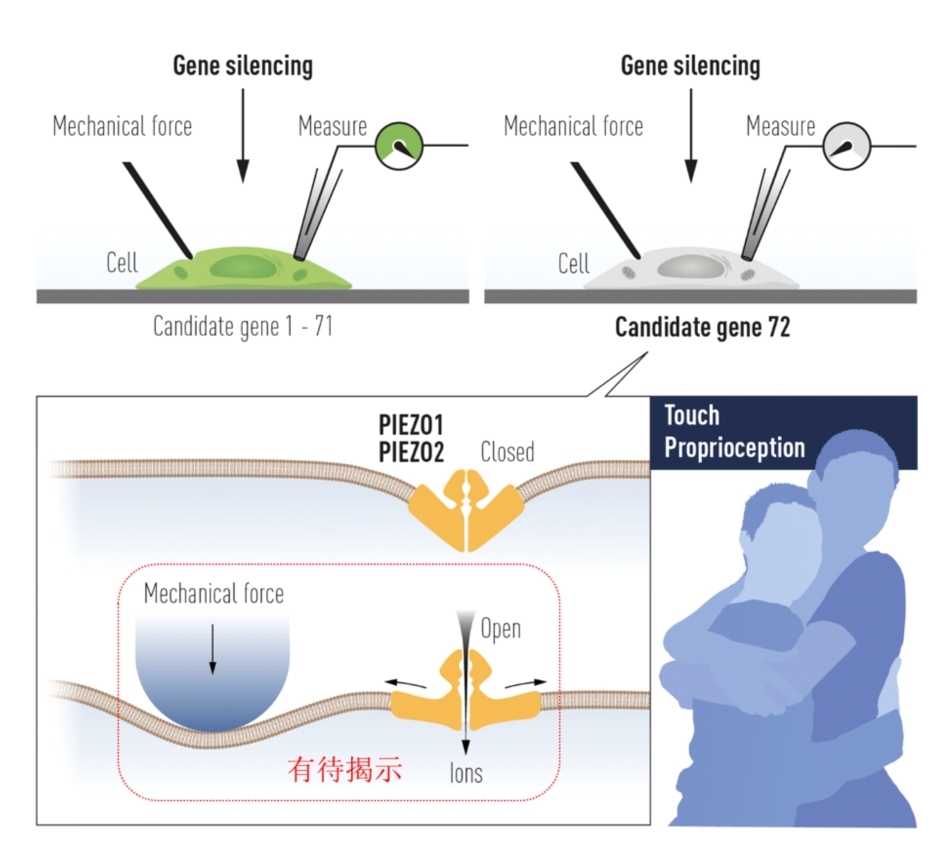
图 1 2021诺贝尔生理学或医学委员会发布的示意图总结了PIEZO的发现(上半部分)、所介导的触觉、本体觉感知等生理病理功能(下半部分右侧)、以及结构模型与机械力感知假说猜想(下半部分左侧)。
那么PIEZO蛋白又是如何将物理机械刺激转化成生物电信号的呢?肖百龙及其团队近10年致力于解答这一核心科学问题。其于2012年在Patapoutian课题组从事博士后研究期间首次证实了PIEZO蛋白是在哺乳动物中鉴定发现的首类机械门控阳离子通道(Nature 2012);随后其课题组与合作者在PIEZO的结构功能机制研究方面取得了一系列重要研究进展,帮助推动了PIEZO的发现与研究成为了2021年的诺贝尔生理学或医学奖研究成果(图2)。

图 2 PIEZO的机械力感知分子机制研究进展总结。
基于肖百龙与李雪明课题组合作解析的PIEZO家族成员PIEZO1(Nature 2018)与PIEZO2(Nature 2019)的三维结构[MacKinnon以及Patapoutian & Ward课题组也同时报导了PIEZO1的结构(eLife 2017; Nature 2018)]以及机制研究(Neuron 2016; Neuron 2020),研究者们提出了PIEZO的机械力感知机制猜想:
PIEZO形成三聚体三叶螺旋桨状离子通道,中心是负责离子通透的孔道部分,外周是三个负责机械力感知的桨叶部分(图1及图3左侧)。非常有趣的是,在孔道处于关闭态,嵌在细胞膜中的桨叶呈现往细胞外高度弯曲的状态,提示其可以弯曲其所在的细胞膜,形成我们称之为纳米碗(nanobowl)状的PIEZO-脂膜体系(图1及图3右侧)。有研究显示PIEZO1蛋白可以在受力刺激下发生可逆的形变(Nature 2019)。基于这些结构功能研究,研究者们提出当细胞膜张力改变时,PIEZO可以从弯曲状变为平展状,带动中间的孔道开放,从而将机械力刺激转化为阳离子流通。

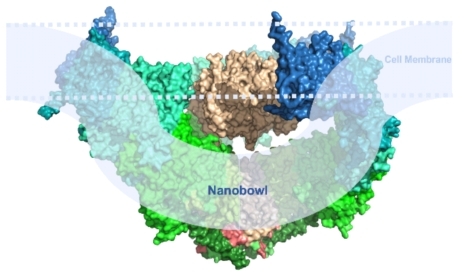
图 3 PIEZO通道的三聚体三叶螺旋桨状(左侧部分,俯视图)与纳米碗状(右侧部分,平视图)三维结构。
但事实上,在2021年诺奖颁布时,研究者们还未能解析出PIEZO受力开放的结构。膜上PIEZO在受力后是否如诺奖示意图中所展示的一样(图1),从弯曲的关闭态进入平展的开放态?这是PIEZO诺奖研究的未解之谜。
得益于冷冻电镜在生物大分子结构解析方面的技术突破,研究者们可以解析出蛋白在静息、游离状态下的结构。但是,生物大分子并不是靠“呆若木鸡”的状态来发挥功能,其千姿百态的变化才是生命奥妙所在,而这些变化往往取决于其组装形式、配体结合和所处的物理状态(膜环境、电势能、温度和力等)。如何在严苛的冷冻样品状态下,引入无形的膜张力来获取PIEZO的不同结构功能状态呢?
肖百龙与李雪明指导四位博士生杨旭中、林超、陈旭东、李首卿对这一极具挑战的科学问题开展研究,借鉴前人把膜蛋白重组进脂质体中,并用冷冻电镜解析其结构的技术(Nature 2009; PNAS 2020),经过反复尝试、摸索,最终首次建立了膜上受力结构解析体系(图 4)。该策略的核心是通过蛋白与脂质体之间的曲率差异(curvature mismatch)来引入膜张力,这对PIEZO蛋白尤为适用,因为PIEZO的114个跨膜结构域形成的跨膜区并不在一个平面上,而是形成纳米碗状的凹陷结构(图3)。

图 4 PIEZO1-脂质体冷冻电镜三维结构解析。
PIEZO1本身的曲率半径接近10 nm,其主要以outside-in的方式重组到脂质体中。在同等大小的脂质体中时,曲率相符呈圆形。当它重组进更大的脂质体中时,曲率半径的差异在两者间产生力,蛋白和膜发生形变,呈水滴状(图4c)。
而当一小部分PIEZO1以outside-out的方式重组到脂质体中(图4b箭头所示),PIEZO1蛋白与脂质体的曲率半径朝向截然相反,膜与蛋白间产生的的作用力变大,导致PIEZO1蛋白处于受力展平的构象状态(图4d)。
研究者们最终得到PIEZO1在膜上契合状态(10 nm曲率半径)和受力展平的两种结构,分别命名为弯曲(Curved)和平展(Flattened)构象,佐证了PIEZO1蛋白具备可逆形变和感知脂膜曲率变化的特殊能力(图5)。
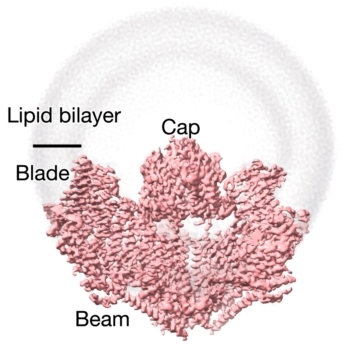

图 5 PIEZO1的弯曲(左侧)和平展状(右侧)三维结构。
通过比较PIEZO1在脂膜上弯曲和平展的两种结构,研究者们对PIEZO1感受膜张力后的动态构象变化、形变参数进行了定量分析,不仅验证了之前所提出的作用机制假说,并定量了PIEZO1的皮牛尺度的机械敏感性,进而建立了其曲率感知理论学说(图6)。
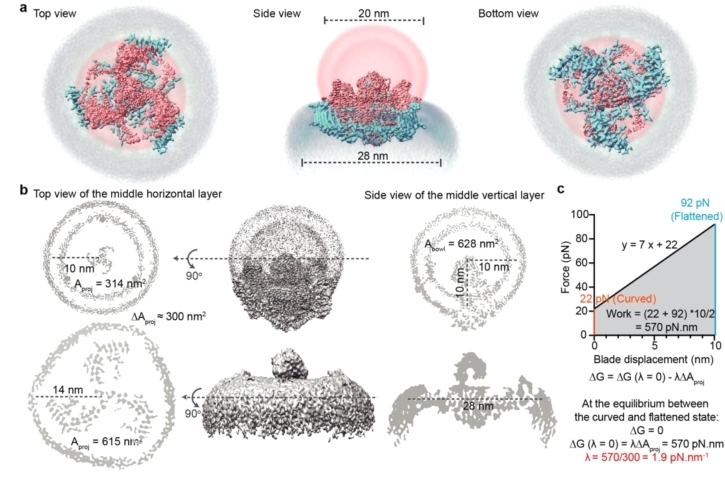
图 6 PIEZO1-liposome从弯曲状到平展状的形变参数测量以及机械敏感性计算。
• PIEZO1的受力形变:Piezo1在受力展平过程中,其末端有10 nm的向下位移、所占膜面积扩张了300 nm2 (图6a, b)。
• 力的感知机制—曲率形变特性:Scheuring与Mackinnon团队合作通过原子力显微镜测得PIEZO1下压距离和所需力之间存在线性弹性关系y=7x+22 (Nature 2019)。引用该公式与自由能变化公式(图6c),10 nm的位移可得出PIEZO1弯曲和平展状态之间存在570 pN.nm的能量垒。而Nanobowl储存了高达300 nm2的膜面积,意味着只需1.9 pN/nm的张力就能实现570 pN.nm做功,这与电生理测量值1.4 pN/nm接近(eLife 2015)。
• 力的传导机制—纳米杠杆原理:力从外周传递到中央孔道区。在展平过程中,胞内Beam长杆在接近中心孔道模块区形成kink,符合之前提出的该位点承担支点的功能推测(图7)。基于省力杠杆原理,Beam不仅具有力的传递与放大功能,且具有形变缓冲作用,使长臂末端3 nm的形变缩小到短臂端1 nm的形变,使其既能控制中央孔道区的门控,又不导致其过度的扩张,从而维持PIEZO通道的阳离子选择性通透能力。
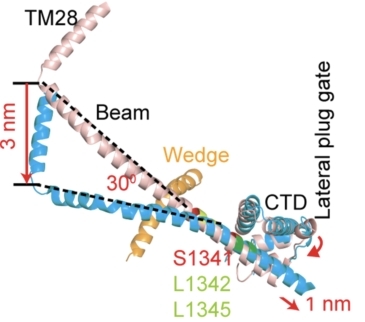
图 7 PIEZO1的纳米杠杆传递机制。
• 力的门控机制—帽子运动,跨膜疏水门打开:PIEZO1受力展平时,使得胞外帽子与桨叶之间的相互作用被打破,帽子发生顺时针旋转,下方的跨膜孔道区发生扩张。与PIEZO2(灰色)紧闭的跨膜区疏水门相比,PIEZO1 展平状态的结构呈现10埃的扩张(图8)。
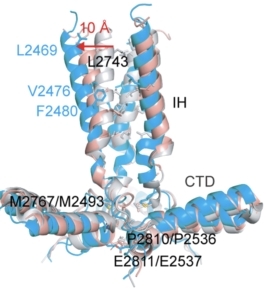
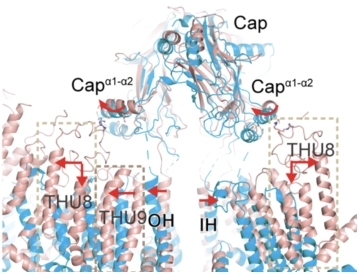
图 8 PIEZO1的帽子-跨膜疏水门孔机制。
综上,研究者们总结出PIEZO通道的受力形变与门控机制(图9)。
• 在静息状态时,PIEZO1使脂膜发生弯曲,形成碗表面积为628nm2、投影面积为314nm2的纳米碗系统,PIEZO1与脂膜处于平衡。
• 膜张力改变时,平衡被打破,膜带动着PIEZO1蛋白一起展平。
• 展平的桨叶带动胞内侧的Beam发生杠杆运动,把形变传递到孔道区胞内侧,可能通过门闩-拴锁机制,打开三个侧向出口闸门(Lateral plug gate),让离子流入细胞 。
• 展平的桨叶使其与帽子之间的相互作用被打破,帽子的旋转运动,加上桨叶的展平运动,共同使得孔道区上半段的疏水阀门打开,离子则由帽子下的空隙,侧向进入孔道。
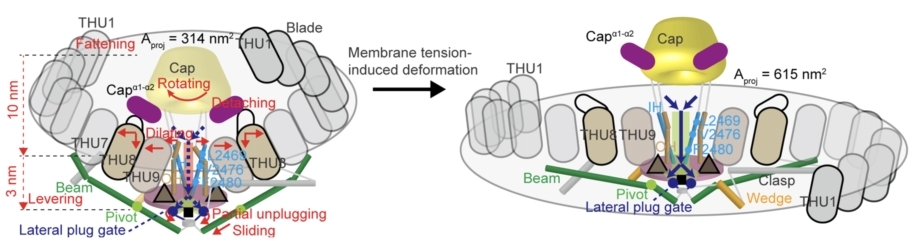
图 9 PIEZO1的受力形变与门控机制模式图。
总结而言,本研究首次实现了对机械力受体PIEZO1通道在脂膜上受力状态下的动态结构解析,揭示了其受力形变与脂膜曲率感知的特性,定量了其皮牛尺度的机械敏感性,建立了其曲率感知理论学说,从根本上解答了其将物理机械刺激转化成生物电信号这一PIEZO诺奖研究的未解之谜。无形的力在物理上可被定义为受力对象的形变。而PIEZO正是利用其纳米尺度的曲率形变去探测皮牛尺度的力,从而成为一类低能耗的超敏机械力感受器,不由让研究者们惊叹生命过程与物理原理的交汇之美!
以上论文于2022年4月6日在《自然》期刊在线刊登,标题为《PIEZO1在脂膜中的结构形变与曲率感知》(Structure deformation and curvature sensing of PIEZO1 in lipid membranes)。
肖百龙教授、李雪明研究员为本论文的共同通讯作者,博士研究生杨旭中、林超、陈旭东、李首卿为共同第一作者。该研究得到了国家科技部“2030科技创新-脑计划与类脑计划”重大研究项目、国家自然科学基金委杰青项目以及重点项目、清华-北大生命科学联合中心、膜生物学国家重点实验室、高精尖结构生物学中心、生物结构前沿研究中心的项目经费支持。感谢清华大学冷冻电镜平台和蛋白质制备与鉴定平台;王宏伟教授团队刘楠、徐洁提供石墨烯载网;闫创业研究员团队分享deep-2D脚本;张馨予、赵天放开发EPicker软件;以及王莉、周珩、姚霞、范潇、雷建林、李晓敏博士给予技术上的帮助。
原文链接:https://www.nature.com/articles/s41586-022-04574-8