
-

生物通官微
陪你抓住生命科技
跳动的脉搏
微生物所冯婕团队在碳青霉烯耐药机制方面取得新进展
【字体: 大 中 小 】 时间:2022年03月29日 来源:中国科学院微生物研究所
编辑推荐:
上述研究为细菌碳青霉烯耐药提供了新的视野,成果已经发表在mBio 期刊上(DOI: 10.1128/mbio.03340-21 ),题为“IS26 veers genomic plasticity and genetic rearrangement toward carbapenem hyperresistance under sublethal antibiotics”

碳青霉烯类耐药肠杆菌科细菌(CRE)的全球传播对公共卫生系统构成了严重的威胁。肠杆菌科细菌主要通过获得碳青霉烯酶来产生耐药性,其中肺炎克雷伯菌碳青霉烯酶(KPCs)最为普遍。产KPCs的CRE已在世界范围内传播,通常伴随着多重耐药性,并成为院内相关感染(HAIs)发病率和死亡率增加的主要原因。更加棘手的是,产KPCs的CRE在常规实验室筛查中往往表现出低水平耐药性,导致误诊或漏诊从而影响治疗效果。虽然不稳定的基因扩增已被认为是导致临床菌株耐药性被低估的关键因素,但迄今为止,由blaKPC-2扩增介导的碳青霉烯类耐药性的确切机制,以及联合用药对于这种耐药的治疗评估仍然还是空白。
中国科学院微生物研究所冯婕团队前期通过流行病学分析揭示了病原菌大肠杆菌ST131通过获得不同类型携带blaKPC-2基因的质粒导致其在院内大规模流行(Front Microbiol,2020)。近期,该团队针对其中一起治疗失败的案例进行深入研究,发现了一株携带blaKPC-2基因的大肠杆菌可以在接触亚致死浓度抗生素后迅速变为高耐药表型,这解释了患者在接受抗生素治疗后死亡的关键原因。进一步研究发现,高耐药的发生是由于插入序列IS26介导的包括blaKPC-2基因在内的多重耐药(MDR)区动态且不稳定的扩增导致的,这种机制可以帮助细菌来逃避碳青霉烯类抗生素的攻击,同时也是CRE逃逸实验室体外耐药检测的重要策略,进而影响抗生素在临床应用中的使用和疗效。另外,该团队评估了联合用药策略的体外治疗效果,实验发现不恰当的药物联用不但不能阻止多重耐药区扩增,反而在一定程度上增加了基因扩增的速率,使后续的治疗更加困难,这对临床用药具有重要的指导意义。
上述研究为细菌碳青霉烯耐药提供了新的视野,成果已经发表在mBio期刊上(DOI: 10.1128/mbio.03340-21),题为“IS26 veers genomic plasticity and genetic rearrangement toward carbapenem hyperresistance under sublethal antibiotics”。中科院微生物所冯婕课题组博士生魏大伟和汕头大学黄乃淇教授为共同第一作者,冯婕研究员为通讯作者。该研究得到了国家自然科学基金委的资助。
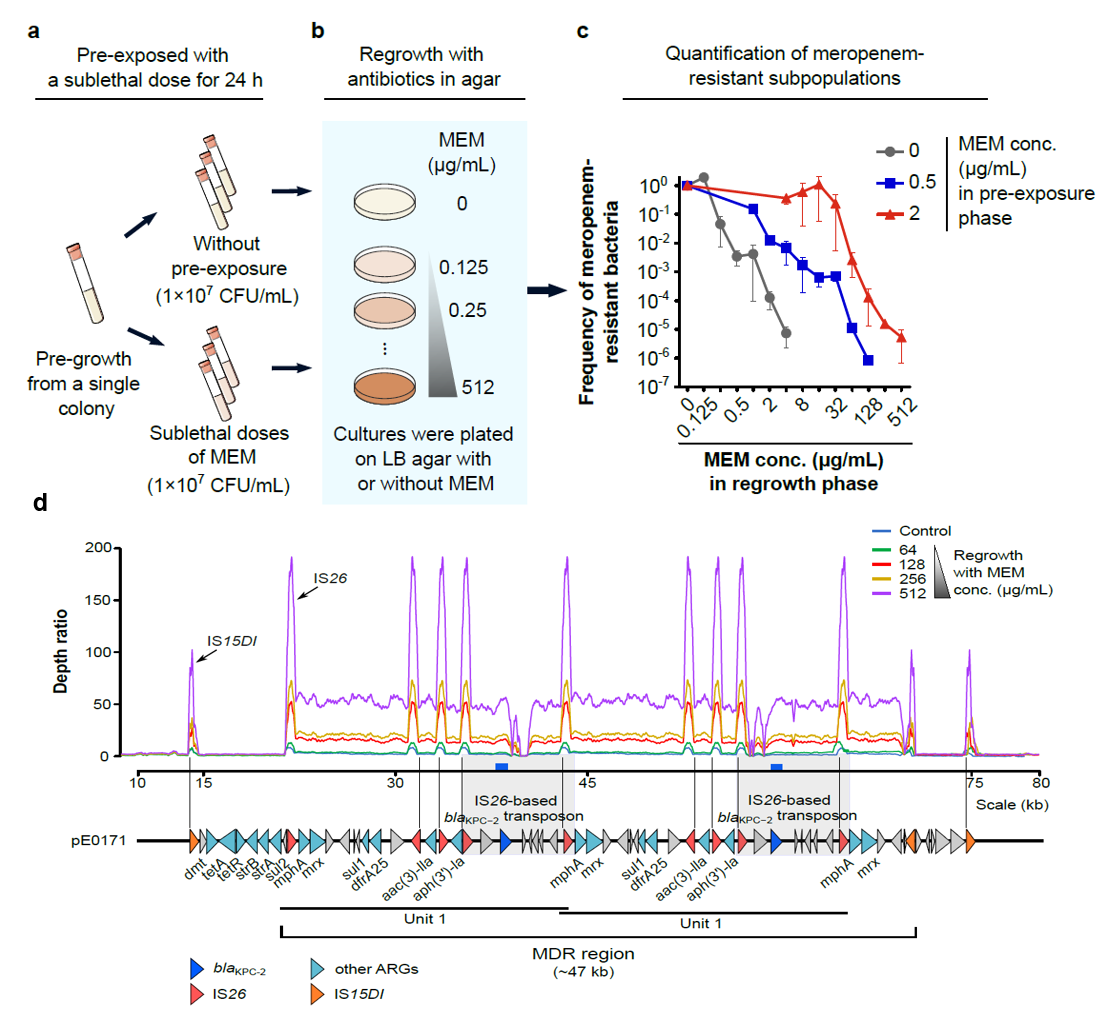
图1 接触亚致死抗生素后菌株通过基因扩增迅速增加碳青霉烯耐药性
10x Genomics閺傛澘鎼isium HD 瀵偓閸氼垰宕熺紒鍡氬劒閸掑棜椴搁悳鍥╂畱閸忋劏娴嗚ぐ鏇犵矋缁屾椽妫块崚鍡樼€介敍锟�
濞嗐垼绻嬫稉瀣祰Twist閵嗗﹣绗夐弬顓炲綁閸栨牜娈慍RISPR缁涙盯鈧鐗哥仦鈧妴瀣暩鐎涙劒鍔�
閸楁洜绮忛懗鐐寸ゴ鎼村繐鍙嗛梻銊ャ亣鐠佹彃鐖� - 濞e崬鍙嗘禍鍡毿掓禒搴n儑娑撯偓娑擃亜宕熺紒鍡氬劒鐎圭偤鐛欑拋鎹愵吀閸掔増鏆熼幑顔垮窛閹貉傜瑢閸欘垵顫嬮崠鏍掗弸锟�
 瀵洟顣悰灞肩瑹鑱絴鑱介懕姘卞妽妤癸妇澹掔紒妯挎皑娴狅綀闃跨紒鍕劅閺佺繝缍嬬憴锝呭枀閺傝顢�>>
瀵洟顣悰灞肩瑹鑱絴鑱介懕姘卞妽妤癸妇澹掔紒妯挎皑娴狅綀闃跨紒鍕劅閺佺繝缍嬬憴锝呭枀閺傝顢�>>  閵嗗苯銇囩亸蹇涚炊缁讳浇鍋涙稉搴′淮鎼撮顓搁悶鍡愨偓宥嗗瘹鐎靛吋鎹i幎銉礉閻愮懓鍤崡鍐插讲閸忓秷鍨傛0鍡楀絿閻㈤潧鐡欓悧鍫熷灗鐎圭偘缍嬪ù閿嬪Г>>
閵嗗苯銇囩亸蹇涚炊缁讳浇鍋涙稉搴′淮鎼撮顓搁悶鍡愨偓宥嗗瘹鐎靛吋鎹i幎銉礉閻愮懓鍤崡鍐插讲閸忓秷鍨傛0鍡楀絿閻㈤潧鐡欓悧鍫熷灗鐎圭偘缍嬪ù閿嬪Г>>  閹活厾顫濋崡鏇犵矎閼崇偞绁存惔锟�-濞e崬鍙嗘禍鍡毿掓潻娆撱€嶅锝呮躬閺€鐟板綁閹存垳婊戝鈧仦鏇狀潠鐎涳妇鐖虹粚鍓佹畱閹垛偓閺堬拷>>
閹活厾顫濋崡鏇犵矎閼崇偞绁存惔锟�-濞e崬鍙嗘禍鍡毿掓潻娆撱€嶅锝呮躬閺€鐟板綁閹存垳婊戝鈧仦鏇狀潠鐎涳妇鐖虹粚鍓佹畱閹垛偓閺堬拷>>  娑撴牜鏅拋妤€鎮昑hermo Fisher鐠ф盯绮鐐扮瑯鐏忔梻顫栭幎鈧幏娑滀粧Field Application Scientist閵嗕府arketing Develop缁涘浜存担宥忕礉鐠囷附鍎忕拠閿嬬叀閻鏁撻悧鈺呪偓姘眽閹靛秴绔堕崷鐑樼埉閻╊噯绱�>>
娑撴牜鏅拋妤€鎮昑hermo Fisher鐠ф盯绮鐐扮瑯鐏忔梻顫栭幎鈧幏娑滀粧Field Application Scientist閵嗕府arketing Develop缁涘浜存担宥忕礉鐠囷附鍎忕拠閿嬬叀閻鏁撻悧鈺呪偓姘眽閹靛秴绔堕崷鐑樼埉閻╊噯绱�>>  閸氼剝顕╂潻鍥ф偋閿涚喕绉存潻锟�14婢垛晛鐤勬宀€鐛ラ崣锝囨畱閼叉繆鍓扮紒鍡氬劒閿涳拷>>
閸氼剝顕╂潻鍥ф偋閿涚喕绉存潻锟�14婢垛晛鐤勬宀€鐛ラ崣锝囨畱閼叉繆鍓扮紒鍡氬劒閿涳拷>>  生物通微信公众号
生物通微信公众号
知名企业招聘
今日动态 | 人才市场 | 新技术专栏 | 中国科学人 | 云展台 | BioHot | 云讲堂直播 | 会展中心 | 特价专栏 | 技术快讯 | 免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号
