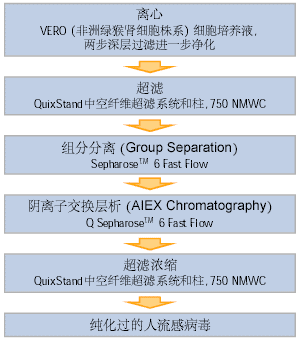
| 各地药审部门近年要求提高疫苗的安全性, 以降低副作用, 纷纷强制改进病毒疫苗的生产和纯化方法。例如,流感病毒疫苗的生产正开始用VERO 细胞取代鸡胚培养。纯化方法已放弃蔗糖密度梯度离心这类传统方法,而走向自动化程度更高、更易于在位清洗的超滤和液相层析技术。以下的人流感病毒疫苗纯化,是一种通用的病毒疫苗纯化策略。
象所有病毒一样,人流感病毒颗粒要比蛋白质、多肽、多糖、核酸分子大的多。首先将预处理过的上清液用QuixStand 或FlexStand 超滤系统配合750 kDa NWCO 中空纤维超滤柱来进行粗纯化和浓缩。中空纤维超滤膜的开放流路解决了病毒颗粒浓缩时易堵膜和对剪切力敏感易聚集的两大问题,提供了较柔和的超滤方法。
所得的流感病毒组分上装填了Sepharose 6 Fast Flow 的INdEX或BPG层析柱,在外水体积中得到人流感病毒(图1)。宿主细胞杂质及培养基成份,例如比病毒分子量小的核酸片段和蛋白质被滞留,并在稍后洗脱过程中被洗脱出来。过程约半小时,可连续多次上样。Sepharose 凝胶过滤层析本身是一种极温和的层析方法,保持病毒回收率。
Q Sepharose Fast Flow 阴离子交换层析可进一步精纯病毒:在上柱流穿部分得到人流感病毒,而核酸分子和其它带负电荷的杂质,如残留的血清蛋白被结合在层析介质上(图2)。由于病毒没有结合离子交换层析柱, 解决了病毒分子等电点不均一的问题。
人流感病毒的最后浓缩可通过QuixStand 或FlexStand系统配合750 kDa 中空纤维超滤柱完成。产品完全满足FDA对流感病毒疫苗纯度的要求。
|
|
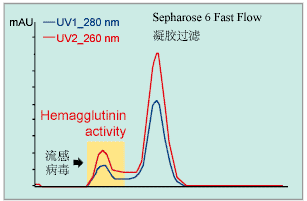
图1. 在Sepharose 6 Fast Flow上进行组分(Group separation
chromatography)
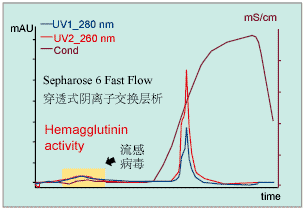
图2. 用阴离子交换层析在Q Sepharose Fast Flow上进一步精纯
人流感病毒疫苗的质量
| -宿主细胞蛋白质(1) |
n.d/ dose |
| - 宿主细胞核酸(2) |
< 10 ng / dose |
| -感染性 |
与蔗糖梯度纯化相同 |
1)n.d.= 未检测出
2) dose = 45 µg HA 抗体(抗体用免疫分析定量)
此方法非常适用于纯化各种病毒疫苗。整个纯化程序可在一天内重复多次。每一步都易于在位清洗,可反复使用上百次,更可按比例线性放大数十至数百倍。 |