

超级增强子(Super enhancer, SE)是一类具有超强转录激活特性的顺式调控元件,2013 年由美国学者 Richard A. Young 首次提出。
与 普 通 增 强 子(Typical enhancer, TE)相比,超级增强子区域跨度范围通常可 达 8-20 Kb,远高于普通增强子的 200-300 bp 跨度范围。更重要的是,超级增强子比普 通增强子具有更强的转录激活相关组蛋白修 饰(H3K27ac 等)、辅因子(Mediator 等) 及转录因子富集密度(图 1-1)。以上特点 决定了超级增强子具有强大的调控功能。
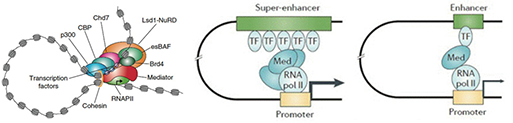
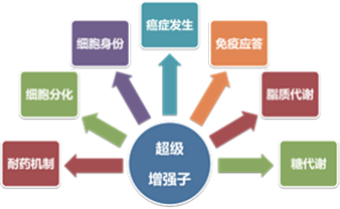
近些年来研究发现,超级增强子在癌症发生、细胞分化、 免疫应答等重要生物学过程中发挥着重要调控功能(图 1-2), 其所调控的基因包含原癌及抑癌基因、细胞身份决定基因、炎症 通路关键基因等。因此,超级增强子具有重要的研究价值,已成 为生物医学领域一个新的研究热点。
根据国内外最新研究进展,表观生物制定了超级增强子 研究策略(如图 1-3),推出超级增强子鉴定、ChIP-seq、 HiChIP、ATAC-seq 等服务,旨在为超级增强子的研究提供强有 力的工具,促进本领域的发展。
超级增强子的鉴定,依据的是增强子转录活性标记分子结合水平强度的差异,这些分子包括辅因子 ( 如 Mediator 和 cohesin)、组蛋白修饰标记 ( 如 H3K27ac 和 H3K4me1)、染色质修饰分子 ( 如 p300) 等。在鉴定过程中,首先通过 ChIP-Seq 分析这些增强子转录活性标记分子在基因组上的富集情况,确定活性增强子位点。之后再对所有活性增强子进 行分析,鉴定得到超级增强子。通过与转录 组测序数据进行关联分析,可发现超级增强子所调控的靶基因。
1. 分析内容全面、准确;
2. 关联转录组数据,获得超级增强子所调控的靶基因;
样本类型:1. 甲醛交联的细胞样本,细胞数量≥ 1×107 ;
2. 组织样本需评估
样本物种:仅限人、大小鼠,其他物种需评估。
常规要求至少 2 组样品,包括对照组和实验组。 样本数建议:3 VS 3。
测序平台:Illumina HiSeq X10/Hiseq 4000
测序模式:PE 150
测序数据量: 12G;
1. TE 与 SE 鉴定分析;
2. TE 与 SE ChIP-seq 峰图对比;
3. TE 与 SE 信号富集图绘制;
4. TE 与 SE 差异(长度与数目)分析;
5. SE 调控靶基因 GO、KEGG 分析;
6. SE 结合转录因子预测(motif)。
这项研究找到了 42 名包含了各种不同亚型室管膜瘤患者进行实验,来寻找可以作为靶点的超级增强子,并验证靶向 超级增强子治疗癌症的可行性。
通过 ChIP-seq、全外显子测序(WES)、全基因组测序(WGS)、转录组分析、DNA 复制数分析以及 DNA 甲基化 数据,研究人员从 42 名室管膜瘤患者的癌细胞中找到了近 1700 种癌细胞依赖的超级增强子,以及与之相关的致癌基因。 研究者将这个结果与目前已知的标准超级增强子数据库进行对比,发现这些超级增强子都具有显著的肿瘤特异性,主要在 肿瘤细胞中被激活,其中一些超级增强子还在其他类型的癌症中起作用。
随后,为了确定这些超级增强子对癌细胞的重要程度,研究人员构建了 shRNA 对它们进行逐一筛选,最后确定了 15 个室管膜瘤癌细胞最依赖的超级增强子,缺少这 15 个超级增强子中的任意一个,癌细胞的生存能力下降至少 50%。同时, 在这 1700 个超级增强子中,有 60% 都是癌细胞所依赖的。这进一步证明了,超级增强子是理想的抗癌靶点。 图 1-5. H3K27ac ChIP-seq 结果 通过靶向 H3K27ac 的 ChIP-seq,从 Heidelberg 患者组鉴定得 2,196 个超级增强子。 图 1-6. 超级增强子功能缺失性实验 研究者针对 15 个排名最前的室管癌超级增强子设计了 shRNA,抑制它们的表达, 发现其中每一个 SE 的缺失都能使癌细胞的存活率减少至少 50%。 最后,研究人员将自己的实验数据与华盛顿大学药物与基因作用数据库进行比对,找到了一种小分子物质,可以特异 性抑制超级增强子对于室管膜瘤细胞内关键致癌基因 CACNA1H 的增强作用。同时,在室管膜瘤小鼠体内,研究人员发现, 这种小分子物质可以使室管膜瘤小鼠生存期延长 40%,并且几乎不会影响正常组织细胞存活。
最后,研究人员将自己的实验数据与华盛顿大学药物与基因作用数据库进行比对,找到了一种小分子物质,可以特异 性抑制超级增强子对于室管膜瘤细胞内关键致癌基因 CACNA1H 的增强作用。同时,在室管膜瘤小鼠体内,研究人员发现, 这种小分子物质可以使室管膜瘤小鼠生存期延长 40%,并且几乎不会影响正常组织细胞存活。
目前,组蛋白修饰和转录因子最常用研究方法为染色质免疫共沉淀测序(chromatin immunoprecipitation sequencing, ChIP-seq)。表观生物技术团队具备丰富的 ChIP 实验经验,利用经验证的 ChIP 级抗体,提供高质量组蛋 白修饰 H3K27ac 和转录因子 BRD4、P300 免疫共沉淀服务,并结合新一代高通量测序技术,为生物医学研究人员提供转 录因子研究整体服务。
首先通过甲醛(formaldehyde,有时使用 UV 或戊二醛)处理细胞 , 将目的蛋白质与 DNA 交联固定;随后用超声将基因组 DNA 打断,并 利用目的蛋白质抗体进行免疫共沉淀;最后通过蛋白酶处理降解蛋白质,分离获得与目的蛋白交联的 DNA 片段 , 然后在其两端加上接头 (linker),进行高通量测序分析。
1. 检测全基因组内与组蛋白、转录因子等特定蛋因子相互
结合的 DNA 位点
2. 鉴定超级增强子,详见第 XX 页
与芯片技术相比,ChIP-seq 技术具有更高的准确性和更大 的覆盖范围。
样本类型:1. 甲醛交联细胞样本,细胞数量≥ 1×107
2. 组织样本需评估
样本物种:仅限人、大小鼠,其他物种需评估
1. 常规要求至少 2 组样品,包括对照组和实验组
2. 样本数建议:3 VS 3。
常规要求至少 2 组样品,包括对照组和实验组。 样本数建议:3 VS 3。
测序平台:Illumina HiSeq X10/Nova
测序模式:PE 150
测序数据量: 12G
一、标准信息分析
1. 去接头污染,去低质量 reads 和测序质量评估;
2. ChIP 测序序列与参考基因组序列的比对;
3. ChIP 测序唯一 reads 在全基因组的分布;
4. Peak 鉴定及基因原件分析;
5. Peak 相关基因筛选与 GO 功能聚类分析、Pathway 分析。
二、高级分析
超级增强子鉴定
参考文献
[1] Mack S C, Pajtler K W, Chavez L, et al. Therapeutic targeting of ependymoma as informed by oncogenic
enhancer profiling[J]. Nature,2018,553(7686):101~105.
[2] Ko J Y, Oh S, Yoo K H. Functional Enhancers As Master Regulators of Tissue-Specific Gene Regulation and
Cancer Development[J]. Mol Cells,2017,40(3):169~177.