
-

生物通官微
陪你抓住生命科技
跳动的脉搏
生科院林爱福课题组在Nature Metabolism发文揭示RNA介导的细胞器...
【字体: 大 中 小 】 时间:2022年08月25日 来源:浙江大学生命科学学院
编辑推荐:
202 2 年 8 月 22 日,浙 江大学生命科学学院林爱福课题组在 Nature Metabolism 杂志在线发表题为“ Long non-coding RNA SNHG6 couples cholesterol sensing with mTORC1 activation in hepatocellular carcinoma ” 的研究论文

细胞器作为物质和能量代谢的重要载体,其独特的生物功能分子有序调控,支持区室内各类生化反应的高效进行。如定位于内质网表面的甾醇结合蛋白SREBPs (sterol-regulatory element binding proteins,SREBPs),能够迅速感应细胞内脂质水平变化,调控脂质合成速率、维持细胞代谢平衡。溶酶体RAGs蛋白(Ras-related GTP-binding proteins, RAGs)能够将mTORC1招募到溶酶体表面完成后续激活,维持细胞物质能量供求平衡。探究细胞器节点生物功能分子的动态调控机制有助于深入了解细胞器代谢调控功能异常与肿瘤等恶性疾病之间的变化规律。
胆固醇作为重要脂质分子元件,参与机体诸多重要生理生化过程。细胞内胆固醇异常升高,一方面为细胞增殖、转移提供了物料保障,一方面通过干扰细胞信号转导驱动多种原癌基因异常高表达,加速肿瘤等多种恶性疾病发生发展。近年来,不断有报道指出胆固醇通过细胞器互作的方式,在线粒体、溶酶体、内质网以及细胞质膜等细胞器之间动态分布。目前对胆固醇介导细胞器互作在肿瘤相关信号转导及代谢调控异常中的作用仍缺乏深入理解。深入解析细胞器互作区域胆固醇代谢调控在肿瘤病变进程中的动态演变规律、效应模式特征,将为肿瘤临床诊断治疗提供潜在新靶点和新策略。
目前已知,90%以上的人类核酸转录本为非编码RNA,长链非编码RNA(LncRNA)作为其中占比最大的类型,在信号转导、细胞代谢、肿瘤发生等进程中发挥重要调控作用。浙江大学林爱福课题组,通过建立细胞器免疫亲和纯化体系,绘制了细胞器LncRNA图谱,揭示了LncRNA的区室化分布特征, 其中响应细胞代谢环境压力,特异性定位于线粒体的LncRNA GAS5能够介导TCA循环代谢区室解离抑制线粒体代谢,展现了区室化LncRNA 在细胞器稳态调控中的重要功能 (Nature Metabolism, 2021)。深入探究LncRNA作为新型调控元件,在多种亚细胞区室的时空分布规律及相关调控功能的动态特性,将拓宽现阶段对lncRNA功能模式及作用方式的认知。
2022年8月22日,浙江大学生命科学学院林爱福课题组在Nature Metabolism杂志在线发表题为“ Long non-coding RNA SNHG6 couples cholesterol sensing with mTORC1 activation in hepatocellular carcinoma”的研究论文。该研究发现肝癌细胞内异常增高的胆固醇,通过诱导LncRNA SNHG6定位于内质网-溶酶体互作区域,激活mTORC1信号通路,促进由非酒精性脂肪肝到肝癌的恶性病变。阐释了区室化LncRNA SNHG6从分子细胞到组织器官多尺度下感应细胞内营养信号、介导细胞器行为调控、促进疾病发生的动态性和可塑性。
该研究基于前期细胞器LncRNA图谱绘制和探索,发现LncRNA SNHG6(small nucleolar RNA host gene 6)特异性响应胆固醇,分布于溶酶体及内质网互作区域,促进肝癌的恶性增殖及不良预后。那么SNHG6是如何具有独特的亚细胞分布特征呢?研究人员利用高通量蛋白组学技术解析了SNHG6在内质网及溶酶体定位的关键连接分子,发现胆固醇能够促进SNHG6与内质网表面蛋白FAF2 (Fas associated factor 2)及mTOR ( mechanistic target of rapamycin kinase) 相互作用。随后,深入解析SNHG6与FAF2/mTOR的结合区域及不同SNHG6截短体在溶酶体、内质网上的定位状态,揭示胆固醇通过调控SNHG6-FAF2-mTOR 信号复合物装配,促使LncRNA SNHG6在内质网-溶酶体互作区域实现动态分布。在此基础上,研究人员进一步解析了SNHG6-FAF2-mTOR 复合物感应及调控胆固醇代谢的分子机制,发现细胞内胆固醇特异性结合FAF2P354并改变蛋白构象,使FAF2能够与SNHG6-mTOR相互作用形成多元复合物,调控mTORC1溶酶体招募及活化过程, 加速细胞胆固醇合成。上述结果表明SNHG6通过与细胞内胆固醇建立正反馈调控机制促进肝癌恶性增殖。
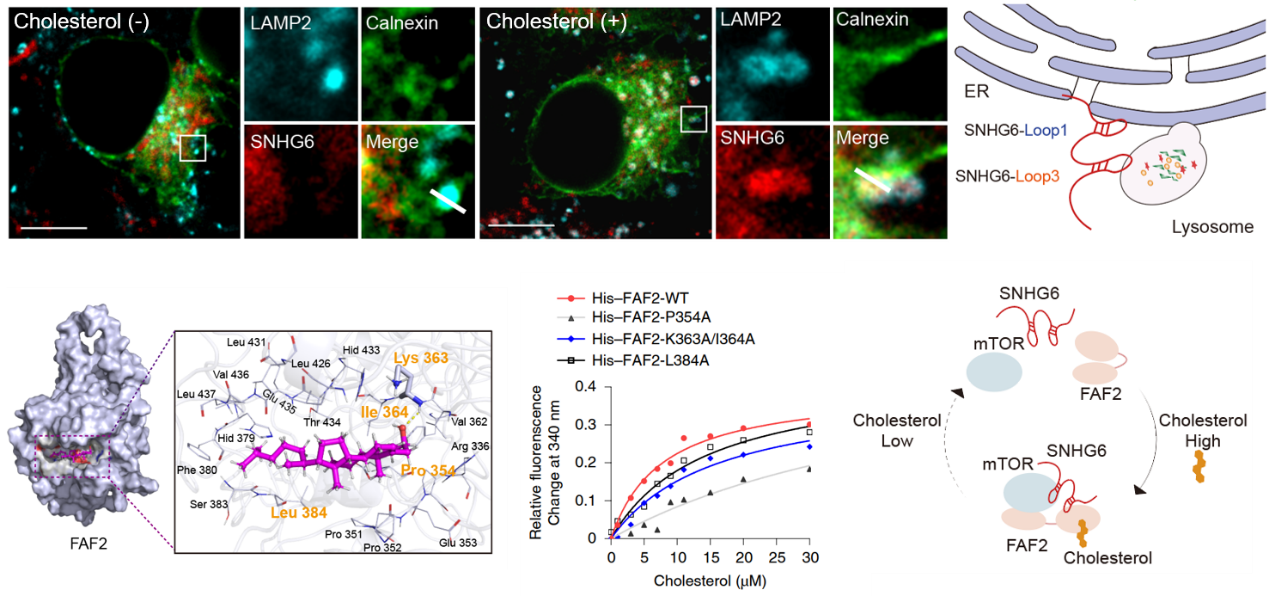
图1 胆固醇在细胞器互作区域调控SNHG6-FAF2-mTOR信号复合物组装
进一步,作者利用胆固醇诱导的NAFLD-HCC小鼠模型以确认SNHG6在肿瘤动态演进过程中的调控作用,发现在小鼠肝脏中过表达 SNHG6将促进胆固醇诱导的mTORC1信号通路活化,加速小鼠肝脏从非酒精性脂肪肝到肝癌的恶性病变过程。并且,通过敲低肝癌病人组织来源PDX模型中的SNHG6显著抑制了肿瘤的发生发展,为临床肿瘤诊断治疗提供新靶点。
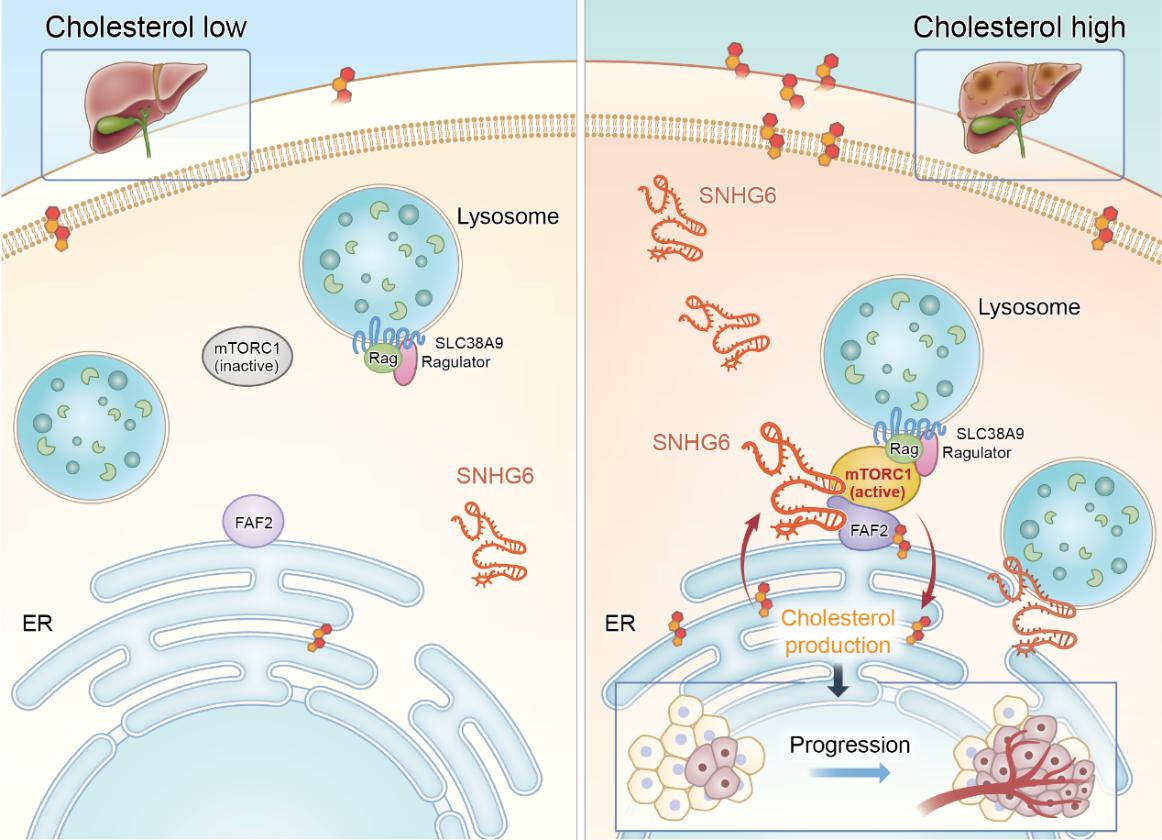
图2 SNHG6在细胞器互作区域内调控胆固醇依赖性的mTORC1活化模式图
综上,该研究通过深入与系统解析细胞器LncRNA SNHG6介导细胞内膜系统精细区域的时空动态代谢调控机制,明确LncRNA定位与功能之间的关系,将拓宽对细胞器动态行为及功能认知的广度和深度,为揭示亚细胞层级代谢及信号调控对肿瘤等人类疾病进展的作用提供崭新视角和理论基础。
浙江大学生科院博士生刘方舟、张祯与暨南大学田甜博士为论文的共同第一作者。该工作得到了国家重点研发计划、国家自然科学基金、浙江省自然科学基金、浙江大学****、浙江大学齐鲁联合研究院科研项目基金等资助。
原文链接:https://www.nature.com/articles/s42255-022-00616-7
 闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤濠€閬嶅焵椤掑倹鍤€閻庢凹鍙冨畷宕囧鐎c劋姹楅梺鍦劋閸ㄥ綊宕愰悙宸富闁靛牆妫楃粭鎺撱亜閿斿灝宓嗙€殿喗鐓¢、鏃堝醇閻旇渹鐢绘繝鐢靛Т閿曘倝宕幍顔句笉濠电姵纰嶉悡鏇㈡煃鐟欏嫬鍔ゅù婊呭亾娣囧﹪鎮欓鍕ㄥ亾閺嶎偅鏆滃┑鐘叉处閸ゅ嫰鏌涢锝嗙闁绘挻绻堥弻鐔煎礈瑜忕敮娑㈡煟閹惧娲撮柡灞剧☉閳藉宕¢悙鍏稿摋闂備礁鐤囬褔鎮ч幘璇茶摕闁哄洢鍨归獮銏ゆ煛閸モ晛顎屾俊宸櫍濮婅櫣鈧湱濯崵娆撴⒑鐢喚绉柣娑卞枛椤粓鍩€椤掆偓閻e嘲顫滈埀顒勭嵁閹捐绠抽柟鎯х摠椤撶懓鈹戦悩娈挎殰缂佽鲸娲熷畷鎴﹀箣閿曗偓绾惧綊鏌″搴″箹缂佺姵婢樿灃闁挎繂鎳庨弳娆戠棯閹岀吋闁哄矉缍佸顒勫垂椤旇棄鈧垶姊虹粙娆惧剱闁挎洏鍨藉濠氬即閻旈绐為梺鍓插亝缁诲倹鎱ㄦ径鎰拺閻炴稈鈧厖澹曞┑鐐差嚟婵挳顢栭崨顖滀笉闁规儼濮ら悡娆撴煙椤栨粌顣兼い銉ヮ槺閻ヮ亪骞嗚缁夋椽鏌″畝鈧崰鏍箖瑜斿畷濂告偄閸濆嫬娈ョ紓鍌欒兌閸嬫捇宕曢幎瑙b偓锕傛倻閽樺鎽曢梺缁樻⒒閸樠呯矆閸垺鍠愰煫鍥ㄦ礃閺嗘粍绻涢幋娆忕仾闁绘挻娲熼幃妤呮晲鎼存繄鐩庨梺閫炲苯澧繛灏栤偓鎰佸殨濠电姵鑹鹃崡鎶芥煏韫囨洖鈻堥柛鐐舵硾閳规垿鎮╅懠顑跨驳闂佸憡姊归悧妤呭疾閵夆晜鈷掗柛灞剧懆閸忓瞼绱掗鍛仸妤犵偞鍔栭妶锝夊礃閵娧呭炊闂備礁鎼粙渚€宕㈡總鍛婂珔闁绘柨鍚嬮悡銉╂煟閺傛寧鎯堢€涙繄绱撴担鎻掍壕闂佸憡鍔﹂崰妤呮偂韫囨挴鏀介柣鎰皺娴犮垽鏌涢弮鈧悷褏妲愰幒妤€惟闁靛牆娲ㄩ悡鎾斥攽椤旂》榫氭繛鍜冪悼閸掓帒鈻庨幘宕囶唶闁瑰吋鐣崹褰掓⒒椤栨埃鏀介柣妯虹仛閺嗏晠鏌涚€n偄濮嶇€规洘鍨块獮妯肩磼濡攱瀚奸梻浣告啞缁诲倻鈧凹鍨抽埀顒佺婢瑰棛妲愰幒鎾崇窞閻忕偠妫勯獮瀣磼閳╁啯灏柕鍡樺笒椤繈鏁愰崨顒€顥氶梻鍌欑閹碱偊寮甸鍕剮妞ゆ牜鍋熷畵浣逛繆椤栨氨姣為柛瀣崌濡啫鈽夊▎蹇旀畼闂備線娼荤徊濂稿础閹惰棄绠栨俊銈呭暞閸犲棝鏌涢弴銊ュ妞わ负鍔戝娲川婵犲啠鎷归梺鑽ゅ枂閸庣敻骞冮悙顒夋Ч閹艰揪绲块悡鎾斥攽閻愬弶顥犻柛瀣尵閳ь剟娼ч惌鍌炲蓟閿濆牏鐤€闁规儳澧庨澶愭⒑缂佹﹩娈曟繛鍙夅缚缁顓兼径濠勭暰閻熸粌顑夐崺鈧い鎺嶇缁楁帗銇勯锝囩疄闁轰焦鍔欏畷銊╊敆閳ь剟藟濮樿埖鈷戦悹鍥ㄥ絻椤掋垺銇勯弮鈧悧鐘茬暦閺夎鏃堝川椤撶媭鍞堕梻浣瑰劤濞存岸宕戦崨鏉戠煑闊洦绋掗悡鍐喐濠婂牆绀堥柣鏃傚帶閽冪喖鏌ㄥ┑鍡樺晵闁绘柨鍚嬮崵鎺楁煏閸繃鍣藉ù鐘层偢濮婄粯鎷呯憴鍕哗闂佺ǹ瀵掗崹璺虹暦濠靛洦鍎熼柕濞垮劚閸嬪秹姊绘笟鍥у缂佸鏁婚崺娑㈠箣閿旂晫鍘搁梺绋挎湰閿氶柛鏃€绮嶇换娑㈠川椤撶喎娈楅梺鍝勬湰閻╊垶骞冮姀銈呯骇闁瑰瓨绻嶉悗瀵哥磽閸屾瑧顦﹂柛濠傛贡閺侇噣鏁撻悩鍙夌€梺绋跨灱閸嬫稓绮堥崼銏″枑闊洦绋掗弲顒佺節婵犲倸鏋ゆ繛鎾愁煼閺屾洟宕煎┑鍥舵!闂佺粯鎸鹃崰鏍蓟濞戙垹妫橀柤鎰佸灠椤忣參鏌i幘鍗炩偓婵嬪蓟閵娾晛鍗抽柣鎰ゴ閸嬫捇骞栨担鐟颁簵闂佸搫娲㈤崹娲偂濞嗘挸绾ч柛顐犲劤閻g儤淇婄紒銏犳珝闁哄本绋撻埀顒婄到婢у海绮旈鈧弻锛勪沪閸撗勫垱婵犵绱曢崗姗€銆佸▎鎾村殥闁靛牆娲﹂弲銊╂⒒閸屾瑧鍔嶉柣顏勭秺瀹曟繆绠涢幘顖涚€洪梺鎸庣箓濞诧箓锝為弴銏$厵闁绘垶锕╁▓鏇㈡煕鐎n偄濮嶉柡灞剧洴楠炲洭顢橀悩顔间沪闂備礁鎼鍡涙偡閳轰緡娼栨繛宸簻娴肩娀鏌涢弴銊ュ闁圭柉浜槐鎾存媴閸撴彃鍓遍梺鍦嚀濞差厼鐣峰ú顏勭劦妞ゆ帊闄嶆禍婊堟煙閻戞ê鐓€闁告梻鍠撶槐鎺撳緞鐏炵偓姣堥梺鍝勬湰閻╊垶鐛Ο灏栧亾闂堟稒鍟為柛锝勫嵆濮婅櫣鍖栭弴鐔告緭闂佹悶鍔忓Λ鍕偩闁垮闄勭紒瀣硶閸橆剟姊虹€圭姵銆冩俊鐐村笚缁旂喖寮撮姀锛勫幗闂佺粯鏌ㄩ幗婊堝箠閸愵喗鍊垫慨妯煎帶楠炴ḿ绱掗鑲╁ⅵ鐎规洘锕㈤、娆撴偩鐏炶棄绠為梻鍌欑窔濞佳勭仚闂佺ǹ瀛╅悡鈥崇暦閹达箑唯闁冲搫鍊婚崢钘夆攽閻愭潙鐏ョ€规洦鍓欓埢宥咁吋閸ワ絽浜鹃悷娆忓缁€鈧梺缁樼墪閵堟悂濡存担鑲濇梹鎷呴悷閭︹偓鎾绘⒒閸屾浜鹃梺褰掑亰閸犳氨绮旈崸妤佲拻闁稿本鑹鹃埀顒勵棑缁牊鎷呴崷顓犲骄婵犵數濮村ú銈囧婵犳碍鐓曟繛鎴濆船閻忥紕鈧娲橀悡锟犲蓟瀹ュ牜妾ㄩ梺鍛婃尵閸犳牕顕f繝姘櫜濠㈣泛饪村ḿ濠囨⒑缂佹ḿ鎲块柛瀣崌閺岋綁骞橀悙钘変划闂佸搫澶囬埀顒€纾弳鍡涙倵閿濆骸澧扮悮锕傛⒒娴g瓔鍤冮柛鐘虫崌瀹曞綊鎸婃径灞炬濡炪倖鍔х粻鎴濇暜闁荤喐绮岀换妯虹暦閵忋倕绠抽柟瀛樻⒐閺傗偓闂備胶绮敃鈺呭磻閸涱喖鍨斿ù鐓庣摠閻撴洟鏌¢崶鈺佷户濞寸姵鐩弻锝夋晲閸涱偄浠┑顔硷功閸庛倕岣块鍫濈妞ゆ棁娉曢悰銉╂⒒娴e憡鎲稿┑顔炬暬閹囨倷閻戞ê鈧爼鏌涢幇闈涙灍闁抽攱鍨块弻娑樷槈濮楀牊顣肩紓浣哥埣娴滃爼寮诲☉妯滅喖骞侀幒鎴滃垝婵°倗濮烽崑娑樜涘┑瀣畺婵炲棙鎸婚崐缁樹繆椤栫偞鏁遍悗姘冲亹缁辨捇宕掑▎鎴М濡炪倖鍨靛Λ娑㈠焵椤掑倻鎳楅柛鎰劵閳ь剙娼¢弻鐔封枔閸喗鐏撶紒鐐劤閸氬濡甸崟顖氭闁割煈鍠楅崐顖炴⒑閸︻厽顏熺紒韫矙閳ワ妇鎹勯妸锕€鏋傞梺鍛婃处閸撴盯藝閵娧呯=濞达綀濮ら妴鍐磼椤旂晫鎳冮柣锝囧厴婵℃悂鏁傞崜褏妲囬梻浣告啞濞诧箓宕戦崟顓犱笉闁绘劖绁撮弨浠嬫煟濡櫣浠涢柡鍡忔櫊閺屾稓鈧綆鍋嗛埥澶愭懚閻愮繝绻嗛柕鍫濆€告禍楣冩⒒閸パ屾Ч闁逛究鍔岄~婊堝幢濡も偓婵箓姊洪幐搴g畵闁绘瀚粋宥堛亹閹烘挾鍘甸梺缁樺灦钃遍悘蹇e弮閺屽秷顧侀柛鎾寸懇閹儲绺介崨濠備簵濡炪倖鍔х粻鎴︽倷婵犲洦鐓忓璺虹墕閸旀艾鈹戦鍝勭伈婵﹦鍎ょ€电厧鈻庨幋鐐蹭还闂備浇妗ㄧ粈渚€鈥﹀畡閭﹀殨濠电姵鑹鹃悘宕団偓瑙勬礀濞诧箑鈻撻弴銏♀拺闂侇偆鍋涢懟顖涙櫠鐎电硶鍋撶憴鍕;闁告鍟块锝嗙鐎e灚鏅i梺缁樺姈椤旀牠宕崶顒佺厽闁绘柨鎽滈惌灞筋熆瑜庨〃鍫ュ极椤曗偓閸╋繝宕ㄩ鐔衡偓顒勬⒑閸涘﹤濮﹂柛鐘愁殜閹繝濡烽敂鍓х槇闂傚倸鐗婄粙鎺椝夐悙鐢电<濞达絽寮跺▍鍡椙庨崶褝韬€规洩绲惧鍕節鎼淬埄妫嗙紓鍌氬€峰ù鍥ㄣ仈閹间礁绠查柛銉戝懏娈鹃梺鍦劋閸ㄧ喖寮告惔銊︾厵闁圭⒈鍘奸獮妤冩偖閿曞倹鈷掗柛灞剧懆閸忓矂寮搁鍫熺叆闁哄洦锚閳ь剚娲熼弫鍐閵堝棛鍔堕悗骞垮劚閹冲繘鎮楅鈧—鍐Χ閸℃ḿ锛曢梺绋款儐閹瑰洭寮婚悢纰辨晩闁伙絽鏈崳浼存倵鐟欏嫭澶勯柛瀣工閻g兘鎮㈢喊杈ㄦ櫍闂佺粯鍔栭悾顐﹀即閻愨晜鏂€闂佹寧绋戠€氼剚绂嶆總鍛婄厱濠电姴鍟版晶閬嶆煛娓氬洤娅嶆鐐村笒铻栧ù锝堫潐閻濇牠姊绘担鐟邦嚋闁哄被鍔嶉弲鑸电鐎n偄鍓归梺鐟板⒔缁垶鎮¢悢鍏肩厪闊洦娲栨牎闂佸摜鍠撻崑銈夊蓟閿濆绠婚悗娑欋缚椤︿即姊虹拠鈥虫灍妞ゃ劌锕顐﹀箛椤撶喎鍔呭┑鐘绘涧閻楀繐鈻旈幐搴濈箚闁绘劦浜滈埀顒佹礈閹广垽宕卞☉妯兼煣闂佺粯枪椤曆囨嫅閻旇 鍋撻獮鍨姎婵炲眰鍔庢竟鏇㈠礂闂傚绠氬銈嗙墬缁诲秹宕靛▎鎴犳/闂佹鍨卞▍鍥╃磼鏉堛劍灏伴柟宄版嚇瀹曨偊宕熼幋顖滅М闁哄矉缍侀崺鈩冪節閸屾粈妗撻梻浣虹帛娓氭宕伴弽顓ㄧ稏婵犲﹤鐗嗛悞鍨亜閹烘垵顏ラ柍褜鍏涚粈渚€鍩ユ径濞㈢喖鏌ㄧ€e灚缍屽┑鐘垫暩閸嬫稑螞濞嗘挸绀夐柡宥庡亝椤愯姤銇勯幇鍓佹偧缂佲檧鍋撶紓浣哄亾濠㈡﹢藝鏉堚晛顥氶柛褎顨嗛悡鏇㈡倵閿濆骸浜滈柣蹇擃嚟閳ь剝顫夊ú姗€宕濆▎蹇e殨闁稿﹦鍣ュ銊モ攽閻愭彃鎮戦柣妤佹礋閸╃偤骞嬮敂钘変汗閻庤娲栧ù鍌炲汲閿熺姵鈷戠紒瀣儥閸庡繘鏌涙繝鍌滅Ш濠碉紕鏁诲畷鐔碱敍濮樿京鏉搁梺鑽ゅ█缂傛艾鈻嶉敐鍛傦綁鏁愭径瀣ф嫼闁哄鍋炴竟鍡浰囬敃鍌涚厱濠电姴鍊归崑銉р偓娈垮枦椤曆囧煡婢舵劕顫呴柣妯诲絻缁侇噣姊绘笟鈧ḿ褎鐏欓梺绋挎唉娴滎剛鍒掓繝姘紶闁告洏鍔嶉弬鈧梻浣虹帛閸旀ḿ浜稿▎鎰珷婵炴垯鍨洪悡鏇㈠箹濞n剙鐏╅柍缁樻礋閺屽秹濡烽敂绛嬫閻庤娲橀敃銏ゃ€佸▎鎾冲簥濠㈣鍨板ú锕傛偂閺囥垺鐓冮柍杞扮閺嬨倖绻涢崼鐕傝€块柡宀嬬秮閹垻绮欓崹顕呮綋闂備礁鐤囬~澶愬垂閸ф鏋佺€广儱顦粈瀣亜閹般劌澧查柛鏇炲暣濮婂搫效閸パ呭姶闂佹悶鍔嶆繛濠傜暦閹达箑围濠㈣泛鑻粊锕傛⒑绾懏褰х紒鐘冲灴閿濈偤宕ㄧ€涙ḿ鍘梺鍓插亝缁诲啴宕宠ぐ鎺撶厾闁哄娉曟禒銏ゆ煃鐟欏嫬鐏撮柟顔界懇瀵爼骞嬮悩杈敇闂傚倷娴囧畷鐢稿疮濞嗘挸鐐婄憸蹇涙偂閹达附鈷戦柛娑橈工婵倿鏌涢弬娆炬█鐎殿喓鍔嶇粋鎺斺偓锝庡亞閸樻捇姊洪懞銉冾亪藝娴兼澶娾堪閸喓鍘介棅顐㈡储閸庡磭绮旈鈧弻鐔碱敊鐟欐帒婀辩划璇测槈濮橈絽浜鹃柨婵嗙凹缁ㄧ粯銇勯鈧鍛村煘閹达箑鐏抽柛鎰皺妤犲洭姊洪崨濠冣拹婵炶尙鍠栭弫鎰版倷濞村鏂€闁诲函缍嗛崑鍕枔濠靛鈷戞慨鐟版搐閻忓弶绻涙担鍐叉川瀹撲線鏌熼幍顔碱暭闁抽攱甯掗湁闁挎繂鎳忛崯鐐烘煕閻斿搫浠遍柡灞剧洴瀵噣鍩€椤掑嫬鍨傞柛顭戝枤閺嗭附绻濋棃娑欏闁稿海鍠栭弻鏇$疀婵犲倸鈷夐梺缁樼箓閸㈡煡鍩為幋锔藉€烽柡澶嬪灩娴犙囨⒑閹肩偛濡芥俊鐐扮矙楠炲啴鏁撻悩鎻掑祮闂侀潧绻掓慨鐑筋敊閹扮増鐓涘璺猴功婢ф洖顭胯閺咁偅绔熼弴銏犻敜婵°倓鑳堕崢浠嬫椤愩垺澶勯柣顓у櫍瀹曘儵顢曢妶鍥╋紲闁哄鐗勯崝宀€绮顓犵闁绘挸娴风粻璇测攽閳╁啯鍊愬┑锛勬焿椤т線鏌涙惔锛勭劯婵﹦绮粭鐔煎焵椤掑嫬鐒垫い鎺戝€告禒婊堟煠濞茶鐏¢柡鍛埣瀹曟粏顦寸痪鍓ф櫕閳ь剙绠嶉崕閬嶅箠韫囨蛋澶愬閳垛晛浜鹃悷娆忓缁€鍐煕閵娿儲鍋ラ柣娑卞櫍楠炴帡骞婇搹顐n棃闁糕斁鍋撳銈嗗笒閸婃悂藟濮樿埖鐓曠憸搴ㄣ€冮崱娑欏亗闊洦鎼╅悢鍡涙煠閸濄儲鏆╅柍钘夘槹閵囧嫰鍩℃繝鍌氼潾缂備浇椴哥敮锟犲箖閳哄懎绠甸柟鍝勬鐎垫牠姊绘笟鈧埀顒傚仜閼活垱鏅舵导瀛樼厵闁惧浚鍋呯亸鎵磼閺冨倸鏋戠紒缁樼箞瀹曟儼顦撮柣娑栧劦濮婃椽宕崟顓涙瀱闂佸憡蓱閸庢娊鎮鹃崹顐e闂侇偅绋撶粻姘舵⒑闂堟稓澧曢柟鍐查叄瀵娊鎮㈤搹瑙勶紡闂佺顫夐崝鏇熺閸︻厾纾奸弶鍫涘妽鐏忎即鏌熷畡鐗堝櫧闁瑰嘲缍婇、娑樷堪閸涱垳宕剁紓鍌氬€搁崐鐑芥嚄閼稿灚鍙忛柣鎴f绾剧粯绻涢幋娆忕仼闁绘挻锕㈤弻鐔告綇閹呮В闂佽桨绀侀敃顏堝蓟閿濆鍋勭痪鎷岄哺濞堛儲绻濋姀锝庢綈婵炶尙鍠庨~蹇旂節濮橆剛锛滃┑鐐叉閸ㄥ灚淇婃禒瀣厽閹艰揪绲块幊妤呮煕濞戝崬鏋涢幖鏉戯躬濮婅櫣绮欓幐搴㈡嫳婵犮垼顫夊ú鐔风暦閹达箑绠婚柡鍌樺劜椤秹姊洪崷顓炲妺闁圭ǹ顭烽幃鐢稿冀椤愩倗锛濇繛杈剧稻閸ㄦ繈宕ラ锔界厱閻庯絻鍔岄埀顒佹礋閹箖鏌ㄧ€n剟妾紓浣割儓椤曟娊濡搁埡鍌滃弳闂佸搫鍟犻崑鎾绘煕鎼淬垹鈻曢柣娑卞枛铻栭柛娑卞枓閹风粯绻涢幘鏉戠劰闁稿鎸荤换娑欐媴閸愬弶鍣虹€规洘鐓¢弻娑㈠焺閸愵亖妲堥梺姹囧€楅崑鎾舵崲濞戙垹绠f繛鍡楃箳娴犻箖姊虹粙鍖″伐闁绘牕銈稿濠氬Ω閵夈垺鏂€闂佺硶妾ч弲婊勬櫏闂傚倷鑳剁划顖炲箰鐠囪娲偄閻撳海鐣哄┑掳鍊曢幊蹇涘疾閺屻儱绠圭紒顔煎帨閸嬫捇骞囨担閫涙唉闂傚倸鍊风粈渚€骞栭锔绘晞闁告稑鐡ㄩ悡鈧梺鎸庣箓閹虫劙寮抽敃鍌涚叆闁绘柨鎼牎闂佺粯甯熼崑鎰板焵椤掆偓缁犲秹宕曢崡鐐嶆稑鈽夐姀鐘插亶闂佹眹鍨归幉锟犲煕閹寸姷纾藉ù锝囨娓氭稒绻涢崼鐔割棃闁哄矉绲借灃闁逞屽墴閺佸啴鏁冮埀顒勫煝鎼淬劌顫呴柕鍫濇濞堛倕顪冮妶鍡楃瑨闁稿﹤顭烽弫宥呪堪閸啿鎷虹紓鍌欑劍閳笺倝顢旈崼婵堟焾闂佺鍕垫當闁绘挻绻堥弻锟犲炊閵夈儳浠鹃梺缁樻尰缁嬫捇鍩€椤掆偓閸樻粓宕戦幘缁樼厓鐟滄粓宕滈悢椋庢殾濞村吋娼欓崘鈧悷婊冪箻瀵娊鏁傞懞銉ュ伎濠碉紕鍋犻褎绂嶆ィ鍐┾拺闁荤喐澹嗛敍宥呪攽閻愨晛浜炬俊鐐€戦崹娲€冮崱娆愬床婵犻潧顑呯粈瀣亜閹炬瀚呴敃鍌涒拻闁稿本鑹鹃埀顒佹倐瀹曟劖顦版惔锝囩劶婵炴挻鍩冮崑鎾搭殽閻愭惌娈旀顏冨嵆瀹曠喖顢楅埀顒€顕i崸妤佲拺婵懓娲ら悘鈺呮煙鐠囇呯瘈鐎规洘鍨归埀顒婄秵閸犳鎮¢悢闀愮箚妞ゆ牗绻傛禍褰掓偨椤栨稓娲撮柡灞剧〒閳ь剨缍嗛崐鏍箣閿曗偓妗呴梺鍛婃处閸ㄤ即宕¢搹顐$箚闁靛牆鍊告禍鐐箾鐎涙ḿ鐭嬮柛搴$枃閻忓啴姊虹紒姗堣€挎繛浣冲嫮顩锋繝濠傚缁犲墽鈧懓澹婇崰鏍ь嚕椤曗偓閺屾洟宕遍弴鐙€妲銈庡亝缁捇宕洪埀顒併亜閹烘垵顏╃紒鐘崇墵閺屾洝绠涢弴鐐愩儵鏌¢崱妤婂剶闁哄备鍓濆鍕償椤斿吋顔曢梻渚€娼ч悧鍡浰囨导鏉戠厱闁圭儤顨嗛悡鏇㈡倶閻愭彃鈷旈柟鍐叉嚇閺屾盯寮捄銊愌囨煙椤旂瓔娈樼紒顕呭幖閳藉螣鐠囧弶顏¢柣搴ゎ潐濞叉﹢鎮¢敓鐘茶摕婵炴垶鐭▽顏嗙磽娴i潧鐏╂繛鍫㈠帶閳规垿鎮欓弶鎴犱户闂佺硶鏅涚€氭澘顕i锕€鐐婃い鎺嶈兌閸橆亪妫呴銏″婵炲弶鐗犻悗鐑芥煟閻愬顣茬紒璇茬墕椤繒绱掑Ο璇差€撻柣鐔哥懃鐎氼剚绂掗埡鍛拺缂佸鐏濋惁銊╂煕閵娿劍纭鹃柣锝呭槻閳规垿宕堕妸銉ュΤ闂備焦瀵х换鍌炲箠鎼淬倐鍙㈤梻鍌氬€风欢姘跺焵椤掑倸浠滈柤娲诲灡閺呭墎鈧稒蓱閸欏繐鈹戦悩鎻掆偓褰掑箚閸儱鏋侀柛顐犲劜閻撴洟鏌曟径瀣仴闁瑰啿绉跺Σ鎰枎閹邦喚鐦堥梺姹囧灲濞佳勭閹烘鐓曢柡宥庡亜閳诲牏鈧娲滈崰鏍€佸Ο娆炬Ъ缂備椒绶¢崑鍛崲濠靛鍋ㄩ梻鍫熷垁閵忋倖鐓ラ柡鍥埀顒侇殜閸┾偓妞ゆ帊绀侀幖鎼佹煕閺傝法肖缂侇喖顑呴濂稿川椤忓嫮澧梻浣稿閸嬪棝宕伴幘璇插偍闁归棿鐒﹂埛鎴︽煙閼测晛浠滈柛鏃€锕㈤弻娑欐償閵堝鎽垫繛锝呮搐閿曨亜鐣峰Δ鍐ㄦ瀳閺夊牜鐓堥崯宥夋⒒娴h櫣甯涢柛鏃€鐗犻獮鍡欎沪鐟欙絾鐏佸┑鐘诧工閻楀﹪鎮″☉銏″€堕柣鎰絻閳锋梹绻涢幓鎺旀憼妞ゃ劊鍎甸幃娆撳级閹寸偠鐧佹俊銈囧Х閸嬫盯顢栨径鎰┾偓浣糕槈濮楀棙鍍靛銈嗗笒椤︽澘霉閸℃稒鈷掗柛灞捐壘閳ь剟顥撳▎銏狀潩鐠鸿櫣鍔﹀銈嗗笒閸婂憡绂掑⿰鍫熺厾婵炶尪顕ч悘锟犳煛閸涱厼顣抽柍褜鍓氱粙鎺戠幓鐠恒劎涓嶉柟顖g亹瑜版帗鏅查柛娑卞幗濮f劕鈹戦悙鑼勾闁稿﹥顨堥崚鎺撶節濮橆厼鈧粯淇婇婵嗕汗闁伙箑鐗婄换婵嬫偨闂堟刀銏ゆ煕婵犲倻绉虹€规洝娅曠粋鎺斺偓锝庡亞閸樿棄顪冮妶鍡樺暗闁稿鍋よ棢婵犲﹤鐗婇悡鍐偡濞嗗繐顏╅柣蹇旀尦閺岀喖顢欑憴鍕彋閻庤娲╃徊鎯ь嚗閸曨剛绡€閹肩补鎳i悢鍏尖拻闁稿本鐟ㄩ崗宀€绱掗鍛仸妤犵偞鍔欓獮鏍ㄦ媴閸濄儲鐒惧┑鐐存綑閸氬岣垮▎鎴犱笉闁绘棁娅g壕濂告倵閿濆簼绨芥慨妯稿姂閺屾盯顢曢锟犲仐闂佸搫鏈惄顖炪€侀弴銏℃櫜闁搞儮鏅濋弳顓熶繆閻愵亜鈧呪偓闈涚焸瀹曪綁宕橀…鎴炵稁闂佹儳绻愬﹢杈╁閸忛棿绻嗘い鏍ㄧ箓閸氬綊鏌涘▎蹇旑棞妞ゎ亜鍟存俊鍫曞礃閵娿儺鐎冲┑掳鍊楁慨閿嬬仚闂佺粯绮岄…宄扮暦缁嬭鏃堝焵椤掑嫬绀冮柍褜鍓熼幃宄扳堪閸愮偓鈻堥悗娈垮枔閸斿秶绮嬮幒鏂哄亾閿濆骸浜為柛妯挎閳规垿鍩ラ崱妤冧淮濠电偛鎷戠紞浣割嚕閹间礁绀冩い顓熷灩閸炵敻鏌i悢鍝ユ噧閻庢哎鍎崇槐鎾愁潩鏉堚晝锛滈柡澶婄墑閸斿苯霉椤曗偓閺屾盯鍩為幆褌澹曞┑锛勫亼閸婃牜鏁幒鏂哄亾濮樼厧澧扮紒顔肩墦瀹曟﹢顢欓悾灞藉笚闂備浇宕甸崰鏇㈠春閸ャ劎顩烽柟鐑樻⒒绾惧ジ鏌曟繛鍨姶闁绘挸鍚嬮幈銊︾節閸涱噮浠╅梺鐟板级閹稿啿鐣烽悢纰辨晝闁靛牆瀛╄ⅷ婵犵數濮烽弫鎼佸磻濞戔懞鍥ㄥ鐎涙ê鍓銈嗙墬閸戝綊宕甸弴銏$厵闂傚倸顕ˇ锔剧磼椤愩垻效闁哄本鐩、鏇㈠Χ閸涱喚浜栭梻浣告啞閿曗晜绂嶉鍕垫綎闁惧繒鎳撶€垫煡鏌¢崶鈺佷粶闁冲嘲顦—鍐Χ閸愩劌顬夐梺鍛婃⒐閻熴儵鎮惧畡鎵虫斀閻庯綆鍋勬禍婊堟⒑閹呯婵犫偓闁秵鏅繝濠傜墛閻撴稑顭跨捄鐚村姛濠⒀勫灴閺屾盯寮捄銊愩倕霉濠婂啯鍟為悗浣冨亹閳ь剚绋掑玻鍧楀储閻㈠憡鍊甸柣鐔告緲椤忣偄顭胯椤ㄥ﹤鐣烽幎鑺ユ優闁革富鍘鹃敍婊堟⒑缁嬫寧婀扮紒瀣灩缁叀顦归柡灞界Х椤т線鏌涢幘鍗炲缂佽京鍋ゅ畷鍗炍熺喊杈ㄩ敜婵犵數濞€濞佳囶敄閸涱垳涓嶉柣妯虹-缁犻箖鏌涢埄鍏╂垹浜告导瀛樼厓闂佸灝顑呴悘锕傛煙娓氬灝濮傞柟顔惧厴閹囧醇閻旂ǹ鈧兘姊绘担铏瑰笡閻㈩垱顨呴—鍐╃鐎n亣鎽曞┑鐐村灍閹冲洭鍩€椤掑﹦鐣垫鐐差儏楗即宕煎┑鍛幓闂傚倸鍊烽懗鍓佹兜閸洖妫樺〒姘e亾鐎规洘鍨块獮姗€骞囨担鐟扮槣闂備線娼ч悧鍡椢涘Δ鍛敜濠电姴娲﹂悡鏇㈡倵閿濆骸浜濋悘蹇曟暬閺岋綁濡烽鑽ゆ晼缂備浇椴哥敮鈩冩叏閳ь剟鏌eΟ鍨毢闁活偄瀚伴弻锝嗘償閵忊晛鏅遍梺鍝ュУ椤ㄥ棛鎹㈠☉娆戠瘈闁搞儜鍕偓顒勬⒑閸涘﹤濮﹂柛鐘崇墱婢规洟宕楅懖鈺冾啎闂佺懓顕崑鐘崇珶濡椿娈介柣鎰儗濞堟粍鎱ㄦ繝鍕笡闁瑰嘲鎳樺畷銊︾節閸愩劌澹嶉梻鍌欑閹芥粓宕抽妷鈺佺;濠电姴鍊婚弳锕傛煙閹殿喖顣奸柛瀣ㄥ妿缁辨帞鈧綆鍘界涵鑸点亜閺傛寧顥㈡慨濠呮閹瑰嫰濡搁妷锔句簴濠电姵顔栭崰姘跺极婵犳艾绠栭柍銉︽灱濡插牊淇婇姘辩缂傚秴锕顐﹀箛閺夊灝鎯為梺鑺ッˇ杈╃矓閾忓厜鍋撳▓鍨灍濠电偛锕獮鍐ㄢ枎閹炬潙鈧粯淇婇婊冨付閻㈩垶绠栧缁樻媴鐟欏嫬浠╅梺绋垮缁挸鐣峰鈧畷锝夊Ψ瑜忛敍鐐寸節瀵伴攱婢橀埀顒侇殕閹便劑鎮滈挊澶岋紱濠电偞鍨堕埣銈吤洪宥嗘櫍闂侀潧绻掓慨闈浳i鍕拺闁哄倶鍎插▍鍛存煕閻曚礁鐏¢柛鎺戯躬楠炴﹢顢欓懖鈺呯崜闂備胶绮崝娆忈缚瑜旈妴鍌涚附閸涘﹦鍘遍柣搴秵娴滄繈宕甸崶銊﹀弿濠电姴鍋嗛悡鑲┾偓瑙勬礃鐢帡锝炲┑瀣垫晞闁芥ê顦竟鏇㈡⒑瑜版帗锛熼梻鍕Ч瀹曟垿骞嬮敂鐣屽幗闂侀潧绻堥崹娲汲閳轰讲妲堥柟鎯х-鏁堥梺鍝勭灱閸犳牠骞冨▎鎿冩晢闁逞屽墯閺呭爼顢涘☉姘鳖啎闂佺ǹ绻楅崑鎰櫠椤忓牊鐓冮悷娆忓閻忔挳鏌熼瑙勬珖闁逞屽墮濠€杈ㄦ叏閹绢啟澶娾攽閸垻锛滈梺缁樺姦閸撴瑩宕濋妶澶嬬厱婵﹩鍓﹂崕鎴︽煙楠炲灝鐏╅柍钘夘樀婵偓闁绘ǹ灏埀顒€鐏濋埞鎴﹀煡閸℃浠╅梺鍦拡閸嬪﹪鏁愰悙瀛樺劅闁靛⿵鑵归幏娲⒒閸屾氨澧涚紒瀣尰閺呰泛鈽夊▎鎴犵槇闂侀潧绻嗗Σ鍕嚀閸ф鐓曢柍鍝勫暙娴犺鲸顨ラ悙宸剶闁轰礁鍟撮崺鈧い鎺戝閸婃寧绻涘顔荤凹闁绘挻娲熼弻鐔煎级閸噮鏆㈢紓浣介哺婢瑰棛妲愰幒妤婃晩缁炬媽浜崥瀣攽椤旂》鏀绘俊鐐舵閻g兘濡搁敂鍓х槇闂佸憡鍔х徊鍓р偓姘煼濮婄粯鎷呯憴鍕哗闂佸憡鏌ㄩ懟顖氱幓閸ф鏅搁柣妯哄暱娴犳帒顪冮妶鍡樷拻闁哄拋鍋嗗褔鍩€椤掑嫭鈷戠紒瀣儥閸庢挸鈹戦鍝勨偓鏇$亱闂佸憡鍔戦崝搴ㄥ汲閿曞倹鐓忓┑鐐靛亾濞呮捇鏌℃担鍛婂枠闁哄矉绲介埢搴d沪閹存帒顥氬┑鐘茬棄閵堝懓鏁垮┑鐐差槹閻╊垶宕洪悙鍝勭闁挎棁妫勯埀顒傚厴閺屻倝骞栨担瑙勯敪濠电偞鍤崨顖滐紳婵炶揪绲块幊鎾跺緤缂佹ḿ绠剧痪顓㈩棑缁♀偓闂佺粯渚楅崰妤冩崲濠靛鐐婄憸蹇涱敊閹烘鐓熼幖娣灮閳洟鏌ㄥ鑸电厱闁哄倹瀵ч崳铏圭磼缂佹ḿ绠為柟顔荤矙濡啫霉闊彃鐏查柡灞剧⊕缁绘繈宕熼浣圭槗闁诲孩顔栭崰鎾诲礉瀹ュ洨鐭夐柟鐑樻煛閸嬫捇鏁愭惔鈥茬敖闂佸憡枪濡嫰鍩為幋锕€鐓¢柛鈩冾殘娴犳挳姊虹粙娆惧剱闁告梹顨婂顐︻敊鐏忔牗顫嶅┑鐐叉閸ㄥ綊顢欓弴銏♀拺闁荤喐婢橀弳閬嶆煕閵忊€崇祷閻撱倝鏌ㄩ弴鐐测偓褰掑磻閸岀偞鐓熼柡鍐ㄧ墛濞呮粎绱掔拠鍙夘棦闁哄本娲熷畷鐓庘攽閸″繐浜鹃柛娑橈功椤╂煡鏌涢幘妤€鎳愰敍婵囩箾鏉堝墽绉繛鍜冪悼閺侇喖鈽夐姀鈥充缓濡炪倖鐗楃划灞剧鏉堚斁鍋撶憴鍕鐎光偓閹间胶宓侀柟鐑樺殾閺冨牆鐒垫い鎺戝閻撲線鏌涢妷顔煎闁绘挾鍠栭弻锟犲礃閵婏箑顦╁銈呯箳婵炩偓闁哄矉缍侀弫鍐焵椤掑嫭鍋嬮柟鐐墯濞兼牗绻涘顔荤盎缂佺姴缍婇弻锝夊箛椤撶偟绁锋繝娈垮枛閻倸顫忓ú顏勫窛濠电姴鍟伴崣鍡涙⒑濞茶骞栭柛濠傜仢閻e嘲煤椤忓嫮鍔﹀銈嗗笂闂勫秵绂嶅⿰鍫熺厵闁绘垶锚閻忋儵鏌嶈閸撴瑧绱炴繝鍌ゅ殨闁瑰墎鐡旈弫鍡涙煕閺囥劌澧伴柛妯绘倐閺岋綀绠涢弴鐐板摋濡炪倖娉﹂崟顏嗙畾婵犻潧鍊搁幉锟犳偂閸愵喗鍋℃繛鍡楃箰椤忊晠鏌h箛鎿冨殶闁逞屽墲椤煤閺嵮呮殾妞ゆ帒瀚悡鈥愁熆閼搁潧濮囩紒鐘劚闇夐柨婵嗩槹濞呮粌顭跨憴鍕闁宠鍨堕獮濠囨煕婵犲啫濮嶇€规洘鍨块獮妯呵庨璺ㄧ泿婵$偑鍊栭幐鎾焵椤掆偓閸熸寧鎱ㄥ畡閭︽富闁靛洤宕崐鑽ょ玻閺冨牊鐓涢悘鐐插⒔濞叉潙鈹戦埄鍐╁€愬┑锛勬焿椤︽煡鏌i幘璺烘灈闁诡喗顨呴埢鎾诲垂椤旂晫浠屾俊鐐€栧▔锕傚炊瑜忛崣鈧┑鐘灱閸╂牠宕濋弴顫稏闁告稑鐡ㄩ悡鍐煏婢跺牆鍔氶悽顖滃У閹便劎鎲撮崟鍨杹濠殿喖锕︾划顖炲箯閸涙潙宸濆┑鐘插€瑰▓姗€姊绘担钘夊惞闁哥姴妫濆畷鏇熸媴閸愨晩妫ㄩ梻鍌欐祰婵倝鏁嬮梺鎸庣☉椤︻垶鍩ユ径鎰潊闁斥晛鍟悵鏍⒒娴e懙褰掑嫉椤掑倻鐭欓柛顐犲劚缁狀垱绻涘顔荤凹闁抽攱鍨块弻娑樷槈濮楀牆濮涚紓浣哄У閹瑰洭骞冨Δ鈧~婵嬫偂鎼达絼妗撻梻浣瑰缁诲嫰宕戦妶澶婃瀬闁告劦鍠栫壕鍏肩箾閹寸偠澹樻鐐茬墦濮婄粯鎷呴崨濠冨創闂佺ǹ锕ㄥΛ鍕煝閺冨牆鍗抽柕蹇娾偓鏂ュ亾閸ф鐓欓梻鍌氼嚟閸斿秹鏌i幘瀛樼闁哄苯绉瑰畷顐﹀礋椤愶絾顔勫┑鐐差嚟婵偓銇旈幖浣碘偓鍐Ψ閳哄倸鈧鈧懓澹婇崰鏍礈閸洘鈷戦弶鐐村椤︼箓鏌涢悢鍛婂唉鐎规洘妞介崺鈧い鎺嶉檷娴滄粓鏌熼悜妯虹仴妞ゅ浚鍋嗛埀顒冾潐閹搁娆㈠璺鸿摕闁哄浄绱曢悿鈧繝鐢靛仦閸庤櫕绂嶆ィ鍐╃厾缁炬澘宕晶浼存煟閿濆洤浜惧ǎ鍥э躬閹瑩顢旈崟銊ヤ壕闁哄稁鍘介崑瀣繆閵堝懎鏆欓柛銊︾箘閳ь剙鍘滈崑鎾绘煕閺囥劌浜炴い锔诲櫍閺岋絾鎯旈婊呅i梺绋款儎閻掞妇绮嬪鍛牚闁割偁鍨硅ぐ鍕⒑閹肩偛鍔橀柛鏂跨Ф缁牓鍩€椤掑嫭鈷戦悗鍦閸ゆ瑩鏌eΔ鈧敃顏堢嵁閸儱惟闁挎柨澧介惁鍫ユ⒑閸涘﹥澶勯柛妯垮亹缁參鏁撻悩鏂ユ嫼闂佽崵鍠愬妯何f繝姘厵闁惧浚鍊嬮鍫熷仼闁绘垼妫勬儫闂佹寧鏌ㄦ晶浠嬫儊閸儲鈷戦柛娑橈工婵倿鏌涢弬鎸庢拱缂佹梻鍠庨濂稿川椤忓懏鏉搁梻浣瑰缁嬫垹鈧凹鍓氱粋宥嗙附閸涘﹦鍘辨繝鐢靛Т閸熺増鏅堕悽纰樺亾鐟欏嫭绀€缂傚秴锕獮鍐偩瀹€鈧惌娆撴偣娓氼垳鍘滅紒槌栧櫍濮婄粯鎷呯粙娆炬闂佺粯鎸搁悧鎾崇暦閺夋娼╅悹铏瑰劋鏉堝牓姊洪幐搴㈢闁稿﹤缍婇幃鈥斥枎閹惧磭楠囬梺鍓插亝缁诲倿鍩涢弮鍫熺厽闁挎繂鐗呴崥顐ょ磼鏉堛劌娴柟顔规櫊瀹曨偊宕熼锝呭姃缂傚倸鍊峰ù鍥ㄣ仈閹间礁绠板┑鐘宠壘缁狀垶鏌涘☉鍗炴珮婵炲牅绮欓弻鏇熺節韫囨洜鏆犻梺鍛婄箘閸庛倝銆冮妷鈺傚€烽柤纰卞墰椤斿﹦绱撴担浠嬪摵閻㈩垱甯熼悘鎺楁⒑閸忚偐銈撮柡鍛櫊瀹曨垱鎯旈妸锔规嫼闂佸憡绻傜€氬嘲危閹间焦鐓熸俊銈傚亾婵☆偅鐟╁鏌ユ嚋閻㈡娴勯柣搴秵娴滅偤藝椤愶絿绠鹃悗鐢登圭敮鍫曟煟鎺抽崝鎴﹀箖閳ユ枼鏋庨柟鐐綑娴狀垶姊洪幖鐐插姎婵炲眰鍊濋獮濠囧箛閻楀牆鍓ㄩ梺鍓插亝閹﹪寮崼鐔蜂汗闂傚倸鐗婄粙鎰垝鐠鸿 鏀介柍钘夋娴滄繄绱掔拠鎻掆偓鍧楀箖妤e啯鐓ラ悗锝庡墴濡绢喚绱撴担鍓插創妞ゆ洘濞婃俊鎼佸煛閸屾粌寮抽梻浣告惈閸熺娀宕戦幘缁樼厱閹兼番鍨归埢鏇㈡煟濞戝崬娅嶇€规洜鍘ч埞鎴﹀礃閳哄倹婢戦梻鍌欒兌缁垶鏁嬮梺璇茬箲瀹€绋款嚕閹惰棄鐓涘ù锝呭级閺傗偓婵$偑鍊栧Λ浣肝涢崟顖氱厺闁哄洢鍨洪悡娆撴煣韫囷絽浜芥繛鍫熺矌閳ь剝顫夊ú鏍Χ缁嬫鍤曢柟缁㈠枟閸嬪嫮鈧懓瀚姗€藟濡も偓閳规垿鎮╅崹顐f瘎闂佺ǹ顑嗙粙鎴g亱濠电偛妫欓幐鍝ョ不閺夊簱鏀介柣妯虹-椤f煡鏌涚€n亜鈧潡寮婚弴鐔风窞婵炴垶锕╁ú顓犵磽娴e弶顎嗛柛瀣崌濮婂宕掑顑藉亾閹间焦鍋嬪┑鐘插閻瑩鏌熼幆褏鎽犳繛鍛█閺岋繝宕堕埡鈧槐宕囨喐閻楀牆绗氶柛瀣灴閺屾稑鈽夐崡鐐插濠电偛妯婇崣鍐潖濞差亝鐒婚柣鎰蔼鐎氭澘顭胯閸o綁寮婚敐鍫㈢杸闁哄啫娲らˉ婵嗩渻閵堝骸骞栭柣蹇旂箚閻忔帡鏌h箛鎾剁闁绘娲樼粋宥夋倷椤掍礁寮垮┑顔筋殔濡绂嶅⿰鍛亾鐟欏嫭灏俊顐g箞瀵鏁愰崨顏咁潔闂佸憡顨堥崑鐐烘偟濠靛鍊甸悷娆忓缁€鈧梺缁樼墪閵堟悂濡存担鑲濇棃宕ㄩ鐘插Е婵$偑鍊栫敮鎺斺偓姘煎弮瀹曟垿宕掑☉娆忓伎濠碉紕鍋犻褎绂嶆ィ鍐┾拺闁告繂瀚悘閬嶆煕閻樺磭澧甸柕鍡曠閳藉濮€閻樿尪鈧灝鈹戞幊閸婃劙宕戦幘缁樼厓鐟滄粓宕滃璺虹畺闁稿本绻冮敍鍌涚節濞堝灝鏋熼柨鏇楁櫊瀹曟顫滈埀顒€顕i妸锔绢浄閻庯綆鍋嗛崢浠嬫⒑瑜版帒浜伴柛鎾寸洴楠炴鎮╃紒妯衡偓鍫曠叓閸パ囶€楃€规挸妫濋弻锛勪沪閸撗勫垱闂佺硶鏂侀崜婵嬪箯閸涙潙宸濆┑鐘插枤閸熷姊虹拠鍙夊攭妞ゎ偄顦叅婵せ鍋撶€规洖缍婂畷绋课旈崘銊с偊婵犵妲呴崹鐢稿磻閹邦喖顥氶柛蹇涙?缁诲棙銇勯弽銊х煀閻㈩垵鍩栭〃銉╂倷閺夋垵顫岄梺瀹狀潐閸ㄥ潡骞冨▎鎾村殝闂傚牊绋掗柨顓犵磽閸屾艾鈧摜绮旈鈧畷鎴﹀箻閹颁焦瀵岄梺闈涚墕妤犲憡绂嶅⿰鍕╀簻闁挎棁顕ч悘锕傛煙椤旇棄鍔ら柣锝忕節楠炲秹顢欓懞銉ф殾闂傚倷绀侀幉鈥趁洪敃鍌氱婵炴垯鍨归崒銊╂煕濞戞﹫鍔熺紒鐘荤畺瀵爼宕煎┑鍡忔寖缂備礁顦介崜姘跺Φ閸曨垼鏁冮柕蹇婃櫆绗戦梻浣风串缁蹭粙宕查弻銉﹀仼婵犻潧顑呯粈瀣亜閹烘垵鈧悂鐛幇顑芥斀闁绘劘鍩栬ぐ褏绱撳浣镐壕婵$偑鍊ら崑鍕囬鐐村仼鐎瑰嫭澹嗛弳鍡涙煕閺囥劌澧伴柛妯烘啞缁绘稒娼忛崜褏袣濡炪値鍋勯ˇ顖炴偩瀹勬壆鏆嗛柛鏇ㄥ墰閸樺憡绻涙潏鍓хК妞ゎ偄顦悾宄扮暆閸曨剛鍘告繛杈剧秬椤鐣峰畝鍕厸濞达綀顫夊畷宀勬煛娴h宕岄柡浣规崌閺佹捇鏁撻敓锟�>>
闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤濠€閬嶅焵椤掑倹鍤€閻庢凹鍙冨畷宕囧鐎c劋姹楅梺鍦劋閸ㄥ綊宕愰悙宸富闁靛牆妫楃粭鎺撱亜閿斿灝宓嗙€殿喗鐓¢、鏃堝醇閻旇渹鐢绘繝鐢靛Т閿曘倝宕幍顔句笉濠电姵纰嶉悡鏇㈡煃鐟欏嫬鍔ゅù婊呭亾娣囧﹪鎮欓鍕ㄥ亾閺嶎偅鏆滃┑鐘叉处閸ゅ嫰鏌涢锝嗙闁绘挻绻堥弻鐔煎礈瑜忕敮娑㈡煟閹惧娲撮柡灞剧☉閳藉宕¢悙鍏稿摋闂備礁鐤囬褔鎮ч幘璇茶摕闁哄洢鍨归獮銏ゆ煛閸モ晛顎屾俊宸櫍濮婅櫣鈧湱濯崵娆撴⒑鐢喚绉柣娑卞枛椤粓鍩€椤掆偓閻e嘲顫滈埀顒勭嵁閹捐绠抽柟鎯х摠椤撶懓鈹戦悩娈挎殰缂佽鲸娲熷畷鎴﹀箣閿曗偓绾惧綊鏌″搴″箹缂佺姵婢樿灃闁挎繂鎳庨弳娆戠棯閹岀吋闁哄矉缍佸顒勫垂椤旇棄鈧垶姊虹粙娆惧剱闁挎洏鍨藉濠氬即閻旈绐為梺鍓插亝缁诲倹鎱ㄦ径鎰拺閻炴稈鈧厖澹曞┑鐐差嚟婵挳顢栭崨顖滀笉闁规儼濮ら悡娆撴煙椤栨粌顣兼い銉ヮ槺閻ヮ亪骞嗚缁夋椽鏌″畝鈧崰鏍箖瑜斿畷濂告偄閸濆嫬娈ョ紓鍌欒兌閸嬫捇宕曢幎瑙b偓锕傛倻閽樺鎽曢梺缁樻⒒閸樠呯矆閸垺鍠愰煫鍥ㄦ礃閺嗘粍绻涢幋娆忕仾闁绘挻娲熼幃妤呮晲鎼存繄鐩庨梺閫炲苯澧繛灏栤偓鎰佸殨濠电姵鑹鹃崡鎶芥煏韫囨洖鈻堥柛鐐舵硾閳规垿鎮╅懠顑跨驳闂佸憡姊归悧妤呭疾閵夆晜鈷掗柛灞剧懆閸忓瞼绱掗鍛仸妤犵偞鍔栭妶锝夊礃閵娧呭炊闂備礁鎼粙渚€宕㈡總鍛婂珔闁绘柨鍚嬮悡銉╂煟閺傛寧鎯堢€涙繄绱撴担鎻掍壕闂佸憡鍔﹂崰妤呮偂韫囨挴鏀介柣鎰皺娴犮垽鏌涢弮鈧悷褏妲愰幒妤€惟闁靛牆娲ㄩ悡鎾斥攽椤旂》榫氭繛鍜冪悼閸掓帒鈻庨幘宕囶唶闁瑰吋鐣崹褰掓⒒椤栨埃鏀介柣妯虹仛閺嗏晠鏌涚€n偄濮嶇€规洘鍨块獮妯肩磼濡攱瀚奸梻浣告啞缁诲倻鈧凹鍨抽埀顒佺婢瑰棛妲愰幒鎾崇窞閻忕偠妫勯獮瀣磼閳╁啯灏柕鍡樺笒椤繈鏁愰崨顒€顥氶梻鍌欑閹碱偊寮甸鍕剮妞ゆ牜鍋熷畵浣逛繆椤栨氨姣為柛瀣崌濡啫鈽夊▎蹇旀畼闂備線娼荤徊濂稿础閹惰棄绠栨俊銈呭暞閸犲棝鏌涢弴銊ュ妞わ负鍔戝娲川婵犲啠鎷归梺鑽ゅ枂閸庣敻骞冮悙顒夋Ч閹艰揪绲块悡鎾斥攽閻愬弶顥犻柛瀣尵閳ь剟娼ч惌鍌炲蓟閿濆牏鐤€闁规儳澧庨澶愭⒑缂佹﹩娈曟繛鍙夅缚缁顓兼径濠勭暰閻熸粌顑夐崺鈧い鎺嶇缁楁帗銇勯锝囩疄闁轰焦鍔欏畷銊╊敆閳ь剟藟濮樿埖鈷戦悹鍥ㄥ絻椤掋垺銇勯弮鈧悧鐘茬暦閺夎鏃堝川椤撶媭鍞堕梻浣瑰劤濞存岸宕戦崨鏉戠煑闊洦绋掗悡鍐喐濠婂牆绀堥柣鏃傚帶閽冪喖鏌ㄥ┑鍡樺晵闁绘柨鍚嬮崵鎺楁煏閸繃鍣藉ù鐘层偢濮婄粯鎷呯憴鍕哗闂佺ǹ瀵掗崹璺虹暦濠靛洦鍎熼柕濞垮劚閸嬪秹姊绘笟鍥у缂佸鏁婚崺娑㈠箣閿旂晫鍘搁梺绋挎湰閿氶柛鏃€绮嶇换娑㈠川椤撶喎娈楅梺鍝勬湰閻╊垶骞冮姀銈呯骇闁瑰瓨绻嶉悗瀵哥磽閸屾瑧顦﹂柛濠傛贡閺侇噣鏁撻悩鍙夌€梺绋跨灱閸嬫稓绮堥崼銏″枑闊洦绋掗弲顒佺節婵犲倸鏋ゆ繛鎾愁煼閺屾洟宕煎┑鍥舵!闂佺粯鎸鹃崰鏍蓟濞戙垹妫橀柤鎰佸灠椤忣參鏌i幘鍗炩偓婵嬪蓟閵娾晛鍗抽柣鎰ゴ閸嬫捇骞栨担鐟颁簵闂佸搫娲㈤崹娲偂濞嗘挸绾ч柛顐犲劤閻g儤淇婄紒銏犳珝闁哄本绋撻埀顒婄到婢у海绮旈鈧弻锛勪沪閸撗勫垱婵犵绱曢崗姗€銆佸▎鎾村殥闁靛牆娲﹂弲銊╂⒒閸屾瑧鍔嶉柣顏勭秺瀹曟繆绠涢幘顖涚€洪梺鎸庣箓濞诧箓锝為弴銏$厵闁绘垶锕╁▓鏇㈡煕鐎n偄濮嶉柡灞剧洴楠炲洭顢橀悩顔间沪闂備礁鎼鍡涙偡閳轰緡娼栨繛宸簻娴肩娀鏌涢弴銊ュ闁圭柉浜槐鎾存媴閸撴彃鍓遍梺鍦嚀濞差厼鐣峰ú顏勭劦妞ゆ帊闄嶆禍婊堟煙閻戞ê鐓€闁告梻鍠撶槐鎺撳緞鐏炵偓姣堥梺鍝勬湰閻╊垶鐛Ο灏栧亾闂堟稒鍟為柛锝勫嵆濮婅櫣鍖栭弴鐔告緭闂佹悶鍔忓Λ鍕偩闁垮闄勭紒瀣硶閸橆剟姊虹€圭姵銆冩俊鐐村笚缁旂喖寮撮姀锛勫幗闂佺粯鏌ㄩ幗婊堝箠閸愵喗鍊垫慨妯煎帶楠炴ḿ绱掗鑲╁ⅵ鐎规洘锕㈤、娆撴偩鐏炶棄绠為梻鍌欑窔濞佳勭仚闂佺ǹ瀛╅悡鈥崇暦閹达箑唯闁冲搫鍊婚崢钘夆攽閻愭潙鐏ョ€规洦鍓欓埢宥咁吋閸ワ絽浜鹃悷娆忓缁€鈧梺缁樼墪閵堟悂濡存担鑲濇梹鎷呴悷閭︹偓鎾绘⒒閸屾浜鹃梺褰掑亰閸犳氨绮旈崸妤佲拻闁稿本鑹鹃埀顒勵棑缁牊鎷呴崷顓犲骄婵犵數濮村ú銈囧婵犳碍鐓曟繛鎴濆船閻忥紕鈧娲橀悡锟犲蓟瀹ュ牜妾ㄩ梺鍛婃尵閸犳牕顕f繝姘櫜濠㈣泛饪村ḿ濠囨⒑缂佹ḿ鎲块柛瀣崌閺岋綁骞橀悙钘変划闂佸搫澶囬埀顒€纾弳鍡涙倵閿濆骸澧扮悮锕傛⒒娴g瓔鍤冮柛鐘虫崌瀹曞綊鎸婃径灞炬濡炪倖鍔х粻鎴濇暜闁荤喐绮岀换妯虹暦閵忋倕绠抽柟瀛樻⒐閺傗偓闂備胶绮敃鈺呭磻閸涱喖鍨斿ù鐓庣摠閻撴洟鏌¢崶鈺佷户濞寸姵鐩弻锝夋晲閸涱偄浠┑顔硷功閸庛倕岣块鍫濈妞ゆ棁娉曢悰銉╂⒒娴e憡鎲稿┑顔炬暬閹囨倷閻戞ê鈧爼鏌涢幇闈涙灍闁抽攱鍨块弻娑樷槈濮楀牊顣肩紓浣哥埣娴滃爼寮诲☉妯滅喖骞侀幒鎴滃垝婵°倗濮烽崑娑樜涘┑瀣畺婵炲棙鎸婚崐缁樹繆椤栫偞鏁遍悗姘冲亹缁辨捇宕掑▎鎴М濡炪倖鍨靛Λ娑㈠焵椤掑倻鎳楅柛鎰劵閳ь剙娼¢弻鐔封枔閸喗鐏撶紒鐐劤閸氬濡甸崟顖氭闁割煈鍠楅崐顖炴⒑閸︻厽顏熺紒韫矙閳ワ妇鎹勯妸锕€鏋傞梺鍛婃处閸撴盯藝閵娧呯=濞达綀濮ら妴鍐磼椤旂晫鎳冮柣锝囧厴婵℃悂鏁傞崜褏妲囬梻浣告啞濞诧箓宕戦崟顓犱笉闁绘劖绁撮弨浠嬫煟濡櫣浠涢柡鍡忔櫊閺屾稓鈧綆鍋嗛埥澶愭懚閻愮繝绻嗛柕鍫濆€告禍楣冩⒒閸パ屾Ч闁逛究鍔岄~婊堝幢濡も偓婵箓姊洪幐搴g畵闁绘瀚粋宥堛亹閹烘挾鍘甸梺缁樺灦钃遍悘蹇e弮閺屽秷顧侀柛鎾寸懇閹儲绺介崨濠備簵濡炪倖鍔х粻鎴︽倷婵犲洦鐓忓璺虹墕閸旀艾鈹戦鍝勭伈婵﹦鍎ょ€电厧鈻庨幋鐐蹭还闂備浇妗ㄧ粈渚€鈥﹀畡閭﹀殨濠电姵鑹鹃悘宕団偓瑙勬礀濞诧箑鈻撻弴銏♀拺闂侇偆鍋涢懟顖涙櫠鐎电硶鍋撶憴鍕;闁告鍟块锝嗙鐎e灚鏅i梺缁樺姈椤旀牠宕崶顒佺厽闁绘柨鎽滈惌灞筋熆瑜庨〃鍫ュ极椤曗偓閸╋繝宕ㄩ鐔衡偓顒勬⒑閸涘﹤濮﹂柛鐘愁殜閹繝濡烽敂鍓х槇闂傚倸鐗婄粙鎺椝夐悙鐢电<濞达絽寮跺▍鍡椙庨崶褝韬€规洩绲惧鍕節鎼淬埄妫嗙紓鍌氬€峰ù鍥ㄣ仈閹间礁绠查柛銉戝懏娈鹃梺鍦劋閸ㄧ喖寮告惔銊︾厵闁圭⒈鍘奸獮妤冩偖閿曞倹鈷掗柛灞剧懆閸忓矂寮搁鍫熺叆闁哄洦锚閳ь剚娲熼弫鍐閵堝棛鍔堕悗骞垮劚閹冲繘鎮楅鈧—鍐Χ閸℃ḿ锛曢梺绋款儐閹瑰洭寮婚悢纰辨晩闁伙絽鏈崳浼存倵鐟欏嫭澶勯柛瀣工閻g兘鎮㈢喊杈ㄦ櫍闂佺粯鍔栭悾顐﹀即閻愨晜鏂€闂佹寧绋戠€氼剚绂嶆總鍛婄厱濠电姴鍟版晶閬嶆煛娓氬洤娅嶆鐐村笒铻栧ù锝堫潐閻濇牠姊绘担鐟邦嚋闁哄被鍔嶉弲鑸电鐎n偄鍓归梺鐟板⒔缁垶鎮¢悢鍏肩厪闊洦娲栨牎闂佸摜鍠撻崑銈夊蓟閿濆绠婚悗娑欋缚椤︿即姊虹拠鈥虫灍妞ゃ劌锕顐﹀箛椤撶喎鍔呭┑鐘绘涧閻楀繐鈻旈幐搴濈箚闁绘劦浜滈埀顒佹礈閹广垽宕卞☉妯兼煣闂佺粯枪椤曆囨嫅閻旇 鍋撻獮鍨姎婵炲眰鍔庢竟鏇㈠礂闂傚绠氬銈嗙墬缁诲秹宕靛▎鎴犳/闂佹鍨卞▍鍥╃磼鏉堛劍灏伴柟宄版嚇瀹曨偊宕熼幋顖滅М闁哄矉缍侀崺鈩冪節閸屾粈妗撻梻浣虹帛娓氭宕伴弽顓ㄧ稏婵犲﹤鐗嗛悞鍨亜閹烘垵顏ラ柍褜鍏涚粈渚€鍩ユ径濞㈢喖鏌ㄧ€e灚缍屽┑鐘垫暩閸嬫稑螞濞嗘挸绀夐柡宥庡亝椤愯姤銇勯幇鍓佹偧缂佲檧鍋撶紓浣哄亾濠㈡﹢藝鏉堚晛顥氶柛褎顨嗛悡鏇㈡倵閿濆骸浜滈柣蹇擃嚟閳ь剝顫夊ú姗€宕濆▎蹇e殨闁稿﹦鍣ュ銊モ攽閻愭彃鎮戦柣妤佹礋閸╃偤骞嬮敂钘変汗閻庤娲栧ù鍌炲汲閿熺姵鈷戠紒瀣儥閸庡繘鏌涙繝鍌滅Ш濠碉紕鏁诲畷鐔碱敍濮樿京鏉搁梺鑽ゅ█缂傛艾鈻嶉敐鍛傦綁鏁愭径瀣ф嫼闁哄鍋炴竟鍡浰囬敃鍌涚厱濠电姴鍊归崑銉р偓娈垮枦椤曆囧煡婢舵劕顫呴柣妯诲絻缁侇噣姊绘笟鈧ḿ褎鐏欓梺绋挎唉娴滎剛鍒掓繝姘紶闁告洏鍔嶉弬鈧梻浣虹帛閸旀ḿ浜稿▎鎰珷婵炴垯鍨洪悡鏇㈠箹濞n剙鐏╅柍缁樻礋閺屽秹濡烽敂绛嬫閻庤娲橀敃銏ゃ€佸▎鎾冲簥濠㈣鍨板ú锕傛偂閺囥垺鐓冮柍杞扮閺嬨倖绻涢崼鐕傝€块柡宀嬬秮閹垻绮欓崹顕呮綋闂備礁鐤囬~澶愬垂閸ф鏋佺€广儱顦粈瀣亜閹般劌澧查柛鏇炲暣濮婂搫效閸パ呭姶闂佹悶鍔嶆繛濠傜暦閹达箑围濠㈣泛鑻粊锕傛⒑绾懏褰х紒鐘冲灴閿濈偤宕ㄧ€涙ḿ鍘梺鍓插亝缁诲啴宕宠ぐ鎺撶厾闁哄娉曟禒銏ゆ煃鐟欏嫬鐏撮柟顔界懇瀵爼骞嬮悩杈敇闂傚倷娴囧畷鐢稿疮濞嗘挸鐐婄憸蹇涙偂閹达附鈷戦柛娑橈工婵倿鏌涢弬娆炬█鐎殿喓鍔嶇粋鎺斺偓锝庡亞閸樻捇姊洪懞銉冾亪藝娴兼澶娾堪閸喓鍘介棅顐㈡储閸庡磭绮旈鈧弻鐔碱敊鐟欐帒婀辩划璇测槈濮橈絽浜鹃柨婵嗙凹缁ㄧ粯銇勯鈧鍛村煘閹达箑鐏抽柛鎰皺妤犲洭姊洪崨濠冣拹婵炶尙鍠栭弫鎰版倷濞村鏂€闁诲函缍嗛崑鍕枔濠靛鈷戞慨鐟版搐閻忓弶绻涙担鍐叉川瀹撲線鏌熼幍顔碱暭闁抽攱甯掗湁闁挎繂鎳忛崯鐐烘煕閻斿搫浠遍柡灞剧洴瀵噣鍩€椤掑嫬鍨傞柛顭戝枤閺嗭附绻濋棃娑欏闁稿海鍠栭弻鏇$疀婵犲倸鈷夐梺缁樼箓閸㈡煡鍩為幋锔藉€烽柡澶嬪灩娴犙囨⒑閹肩偛濡芥俊鐐扮矙楠炲啴鏁撻悩鎻掑祮闂侀潧绻掓慨鐑筋敊閹扮増鐓涘璺猴功婢ф洖顭胯閺咁偅绔熼弴銏犻敜婵°倓鑳堕崢浠嬫椤愩垺澶勯柣顓у櫍瀹曘儵顢曢妶鍥╋紲闁哄鐗勯崝宀€绮顓犵闁绘挸娴风粻璇测攽閳╁啯鍊愬┑锛勬焿椤т線鏌涙惔锛勭劯婵﹦绮粭鐔煎焵椤掑嫬鐒垫い鎺戝€告禒婊堟煠濞茶鐏¢柡鍛埣瀹曟粏顦寸痪鍓ф櫕閳ь剙绠嶉崕閬嶅箠韫囨蛋澶愬閳垛晛浜鹃悷娆忓缁€鍐煕閵娿儲鍋ラ柣娑卞櫍楠炴帡骞婇搹顐n棃闁糕斁鍋撳銈嗗笒閸婃悂藟濮樿埖鐓曠憸搴ㄣ€冮崱娑欏亗闊洦鎼╅悢鍡涙煠閸濄儲鏆╅柍钘夘槹閵囧嫰鍩℃繝鍌氼潾缂備浇椴哥敮锟犲箖閳哄懎绠甸柟鍝勬鐎垫牠姊绘笟鈧埀顒傚仜閼活垱鏅舵导瀛樼厵闁惧浚鍋呯亸鎵磼閺冨倸鏋戠紒缁樼箞瀹曟儼顦撮柣娑栧劦濮婃椽宕崟顓涙瀱闂佸憡蓱閸庢娊鎮鹃崹顐e闂侇偅绋撶粻姘舵⒑闂堟稓澧曢柟鍐查叄瀵娊鎮㈤搹瑙勶紡闂佺顫夐崝鏇熺閸︻厾纾奸弶鍫涘妽鐏忎即鏌熷畡鐗堝櫧闁瑰嘲缍婇、娑樷堪閸涱垳宕剁紓鍌氬€搁崐鐑芥嚄閼稿灚鍙忛柣鎴f绾剧粯绻涢幋娆忕仼闁绘挻锕㈤弻鐔告綇閹呮В闂佽桨绀侀敃顏堝蓟閿濆鍋勭痪鎷岄哺濞堛儲绻濋姀锝庢綈婵炶尙鍠庨~蹇旂節濮橆剛锛滃┑鐐叉閸ㄥ灚淇婃禒瀣厽閹艰揪绲块幊妤呮煕濞戝崬鏋涢幖鏉戯躬濮婅櫣绮欓幐搴㈡嫳婵犮垼顫夊ú鐔风暦閹达箑绠婚柡鍌樺劜椤秹姊洪崷顓炲妺闁圭ǹ顭烽幃鐢稿冀椤愩倗锛濇繛杈剧稻閸ㄦ繈宕ラ锔界厱閻庯絻鍔岄埀顒佹礋閹箖鏌ㄧ€n剟妾紓浣割儓椤曟娊濡搁埡鍌滃弳闂佸搫鍟犻崑鎾绘煕鎼淬垹鈻曢柣娑卞枛铻栭柛娑卞枓閹风粯绻涢幘鏉戠劰闁稿鎸荤换娑欐媴閸愬弶鍣虹€规洘鐓¢弻娑㈠焺閸愵亖妲堥梺姹囧€楅崑鎾舵崲濞戙垹绠f繛鍡楃箳娴犻箖姊虹粙鍖″伐闁绘牕銈稿濠氬Ω閵夈垺鏂€闂佺硶妾ч弲婊勬櫏闂傚倷鑳剁划顖炲箰鐠囪娲偄閻撳海鐣哄┑掳鍊曢幊蹇涘疾閺屻儱绠圭紒顔煎帨閸嬫捇骞囨担閫涙唉闂傚倸鍊风粈渚€骞栭锔绘晞闁告稑鐡ㄩ悡鈧梺鎸庣箓閹虫劙寮抽敃鍌涚叆闁绘柨鎼牎闂佺粯甯熼崑鎰板焵椤掆偓缁犲秹宕曢崡鐐嶆稑鈽夐姀鐘插亶闂佹眹鍨归幉锟犲煕閹寸姷纾藉ù锝囨娓氭稒绻涢崼鐔割棃闁哄矉绲借灃闁逞屽墴閺佸啴鏁冮埀顒勫煝鎼淬劌顫呴柕鍫濇濞堛倕顪冮妶鍡楃瑨闁稿﹤顭烽弫宥呪堪閸啿鎷虹紓鍌欑劍閳笺倝顢旈崼婵堟焾闂佺鍕垫當闁绘挻绻堥弻锟犲炊閵夈儳浠鹃梺缁樻尰缁嬫捇鍩€椤掆偓閸樻粓宕戦幘缁樼厓鐟滄粓宕滈悢椋庢殾濞村吋娼欓崘鈧悷婊冪箻瀵娊鏁傞懞銉ュ伎濠碉紕鍋犻褎绂嶆ィ鍐┾拺闁荤喐澹嗛敍宥呪攽閻愨晛浜炬俊鐐€戦崹娲€冮崱娆愬床婵犻潧顑呯粈瀣亜閹炬瀚呴敃鍌涒拻闁稿本鑹鹃埀顒佹倐瀹曟劖顦版惔锝囩劶婵炴挻鍩冮崑鎾搭殽閻愭惌娈旀顏冨嵆瀹曠喖顢楅埀顒€顕i崸妤佲拺婵懓娲ら悘鈺呮煙鐠囇呯瘈鐎规洘鍨归埀顒婄秵閸犳鎮¢悢闀愮箚妞ゆ牗绻傛禍褰掓偨椤栨稓娲撮柡灞剧〒閳ь剨缍嗛崐鏍箣閿曗偓妗呴梺鍛婃处閸ㄤ即宕¢搹顐$箚闁靛牆鍊告禍鐐箾鐎涙ḿ鐭嬮柛搴$枃閻忓啴姊虹紒姗堣€挎繛浣冲嫮顩锋繝濠傚缁犲墽鈧懓澹婇崰鏍ь嚕椤曗偓閺屾洟宕遍弴鐙€妲銈庡亝缁捇宕洪埀顒併亜閹烘垵顏╃紒鐘崇墵閺屾洝绠涢弴鐐愩儵鏌¢崱妤婂剶闁哄备鍓濆鍕償椤斿吋顔曢梻渚€娼ч悧鍡浰囨导鏉戠厱闁圭儤顨嗛悡鏇㈡倶閻愭彃鈷旈柟鍐叉嚇閺屾盯寮捄銊愌囨煙椤旂瓔娈樼紒顕呭幖閳藉螣鐠囧弶顏¢柣搴ゎ潐濞叉﹢鎮¢敓鐘茶摕婵炴垶鐭▽顏嗙磽娴i潧鐏╂繛鍫㈠帶閳规垿鎮欓弶鎴犱户闂佺硶鏅涚€氭澘顕i锕€鐐婃い鎺嶈兌閸橆亪妫呴銏″婵炲弶鐗犻悗鐑芥煟閻愬顣茬紒璇茬墕椤繒绱掑Ο璇差€撻柣鐔哥懃鐎氼剚绂掗埡鍛拺缂佸鐏濋惁銊╂煕閵娿劍纭鹃柣锝呭槻閳规垿宕堕妸銉ュΤ闂備焦瀵х换鍌炲箠鎼淬倐鍙㈤梻鍌氬€风欢姘跺焵椤掑倸浠滈柤娲诲灡閺呭墎鈧稒蓱閸欏繐鈹戦悩鎻掆偓褰掑箚閸儱鏋侀柛顐犲劜閻撴洟鏌曟径瀣仴闁瑰啿绉跺Σ鎰枎閹邦喚鐦堥梺姹囧灲濞佳勭閹烘鐓曢柡宥庡亜閳诲牏鈧娲滈崰鏍€佸Ο娆炬Ъ缂備椒绶¢崑鍛崲濠靛鍋ㄩ梻鍫熷垁閵忋倖鐓ラ柡鍥埀顒侇殜閸┾偓妞ゆ帊绀侀幖鎼佹煕閺傝法肖缂侇喖顑呴濂稿川椤忓嫮澧梻浣稿閸嬪棝宕伴幘璇插偍闁归棿鐒﹂埛鎴︽煙閼测晛浠滈柛鏃€锕㈤弻娑欐償閵堝鎽垫繛锝呮搐閿曨亜鐣峰Δ鍐ㄦ瀳閺夊牜鐓堥崯宥夋⒒娴h櫣甯涢柛鏃€鐗犻獮鍡欎沪鐟欙絾鐏佸┑鐘诧工閻楀﹪鎮″☉銏″€堕柣鎰絻閳锋梹绻涢幓鎺旀憼妞ゃ劊鍎甸幃娆撳级閹寸偠鐧佹俊銈囧Х閸嬫盯顢栨径鎰┾偓浣糕槈濮楀棙鍍靛銈嗗笒椤︽澘霉閸℃稒鈷掗柛灞捐壘閳ь剟顥撳▎銏狀潩鐠鸿櫣鍔﹀銈嗗笒閸婂憡绂掑⿰鍫熺厾婵炶尪顕ч悘锟犳煛閸涱厼顣抽柍褜鍓氱粙鎺戠幓鐠恒劎涓嶉柟顖g亹瑜版帗鏅查柛娑卞幗濮f劕鈹戦悙鑼勾闁稿﹥顨堥崚鎺撶節濮橆厼鈧粯淇婇婵嗕汗闁伙箑鐗婄换婵嬫偨闂堟刀銏ゆ煕婵犲倻绉虹€规洝娅曠粋鎺斺偓锝庡亞閸樿棄顪冮妶鍡樺暗闁稿鍋よ棢婵犲﹤鐗婇悡鍐偡濞嗗繐顏╅柣蹇旀尦閺岀喖顢欑憴鍕彋閻庤娲╃徊鎯ь嚗閸曨剛绡€閹肩补鎳i悢鍏尖拻闁稿本鐟ㄩ崗宀€绱掗鍛仸妤犵偞鍔欓獮鏍ㄦ媴閸濄儲鐒惧┑鐐存綑閸氬岣垮▎鎴犱笉闁绘棁娅g壕濂告倵閿濆簼绨芥慨妯稿姂閺屾盯顢曢锟犲仐闂佸搫鏈惄顖炪€侀弴銏℃櫜闁搞儮鏅濋弳顓熶繆閻愵亜鈧呪偓闈涚焸瀹曪綁宕橀…鎴炵稁闂佹儳绻愬﹢杈╁閸忛棿绻嗘い鏍ㄧ箓閸氬綊鏌涘▎蹇旑棞妞ゎ亜鍟存俊鍫曞礃閵娿儺鐎冲┑掳鍊楁慨閿嬬仚闂佺粯绮岄…宄扮暦缁嬭鏃堝焵椤掑嫬绀冮柍褜鍓熼幃宄扳堪閸愮偓鈻堥悗娈垮枔閸斿秶绮嬮幒鏂哄亾閿濆骸浜為柛妯挎閳规垿鍩ラ崱妤冧淮濠电偛鎷戠紞浣割嚕閹间礁绀冩い顓熷灩閸炵敻鏌i悢鍝ユ噧閻庢哎鍎崇槐鎾愁潩鏉堚晝锛滈柡澶婄墑閸斿苯霉椤曗偓閺屾盯鍩為幆褌澹曞┑锛勫亼閸婃牜鏁幒鏂哄亾濮樼厧澧扮紒顔肩墦瀹曟﹢顢欓悾灞藉笚闂備浇宕甸崰鏇㈠春閸ャ劎顩烽柟鐑樻⒒绾惧ジ鏌曟繛鍨姶闁绘挸鍚嬮幈銊︾節閸涱噮浠╅梺鐟板级閹稿啿鐣烽悢纰辨晝闁靛牆瀛╄ⅷ婵犵數濮烽弫鎼佸磻濞戔懞鍥ㄥ鐎涙ê鍓銈嗙墬閸戝綊宕甸弴銏$厵闂傚倸顕ˇ锔剧磼椤愩垻效闁哄本鐩、鏇㈠Χ閸涱喚浜栭梻浣告啞閿曗晜绂嶉鍕垫綎闁惧繒鎳撶€垫煡鏌¢崶鈺佷粶闁冲嘲顦—鍐Χ閸愩劌顬夐梺鍛婃⒐閻熴儵鎮惧畡鎵虫斀閻庯綆鍋勬禍婊堟⒑閹呯婵犫偓闁秵鏅繝濠傜墛閻撴稑顭跨捄鐚村姛濠⒀勫灴閺屾盯寮捄銊愩倕霉濠婂啯鍟為悗浣冨亹閳ь剚绋掑玻鍧楀储閻㈠憡鍊甸柣鐔告緲椤忣偄顭胯椤ㄥ﹤鐣烽幎鑺ユ優闁革富鍘鹃敍婊堟⒑缁嬫寧婀扮紒瀣灩缁叀顦归柡灞界Х椤т線鏌涢幘鍗炲缂佽京鍋ゅ畷鍗炍熺喊杈ㄩ敜婵犵數濞€濞佳囶敄閸涱垳涓嶉柣妯虹-缁犻箖鏌涢埄鍏╂垹浜告导瀛樼厓闂佸灝顑呴悘锕傛煙娓氬灝濮傞柟顔惧厴閹囧醇閻旂ǹ鈧兘姊绘担铏瑰笡閻㈩垱顨呴—鍐╃鐎n亣鎽曞┑鐐村灍閹冲洭鍩€椤掑﹦鐣垫鐐差儏楗即宕煎┑鍛幓闂傚倸鍊烽懗鍓佹兜閸洖妫樺〒姘e亾鐎规洘鍨块獮姗€骞囨担鐟扮槣闂備線娼ч悧鍡椢涘Δ鍛敜濠电姴娲﹂悡鏇㈡倵閿濆骸浜濋悘蹇曟暬閺岋綁濡烽鑽ゆ晼缂備浇椴哥敮鈩冩叏閳ь剟鏌eΟ鍨毢闁活偄瀚伴弻锝嗘償閵忊晛鏅遍梺鍝ュУ椤ㄥ棛鎹㈠☉娆戠瘈闁搞儜鍕偓顒勬⒑閸涘﹤濮﹂柛鐘崇墱婢规洟宕楅懖鈺冾啎闂佺懓顕崑鐘崇珶濡椿娈介柣鎰儗濞堟粍鎱ㄦ繝鍕笡闁瑰嘲鎳樺畷銊︾節閸愩劌澹嶉梻鍌欑閹芥粓宕抽妷鈺佺;濠电姴鍊婚弳锕傛煙閹殿喖顣奸柛瀣ㄥ妿缁辨帞鈧綆鍘界涵鑸点亜閺傛寧顥㈡慨濠呮閹瑰嫰濡搁妷锔句簴濠电姵顔栭崰姘跺极婵犳艾绠栭柍銉︽灱濡插牊淇婇姘辩缂傚秴锕顐﹀箛閺夊灝鎯為梺鑺ッˇ杈╃矓閾忓厜鍋撳▓鍨灍濠电偛锕獮鍐ㄢ枎閹炬潙鈧粯淇婇婊冨付閻㈩垶绠栧缁樻媴鐟欏嫬浠╅梺绋垮缁挸鐣峰鈧畷锝夊Ψ瑜忛敍鐐寸節瀵伴攱婢橀埀顒侇殕閹便劑鎮滈挊澶岋紱濠电偞鍨堕埣銈吤洪宥嗘櫍闂侀潧绻掓慨闈浳i鍕拺闁哄倶鍎插▍鍛存煕閻曚礁鐏¢柛鎺戯躬楠炴﹢顢欓懖鈺呯崜闂備胶绮崝娆忈缚瑜旈妴鍌涚附閸涘﹦鍘遍柣搴秵娴滄繈宕甸崶銊﹀弿濠电姴鍋嗛悡鑲┾偓瑙勬礃鐢帡锝炲┑瀣垫晞闁芥ê顦竟鏇㈡⒑瑜版帗锛熼梻鍕Ч瀹曟垿骞嬮敂鐣屽幗闂侀潧绻堥崹娲汲閳轰讲妲堥柟鎯х-鏁堥梺鍝勭灱閸犳牠骞冨▎鎿冩晢闁逞屽墯閺呭爼顢涘☉姘鳖啎闂佺ǹ绻楅崑鎰櫠椤忓牊鐓冮悷娆忓閻忔挳鏌熼瑙勬珖闁逞屽墮濠€杈ㄦ叏閹绢啟澶娾攽閸垻锛滈梺缁樺姦閸撴瑩宕濋妶澶嬬厱婵﹩鍓﹂崕鎴︽煙楠炲灝鐏╅柍钘夘樀婵偓闁绘ǹ灏埀顒€鐏濋埞鎴﹀煡閸℃浠╅梺鍦拡閸嬪﹪鏁愰悙瀛樺劅闁靛⿵鑵归幏娲⒒閸屾氨澧涚紒瀣尰閺呰泛鈽夊▎鎴犵槇闂侀潧绻嗗Σ鍕嚀閸ф鐓曢柍鍝勫暙娴犺鲸顨ラ悙宸剶闁轰礁鍟撮崺鈧い鎺戝閸婃寧绻涘顔荤凹闁绘挻娲熼弻鐔煎级閸噮鏆㈢紓浣介哺婢瑰棛妲愰幒妤婃晩缁炬媽浜崥瀣攽椤旂》鏀绘俊鐐舵閻g兘濡搁敂鍓х槇闂佸憡鍔х徊鍓р偓姘煼濮婄粯鎷呯憴鍕哗闂佸憡鏌ㄩ懟顖氱幓閸ф鏅搁柣妯哄暱娴犳帒顪冮妶鍡樷拻闁哄拋鍋嗗褔鍩€椤掑嫭鈷戠紒瀣儥閸庢挸鈹戦鍝勨偓鏇$亱闂佸憡鍔戦崝搴ㄥ汲閿曞倹鐓忓┑鐐靛亾濞呮捇鏌℃担鍛婂枠闁哄矉绲介埢搴d沪閹存帒顥氬┑鐘茬棄閵堝懓鏁垮┑鐐差槹閻╊垶宕洪悙鍝勭闁挎棁妫勯埀顒傚厴閺屻倝骞栨担瑙勯敪濠电偞鍤崨顖滐紳婵炶揪绲块幊鎾跺緤缂佹ḿ绠剧痪顓㈩棑缁♀偓闂佺粯渚楅崰妤冩崲濠靛鐐婄憸蹇涱敊閹烘鐓熼幖娣灮閳洟鏌ㄥ鑸电厱闁哄倹瀵ч崳铏圭磼缂佹ḿ绠為柟顔荤矙濡啫霉闊彃鐏查柡灞剧⊕缁绘繈宕熼浣圭槗闁诲孩顔栭崰鎾诲礉瀹ュ洨鐭夐柟鐑樻煛閸嬫捇鏁愭惔鈥茬敖闂佸憡枪濡嫰鍩為幋锕€鐓¢柛鈩冾殘娴犳挳姊虹粙娆惧剱闁告梹顨婂顐︻敊鐏忔牗顫嶅┑鐐叉閸ㄥ綊顢欓弴銏♀拺闁荤喐婢橀弳閬嶆煕閵忊€崇祷閻撱倝鏌ㄩ弴鐐测偓褰掑磻閸岀偞鐓熼柡鍐ㄧ墛濞呮粎绱掔拠鍙夘棦闁哄本娲熷畷鐓庘攽閸″繐浜鹃柛娑橈功椤╂煡鏌涢幘妤€鎳愰敍婵囩箾鏉堝墽绉繛鍜冪悼閺侇喖鈽夐姀鈥充缓濡炪倖鐗楃划灞剧鏉堚斁鍋撶憴鍕鐎光偓閹间胶宓侀柟鐑樺殾閺冨牆鐒垫い鎺戝閻撲線鏌涢妷顔煎闁绘挾鍠栭弻锟犲礃閵婏箑顦╁銈呯箳婵炩偓闁哄矉缍侀弫鍐焵椤掑嫭鍋嬮柟鐐墯濞兼牗绻涘顔荤盎缂佺姴缍婇弻锝夊箛椤撶偟绁锋繝娈垮枛閻倸顫忓ú顏勫窛濠电姴鍟伴崣鍡涙⒑濞茶骞栭柛濠傜仢閻e嘲煤椤忓嫮鍔﹀銈嗗笂闂勫秵绂嶅⿰鍫熺厵闁绘垶锚閻忋儵鏌嶈閸撴瑧绱炴繝鍌ゅ殨闁瑰墎鐡旈弫鍡涙煕閺囥劌澧伴柛妯绘倐閺岋綀绠涢弴鐐板摋濡炪倖娉﹂崟顏嗙畾婵犻潧鍊搁幉锟犳偂閸愵喗鍋℃繛鍡楃箰椤忊晠鏌h箛鎿冨殶闁逞屽墲椤煤閺嵮呮殾妞ゆ帒瀚悡鈥愁熆閼搁潧濮囩紒鐘劚闇夐柨婵嗩槹濞呮粌顭跨憴鍕闁宠鍨堕獮濠囨煕婵犲啫濮嶇€规洘鍨块獮妯呵庨璺ㄧ泿婵$偑鍊栭幐鎾焵椤掆偓閸熸寧鎱ㄥ畡閭︽富闁靛洤宕崐鑽ょ玻閺冨牊鐓涢悘鐐插⒔濞叉潙鈹戦埄鍐╁€愬┑锛勬焿椤︽煡鏌i幘璺烘灈闁诡喗顨呴埢鎾诲垂椤旂晫浠屾俊鐐€栧▔锕傚炊瑜忛崣鈧┑鐘灱閸╂牠宕濋弴顫稏闁告稑鐡ㄩ悡鍐煏婢跺牆鍔氶悽顖滃У閹便劎鎲撮崟鍨杹濠殿喖锕︾划顖炲箯閸涙潙宸濆┑鐘插€瑰▓姗€姊绘担钘夊惞闁哥姴妫濆畷鏇熸媴閸愨晩妫ㄩ梻鍌欐祰婵倝鏁嬮梺鎸庣☉椤︻垶鍩ユ径鎰潊闁斥晛鍟悵鏍⒒娴e懙褰掑嫉椤掑倻鐭欓柛顐犲劚缁狀垱绻涘顔荤凹闁抽攱鍨块弻娑樷槈濮楀牆濮涚紓浣哄У閹瑰洭骞冨Δ鈧~婵嬫偂鎼达絼妗撻梻浣瑰缁诲嫰宕戦妶澶婃瀬闁告劦鍠栫壕鍏肩箾閹寸偠澹樻鐐茬墦濮婄粯鎷呴崨濠冨創闂佺ǹ锕ㄥΛ鍕煝閺冨牆鍗抽柕蹇娾偓鏂ュ亾閸ф鐓欓梻鍌氼嚟閸斿秹鏌i幘瀛樼闁哄苯绉瑰畷顐﹀礋椤愶絾顔勫┑鐐差嚟婵偓銇旈幖浣碘偓鍐Ψ閳哄倸鈧鈧懓澹婇崰鏍礈閸洘鈷戦弶鐐村椤︼箓鏌涢悢鍛婂唉鐎规洘妞介崺鈧い鎺嶉檷娴滄粓鏌熼悜妯虹仴妞ゅ浚鍋嗛埀顒冾潐閹搁娆㈠璺鸿摕闁哄浄绱曢悿鈧繝鐢靛仦閸庤櫕绂嶆ィ鍐╃厾缁炬澘宕晶浼存煟閿濆洤浜惧ǎ鍥э躬閹瑩顢旈崟銊ヤ壕闁哄稁鍘介崑瀣繆閵堝懎鏆欓柛銊︾箘閳ь剙鍘滈崑鎾绘煕閺囥劌浜炴い锔诲櫍閺岋絾鎯旈婊呅i梺绋款儎閻掞妇绮嬪鍛牚闁割偁鍨硅ぐ鍕⒑閹肩偛鍔橀柛鏂跨Ф缁牓鍩€椤掑嫭鈷戦悗鍦閸ゆ瑩鏌eΔ鈧敃顏堢嵁閸儱惟闁挎柨澧介惁鍫ユ⒑閸涘﹥澶勯柛妯垮亹缁參鏁撻悩鏂ユ嫼闂佽崵鍠愬妯何f繝姘厵闁惧浚鍊嬮鍫熷仼闁绘垼妫勬儫闂佹寧鏌ㄦ晶浠嬫儊閸儲鈷戦柛娑橈工婵倿鏌涢弬鎸庢拱缂佹梻鍠庨濂稿川椤忓懏鏉搁梻浣瑰缁嬫垹鈧凹鍓氱粋宥嗙附閸涘﹦鍘辨繝鐢靛Т閸熺増鏅堕悽纰樺亾鐟欏嫭绀€缂傚秴锕獮鍐偩瀹€鈧惌娆撴偣娓氼垳鍘滅紒槌栧櫍濮婄粯鎷呯粙娆炬闂佺粯鎸搁悧鎾崇暦閺夋娼╅悹铏瑰劋鏉堝牓姊洪幐搴㈢闁稿﹤缍婇幃鈥斥枎閹惧磭楠囬梺鍓插亝缁诲倿鍩涢弮鍫熺厽闁挎繂鐗呴崥顐ょ磼鏉堛劌娴柟顔规櫊瀹曨偊宕熼锝呭姃缂傚倸鍊峰ù鍥ㄣ仈閹间礁绠板┑鐘宠壘缁狀垶鏌涘☉鍗炴珮婵炲牅绮欓弻鏇熺節韫囨洜鏆犻梺鍛婄箘閸庛倝銆冮妷鈺傚€烽柤纰卞墰椤斿﹦绱撴担浠嬪摵閻㈩垱甯熼悘鎺楁⒑閸忚偐銈撮柡鍛櫊瀹曨垱鎯旈妸锔规嫼闂佸憡绻傜€氬嘲危閹间焦鐓熸俊銈傚亾婵☆偅鐟╁鏌ユ嚋閻㈡娴勯柣搴秵娴滅偤藝椤愶絿绠鹃悗鐢登圭敮鍫曟煟鎺抽崝鎴﹀箖閳ユ枼鏋庨柟鐐綑娴狀垶姊洪幖鐐插姎婵炲眰鍊濋獮濠囧箛閻楀牆鍓ㄩ梺鍓插亝閹﹪寮崼鐔蜂汗闂傚倸鐗婄粙鎰垝鐠鸿 鏀介柍钘夋娴滄繄绱掔拠鎻掆偓鍧楀箖妤e啯鐓ラ悗锝庡墴濡绢喚绱撴担鍓插創妞ゆ洘濞婃俊鎼佸煛閸屾粌寮抽梻浣告惈閸熺娀宕戦幘缁樼厱閹兼番鍨归埢鏇㈡煟濞戝崬娅嶇€规洜鍘ч埞鎴﹀礃閳哄倹婢戦梻鍌欒兌缁垶鏁嬮梺璇茬箲瀹€绋款嚕閹惰棄鐓涘ù锝呭级閺傗偓婵$偑鍊栧Λ浣肝涢崟顖氱厺闁哄洢鍨洪悡娆撴煣韫囷絽浜芥繛鍫熺矌閳ь剝顫夊ú鏍Χ缁嬫鍤曢柟缁㈠枟閸嬪嫮鈧懓瀚姗€藟濡も偓閳规垿鎮╅崹顐f瘎闂佺ǹ顑嗙粙鎴g亱濠电偛妫欓幐鍝ョ不閺夊簱鏀介柣妯虹-椤f煡鏌涚€n亜鈧潡寮婚弴鐔风窞婵炴垶锕╁ú顓犵磽娴e弶顎嗛柛瀣崌濮婂宕掑顑藉亾閹间焦鍋嬪┑鐘插閻瑩鏌熼幆褏鎽犳繛鍛█閺岋繝宕堕埡鈧槐宕囨喐閻楀牆绗氶柛瀣灴閺屾稑鈽夐崡鐐插濠电偛妯婇崣鍐潖濞差亝鐒婚柣鎰蔼鐎氭澘顭胯閸o綁寮婚敐鍫㈢杸闁哄啫娲らˉ婵嗩渻閵堝骸骞栭柣蹇旂箚閻忔帡鏌h箛鎾剁闁绘娲樼粋宥夋倷椤掍礁寮垮┑顔筋殔濡绂嶅⿰鍛亾鐟欏嫭灏俊顐g箞瀵鏁愰崨顏咁潔闂佸憡顨堥崑鐐烘偟濠靛鍊甸悷娆忓缁€鈧梺缁樼墪閵堟悂濡存担鑲濇棃宕ㄩ鐘插Е婵$偑鍊栫敮鎺斺偓姘煎弮瀹曟垿宕掑☉娆忓伎濠碉紕鍋犻褎绂嶆ィ鍐┾拺闁告繂瀚悘閬嶆煕閻樺磭澧甸柕鍡曠閳藉濮€閻樿尪鈧灝鈹戞幊閸婃劙宕戦幘缁樼厓鐟滄粓宕滃璺虹畺闁稿本绻冮敍鍌涚節濞堝灝鏋熼柨鏇楁櫊瀹曟顫滈埀顒€顕i妸锔绢浄閻庯綆鍋嗛崢浠嬫⒑瑜版帒浜伴柛鎾寸洴楠炴鎮╃紒妯衡偓鍫曠叓閸パ囶€楃€规挸妫濋弻锛勪沪閸撗勫垱闂佺硶鏂侀崜婵嬪箯閸涙潙宸濆┑鐘插枤閸熷姊虹拠鍙夊攭妞ゎ偄顦叅婵せ鍋撶€规洖缍婂畷绋课旈崘銊с偊婵犵妲呴崹鐢稿磻閹邦喖顥氶柛蹇涙?缁诲棙銇勯弽銊х煀閻㈩垵鍩栭〃銉╂倷閺夋垵顫岄梺瀹狀潐閸ㄥ潡骞冨▎鎾村殝闂傚牊绋掗柨顓犵磽閸屾艾鈧摜绮旈鈧畷鎴﹀箻閹颁焦瀵岄梺闈涚墕妤犲憡绂嶅⿰鍕╀簻闁挎棁顕ч悘锕傛煙椤旇棄鍔ら柣锝忕節楠炲秹顢欓懞銉ф殾闂傚倷绀侀幉鈥趁洪敃鍌氱婵炴垯鍨归崒銊╂煕濞戞﹫鍔熺紒鐘荤畺瀵爼宕煎┑鍡忔寖缂備礁顦介崜姘跺Φ閸曨垼鏁冮柕蹇婃櫆绗戦梻浣风串缁蹭粙宕查弻銉﹀仼婵犻潧顑呯粈瀣亜閹烘垵鈧悂鐛幇顑芥斀闁绘劘鍩栬ぐ褏绱撳浣镐壕婵$偑鍊ら崑鍕囬鐐村仼鐎瑰嫭澹嗛弳鍡涙煕閺囥劌澧伴柛妯烘啞缁绘稒娼忛崜褏袣濡炪値鍋勯ˇ顖炴偩瀹勬壆鏆嗛柛鏇ㄥ墰閸樺憡绻涙潏鍓хК妞ゎ偄顦悾宄扮暆閸曨剛鍘告繛杈剧秬椤鐣峰畝鍕厸濞达綀顫夊畷宀勬煛娴h宕岄柡浣规崌閺佹捇鏁撻敓锟�>>  闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁诡垎鍐f寖闂佺娅曢幑鍥灳閺冨牆绀冩い蹇庣娴滈箖鏌ㄥ┑鍡欏嚬缂併劎绮妵鍕箳鐎n亞浠鹃梺闈涙搐鐎氫即鐛崶顒夋晬婵絾瀵ч幑鍥蓟閻斿摜鐟归柛顭戝枛椤牆顪冮妶搴′簼缂侇喗鎸搁悾鐑藉础閻愬秵妫冮崺鈧い鎺戝瀹撲礁鈹戦悩鎻掝伀缁惧彞绮欓弻娑氫沪閹规劕顥濋梺閫炲苯澧伴柟铏崌閿濈偛鈹戠€n€晠鏌嶆潪鎷屽厡闁汇倕鎳愮槐鎾存媴閸撴彃鍓卞銈嗗灦閻熲晛鐣烽妷褉鍋撻敐搴℃灍闁绘挻娲橀妵鍕箛闂堟稐绨肩紓浣藉煐濮樸劎妲愰幘璇茬闁冲搫鍊婚ˇ銉╂⒑鐎圭媭娼愰柛銊ユ健楠炲啴鍩¢崨顔兼濡炪倖甯婄欢鈥澄涢崟顖涒拻濞达絽鎲¢幆鍫熴亜閿旇鐏i柤娲憾閺屽棗顓奸崨顖ょ幢闂備浇顫夊畷姗€顢氳瀹曪繝骞庨懞銉у帾闂婎偄娲﹀ú鏍ф毄闂備焦鐪归崐鏇灻洪鐐嶆盯宕ㄩ幖顓熸櫇闂侀潧绻嗛埀顒佸墯濡茶京绱撻崒娆戭槮妞ゆ垵妫濆畷褰掑垂椤旂偓娈鹃梺闈涱槶閸斿﹥绂嶈ぐ鎺撶厵闁绘垶蓱鐏忕敻鏌涘Ο鍏兼毈婵﹦绮粭鐔煎炊瑜嶆导搴g磽娴e搫校闁搞劌娼¢幃浼搭敋閳ь剟鐛€n亶鐔嗘繝闈涚墛閸も偓濡ゆ浜欓崡鍐茬暦閻旂⒈鏁囬柣姗€娼х敮銊╂⒒閸屾瑧顦﹂柟纰卞亝瀵板嫰宕堕鈧悞鍨亜閹哄秶顦﹀褜鍨堕弻娑橆潩椤掑鍓跺Δ鐘靛仦閻楁粓宕氶幒妤€绀傚璺猴梗婢规洟姊洪懖鈹炬嫛闁告挻绋戦埢鏃堝箰鎼达絿鐦堥梺姹囧灲濞佳勭濠婂嫨浜滈柡鍥ュ妼楠炴鏌熸笟鍨闁诡喕绮欏Λ鍐ㄢ槈濡棿鍠婇梺璇查閸樻粓宕戦幘缁樼厱闁哄洦顨嗛弶褰掓煕鐎n偅宕岀€规洏鍔戦、娆愩偅閸愨晩鈧秶绱撻崒娆戭槮妞ゆ垵鎳橀幃妯衡攽閸垻骞撳┑鐐村灟閸ㄦ椽鎮¢悢鐓庣婵烇綆鍓欓悘顕€鏌嶉娑欑闁圭缍佹俊鑸靛緞鐎n剙骞嶉梻鍌欑閻忔繈顢栭崱娑樜︽繝闈涙处閸欏繐鈹戦悩鍙夊櫤妞ゅ繒濮电换娑㈠箣閻樿櫕姣堥悗瑙勬磸閸旀垿銆佸Ο琛℃斀闁搞儮鏅滅紞搴ㄦ⒒閸屾艾鈧兘鎳楅懜鐢典粴婵$偑鍊栭崹闈浳涘┑瀣畾闁告洦鍨奸弫宥嗘叏濡潡鍝烘繛鍫熷劤閳规垿鎮╃紒妯婚敪闂佸搫鑻悧鎾愁嚕椤曗偓瀹曠厧鈹戦崱娆戝春濠碉紕鍋戦崐鏍ь潖瑜版帒纾块柟鍓佹櫕瀹撲線鏌熼幍顔碱暭闁抽攱甯掗湁闁挎繂鎳忛崯鐐烘煕閻斿搫浠滈柕鍡樺笒椤繈顢樿閻や線鎮楃憴鍕婵犮垺锕㈤敐鐐测攽閸喎纾梺鎯х箰濠€閬嶅几閸愵喗鈷掑ù锝堫潐閸嬬娀鏌涙惔銏°仢鐎规洘绮岄~婵嬫嚋闂堟稐绨垫繝鐢靛仜濡瑩宕濋幋鐐殿洸婵犲﹤鐗婇悡娑㈡煕閹板墎鍒板ù婊堢畺濮婅櫣绮欓幐搴℃敪濠电偛鎳忓ú婊呭垝鐎n喖绠虫俊銈勭劍濞呭棝姊洪崨濠冨瘷闁告粌鍟版惔濠勭磽閸屾艾鈧悂宕愰悜鑺ュ€块柨鏇楀亾闁绘粏宕甸幑鍕Ω瑜岀粭澶愭⒑缂佹ê濮夋い锝勭矙瀹曟垿骞橀懜闈涙瀭闂佸憡娲﹂崜娑⑺囬妷鈺傗拺缂備焦岣挎晶顏堟煏閸懚褰掓偩瀹勬噴娲敂閸曨厼濮堕梻浣告啞閸斿繘寮插☉銏╂晛闁瑰墽绮埛鎴︽煕濞戞﹫鍔熺紓鍌涘哺閺屾稒鎯旈妸銈嗗枤濡炪們鍨哄畝鎼佸蓟閸℃鍚嬮柛鈥崇箲鐎氫粙姊绘担鍛靛綊寮甸鍕殞濡わ絽鍟悞鍨亜閹烘垵鈧悂宕㈤幘顔界厵妞ゆ梹鍎虫禒閬嶆煛娴gǹ鏆g€规洘甯掗~婵囨綇閳哄倹鐦掗梻鍌氬€风粈浣圭珶婵犲洤纾婚柛娑卞姸濞差亜鍐€妞ゆ劑鍩勫Λ婊堟⒑閸︻厐鍦姳閻戞ḿ顩叉繝濠傜墛閻撴稓鈧箍鍎辨鍛婄濠婂厾褰掓偐瀹曞洨鐓傜紓浣介哺鐢繝宕洪埀顒併亜閹哄秶顦︾紒鍓佸仱閺岀喖鏌囬敃鈧晶鐗堛亜閺冣偓閸旀洟鍩為幋锔藉€婚柛銉㈡櫇鏍¢梻浣告啞閹稿鎮烽敂鐣屸攳濠电姴娲ょ粈鍌炴煕韫囨稒锛熸慨姗堢畱閳规垿鎮╃紒妯婚敪濡炪倖鍨靛Λ婵嬪春濞戙垹绠i柨鏃傛櫕閸橀亶姊洪幐搴㈩梿妞ゆ泦鍥╁祦闁哄稁鍘介悡鏇㈡煛閸屾侗鍎ラ柛搴㈠姍閺屾洟宕惰椤忣厼鈹戦埄鍐╁€愬┑锛勫厴閺佸倻绱掑鍫㈢闂傚倸鍊峰ù鍥敋閺嶎厼闂い鏍ㄧ矋瀹曞弶绻濋棃娑卞剰缂佺姵鐗犻弻鏇$疀鐎n亖鍋撻弴鐘电焼闁稿瞼鍋為悡鐘崇箾閺夋埈鍎愭繛鍛噺椤ㄣ儵鎮欓懠顑勬叏婵犲偆鐓肩€规洘甯掗埢搴ㄥ箣閿濆洨宕堕梻鍌欑閹诧繝鎮烽妷褎宕查柟鐑樻煥閸ㄦ繂鈹戦悩瀹犲缂佺媴缍侀弻锝夊箛椤掑倹鎲奸梺缁樼箞閺€杈ㄧ┍婵犲洤围闊洦娲栭崺宀勬⒑閸濄儱娅忛柛銊ョ埣楠炲啴鏁撻悩鎻掑祮闂侀潧楠忕槐鏇㈠储閹间焦鈷戦柛娑橈工婵倿鏌涢弬璺ㄧ劯闁糕斁鍋撳銈嗗笂閻掞箓宕愰幇顔瑰亾濞堝灝鏋熼柟顔煎€搁锝夘敋閳ь剙鐣烽幒鎴斿牚闁告粌鍟版惔濠囨⒒娴e憡鎯堟い锔诲灦閹囧礋椤栨氨顦悗鍏夊亾闁逞屽墰閸掓帡顢橀悜鍡樺兊濡炪倖鎸炬慨鐑筋敊閺囥垺鈷戠紓浣股戠亸顓熺箾閹绢噮妫戠紒顔垮吹閹风姴霉鐎n偅鏉搁梻浣规灱閺呮盯宕鐐茬9闁归偊鍏橀弨浠嬫煥濞戞ê顏柣鎺撳閵囧嫯顦辩紒鑸靛哺瀵鈽夊▎鎰妳闂佹寧绋戠€氼噣宕濋姘f斀妞ゆ梻銆嬮崝鐔虹磼椤曞懎鐏︽鐐茬箻瀹曘劎鈧稒锚閳ь剛绮穱濠囶敍濠婂啫濡洪梺浼欑秵閸撶喎顫忕紒妯诲閻熸瑥瀚禒鈺呮⒑閹肩偛濡芥俊鐐扮矙楠炲啴鏁撻悩铏闂佺粯锕╅崰鎺楀磻閹惧鐟归柍褜鍓欓锝嗙鐎n€晠鏌曟竟顖氭噽瀹撲線姊婚崒娆戭槮缂傚秴锕畷鎴炵節閸パ咁槶濠电偞鍨崺鍕极婵犲洦鐓欓柟娈垮枛椤eジ鏌涚€Q冨⒉缂佺粯绻冪换婵嬪磼濞戞ɑ顏犳俊鐐€х徊浠嬪Χ閹间礁绠栧ù鐘差儛閺佸秵淇婇妶鍕妽闁绘繃宀搁幃妤€鈻撻崹顔界彯闂佺ǹ顑呴敃銈夋偩瀹勯偊娼ㄩ柍褜鍓熼妴浣糕枎閹炬潙浠奸柣蹇曞仩濡嫭淇婇崶顒佲拻闁稿本鐟чˇ锕€顭块悷甯含鐎规洘鍨垮畷銊╊敍濞戞ê绨ラ梻浣呵归惉濂稿磻濞戞褔宕f径宀€顔曢梺绯曞墲椤ㄥ牏鎷归埡鍐╁枑闁绘鐗嗙粭姘舵煕鐎n偄濮嶉柡灞剧洴楠炲洭顢楅埀顒傜棯瑜旈幃褰掑炊閳轰椒绮堕梺瀹狀潐閸ㄥ潡銆佸▎鎴炲厹鐎瑰嫰顣︾槐锝嗕繆閻愵亜鈧倝宕㈡總绋垮簥闁哄被鍎查崑鈺呮煟閹达絾顥夌紒鐘冲▕閺岀喓鈧稒蓱閳锋劙鏌f惔鈽嗙吋婵﹥妞藉畷鐑筋敇閻愭彃顬嗛梻浣规偠閸斿酣寮幖浣告瀬妞ゆ洍鍋撴い銏$洴閹瑧鍒掔憴鍕伖闂傚倷绀侀幉锛勬崲閸屾壕鍋撳鍗炲幋鐎规洘娲栭埥澶娢熻箛鏇熷殌妤楊亙鍗冲畷鐔碱敇閻樺灚婢栨繝鐢靛Х椤n喚妲愰弴銏犳瀬閻犲洩灏欓弳锕傛煟閺冨倵鎷¢柡浣哥У閹便劌顫滈埀顒傛兜閹间礁瑙﹂柛娑卞枤缁♀偓闂佹眹鍨藉ḿ褔鍩㈤崼鐔虹濞达絽鍟块崢鎹愩亹閹烘垹锛滃┑顕嗙到閸氬鎯勯娑楃箚闁割偅娲栭悙濠囨煃閸濆嫬鏋︾紒鍗炲暱閳规垿鎮欑€涙ê闉嶉梺鑹邦潐閸庡磭鍙呴梺闈涚墕椤︻垶宕欓悩缁樼厽闁哄倸鐏濋幃鎴︽煟閹捐泛鏋涢柡宀嬬秮瀵剟宕归楣冪崜婵犵數鍋涢幊搴ㄦ晝椤忓牆钃熼柨婵嗘噳濡插牓鏌涘Δ鍐ㄤ沪闁绘繃绻傝灃闁绘﹢娼ф禒锕傛偨椤栨稑绗╅柣蹇撳暣濮婃椽鏌呴悙鑼跺濠⒀傚嵆閺岋絽顫濋鐐插Б濡炪倖鎸搁崥瀣嚗閸曨厸鍋撻敐搴″妤犵偛鐗撳铏规嫚閼碱剛顔婇梺绋款儐缁嬫帡寮查懜鐢殿浄閻庯綆鍋勯崜褰掓倵閸忓浜鹃梺鍛婃处閸撴盯宕㈤崡鐐╂斀妞ゆ梻鐡斿▓鏃€淇婇锝庢疁闁诡喗锕㈤幃鈺冪磼濡厧甯楅梺鑽ゅ枑閻熴儳鈧凹鍓熼幃姗€骞橀鐣屽幍濡炪倖妫侀~澶娾枍婵犲啨浜滈柕蹇ョ磿閹冲洭鏌熼搹顐ゅ⒌闁糕晪绻濋崺鈧い鎺戝€归~鏇熶繆椤栨繂鍚圭紒鈾€鍋撻梻浣圭湽閸ㄨ棄岣胯缁傛帒饪伴崟鈺€绨婚梺鎸庢煥閻忔繂鐣甸崱娑欑厵妞ゆ牗鑹鹃顓熴亜閵忥紕娲撮柟顔界懇椤㈡梹鎷呴梹鎰棜濠电偞鎸婚崺鍐磻閹惧灈鍋撳▓鍨灆缂侇喗鐟╅妴浣割潨閳ь剟骞冨▎鎾村殤闁搞劍绋戞禍楣冩煕椤垵鏋撻柡鈧禒瀣厽闁归偊鍘界紞鎴︽煟韫囥儳鐣遍柣锝嗙箞閺佹劙宕ㄩ闂存樊闂備浇妗ㄧ粈浣虹矓瑜版帒绠栭柕蹇嬪€曠粈鍌炴倶韫囨梻澧悗姘冲亹缁辨捇宕掑顑藉亾閻戣姤鍊块柨鏇氱劍閹冲矂姊绘担铏瑰笡闁圭ǹ鐖煎畷鏇㈡偨缁嬭儻鎽曞┑鐐村灦閿曗晛岣块埡鍌樹簻闁圭儤鍩堝Σ鎼佹煕閹惧磭鍩f慨濠呮閹风娀鍨鹃搹顐ゅ讲缂傚倷鑳剁划顖滄崲閸岀偞鍋╃€瑰嫰鍋婂ḿ銊╂煃瑜滈崜鐔煎Υ娴g硶鏋庨柟鐐綑娴犲ジ鏌h箛鏇炰哗婵☆偄瀚穱濠囧炊閵娧呯槇闂佹眹鍨藉ḿ褑鈪烽梻浣规偠閸斿酣宕㈣閸┿垽寮惔鎾搭潔闂侀潧绻嗛埀顒€鍘栫純鏇㈡⒒娴h櫣銆婇柛鎾寸箘缁瑩骞嬮悩鐢电劶婵犮垼娉涢鍡涘矗韫囨柧绻嗘い鏍ㄥ搸娴犳帡鏌涘鐓庝簽闁汇儺浜獮鍡氼槹闁稿鍨介弻鈥崇暆鐎n剙鍩岄梺瀹狀嚙闁帮綁鐛崶顒夋晩闁芥ê顦伴悵锝夋⒒娴g瓔鍤欓悗娑掓櫊瀹曟瑧鎲撮崟顓ф锤闂佺粯鍔曢幖顐ょ不閺屻儲鐓忛煫鍥ь儏閳ь剚娲熼悰顕€濮€閳ヨ尙绠氬銈嗙墱閸嬬偛鈻嶅⿰鍛<闁靛ǹ鍎洪悡鍏兼叏婵犲啯銇濈€规洦鍋婂畷鐔碱敇婢跺苯鈻堥柡灞剧洴瀵剟宕稿Δ鈧浼存倵鐟欏嫭澶勯柛銊ㄦ硾椤曪絾绻濆顑┿劑鏌ㄩ弮鍌滃笡妞ゃ儱锕ユ穱濠囨倷椤忓嫧鍋撻弽顐f殰闁圭儤顧傞崶顒夋晬婵炴垶鐟﹂悵鐑芥⒑閸︻叀妾搁柛鐘愁殜閹€斥槈閵忊€斥偓鍫曟煟閹邦喗鏆╅柕鍡楋躬閺屾稓鈧綆鍋呯亸顓㈡煟閿濆洤鍘寸€规洖鐖兼俊鎼佹晜閻愵剚顔曢梻鍌氬€搁崐椋庢濮樿泛鐒垫い鎺戝€告禒婊堟煠濞茶鐏¢柡鍛閳ь剛鏁哥涵鍫曞磻閹捐埖鍠嗛柛鏇ㄥ墰閿涙盯姊洪崨濠庢當闁哥喎娼¢、姘舵晲婢跺﹦锛欓梺缁樻磻閻掞箓鐎烽梻鍌氬€风粈渚€骞栭鈶芥盯骞橀瑙f寖闂佸憡娲﹂崜娑㈠煘瀹ュ應鏀介柣妯哄级閹兼劙宕堕幘顔解拺闁告稑锕g欢閬嶆煕閻樺磭澧柍璇茬Ч閺佹劙宕堕埡鍐跨闯濠电偠鎻徊鎹愩亹閸愨晝顩插Δ锝呭暞閳锋垹绱掔€n厽纭堕柣蹇涗憾閺屾稓鈧綆鍓欐禒閬嶆煙椤曞棛绡€闁诡喓鍨藉畷妤呮嚃閳轰礁绠ラ梻鍌欒兌缁垶宕濋敃鍌氱婵炲棙鎸搁悡婵嬫煛閸モ晛鏋傚ù婊勭矒楠炴牕菐椤掆偓閻掔儤绻涢崼鐔虹煉闁哄备鈧磭鏆嗛悗锝庡墰閻﹀牓姊虹化鏇熸澒闁稿鎸搁—鍐Χ閸℃鐟ㄩ柣搴㈡皑閸忔ê顕i锕€鐐婃い鎺嶈兌閸樹粙姊洪崫鍕偓鎼佹倶濠靛鈧倸鐣烽崶鈺冿紲闂佺粯锚閸熷潡宕悜妯诲弿濠电姴鎳忛鐘电磼鏉堛劌绗掗摶锝夋煕濠靛棗鐝旈柡鍥╁枔缁犻箖鎮楀☉娆嬬細闁活厼顑囩槐鎺楊敊閼恒儱纾抽悗瑙勬礃濡炰粙宕洪埀顒併亜閹哄秹妾峰ù婊勭矒閺岀喖宕崟顓夈倖銇勯敂鑲╃暤闁哄矉缍€缁犳盯骞欓崘銊︻啀闂備線鈧偛鑻晶鍙夈亜椤愩埄妲搁悡銈嗕繆椤栨哎鍋ㄦ繛宸簼閸嬪嫬鈹戦崒姘兼Ц婵炲牄鍔嶇换婵嬫偨闂堟刀锝夋煠鐟欏嫬鍔ら柡渚囧櫍濮婄粯绗熼埀顒€岣胯閺佸秷绠涢弴姘媰闂佸吋浜介崕鎻捫掓径鎰拻闁稿本鑹鹃埀顒佹倐瀹曟劙鎮滈懞銉モ偓鍧楁煥閺囩偛鈧摜绮婚弽顓熺厱妞ゆ劧绲剧粈鈧紒鍓у亾鐎笛呮崲濞戞﹩鍟呮い鏃囧吹閻╁海绱撴担鎻掍壕闂佺ǹ鏈粙鎾剁不妤e啯鐓曢柍鈺佸彁閹寸姳鐒婃い鎾卞灪閻撶喖鏌熼悜妯虹仼濞寸姵鐩弻鏇㈠炊瑜嶉顓燁殽閻愬樊鍎旈柡浣瑰姍瀹曞崬鈻庡浣镐壕濠电姴鍋嗗〒濠氭煏閸繄绠烘い鎾存そ濮婂宕熼銏╀純婵犵绱曢弫璇茬暦閻旂⒈鏁嶉柨婵嗘濞呭洭姊绘担鐟邦嚋缂佽鍊哥叅闁靛ň鏅滈崑鍌氼熆閼搁潧濮堥柍閿嬪灩缁辨帡顢涘☉娆戭槰闂佸搫顦紞濠囧蓟濞戞埃鍋撻敐搴′簼閻忓浚鍘介妵鍕敂閸曨偅娈绘繝纰樷偓宕囧煟鐎规洖宕灃闁告劦浜濋崳顖炴⒒娴g瓔鍤欓悗娑掓櫊瀹曟瑨銇愰幒鎴犵崶闂佸搫绋侀崢浠嬪磻閳哄懏鐓曟い顓熷灥娴滅偤鏌i悢椋庣Ш闁哄苯绉烽¨渚€鏌涢幘璺烘瀻妞ゆ洩绲剧换婵嗩潩椤掑倷绱滈梻浣哥秺椤o妇绮堟笟鈧獮鍐箣閿旇В鎷洪梺鍛婄☉閿曘倖鎱ㄩ崒鐐寸厱闁哄倽娉曢悞鎼佹煃閵夛妇澧€垫澘瀚埀顒婄秵閸撴盯鎯侀崼婵冩斀闁绘劘灏欐晶鏇㈡煟韫囨梻绠為柟顔斤耿閺佹捇鎮╁畷鍥у箥闂備礁鎲$粙鎴︽晝閵堝鐓濋柡鍥╁Л閸嬫挸鈻撻崹顔界亪濡炪値鍘鹃崗妯侯嚕椤愶箑绠涙い鎾跺仧缁愮偤鏌f惔顖滅У濞存粍鐟ч懞閬嶆嚒閵堝洨锛濇繛杈剧到閹碱偅绂嶉幆褉鏀芥い鏍ㄧ箓琚氶梺闈涙处濮婅崵鍒掑▎鎰劅闁规儳顕禍鏍⒒娓氣偓濞佳囁囬锕€鐤炬繝濠傜墕閻撴洟鏌熸潏楣冩闁绘挻娲樼换娑㈠箣閻戝洤鍙曢梺鍛婃⒒閸犳挾妲愰幒妤佸亹鐎规洖娲ら~褔姊洪棃娑欐悙閻庢氨澧楁穱濠囧箹娴h倽銊︺亜閺嶃劎鐓紒鎲嬬稻娣囧﹪鎮欓鍕ㄥ亾閵堝纾婚柛鏇ㄥ幗瀹曟煡鏌熼悜妯烩拹妞ゎ偅娲熼弻鐔兼倻濡儤顔曢梺缁樻⒒閸庛倗鈧碍姘ㄩ埀顒傛嚀婢瑰﹪宕伴幒妤€纾婚柟鎹愵嚙缁犺崵绱撴担楠ㄦ岸骞忓ú顏呪拺閻犲洠鈧磭鈧鏌涘☉鍗炵伇闁哥偛澧庣槐鎾诲磼濞嗘帒鍘℃繝娈垮枛椤曨厾鍒掗弮鍥ヤ汗闁圭儤鍨跺Σ顒勬⒑闁偛鑻晶顖炴煏閸パ冾伃妤犵偞甯″畷鍗烆渻閹屾闂傚倸鍊烽悞锔锯偓绗涘厾娲晜閻e矈娲稿銈呯箰鐎氱兘宕甸弴銏″仯闁搞儯鍔庨妶瀛樹繆閹绘帞澧﹂柡灞炬礉缁犳盯寮撮悙鎰╁劜閵囧嫰寮埀顒傛暜閿熺姴钃熼柨婵嗘閸庣喖鏌曟繝蹇涙闂佹鍙冨铏规兜閸涱厜鎾剁磼椤旇姤宕屾鐐插暣瀹曠ǹ螖閳ь剛绮堢€n偁浜滈柡宥冨妿閳藉鏌嶈閸撴盯寮繝姘畺鐎瑰嫭澹嬮弸搴ㄧ叓閸ャ劍鎯勫ù鐘插⒔缁辨挻鎷呴幓鎺嶅闂備礁鎲¢崝锔界閻愰潧顥氬┑鍌氭啞閸嬶綁鏌涢妷鎴濆暟妤犲洤顪冮妶鍐ㄥ姢濠殿噣顥撳Σ鎰板箳濡ゅ﹥鏅╁┑鐐叉閸庡啿鈻撻銏♀拺閻庡湱濮甸ˉ澶嬨亜閿旇鐏ラ柣蹇斿浮濮婄粯鎷呴崫銉よ檸濡炪倖鍨堕崝鏇炵幓閸ф绫嶉柍褜鍓涢幑銏犫攽閸繃鐎冲┑鈽嗗灡濡炲灝岣块幋锔解拺闁硅偐鍋涙俊钘夆攽閻愯鏀诲ǎ鍥э功閳ь剛鏁哥涵鍫曞磻閹剧粯鏅查幖绮光偓鎰佹浇婵$偑鍊ら崑鍛洪悢濂夋綎婵炲樊浜堕弫鍡涙煃瑜滈崜娑氬垝閺冨牊鍋ㄧ紒瀣硶閸橀亶姊洪崷顓炲妺闁搞倖淇洪妵鎰板箳閹惧瓨鐝抽梻浣告啞娓氭宕伴弽顓炴辈闁割偁鍎查悡鐔兼煟濡搫鏆卞┑顔ㄥ懐纾肩紓浣贯缚缁犵偟鈧鍠涢褔鍩ユ径濠庢僵闁挎繂鎳嶆竟鏇㈡⒑閹稿海绠撳Δ鐘叉啞缁傚秴鈹戦崼姘壕閻熸瑥瀚粈鈧梺娲诲墮閵堟悂宕洪埀顒併亜閹烘垵鏋ゆ繛鍏煎姈缁绘盯宕f径鍛窗闂佸憡甯楃敮鎺楁偩濠靛绀嬮柛鎾茶兌閳笺倖绻濋悽闈涒枅婵炰匠鍥ㄥ亱濠电姴鍊婚弳锕€顭跨捄濂斤繝寮崼鐔告珖闂侀€炲苯澧寸€殿喗褰冮埞鎴犫偓锝庝簻瀹撳棝姊洪棃娑㈢崪缂佽鲸娲熷畷銏$鐎n偆鍘甸梺绋跨箰閸氬宕曞Δ鍛厱闁靛ǹ鍎抽敍宥囩磼椤旇姤顥堥柟顔荤矙瀹曘劍绻濋崟顐㈢疄闂傚倷鑳剁划顖濇懌闂佸憡鎸婚懝楣冨煝閹炬枼鍫柛顐ゅ枔閸橀潧顪冮妶鍡樼婵☆偅绋撳褔鍩€椤掑嫭鍊垫繛鍫濈仢閺嬬喖鏌熷灞剧彧闁逛究鍔戦崺鈧い鎺戝閻撱儲绻涢幋鐏活亪顢旈埡鍛仺妞ゆ牗渚楀▓婊勬叏婵犲嫮甯涢柟宄版嚇瀹曨偊濡烽敂閿亾椤斿皷鏀介柍鈺佸暔娴犵娀鏌涢弬鎸庢崳闁告帗甯″畷濂告偄閾忚鍤岄梻渚€鈧偛鑻晶顔姐亜閺囶亞绉鐐寸墬閹峰懘鎳栧顓炴处閻撴洟鏌嶉埡浣告殶闁瑰啿鎳忛妵鍕籍閳ь剙煤閻斿娼栨繛宸簻缁€鍫ユ煙缂佹ê绗傜紒銊ょ矙濮婃椽宕妷銉︾€诲銈嗗灥椤︾敻鎮伴閿亾閿濆骸鏋熼柛濠囶棑閻ヮ亪鎮ч崺铏灴瀵偊妫冨☉鎺撴杸闂佺粯锚閻忔岸寮抽埡浣叉斀妞ゆ棁濮ょ紞鎴︽婢舵劖鐓曠€光偓閳ь剟宕戝☉銏犲嚑濞达綀銆€閸嬫捇鐛崹顔煎濠碘槅鍋呴悷鈺佺暦閿濆牏鐤€闁哄啠鍋撻柛娆忕箲娣囧﹪濡堕崒姘婵犵妲呴崑鍛淬€冮崱娑樼柧闁告挷鐒︾€氭岸鎮锋担椋庮槮缂傚秴锕獮鍐焺閸愨晛鍔呴梺鏂ユ櫅閸燁垶顢欓幒鎾剁瘈婵炲牆鐏濋弸娑㈡煥閺囨ê鍔氭い顏勫暣閹稿﹥寰勭仦鐐啎婵$偑鍊栭崝褏绮婚幋鐘电焼閻庯綆鍋佹禍婊堟煙閹规劖纭剧€涙繃绻濆▓鍨灓闁哄拋鍋嗗Σ鎰板箻鐠囪尙锛滃┑鐐叉閸ㄥ灚淇婃禒瀣拺缂備焦蓱閹牏绱掓潏銊︾闁告帗甯楃换婵嗩潩椤掆偓閸炪劌顪冮妶鍡樺暗濠殿喖顕划濠囨晝閸屾稈鎷虹紓渚囧灡濞叉牗鏅堕懠顒傜<閻庯綆鍋勯悘鈺呮煟濮橆厼鍔ゆい鎾冲悑瀵板嫮鈧綆鍓欓獮鍫熶繆閻愵亜鈧牠宕濊瀵板﹥銈i崘銊э紵闂佸搫娲㈤崹娲偂閸愵喗鐓曟繝闈涙椤忣亪鏌涢敐鍡樸仢闁哄矉缍侀獮姗€宕¢悙鎻捫曢梻浣告惈閻鎹㈠┑鍡欐殾闁圭儤鍩堝ḿ鈺傘亜閹达絽袚閻庡灚鐗犲缁樻媴鐟欏嫨浠ч梺鍛娒肩划娆撳箖閻戣棄鐓涢柛娑卞弨閹芥洟姊洪弬銉︽珔闁哥喍鍗抽幃鐤亹閹烘挾鍘遍梺闈涱樈閸ㄦ娊鎮鹃悽鍛婄厱閻庯綆鍋掑▓鏃堟煃鐟欏嫬鐏存い銏$懅濞戦潧鐣¢弶娆炬浆缂傚倸鍊风欢锟犲闯椤曗偓瀹曞綊宕奸弴鐘茬ウ闂婎偄娲︾粙鎴濐啅濠靛鐓涘璺侯儏閻忋儳绱掗幇顓犫姇缂佺粯绻堥幃浠嬫濞磋翰鍨介弻娑欑節閸曨剙娈岄梺宕囩帛閹告悂锝炲⿰鍫濈劦妞ゆ巻鍋撴い顐㈢箳缁辨帒螣鐠囧樊鈧捇姊洪崨濠勭畵閻庢凹鍓氱粋鎺懳熼懖鈺冿紳闂佺ǹ鏈銊ョ摥闂備焦瀵уú鈺備繆閸ヮ剙绀嗛柟鐑樻尵缁♀偓濠殿喗锕╅崜娆撳船閵娿儺娓婚柕鍫濇鐏忔澘顭跨憴鍕鐎规洘鍨块獮妯尖偓闈涙憸閹虫繈姊洪柅鐐茶嫰婢ь喗銇勯弴顏嗙ɑ缂佸倹甯為埀顒婄秵閳ь剦鍘搁弲鐘诲蓟閺囩喓鐝舵い鏍ㄧ閸g晫鈧鎸风欢姘潖婵犳艾纾兼繛鍡樺焾濡差喚绱撻崒姘毙㈤柨鏇ㄤ簻閻g兘骞嬮悙鐢电槇闂佹悶鍎滈崨顖氱倞闂傚倷绀侀幖顐ょ矙娓氣偓瀹曟垿宕卞☉娆忓壒闂佸壊鍋侀崕鏌ユ偂閵夆晜鐓涢柛銉㈡櫅娴犳粓鏌嶈閸撴瑧绱炴繝鍥ф槬婵炴垯鍨圭粻锝夋煟濡櫣浠涢柨娑樼箰椤啴濡堕崱妯烘殫闂佺ǹ顑囬崑銈呯暦閹惰姤鎯為悷娆忓閺嬫垿姊虹涵鍛【闁挎洏鍊曠叅闁挎洖鍊搁悡鏇㈡煙閻戞﹩娈曢柣鎾存礋閺岋繝宕堕妷銉ヮ瀳婵炲瓨绮嶇划宥夊Φ閸曨喚鐤€闁挎繂鎳庣粻濠氭⒑闁偛鑻晶顖涖亜閺冣偓閻楃姴鐣烽弶璇炬棃宕ㄩ闂寸暗闂備浇娉曢崰鎾存叏瀹勬壆鏆ゅ〒姘e亾闁哄瞼鍠栭獮鎴﹀箛闂堟稒顔勭紓鍌欒兌婵儳鈻嶉弴鐘冲床婵犻潧顑嗛ˉ鍫熺箾閹寸偠澹樻い锝嗘そ濮婄儤娼幍顔煎闂佽鍠栭崐鎼侊綖韫囨拋娲敂閸涱厽顓奸梻渚€娼ч悧鍡涘箟濞戙埄鏁嗗ù锝堟椤旀洟姊洪崨濠勭煀闁哥喍鍗抽獮鍐偂楠炵喓鎳撻オ浼村礋椤掆偓閳ь剚鍔曢埞鎴﹀焺閸愨晛鈧劙鏌涢埞鎯у⒉闁瑰嘲鎳忕粭鐔碱敍濞磋翰鍎靛濠氬磼濞嗘帒鍘$紓渚囧櫘閸ㄤ即锝炶箛姘ヤ汗闁圭儤鍨归悾娲⒑閻撳孩鎲搁柡浣规倐閵嗗懘宕f径宀€鐦堟繝鐢靛Т閸婄粯鏅跺☉銏$厽闁规儳顕ú鎾煛鐏炲墽銆掑ù鐙呯畵瀹曟粏顦俊鎻掔墕椤啴濡堕崱妯碱槰缂備緡鍠楅幑鍥ь嚕鐠囨祴妲堥柕蹇曞瑜旈弻娑樷槈閸楃偞鐏堝銈忚吂閺呯姴顫忓ú顏呯劵婵炴垶鍩冮弫鈧梻浣告啞閺屻劎绮旈崼鏇炵闁靛繒濮弨浠嬫倵閿濆簼绨芥い锔哄姂濮婂搫鐣烽崶銊ユ畬闂侀潧娲﹂敃銏ゅ箹鐟欏嫭鍎熼柕蹇嬪灮閻﹀牏绱掗崜褍顣奸拑杈ㄣ亜椤愵澁韬柡灞剧〒閳ь剨缍嗘禍婊堫敂椤撶姭鍋撶憴鍕闁搞劌鐖奸妴渚€寮撮姀鈩冩珖闂侀€炲苯澧撮柟顕嗙節閸ㄩ箖骞囨担鍝勬暩闂佽崵濮惧銊ф媰閿曞倸纾块柟閭﹀枤绾剧晫鈧箍鍎遍幊蹇涘窗濮椻偓閺岋紕浠﹂悙顒傤槰缂備胶绮惄顖氱暦瑜版帩鏁婇柛娆嶅劤濡垶姊婚崒娆愮グ妞ゆ泦鍛床閻庯綆鍓氶鑺ユ叏濮楀棗澧绘繛鍏肩墪閳规垿鎮╃€圭姴顥濈紒鐐劤閸氬鎹㈠☉銏犲耿婵☆垵娅f禒瀛樼節绾版ǚ鍋撻懠顒傜厯濠殿喖锕ㄥ▍锝夊箯閻樿鐏抽柧蹇e亞娴滎亪姊绘担铏瑰笡闁绘绮撳畷銏n樄闁诡喗鍎抽悾锟犲箥閾忣偅鏉搁梻浣虹《閸撴繈鎮烽敃鈧埢鎾诲即閵忊檧鎷洪梻渚囧亞閸嬫盯鎳熼娑欐珷妞ゆ牗绮庣壕濂告煛閸愩劌鈧悂寮稿☉姘e亾濞堝灝鏋熼柟姝屾珪閹便劑鍩€椤掑嫭鐓冮柛婵嗗閳ь剛鎳撻埢宥咁吋婢跺鎷绘繛杈剧秬濞咃絿鏁☉銏″珔閺夊牃鏅滈崰鎰版煛婢跺﹦浠㈤柡鍡秮閺岀喖顢欑紓瀛樺灩閹广垹鈹戠€n亞鍊為梺闈浨归崹铏光偓姘偢濮婄粯鎷呴崨濠傛殘闂佺懓鎲″Σ鎺楀Φ閹版澘绀冮柍鍝勫枤濞叉悂姊虹紒妯哄闁稿簺鍊濋幃锟犲即閵忥紕鍘藉┑鈽嗗灠閹碱偆鐥閺岀喖鎯傞崫銉戠紓浣虹帛閻╊垰鐣烽柆宥呯疀妞ゆ帒鍊风槐娆撴⒒娴g瓔鍤冮柛鐘愁殜閹兘鍩¢崨顓犵暫濠电姴锕ら崥姗€鎮㈤崗鐓庝簵闁硅壈鎻槐鏇㈩敇婵傚憡鈷掗柛灞捐壘閳ь剚鎮傚畷鎰槹鎼淬埄鍋ㄩ梺璺ㄥ枔婵挳鎯屽Δ鍛彄闁搞儯鍔嶇粈鍫濃槈閹惧磭效闁哄瞼鍠愬ḿ蹇涘箚瑜滃ú顓㈡倵鐟欏嫭灏柣鎺炵畵楠炲牓濡搁妷顔藉瘜闁荤姴娲╁鎾寸珶閺囥垺鈷掑ù锝呮啞閹牓鏌¢崼顐㈠缂侇喗鐟╅獮瀣晲閸ワ箒鍩呴梻鍌氬€风欢姘缚閼姐倐鍋撻棃娑氱劯鐎规洏鍨洪妶锝夊礃閳轰椒绨甸梻浣告贡閸嬫捇寮告總绋跨哗闁兼亽鍎禍婊堟煛閸愩劌鈧爼鍩€椤掆偓椤戝鎮¢鍕垫晢闁稿本绮庨敍婵嬫⒑缁嬫寧婀扮紒瀣灴瀹曨偊宕崟銊︽杸闂佹寧绋戠€氼參寮抽渚囨闁绘劕寮堕崰妯尖偓娈垮枛婢у酣骞戦崟顖椻偓锕傚箣濠靛洦姣岄梻鍌氬€搁崐鐑芥嚄閸洖绠犻柟鍓х帛閸嬨倝鏌曟繛褍鍟悘濠囨倵閸忓浜鹃梺鍛婃处閸嬪嫰宕甸幋锔解拺闁告挻褰冩禍鏍煕鎼淬垻鍙€闁糕晜鐩獮鎺楀箠閵娿儳绉洪柡浣瑰姍瀹曘劑顢欓崗鍏肩暭闂傚倷鑳堕、濠勪焊濞嗘劗浠氶梻浣哥枃椤宕归崸妞尖偓浣糕枎閹炬潙鈧攱銇勯幒宥囧妽闁伙附鎹囧缁樼瑹閳ь剙岣胯铻炴俊銈呮噹閻ゎ喗銇勯弽銊х煁鐎规洖寮剁换婵嬫濞戝崬鍓扮紒鐐劤閸氬鎹㈠┑鍥╃瘈闁稿本鍑规禒鎯ь渻閵堝棙鈷愭繛鑼枎椤繒绱掑Ο璇差€撻梺闈╁瘜閸樹粙鎳i崶顒佲拺闁硅偐鍋涙俊璺ㄧ磼椤曞懎鐏﹂柟顔矫埢搴ㄥ箻缁瀚肩紓鍌氬€烽悞锕傛晪缂備焦顨嗙敮锟犲蓟閿濆牏鐤€闁哄倸鐏濋幗鍨節绾板纾块柡浣筋嚙閻g兘鎮㈢喊杈ㄦ櫖濠殿喗锕㈢涵鎼佸船濞差亝鈷掑ù锝囧劋閸も偓闂佸鏉垮闁瑰箍鍨归濂稿幢濞嗘ɑ绁┑掳鍊х徊浠嬪疮椤栫偛鐓曢柟杈鹃檮閻撴瑩鏌熼娑欑凡鐞氭岸姊烘潪鎵獢濞存粌鐖煎璇测槈閵忕姈鈺呮煏婢舵稓鐣卞ù鐘虫尦閹鈻撻崹顔界亪濡炪値鍘鹃崗姗€鐛崘顔碱潊闁靛牆鎳愰ˇ褔姊虹紒妯诲碍閻庢稈鏅犻幃鐐鐎涙ǚ鎷绘繛杈剧到閹芥粓寮搁崘鈺€绻嗘俊鐐靛帶婵″吋銇勯鍕殻妤犵偞甯″顒勫垂椤斿彞鍠婇梻鍌欑婢瑰﹪宕戦崨顒煎搫顫滈埀顒勫春濞戙垹绠i柨鏃囆掗幏鍝勵渻閵堝棗濮傞柛濠冩礃缁傛帒饪伴崼鐔哄幘濠电偠灏褔鎮橀敂閿亾鐟欏嫭纾搁柛銊ょ矙楠炲啯绂掔€n亜绐涙繝鐢靛Т鐎氼剟鐛崼婵冩斀闁绘ê鐏氶弳鈺佲攽椤旇姤灏︾€规洦鍨堕獮宥夘敊閸欍儳鐟濋梻浣烘嚀婢х晫鍒掗鐐村亗闁绘柨鍚嬮悡銉︾節闂堟稒顥為柟鍏煎姍閺屾稑螣閾忚鎲煎銈冨妸閸庣敻骞冨▎鎾宠摕闁靛鍎遍崣濠囨⒒娴g儤鍤€缁剧虎鍙冨畷鎴﹀Χ閸℃洜绠氶梺缁樺灱婵倝寮插⿰鍫熺厽闁挎繂鎳撶€氭壆绱掗埀顒佺瑹閳ь剙顫忔繝姘<婵﹩鍏橀崑鎾搭槹鎼达絿鐒兼繛鎾村焹閸嬫挻顨ラ悙宸█闁糕晛瀚板畷姗€顢旈崱妯烘疄濠电姴鐥夐弶搴撳亾閺囥垹绠犻幖娣妼閸ㄥ倿鏌涘畝鈧崑鐐烘偂閺囩喍绻嗛柕鍫濇噹閺嗘瑥霉濠婂啰绉洪柡宀嬬磿閳ь剨缍嗛崑鍛存偂閵夆晜鎳氶柡宥庡幗閻撱儲绻濋棃娑欘棡闁革絽缍婇弻锟犲幢濞嗗繋妲愰梺鍝勮嫰缁夊綊寮婚妸褉鍋撻敐搴濈敖濞寸厧鐭傚铏规嫚閳ヨ櫕鐏堢紓鍌氱Т閿曨亪鎮伴鐣岀懝闁逞屽墴閻涱噣骞掑Δ鈧粻锝嗙節閸偄濮夐柍褜鍓氭繛濠傤潖缂佹ɑ濯撮柛娑橈攻閸庢挸顪冮妶鍡楃仴婵☆偅绻傞锝嗙節濮橆儵鈺呮煃鏉炴媽鍏岄柛妯绘尦濮婅櫣娑甸崨顔兼锭闁诲酣娼ч惌鍌氼嚕椤愶絿绡€闁告洦鍘介敍蹇涙⒑閸濆嫷妲搁柣蹇旂箞閹虫粎鎲撮崟顓狀啎闂佸壊鍋呯换鍌炪€傚畷鍥╃<閺夊牄鍔嶇亸鎵磼濡ゅ啫鏋涚€规洘鍎奸ˇ鎶芥煟韫囨挾澧︽慨濠呮缁辨帒顫滈崱妯兼殾闂備胶鎳撻幉锟犲箖閸岀偛绠栭柟顖嗗懏娈濋梻渚囧弿闂勫嫬顕欏ú顏呪拺闂侇偆鍋涢懟顖涙櫠閹绢喗鐓忛柛鈩冩礈椤︼箓鏌嶇拠鏌ュ弰妤犵偞锕㈠鍫曞箣濠婂嫬浜濋梻鍌欐祰椤曆呮崲閹烘纾婚柣妯哄棘濞戙垹绀嬫い鎾跺С缁楀姊洪棃娑崇础闁告侗鍨界槐鎶芥⒒娴e懙褰掑嫉椤掑嫭鍤屽Δ锝呭暙閻掑灚銇勯幒宥囧妽闁稿﹥鍔楅埀顒冾潐濞叉﹢宕濆▎鎾崇畺婵犲﹤鐗婇崵宥夋煏婢跺牆鍔楅柛瀣崌瀹曠ǹ螖娴e搫寮抽梻浣告惈濞层劑宕戝☉銏犵劦妞ゆ巻鍋撶紓宥咃工椤曪綁寮婚妷顔芥櫆闂佺硶鍓濋悷褔鏁嶅┑瀣拺缂佸瀵у﹢浼存煟閻旀繂娲ょ粈澶屸偓骞垮劚椤︿即鎮¤箛娑欑厱闁靛绲芥俊鎸庣箾閹绘帩鍤熼柍褜鍓氶鏍窗濡ゅ嫨浜归柛鎰靛枔閸嬫垵霉閸忓吋缍戦梺鍗炴处缁绘繈濮€閳衡偓閹秶绱掗悩铏磳鐎殿喛顕ч埥澶愬閻樻彃绁梻渚€娼ф灙闁稿氦娅曠粋鎺楀煛娴e弶鏂€闂佸疇妫勫Λ妤佺濠靛瀚呴弶鍫氭櫇绾捐偐绱撴担璐細婵炴彃顕埀顒冾潐濞叉牕鐣烽鍕厺閹兼番鍊楅悿鈧柟鑲╄ˉ濡插懎螞濠婂牊鈷掗柛灞剧懅椤︼箓鏌i妶鍛枠妞ゃ垺淇洪ˇ褰掓煙椤斻劌娲ら獮銏$箾閹寸偍缂氶柛妯绘尦濮婅櫣娑甸崨顔兼锭闁诲酣娼ч惌鍌氼嚕椤愶絿绡€闁告洦鍘介敍蹇擃渻閵堝棙灏靛┑顔芥尦瀹曘垻鈧潧鎽滅壕濂告煠缁嬭法浠涚紓宥嗗灴閺屽秶鎲撮崟顐や紝闂佽鍠楅悷鈺佺暦閿濆棗绶炲┑鐘插缁茬晫绱撻崒姘偓鐑芥倿閿曚降浜归柛鎰╁妵缂傛岸鏌嶉妷銉э紞闁哄棴闄勯幈銊ノ熼幐搴c€愮紓浣哄У婵炲﹪寮婚悢琛″亾濞戞鎴﹀煕閹扮増鐓熼幖绮规閻撳吋鎱ㄦ繝鍐┿仢闁诡喚鍏橀弻鍥晝閳ь剙鈻撻崼鏇熲拺缂佸顑欓崕鎰磼鐎n偅灏扮紒鏃傚枛瀵挳濮€閳哄倹娅栭梻浣虹帛閸旀鎮伴妷鈺佺婵炲樊浜濋埛鎺楁煕鐏炵偓鐨戝褎绋戦埥澶愬箻閼搁潧娈岄梺瀹犳椤︻垶锝炲┑瀣垫晝闁挎繂鎳庨蹇涙⒒閸屾瑧顦﹂柛姘儐缁傚秵绂掔€n亞锛熼梺鍦帛瀹曞ジ骞掑Δ鈧獮銏$箾閸℃ê鐏╅柨娑欑箞濮婅櫣绮欓幐搴㈡嫳闂佺厧缍婄粻鏍春閳ь剚銇勯幒宥囧妽闁稿﹥鍔楅埀顒冾潐濞叉﹢宕濆▎鎾跺祦闁哄秲鍔嶆刊鎾煕濠靛嫬鍔电紒槌栧枛閳规垿鏁嶉崟顐$捕濡炪倖鍨甸幊搴ㄦ箒闂佺粯鍨兼慨銈夊磿濡ゅ懏鐓曢柍鈺佸暔娴犵娀鏌嶈閸撴氨鏁幒妤嬬稏婵犻潧顑嗛弲鏌ユ煕濞戝崬澧い銉﹀哺濮婄粯鎷呴挊澹捇鎷戞潏鈺冪<閻犲洩灏欐晶鏇熴亜椤愩垻绠伴悡銈嗐亜韫囨挾校闁哄懌鍨藉娲焻閻愯尪瀚板褎澹嗙槐鎺楊敊閼恒儮鎷婚梺閫炲苯澧存繛浣冲洤绠烘繝濠傜墛閸庢鏌涢埄鍐姇闁绘挻娲熼幃姗€鎮欓幓鎺嗘寖闂佸磭顑曢崕宕囨閹烘梹瀚氶柛娆忣樈濡繝姊洪棃娑欐悙閻庢碍婢橀锝嗙鐎n€晝鎲歌箛娑欏仼闁告繂瀚峰〒濠氭煏閸繃鍣界紒鐘插暱閳规垿鎮欓埡浣峰闂傚倷绀侀幖顐︽儗婢跺本宕叉繝闈涙閺嗭箓姊洪鈧粙渚€寮崶顒佺厽闁瑰瓨绻冮ˉ鐐烘煕閻樼鑰挎慨濠勭帛閹峰懘鎮滃Ο鐑樼暚闁诲孩顔栭崰鏍偉婵傚摜宓侀柛鎰靛枛绾惧ジ鏌i幇顖氱毢闁伙絾妞介幃宄扳堪閸曨剛鍙嗛梺浼欑悼閸忔﹢骞冮埄鍐╁劅婵☆垳绮弶鎼佹⒒娴gǹ顥忛柛瀣╃窔瀹曠懓煤椤忓嫰妫峰銈嗙墬缁海澹曟禒瀣厱閻忕偛澧介幊鍡涙煕韫囨挾鐒搁柡灞剧〒閳ь剨缍嗛崑鍛暦瀹€鈧埀顒冾潐濞叉ê煤閻旇偐宓侀幖娣妽鐎电姴顭跨捄鍝勭彁闁哄洢鍨洪悡鐔煎箹閹碱厼鐏g紒澶屾暬閺屾盯骞樼壕瀣棟闂佷紮绲块崗妯虹暦閿濆棗绶炵€光偓閳ь剟顢欓弴銏♀拺闁荤喐澹嗛幗鐘绘煟閻旀潙鍔﹂柟顔斤耿閸╋繝宕橀鍡床闂備胶绮悷銉╁箠閹邦喚鐭欓柤濮愬€楃壕鑲╃磽娴h疮缂氱紒鐘靛仦娣囧﹪顢曢姀鐘虫闂佸疇妫勯ˇ顖烇綖濠靛鏁勯柤鎭掑劚椤徰呯磽閸屾艾鈧悂宕愬畡鎳婂綊宕堕妸褜娲稿銈嗗笒鐎氼剛澹曟繝姘厪闁割偅绻冩刊鍏肩箾閸忚偐澧甸柡灞剧☉閳规垿宕卞缁樼亞闂備焦鍎崇换妤咃綖婢跺备鍋撳顓炲摵闁哄瞼鍠撶槐鎺懳熼搹璇″剬婵$偑鍊栧褰掑垂閼哥數鈹嶅┑鐘叉处閸婇攱銇勮箛鎾愁仱闁稿鎹囬獮瀣晝閳ь剛绮堟径灞稿亾閸忓浜鹃梺鍛婃处閸撴艾鈻嶉崶顒佲拺闂傚牊绋撴晶鏇熴亜瑜夐崑鎾剁磽閸屾氨校闁绘濞€閹繝顢曢敃鈧悙濠囨煏婵炑€鍋撳┑顔兼喘濮婅櫣鎷犻垾宕囦化闂佺ǹ顑冮崐婵嗩嚕婵犳碍鏅插璺侯儏娴滄粓姊洪崨濠勨槈闁挎洩绠撳畷娆撳灳閹颁焦瀵岄梺闈涚墕濡瑩鎳栭悩缁樼厱闁靛绲芥俊鐑芥煙闁垮銇濇慨濠冩そ瀹曘劍绻濋崟顓犳殼闂佽瀛╅崙褰掑储婵傚壊鏁婇煫鍥ㄦ尨閺€浠嬫倵閿濆骸浜為柛姗€浜堕弻锝嗘償椤栨粎校闂佺ǹ顑呭Λ妤冨弲闂佸湱铏庨崰妤呮偂閺囥垺鐓冮柛婵嗗閳ь剙顭烽崺濠囧即閻橆偄浜鹃柛顭戝亝缁舵煡鎮楀鐓庡箻闁瑰箍鍨归埞鎴﹀炊閵娿儱濡抽梻渚€娼х换鎺撴叏瀹勬嫈锝夋晲婢跺鎷婚梺绋挎湰閻熝呯玻閺冣偓缁绘稒鎷呴崘鍙夊闁稿顑夐弻娑㈠焺閸愵亖妲堥梺姹囧€ら崰妤呭Φ閸曨垰绠涢柛鎾茬椤曡京绱撴担绛嬪殭婵☆偅顨婇崺鐐哄箣閿曗偓绾惧吋鎱ㄥ鍡楀箹闁哄棗鐗撳铏圭磼濡闉嶉梺鑽ゅ暱閺呯姴顕i弰蹇f▉缂備胶濮甸惄顖炲极閹版澘宸濇い鎺戝€诲▔鎸庣節閻㈤潧校妞ゆ梹鐗犲畷浼村冀椤剝妞介弫鍐磼濮g》绠撻弻娑㈠即閵娿儳浠╅梺鍛婎殙濞呮洘绌辨繝鍥舵晬婵﹩鍘介崕鎾寸節濞堝灝鏋熸繛鍙夌矌濡叉劙骞樼€涙ê顎撻梺鎯х箳閹虫挾绮敍鍕=濞达絿鐡旈崵娆撴煟濡も偓濡繈骞冩ィ鍐╁€婚柦妯侯槺閻i箖姊绘笟鍥у伎闂傚嫬瀚伴崺銏犵暆閸曨兘鎷绘繛杈剧秬婵倝濡撮崘顔界厽闁硅櫣鍋涢々顒勬煕閹烘挸绗掗柣锝嗙箞瀹曠喖顢曢妶鍛闂傚倷鑳堕幊鎾活敋椤撱垹纾绘繛鎴炴皑娑撳秹鏌eΟ鑲╁笡闁抽攱鍨圭槐鎺斺偓锝庝簻閻繝鏌¢埀顒佺節濮橆厾鍘甸梺鑽ゅ枔婢ф宕板Ο娲绘闁绘劘顕滃銉╂懚閺嶎厽鐓曟繛鎴濆船瀵噣鏌涢悙鑼煟婵﹥妞藉畷顐﹀礋椤掆偓缁愭盯姊虹粙娆惧剱闁烩晩鍨伴悾鐑藉箣濠垫劕鎮戦梺绯曞墲閻熝囶敊閺囥垺鐓熼幖杈剧稻閺嗏晠寮搁鍡忓亾濞戞瑧绠撴い顏勫暣婵″爼宕卞Δ鍐ф樊婵犵妲呴崑鍛崲閸繄鏆﹂柛婵嗗濡插牓鏌曡箛鏇炐ユい鎾存そ濮婃椽骞愭惔銏╂⒖閻炴碍鐟╅弻鐔风暋闁妇鍚嬪┑顔硷攻濡炶棄鐣峰⿰鍫濈闁瑰搫绉堕弫鏍⒒娴e憡鎲稿┑顔炬暬楠炴垿宕堕妸銈囩畾闂佸湱铏庨崰鏍不閹惰姤鐓涢柛鎰╁妼閳ь剙顭烽弫宥呪堪閸啿鎷虹紓鍌欑劍閿曨偊鎳撻幐搴g濞达絽鍟跨€氼噣銆呴悜鑺モ拺妞ゆ巻鍋撶紒澶屾暬閹€斥槈閵忊€斥偓鍫曟煟閹邦厼绲婚柍閿嬫閺屽秹顢涘☉娆戭槶缂備浇椴哥敮鐐垫閹烘嚦鐔兼嚃閳哄啯婢栭梺璇叉唉椤煤濮椻偓閺佸啴濮€閵堝啠鍋撴笟鈧顕€宕煎┑鍫Ч闂備線娼ф灙闁稿孩鐓″畷鎰板即閵忊檧鎷婚梺绋挎湰閼归箖鍩€椤掑嫷妫戠紒顔肩墛缁楃喖鍩€椤掑嫬绠栭柛褎顨呴悙濠冦亜椤掑澧柣鈺婂灠閻g兘鎮㈢喊杈ㄦ櫖闂侀€炲苯澧寸€规洖鐖奸、妤呭焵椤掑倻涓嶆い鏇楀亾闁哄本鐩獮妯虹暦閸ワ箒妾告繝鐢靛仦缁佹挳寮查悩鍏呯箚闁汇垻枪缁犳盯鏌℃径搴㈢《妞ゆ柨锕铏规喆閸曨偆顦ㄥ┑鐐差槹閻╊垶鎮伴鈧獮鍥偋閸垹骞楅梺纭呭亹鐞涖儵鍩€椤掆偓閸熸寧娼忛崨瀛樷拺缂佸顑欓崕鎰版煙閻熺増鍠樻鐐插暙铻栭柛娑卞枟濞呮粓鏌熼懖鈺勊夐柍褜鍓氶崜姘缚妤e啯鐓熼柣鎰嚟閸熻尙绱掗悩铏碍妞ゎ偄绻掔槐鎺懳熺拠宸偓鎾绘⒑閹呯缂佺姴绉归崺鈧い鎺嗗亾闁挎洦浜濠氭晸閻樻彃绐涘銈嗘煣閸曟﹢鍩€椤掍礁娴柡灞界Х椤т線鏌涢幘瀛樼殤闁哥姴锕ら濂稿椽娴e搫鏁告繝娈垮枟閵囨盯宕戦幘缁樼厵妞ゆ棁妫勯崝銈夋煟閿濆繒绡€闁哄苯娲弫鍌炴寠婢跺瞼澶勯梻鍌氬€风欢姘跺焵椤掑倸浠滈柤娲诲灡閺呭爼骞橀鐣屽帾闂佺硶鍓濆ú婊呯玻閺冨倵鍋撳▓鍨珮闁革綇绲介悾鐑芥偂鎼存ɑ鏂€闂佺硶鍓濋悷褍鐣烽崫鍕ㄦ斀闁挎稑瀚禍濂告煕婵犲啰澧垫鐐村姈閵堬綁宕橀妸褏宕堕梻浣筋潐閸庡磭绮诲鍡欘洸鐟滅増甯楅悡娆戠磽娴i潧鐏╅柡瀣枛閺屽秹鏌ㄧ€n亝璇為梺鍝勬湰缁嬫挻绂掗敃鍌氱闁归偊鍓﹀Λ鐔兼⒒娓氣偓閳ь剛鍋涢懟顖涙櫠椤曗偓閺屾盯濮€閿涘嫬寮ㄥ┑鐘亾濞撴埃鍋撴慨濠冩そ楠炴牠鎮欓幓鎺懶ら梻浣告啞閹碱偆绮婚幘鎰佸殨妞ゆ劑鍊愰崑鎾绘晲鎼粹剝鐏嶉梺缁樻尰缁嬫捇鍩€椤掆偓缁犲秹宕曟潏顭戞闁归棿鑳跺畵渚€鏌″搴″箺闁绘挾鍠栭弻鏇㈠醇濠靛鈧鏌$€n剙鏋涢柡灞炬礋瀹曟儼顦叉い蹇e幗椤ㄣ儵鎮欓崣澶婃灎閻庤娲樼划宥夊箯閸涘瓨鍊绘俊顖涙た閸熷懘姊婚崒姘偓鐑芥嚄閸撲礁鍨濇い鏍仜缁€澶愭煛閸ャ儱鐏柡鍛箞閺屻劑寮撮悙娴嬪亾閸濄儳涓嶉柣鏂垮悑閻撴瑩姊婚崒姘煎殶妞わ讣濡囩槐鎺楊敃閵忊懣褔鏌$仦鍓ф创妞ゃ垺娲熼弫鎰板炊閳哄啯姣庨梻鍌欒兌绾爼寮插┑瀣;闁靛牆鎷嬪ḿ鏍ㄧ箾瀹割喕绨荤紒鈧崼銉︾厵缂備焦锚缁楀倻绱掗妸褍甯堕柍瑙勫灴閹瑩骞撻幒鏃堢崜闂備焦瀵уú蹇涘垂閽樺鏆﹂柛婵嗗濡插牓鏌曡箛鏇炐ユい鎾存そ濮婅櫣绱掑Ο鍓佺窗闂佽桨鐒﹂幃鍌炲极瀹ュ應鏀介柛銉㈡櫇椤旀洟鏌℃径濠勫濠⒀呮櫕缁棃顢楅崟顒傚幈闁诲函缍嗘禍婊堝焵椤掆偓濞硷繝鎮伴閿亾閿濆倹娅囩紒澶婄摠缁绘繈濮€閿濆懐鍘梺鍛婃⒐濞茬喖寮荤€n喖鐐婃い鎺嶈兌閸樹粙姊洪崫鍕殭闁稿﹨宕靛褔鍩€椤掑倻纾藉ù锝夋涧婵″吋銇勯鐐叉Щ妞ゎ偄绻愮叅妞ゅ繐鎷嬪Λ鍐ㄢ攽閻愭潙鐏卞瀛樻倐椤㈡捇宕卞☉娆屾嫽闂佺ǹ鏈懝楣冾敂閳哄懏鍊垫慨妯煎帶閺嬬喓绱掗崒姘毙ф鐐寸墬閹峰懘宕妷顔兼倯濠碉紕鍋戦崐鏍蓟閵婏附娅犲ù鐘差儐閺咁剚绻濇繝鍌滃闁抽攱鍨圭槐鎺斺偓锝庡亜椤曟粍绻濋埀顒勫箥椤斿墽锛滈柣搴秵閸嬪嫰鎮橀妷鈺傤梿濠㈣泛顑冩禍婊堟煛閸愩劌鈧骞楅崒娑氱闁割偅绮庨惌娆撴煛瀹€瀣М妤犵偛娲、妤呭焵椤掑倻妫憸鏃堝蓟濞戙垺鍋愮紒娑氼攰閳ь剙娼¢弻鈥崇暆閳ь剟宕伴弽顓溾偓浣糕枎閹炬緞鈺呮煏婢舵盯妾柟顔界懇濮婄粯鎷呯粙鑳煘濠电偛妯婇崣鍐嚕婵犳艾鍗抽柨娑樺閺夋悂姊洪崫鍕窛闁稿⿴鍋婃慨鈧柕蹇嬪灮閿涙粓姊虹紒妯撶懓鈻嶉弴銏犖︽繝闈涙处閸欏繐鈹戦悩鎻掝伀閻㈩垱鐩弻鐔风暋閻楀牆娅ょ紓浣诡殘閸犳牠銆佸☉妯锋婵炲棙鍔栭澶愭⒒閸屾艾鈧兘鎳楅懜鐢典粴婵$偑鍊栭崹闈浳涘┑鍡欐殾婵犻潧鏌堥弮鍫濆窛妞ゆ挾濮烽弳顐⑩攽閻愬瓨缍戦柛姘儏宀e灝鈻庤箛鏃€娈伴梻鍌氬€风粈渚€鎮块崶褜娴栭柕濞炬櫆閸ゅ嫰鏌涢锝嗙』闁搞儺鍓﹂弫鍥煟閹般劍娅嗛柡鍌楀亾闂傚倷鑳剁划顖氱幓鐠恒劌鍨濇い鏍ㄥ焹濡插牏鎲搁弮鍫濊摕闁挎繂鎲橀弮鍫濈劦妞ゆ帒瀚弲婵嬫煥閺囩偛鈧悂鎮為崹顐犱簻闁瑰搫绉电粊鏉款熆鐟欏媶鎴﹀Φ閸曨垼鏁囬柣妯诲絻楠炲鎮楀▓鍨灈妞ゎ參鏀辨穱濠囧箹娴e摜鍘搁梺绋挎湰閻喚鑺辨繝姘拻濞达絽鎲¢崯鐐电磼鐠囨彃鈧鍩€椤掍浇澹橀柟铏耿瀵偊骞囬鐐电獮闁诲函缍嗛崜娆撶嵁濡ゅ懏鈷掑ù锝囩摂濞兼劙鏌涙惔銏犫枙闁诡喗妞芥俊姝岊槾闁活厼妫濋幃妤呮晲鎼粹剝鐏嶉梺缁樻尰閻燂箓濡甸崟顖氱睄闁稿本绮嶉幉妯衡攽閻愯尙澧涚紒顔芥崌瀵鍩勯崘鈺侇€撻梺鑽ゅ枑濠㈡﹢锝炲澶嬧拺閻犲洠鈧磭浠┑鈽嗗亜閸熸潙鐣峰ú顏呮櫇闁稿本姘ㄩ崝锕€顪冮妶鍡楃瑨閻庢凹鍓涙竟鏇熺節濮橆厾鍘甸梺纭咁潐閸旀洟鎮¢幇顔瑰亾鐟欏嫭绀€妞わ妇鏁诲濠氬即閻旇櫣顔曢悷婊冪Ч楠炲繘骞嬮悩鎰佹綗闂佹儳娴氶崑鍡欏姬閳ь剙鈹戦悙鑼闁诲繑绻堝鎼佹偄閻撳骸鍤戝銈呯箰婵炲﹪鎮烽幍鍐茬墯闁硅偐琛ラ埀顒佸墯濞兼儳鈹戦悩顔肩伇妞ゎ偄顦叅婵☆垵鍋愮槐锕傛煟閿濆懐鐏遍柣顓熺懇閹綊骞侀幒鎴濐潎闂佺粯绋掗幑鍥ь潖缂佹ɑ濯寸紒瀣儥濡矂姊虹粙娆惧剰闁硅櫕鍔欏畷鐗堢節閸屻倕鎮戦梺鍛婁緱娴滄繈鎮楀ú顏呪拺闁告稑锕g欢閬嶆煕閺冣偓閸庡ジ濡甸幇鏉跨闁规儳鍘栧Ч妤佺節閻㈤潧浠滄俊顐n殘閹广垽骞嬮悙鑼獮闂佸憡娲﹂崹閬嶆偂閻斿吋鐓欓柟顖嗗啯姣愰梺鍝勬閸犳牠寮婚悢鍏煎殤妞ゆ垯鍨圭紞濠囧Χ椤忓懎顕遍柡澶嬪灴閸炶泛鈹戦悩缁樻锭闁绘绮屽嵄闁割偅娲橀埛鎺戙€掑锝呬壕濠电偘鍖犻崱妤侇仩闂傚倷绀侀幉鈩冪瑹濡ゅ懎鍨傞柣鎾冲閿濆绠瑰ù锝呭帨閹风粯绻涙潏鍓хК婵炲拑缍佹俊瀛樼節閸ャ劎鍘遍梺瑙勫劤椤曨厾绮诲Ο鑲╃<妞ゆ梻鏅幊鍥殽閻愬樊鍎旈柡浣稿€块幐濠冨緞閸℃ぞ澹曢梺绉嗗嫷娈曢柣鎾存礃閵囧嫰顢橀悢椋庝淮婵炲瓨绮嶉悧鏇㈡箒濠电姴锕ょ€氼噣鎯岄幒妤佺厸鐎光偓閳ь剟宕伴幘璇茬劦妞ゆ帒鍊归弳鈺呭几椤忓娊褰掓偐瀹曞洨鐓夐梺鍝勬湰閻╊垰顕i鍌涘珰婵炴潙顑呮禍鐐節闂堟侗鍎忛柦鍐枛閺屻劌鈹戦崱娆忊叡闂佹眹鍊愰崑鎾斥攽閻樺灚鏆╁┑顔芥尦瀹曨垶顢涢悙鏉戜户闂佸搫绋侀崑鍡欏閽樺褰掓晲閸曨厾鐓撻梺鍛婄箖濡炰粙寮婚悢鐓庡窛濠电姴鍟埀顒佸姈閵囧嫰濮€閳晜鍨圭紓鎾绘偩瀹€鈧惌娆撴煙缁嬭法鏄傚ù鐘灲濮婄粯鎷呴崨濠傛殘闂佸憡妫戠粻鎾崇暦閵忥紕闄勭紒瀣硶閻i箖姊洪崜鎻掍簴闁稿孩鐓¢幃锟犳偄閻撳海顔愬┑鐑囩秵閸撴瑩鎮炲ú顏呯厱闁绘棃顥撶粻濠氭煛鐏炲墽娲撮柟顔规櫅閻g兘宕惰閹蜂即姊绘担鍝勪缓闁稿氦宕电划濠氬箻鐠囪尪鎽曢梺闈浤涢埀顒勫磻閹剧粯鏅查柛灞剧⊕閻濇牜绱撴担鍝勑i柤褰掔畺閸╃偤骞嬮敂缁樻櫓闂佷紮绲介惉濂告偩閻㈠憡鈷戞繛鑼额嚙楠炴牠鏌eΔ鈧Λ妤€鐣甸崟顖涒拺缂備焦锚閻忓崬鈹戦鍝勨偓婵嬪春濞戙垹绠i柣妯兼暩閿涙粓鏌f惔顖滅У闁稿甯″畷鏇㈠Ψ閳哄倻鍘遍柟鍏肩暘閸ㄨ鎱ㄥ澶嬬厸鐎光偓閳ь剟宕伴弽顓炵畺闁绘垼濮ら崑瀣煕椤愶絿绠栭柣蹇撻叄閺岋絾鎯旈姀鈺佹櫛闂侀潻缍嗛崳锝呯暦閹寸偟绡€闁搞儮鏅涚粊锕傛⒑閹肩偛鍔撮柛鎿勭畵瀵偊宕堕浣哄幗闂佸搫鍊搁悘婵單g拠娴嬫斀闂勫洤鈻嶉弴鐘冲床婵犻潧鐗嗛弸鍫熶繆椤栨稒銇熸繛鍏煎灴濮婃椽骞栭悙鎻掝潎濠电偘鍖犻崶銉㈠亾閸涱喚闄勭紒瀣嚦閳哄懏鐓ラ柡鍌氱仢閳锋梻鎲告导瀵哥暫婵﹥妞藉畷顐﹀礋椤掆偓缁愭盯姊虹粙鍨劉闁告梹娲熸俊鎾箳閹惧墎鐦堝┑顔斤供閸橀箖宕㈤鍫熲拺闁告挻褰冩禍婵堢磼鐠囨彃鏆i挊鐔兼煟濡儤鈻曢柣鏂挎閹茬ǹ鈹戦崼顫瑝闂佽宕橀褔鎷戦悢鍝ョ闁瑰鍋熼幊鍛磼閳锯偓閸嬫捇姊绘担鍛婂暈闁告棑闄勭粋宥呪堪閸繄鍘遍梺鍓插亖閸庢煡鍩涢幋锔解拺妞ゆ劑鍊曟禒婊堟煠濞茶鐏¢柡鍛埣椤㈡盯鎮欑€电ǹ骞楅梻浣告惈閸燁垶宕归崹顐f珷閻庢稒锕╁▓浠嬫煟閹邦垰鐨虹紒鐘差煼閺屸剝鎷呯憴鍕3闂佽桨鐒﹂幑鍥极閹剧粯鏅搁柨鐕傛嫹>>
闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁诡垎鍐f寖闂佺娅曢幑鍥灳閺冨牆绀冩い蹇庣娴滈箖鏌ㄥ┑鍡欏嚬缂併劎绮妵鍕箳鐎n亞浠鹃梺闈涙搐鐎氫即鐛崶顒夋晬婵絾瀵ч幑鍥蓟閻斿摜鐟归柛顭戝枛椤牆顪冮妶搴′簼缂侇喗鎸搁悾鐑藉础閻愬秵妫冮崺鈧い鎺戝瀹撲礁鈹戦悩鎻掝伀缁惧彞绮欓弻娑氫沪閹规劕顥濋梺閫炲苯澧伴柟铏崌閿濈偛鈹戠€n€晠鏌嶆潪鎷屽厡闁汇倕鎳愮槐鎾存媴閸撴彃鍓卞銈嗗灦閻熲晛鐣烽妷褉鍋撻敐搴℃灍闁绘挻娲橀妵鍕箛闂堟稐绨肩紓浣藉煐濮樸劎妲愰幘璇茬闁冲搫鍊婚ˇ銉╂⒑鐎圭媭娼愰柛銊ユ健楠炲啴鍩¢崨顔兼濡炪倖甯婄欢鈥澄涢崟顖涒拻濞达絽鎲¢幆鍫熴亜閿旇鐏i柤娲憾閺屽棗顓奸崨顖ょ幢闂備浇顫夊畷姗€顢氳瀹曪繝骞庨懞銉у帾闂婎偄娲﹀ú鏍ф毄闂備焦鐪归崐鏇灻洪鐐嶆盯宕ㄩ幖顓熸櫇闂侀潧绻嗛埀顒佸墯濡茶京绱撻崒娆戭槮妞ゆ垵妫濆畷褰掑垂椤旂偓娈鹃梺闈涱槶閸斿﹥绂嶈ぐ鎺撶厵闁绘垶蓱鐏忕敻鏌涘Ο鍏兼毈婵﹦绮粭鐔煎炊瑜嶆导搴g磽娴e搫校闁搞劌娼¢幃浼搭敋閳ь剟鐛€n亶鐔嗘繝闈涚墛閸も偓濡ゆ浜欓崡鍐茬暦閻旂⒈鏁囬柣姗€娼х敮銊╂⒒閸屾瑧顦﹂柟纰卞亝瀵板嫰宕堕鈧悞鍨亜閹哄秶顦﹀褜鍨堕弻娑橆潩椤掑鍓跺Δ鐘靛仦閻楁粓宕氶幒妤€绀傚璺猴梗婢规洟姊洪懖鈹炬嫛闁告挻绋戦埢鏃堝箰鎼达絿鐦堥梺姹囧灲濞佳勭濠婂嫨浜滈柡鍥ュ妼楠炴鏌熸笟鍨闁诡喕绮欏Λ鍐ㄢ槈濡棿鍠婇梺璇查閸樻粓宕戦幘缁樼厱闁哄洦顨嗛弶褰掓煕鐎n偅宕岀€规洏鍔戦、娆愩偅閸愨晩鈧秶绱撻崒娆戭槮妞ゆ垵鎳橀幃妯衡攽閸垻骞撳┑鐐村灟閸ㄦ椽鎮¢悢鐓庣婵烇綆鍓欓悘顕€鏌嶉娑欑闁圭缍佹俊鑸靛緞鐎n剙骞嶉梻鍌欑閻忔繈顢栭崱娑樜︽繝闈涙处閸欏繐鈹戦悩鍙夊櫤妞ゅ繒濮电换娑㈠箣閻樿櫕姣堥悗瑙勬磸閸旀垿銆佸Ο琛℃斀闁搞儮鏅滅紞搴ㄦ⒒閸屾艾鈧兘鎳楅懜鐢典粴婵$偑鍊栭崹闈浳涘┑瀣畾闁告洦鍨奸弫宥嗘叏濡潡鍝烘繛鍫熷劤閳规垿鎮╃紒妯婚敪闂佸搫鑻悧鎾愁嚕椤曗偓瀹曠厧鈹戦崱娆戝春濠碉紕鍋戦崐鏍ь潖瑜版帒纾块柟鍓佹櫕瀹撲線鏌熼幍顔碱暭闁抽攱甯掗湁闁挎繂鎳忛崯鐐烘煕閻斿搫浠滈柕鍡樺笒椤繈顢樿閻や線鎮楃憴鍕婵犮垺锕㈤敐鐐测攽閸喎纾梺鎯х箰濠€閬嶅几閸愵喗鈷掑ù锝堫潐閸嬬娀鏌涙惔銏°仢鐎规洘绮岄~婵嬫嚋闂堟稐绨垫繝鐢靛仜濡瑩宕濋幋鐐殿洸婵犲﹤鐗婇悡娑㈡煕閹板墎鍒板ù婊堢畺濮婅櫣绮欓幐搴℃敪濠电偛鎳忓ú婊呭垝鐎n喖绠虫俊銈勭劍濞呭棝姊洪崨濠冨瘷闁告粌鍟版惔濠勭磽閸屾艾鈧悂宕愰悜鑺ュ€块柨鏇楀亾闁绘粏宕甸幑鍕Ω瑜岀粭澶愭⒑缂佹ê濮夋い锝勭矙瀹曟垿骞橀懜闈涙瀭闂佸憡娲﹂崜娑⑺囬妷鈺傗拺缂備焦岣挎晶顏堟煏閸懚褰掓偩瀹勬噴娲敂閸曨厼濮堕梻浣告啞閸斿繘寮插☉銏╂晛闁瑰墽绮埛鎴︽煕濞戞﹫鍔熺紓鍌涘哺閺屾稒鎯旈妸銈嗗枤濡炪們鍨哄畝鎼佸蓟閸℃鍚嬮柛鈥崇箲鐎氫粙姊绘担鍛靛綊寮甸鍕殞濡わ絽鍟悞鍨亜閹烘垵鈧悂宕㈤幘顔界厵妞ゆ梹鍎虫禒閬嶆煛娴gǹ鏆g€规洘甯掗~婵囨綇閳哄倹鐦掗梻鍌氬€风粈浣圭珶婵犲洤纾婚柛娑卞姸濞差亜鍐€妞ゆ劑鍩勫Λ婊堟⒑閸︻厐鍦姳閻戞ḿ顩叉繝濠傜墛閻撴稓鈧箍鍎辨鍛婄濠婂厾褰掓偐瀹曞洨鐓傜紓浣介哺鐢繝宕洪埀顒併亜閹哄秶顦︾紒鍓佸仱閺岀喖鏌囬敃鈧晶鐗堛亜閺冣偓閸旀洟鍩為幋锔藉€婚柛銉㈡櫇鏍¢梻浣告啞閹稿鎮烽敂鐣屸攳濠电姴娲ょ粈鍌炴煕韫囨稒锛熸慨姗堢畱閳规垿鎮╃紒妯婚敪濡炪倖鍨靛Λ婵嬪春濞戙垹绠i柨鏃傛櫕閸橀亶姊洪幐搴㈩梿妞ゆ泦鍥╁祦闁哄稁鍘介悡鏇㈡煛閸屾侗鍎ラ柛搴㈠姍閺屾洟宕惰椤忣厼鈹戦埄鍐╁€愬┑锛勫厴閺佸倻绱掑鍫㈢闂傚倸鍊峰ù鍥敋閺嶎厼闂い鏍ㄧ矋瀹曞弶绻濋棃娑卞剰缂佺姵鐗犻弻鏇$疀鐎n亖鍋撻弴鐘电焼闁稿瞼鍋為悡鐘崇箾閺夋埈鍎愭繛鍛噺椤ㄣ儵鎮欓懠顑勬叏婵犲偆鐓肩€规洘甯掗埢搴ㄥ箣閿濆洨宕堕梻鍌欑閹诧繝鎮烽妷褎宕查柟鐑樻煥閸ㄦ繂鈹戦悩瀹犲缂佺媴缍侀弻锝夊箛椤掑倹鎲奸梺缁樼箞閺€杈ㄧ┍婵犲洤围闊洦娲栭崺宀勬⒑閸濄儱娅忛柛銊ョ埣楠炲啴鏁撻悩鎻掑祮闂侀潧楠忕槐鏇㈠储閹间焦鈷戦柛娑橈工婵倿鏌涢弬璺ㄧ劯闁糕斁鍋撳銈嗗笂閻掞箓宕愰幇顔瑰亾濞堝灝鏋熼柟顔煎€搁锝夘敋閳ь剙鐣烽幒鎴斿牚闁告粌鍟版惔濠囨⒒娴e憡鎯堟い锔诲灦閹囧礋椤栨氨顦悗鍏夊亾闁逞屽墰閸掓帡顢橀悜鍡樺兊濡炪倖鎸炬慨鐑筋敊閺囥垺鈷戠紓浣股戠亸顓熺箾閹绢噮妫戠紒顔垮吹閹风姴霉鐎n偅鏉搁梻浣规灱閺呮盯宕鐐茬9闁归偊鍏橀弨浠嬫煥濞戞ê顏柣鎺撳閵囧嫯顦辩紒鑸靛哺瀵鈽夊▎鎰妳闂佹寧绋戠€氼噣宕濋姘f斀妞ゆ梻銆嬮崝鐔虹磼椤曞懎鐏︽鐐茬箻瀹曘劎鈧稒锚閳ь剛绮穱濠囶敍濠婂啫濡洪梺浼欑秵閸撶喎顫忕紒妯诲閻熸瑥瀚禒鈺呮⒑閹肩偛濡芥俊鐐扮矙楠炲啴鏁撻悩铏闂佺粯锕╅崰鎺楀磻閹惧鐟归柍褜鍓欓锝嗙鐎n€晠鏌曟竟顖氭噽瀹撲線姊婚崒娆戭槮缂傚秴锕畷鎴炵節閸パ咁槶濠电偞鍨崺鍕极婵犲洦鐓欓柟娈垮枛椤eジ鏌涚€Q冨⒉缂佺粯绻冪换婵嬪磼濞戞ɑ顏犳俊鐐€х徊浠嬪Χ閹间礁绠栧ù鐘差儛閺佸秵淇婇妶鍕妽闁绘繃宀搁幃妤€鈻撻崹顔界彯闂佺ǹ顑呴敃銈夋偩瀹勯偊娼ㄩ柍褜鍓熼妴浣糕枎閹炬潙浠奸柣蹇曞仩濡嫭淇婇崶顒佲拻闁稿本鐟чˇ锕€顭块悷甯含鐎规洘鍨垮畷銊╊敍濞戞ê绨ラ梻浣呵归惉濂稿磻濞戞褔宕f径宀€顔曢梺绯曞墲椤ㄥ牏鎷归埡鍐╁枑闁绘鐗嗙粭姘舵煕鐎n偄濮嶉柡灞剧洴楠炲洭顢楅埀顒傜棯瑜旈幃褰掑炊閳轰椒绮堕梺瀹狀潐閸ㄥ潡銆佸▎鎴炲厹鐎瑰嫰顣︾槐锝嗕繆閻愵亜鈧倝宕㈡總绋垮簥闁哄被鍎查崑鈺呮煟閹达絾顥夌紒鐘冲▕閺岀喓鈧稒蓱閳锋劙鏌f惔鈽嗙吋婵﹥妞藉畷鐑筋敇閻愭彃顬嗛梻浣规偠閸斿酣寮幖浣告瀬妞ゆ洍鍋撴い銏$洴閹瑧鍒掔憴鍕伖闂傚倷绀侀幉锛勬崲閸屾壕鍋撳鍗炲幋鐎规洘娲栭埥澶娢熻箛鏇熷殌妤楊亙鍗冲畷鐔碱敇閻樺灚婢栨繝鐢靛Х椤n喚妲愰弴銏犳瀬閻犲洩灏欓弳锕傛煟閺冨倵鎷¢柡浣哥У閹便劌顫滈埀顒傛兜閹间礁瑙﹂柛娑卞枤缁♀偓闂佹眹鍨藉ḿ褔鍩㈤崼鐔虹濞达絽鍟块崢鎹愩亹閹烘垹锛滃┑顕嗙到閸氬鎯勯娑楃箚闁割偅娲栭悙濠囨煃閸濆嫬鏋︾紒鍗炲暱閳规垿鎮欑€涙ê闉嶉梺鑹邦潐閸庡磭鍙呴梺闈涚墕椤︻垶宕欓悩缁樼厽闁哄倸鐏濋幃鎴︽煟閹捐泛鏋涢柡宀嬬秮瀵剟宕归楣冪崜婵犵數鍋涢幊搴ㄦ晝椤忓牆钃熼柨婵嗘噳濡插牓鏌涘Δ鍐ㄤ沪闁绘繃绻傝灃闁绘﹢娼ф禒锕傛偨椤栨稑绗╅柣蹇撳暣濮婃椽鏌呴悙鑼跺濠⒀傚嵆閺岋絽顫濋鐐插Б濡炪倖鎸搁崥瀣嚗閸曨厸鍋撻敐搴″妤犵偛鐗撳铏规嫚閼碱剛顔婇梺绋款儐缁嬫帡寮查懜鐢殿浄閻庯綆鍋勯崜褰掓倵閸忓浜鹃梺鍛婃处閸撴盯宕㈤崡鐐╂斀妞ゆ梻鐡斿▓鏃€淇婇锝庢疁闁诡喗锕㈤幃鈺冪磼濡厧甯楅梺鑽ゅ枑閻熴儳鈧凹鍓熼幃姗€骞橀鐣屽幍濡炪倖妫侀~澶娾枍婵犲啨浜滈柕蹇ョ磿閹冲洭鏌熼搹顐ゅ⒌闁糕晪绻濋崺鈧い鎺戝€归~鏇熶繆椤栨繂鍚圭紒鈾€鍋撻梻浣圭湽閸ㄨ棄岣胯缁傛帒饪伴崟鈺€绨婚梺鎸庢煥閻忔繂鐣甸崱娑欑厵妞ゆ牗鑹鹃顓熴亜閵忥紕娲撮柟顔界懇椤㈡梹鎷呴梹鎰棜濠电偞鎸婚崺鍐磻閹惧灈鍋撳▓鍨灆缂侇喗鐟╅妴浣割潨閳ь剟骞冨▎鎾村殤闁搞劍绋戞禍楣冩煕椤垵鏋撻柡鈧禒瀣厽闁归偊鍘界紞鎴︽煟韫囥儳鐣遍柣锝嗙箞閺佹劙宕ㄩ闂存樊闂備浇妗ㄧ粈浣虹矓瑜版帒绠栭柕蹇嬪€曠粈鍌炴倶韫囨梻澧悗姘冲亹缁辨捇宕掑顑藉亾閻戣姤鍊块柨鏇氱劍閹冲矂姊绘担铏瑰笡闁圭ǹ鐖煎畷鏇㈡偨缁嬭儻鎽曞┑鐐村灦閿曗晛岣块埡鍌樹簻闁圭儤鍩堝Σ鎼佹煕閹惧磭鍩f慨濠呮閹风娀鍨鹃搹顐ゅ讲缂傚倷鑳剁划顖滄崲閸岀偞鍋╃€瑰嫰鍋婂ḿ銊╂煃瑜滈崜鐔煎Υ娴g硶鏋庨柟鐐綑娴犲ジ鏌h箛鏇炰哗婵☆偄瀚穱濠囧炊閵娧呯槇闂佹眹鍨藉ḿ褑鈪烽梻浣规偠閸斿酣宕㈣閸┿垽寮惔鎾搭潔闂侀潧绻嗛埀顒€鍘栫純鏇㈡⒒娴h櫣銆婇柛鎾寸箘缁瑩骞嬮悩鐢电劶婵犮垼娉涢鍡涘矗韫囨柧绻嗘い鏍ㄥ搸娴犳帡鏌涘鐓庝簽闁汇儺浜獮鍡氼槹闁稿鍨介弻鈥崇暆鐎n剙鍩岄梺瀹狀嚙闁帮綁鐛崶顒夋晩闁芥ê顦伴悵锝夋⒒娴g瓔鍤欓悗娑掓櫊瀹曟瑧鎲撮崟顓ф锤闂佺粯鍔曢幖顐ょ不閺屻儲鐓忛煫鍥ь儏閳ь剚娲熼悰顕€濮€閳ヨ尙绠氬銈嗙墱閸嬬偛鈻嶅⿰鍛<闁靛ǹ鍎洪悡鍏兼叏婵犲啯銇濈€规洦鍋婂畷鐔碱敇婢跺苯鈻堥柡灞剧洴瀵剟宕稿Δ鈧浼存倵鐟欏嫭澶勯柛銊ㄦ硾椤曪絾绻濆顑┿劑鏌ㄩ弮鍌滃笡妞ゃ儱锕ユ穱濠囨倷椤忓嫧鍋撻弽顐f殰闁圭儤顧傞崶顒夋晬婵炴垶鐟﹂悵鐑芥⒑閸︻叀妾搁柛鐘愁殜閹€斥槈閵忊€斥偓鍫曟煟閹邦喗鏆╅柕鍡楋躬閺屾稓鈧綆鍋呯亸顓㈡煟閿濆洤鍘寸€规洖鐖兼俊鎼佹晜閻愵剚顔曢梻鍌氬€搁崐椋庢濮樿泛鐒垫い鎺戝€告禒婊堟煠濞茶鐏¢柡鍛閳ь剛鏁哥涵鍫曞磻閹捐埖鍠嗛柛鏇ㄥ墰閿涙盯姊洪崨濠庢當闁哥喎娼¢、姘舵晲婢跺﹦锛欓梺缁樻磻閻掞箓鐎烽梻鍌氬€风粈渚€骞栭鈶芥盯骞橀瑙f寖闂佸憡娲﹂崜娑㈠煘瀹ュ應鏀介柣妯哄级閹兼劙宕堕幘顔解拺闁告稑锕g欢閬嶆煕閻樺磭澧柍璇茬Ч閺佹劙宕堕埡鍐跨闯濠电偠鎻徊鎹愩亹閸愨晝顩插Δ锝呭暞閳锋垹绱掔€n厽纭堕柣蹇涗憾閺屾稓鈧綆鍓欐禒閬嶆煙椤曞棛绡€闁诡喓鍨藉畷妤呮嚃閳轰礁绠ラ梻鍌欒兌缁垶宕濋敃鍌氱婵炲棙鎸搁悡婵嬫煛閸モ晛鏋傚ù婊勭矒楠炴牕菐椤掆偓閻掔儤绻涢崼鐔虹煉闁哄备鈧磭鏆嗛悗锝庡墰閻﹀牓姊虹化鏇熸澒闁稿鎸搁—鍐Χ閸℃鐟ㄩ柣搴㈡皑閸忔ê顕i锕€鐐婃い鎺嶈兌閸樹粙姊洪崫鍕偓鎼佹倶濠靛鈧倸鐣烽崶鈺冿紲闂佺粯锚閸熷潡宕悜妯诲弿濠电姴鎳忛鐘电磼鏉堛劌绗掗摶锝夋煕濠靛棗鐝旈柡鍥╁枔缁犻箖鎮楀☉娆嬬細闁活厼顑囩槐鎺楊敊閼恒儱纾抽悗瑙勬礃濡炰粙宕洪埀顒併亜閹哄秹妾峰ù婊勭矒閺岀喖宕崟顓夈倖銇勯敂鑲╃暤闁哄矉缍€缁犳盯骞欓崘銊︻啀闂備線鈧偛鑻晶鍙夈亜椤愩埄妲搁悡銈嗕繆椤栨哎鍋ㄦ繛宸簼閸嬪嫬鈹戦崒姘兼Ц婵炲牄鍔嶇换婵嬫偨闂堟刀锝夋煠鐟欏嫬鍔ら柡渚囧櫍濮婄粯绗熼埀顒€岣胯閺佸秷绠涢弴姘媰闂佸吋浜介崕鎻捫掓径鎰拻闁稿本鑹鹃埀顒佹倐瀹曟劙鎮滈懞銉モ偓鍧楁煥閺囩偛鈧摜绮婚弽顓熺厱妞ゆ劧绲剧粈鈧紒鍓у亾鐎笛呮崲濞戞﹩鍟呮い鏃囧吹閻╁海绱撴担鎻掍壕闂佺ǹ鏈粙鎾剁不妤e啯鐓曢柍鈺佸彁閹寸姳鐒婃い鎾卞灪閻撶喖鏌熼悜妯虹仼濞寸姵鐩弻鏇㈠炊瑜嶉顓燁殽閻愬樊鍎旈柡浣瑰姍瀹曞崬鈻庡浣镐壕濠电姴鍋嗗〒濠氭煏閸繄绠烘い鎾存そ濮婂宕熼銏╀純婵犵绱曢弫璇茬暦閻旂⒈鏁嶉柨婵嗘濞呭洭姊绘担鐟邦嚋缂佽鍊哥叅闁靛ň鏅滈崑鍌氼熆閼搁潧濮堥柍閿嬪灩缁辨帡顢涘☉娆戭槰闂佸搫顦紞濠囧蓟濞戞埃鍋撻敐搴′簼閻忓浚鍘介妵鍕敂閸曨偅娈绘繝纰樷偓宕囧煟鐎规洖宕灃闁告劦浜濋崳顖炴⒒娴g瓔鍤欓悗娑掓櫊瀹曟瑨銇愰幒鎴犵崶闂佸搫绋侀崢浠嬪磻閳哄懏鐓曟い顓熷灥娴滅偤鏌i悢椋庣Ш闁哄苯绉烽¨渚€鏌涢幘璺烘瀻妞ゆ洩绲剧换婵嗩潩椤掑倷绱滈梻浣哥秺椤o妇绮堟笟鈧獮鍐箣閿旇В鎷洪梺鍛婄☉閿曘倖鎱ㄩ崒鐐寸厱闁哄倽娉曢悞鎼佹煃閵夛妇澧€垫澘瀚埀顒婄秵閸撴盯鎯侀崼婵冩斀闁绘劘灏欐晶鏇㈡煟韫囨梻绠為柟顔斤耿閺佹捇鎮╁畷鍥у箥闂備礁鎲$粙鎴︽晝閵堝鐓濋柡鍥╁Л閸嬫挸鈻撻崹顔界亪濡炪値鍘鹃崗妯侯嚕椤愶箑绠涙い鎾跺仧缁愮偤鏌f惔顖滅У濞存粍鐟ч懞閬嶆嚒閵堝洨锛濇繛杈剧到閹碱偅绂嶉幆褉鏀芥い鏍ㄧ箓琚氶梺闈涙处濮婅崵鍒掑▎鎰劅闁规儳顕禍鏍⒒娓氣偓濞佳囁囬锕€鐤炬繝濠傜墕閻撴洟鏌熸潏楣冩闁绘挻娲樼换娑㈠箣閻戝洤鍙曢梺鍛婃⒒閸犳挾妲愰幒妤佸亹鐎规洖娲ら~褔姊洪棃娑欐悙閻庢氨澧楁穱濠囧箹娴h倽銊︺亜閺嶃劎鐓紒鎲嬬稻娣囧﹪鎮欓鍕ㄥ亾閵堝纾婚柛鏇ㄥ幗瀹曟煡鏌熼悜妯烩拹妞ゎ偅娲熼弻鐔兼倻濡儤顔曢梺缁樻⒒閸庛倗鈧碍姘ㄩ埀顒傛嚀婢瑰﹪宕伴幒妤€纾婚柟鎹愵嚙缁犺崵绱撴担楠ㄦ岸骞忓ú顏呪拺閻犲洠鈧磭鈧鏌涘☉鍗炵伇闁哥偛澧庣槐鎾诲磼濞嗘帒鍘℃繝娈垮枛椤曨厾鍒掗弮鍥ヤ汗闁圭儤鍨跺Σ顒勬⒑闁偛鑻晶顖炴煏閸パ冾伃妤犵偞甯″畷鍗烆渻閹屾闂傚倸鍊烽悞锔锯偓绗涘厾娲晜閻e矈娲稿銈呯箰鐎氱兘宕甸弴銏″仯闁搞儯鍔庨妶瀛樹繆閹绘帞澧﹂柡灞炬礉缁犳盯寮撮悙鎰╁劜閵囧嫰寮埀顒傛暜閿熺姴钃熼柨婵嗘閸庣喖鏌曟繝蹇涙闂佹鍙冨铏规兜閸涱厜鎾剁磼椤旇姤宕屾鐐插暣瀹曠ǹ螖閳ь剛绮堢€n偁浜滈柡宥冨妿閳藉鏌嶈閸撴盯寮繝姘畺鐎瑰嫭澹嬮弸搴ㄧ叓閸ャ劍鎯勫ù鐘插⒔缁辨挻鎷呴幓鎺嶅闂備礁鎲¢崝锔界閻愰潧顥氬┑鍌氭啞閸嬶綁鏌涢妷鎴濆暟妤犲洤顪冮妶鍐ㄥ姢濠殿噣顥撳Σ鎰板箳濡ゅ﹥鏅╁┑鐐叉閸庡啿鈻撻銏♀拺閻庡湱濮甸ˉ澶嬨亜閿旇鐏ラ柣蹇斿浮濮婄粯鎷呴崫銉よ檸濡炪倖鍨堕崝鏇炵幓閸ф绫嶉柍褜鍓涢幑銏犫攽閸繃鐎冲┑鈽嗗灡濡炲灝岣块幋锔解拺闁硅偐鍋涙俊钘夆攽閻愯鏀诲ǎ鍥э功閳ь剛鏁哥涵鍫曞磻閹剧粯鏅查幖绮光偓鎰佹浇婵$偑鍊ら崑鍛洪悢濂夋綎婵炲樊浜堕弫鍡涙煃瑜滈崜娑氬垝閺冨牊鍋ㄧ紒瀣硶閸橀亶姊洪崷顓炲妺闁搞倖淇洪妵鎰板箳閹惧瓨鐝抽梻浣告啞娓氭宕伴弽顓炴辈闁割偁鍎查悡鐔兼煟濡搫鏆卞┑顔ㄥ懐纾肩紓浣贯缚缁犵偟鈧鍠涢褔鍩ユ径濠庢僵闁挎繂鎳嶆竟鏇㈡⒑閹稿海绠撳Δ鐘叉啞缁傚秴鈹戦崼姘壕閻熸瑥瀚粈鈧梺娲诲墮閵堟悂宕洪埀顒併亜閹烘垵鏋ゆ繛鍏煎姈缁绘盯宕f径鍛窗闂佸憡甯楃敮鎺楁偩濠靛绀嬮柛鎾茶兌閳笺倖绻濋悽闈涒枅婵炰匠鍥ㄥ亱濠电姴鍊婚弳锕€顭跨捄濂斤繝寮崼鐔告珖闂侀€炲苯澧寸€殿喗褰冮埞鎴犫偓锝庝簻瀹撳棝姊洪棃娑㈢崪缂佽鲸娲熷畷銏$鐎n偆鍘甸梺绋跨箰閸氬宕曞Δ鍛厱闁靛ǹ鍎抽敍宥囩磼椤旇姤顥堥柟顔荤矙瀹曘劍绻濋崟顐㈢疄闂傚倷鑳剁划顖濇懌闂佸憡鎸婚懝楣冨煝閹炬枼鍫柛顐ゅ枔閸橀潧顪冮妶鍡樼婵☆偅绋撳褔鍩€椤掑嫭鍊垫繛鍫濈仢閺嬬喖鏌熷灞剧彧闁逛究鍔戦崺鈧い鎺戝閻撱儲绻涢幋鐏活亪顢旈埡鍛仺妞ゆ牗渚楀▓婊勬叏婵犲嫮甯涢柟宄版嚇瀹曨偊濡烽敂閿亾椤斿皷鏀介柍鈺佸暔娴犵娀鏌涢弬鎸庢崳闁告帗甯″畷濂告偄閾忚鍤岄梻渚€鈧偛鑻晶顔姐亜閺囶亞绉鐐寸墬閹峰懘鎳栧顓炴处閻撴洟鏌嶉埡浣告殶闁瑰啿鎳忛妵鍕籍閳ь剙煤閻斿娼栨繛宸簻缁€鍫ユ煙缂佹ê绗傜紒銊ょ矙濮婃椽宕妷銉︾€诲銈嗗灥椤︾敻鎮伴閿亾閿濆骸鏋熼柛濠囶棑閻ヮ亪鎮ч崺铏灴瀵偊妫冨☉鎺撴杸闂佺粯锚閻忔岸寮抽埡浣叉斀妞ゆ棁濮ょ紞鎴︽婢舵劖鐓曠€光偓閳ь剟宕戝☉銏犲嚑濞达綀銆€閸嬫捇鐛崹顔煎濠碘槅鍋呴悷鈺佺暦閿濆牏鐤€闁哄啠鍋撻柛娆忕箲娣囧﹪濡堕崒姘婵犵妲呴崑鍛淬€冮崱娑樼柧闁告挷鐒︾€氭岸鎮锋担椋庮槮缂傚秴锕獮鍐焺閸愨晛鍔呴梺鏂ユ櫅閸燁垶顢欓幒鎾剁瘈婵炲牆鐏濋弸娑㈡煥閺囨ê鍔氭い顏勫暣閹稿﹥寰勭仦鐐啎婵$偑鍊栭崝褏绮婚幋鐘电焼閻庯綆鍋佹禍婊堟煙閹规劖纭剧€涙繃绻濆▓鍨灓闁哄拋鍋嗗Σ鎰板箻鐠囪尙锛滃┑鐐叉閸ㄥ灚淇婃禒瀣拺缂備焦蓱閹牏绱掓潏銊︾闁告帗甯楃换婵嗩潩椤掆偓閸炪劌顪冮妶鍡樺暗濠殿喖顕划濠囨晝閸屾稈鎷虹紓渚囧灡濞叉牗鏅堕懠顒傜<閻庯綆鍋勯悘鈺呮煟濮橆厼鍔ゆい鎾冲悑瀵板嫮鈧綆鍓欓獮鍫熶繆閻愵亜鈧牠宕濊瀵板﹥銈i崘銊э紵闂佸搫娲㈤崹娲偂閸愵喗鐓曟繝闈涙椤忣亪鏌涢敐鍡樸仢闁哄矉缍侀獮姗€宕¢悙鎻捫曢梻浣告惈閻鎹㈠┑鍡欐殾闁圭儤鍩堝ḿ鈺傘亜閹达絽袚閻庡灚鐗犲缁樻媴鐟欏嫨浠ч梺鍛娒肩划娆撳箖閻戣棄鐓涢柛娑卞弨閹芥洟姊洪弬銉︽珔闁哥喍鍗抽幃鐤亹閹烘挾鍘遍梺闈涱樈閸ㄦ娊鎮鹃悽鍛婄厱閻庯綆鍋掑▓鏃堟煃鐟欏嫬鐏存い銏$懅濞戦潧鐣¢弶娆炬浆缂傚倸鍊风欢锟犲闯椤曗偓瀹曞綊宕奸弴鐘茬ウ闂婎偄娲︾粙鎴濐啅濠靛鐓涘璺侯儏閻忋儳绱掗幇顓犫姇缂佺粯绻堥幃浠嬫濞磋翰鍨介弻娑欑節閸曨剙娈岄梺宕囩帛閹告悂锝炲⿰鍫濈劦妞ゆ巻鍋撴い顐㈢箳缁辨帒螣鐠囧樊鈧捇姊洪崨濠勭畵閻庢凹鍓氱粋鎺懳熼懖鈺冿紳闂佺ǹ鏈銊ョ摥闂備焦瀵уú鈺備繆閸ヮ剙绀嗛柟鐑樻尵缁♀偓濠殿喗锕╅崜娆撳船閵娿儺娓婚柕鍫濇鐏忔澘顭跨憴鍕鐎规洘鍨块獮妯尖偓闈涙憸閹虫繈姊洪柅鐐茶嫰婢ь喗銇勯弴顏嗙ɑ缂佸倹甯為埀顒婄秵閳ь剦鍘搁弲鐘诲蓟閺囩喓鐝舵い鏍ㄧ閸g晫鈧鎸风欢姘潖婵犳艾纾兼繛鍡樺焾濡差喚绱撻崒姘毙㈤柨鏇ㄤ簻閻g兘骞嬮悙鐢电槇闂佹悶鍎滈崨顖氱倞闂傚倷绀侀幖顐ょ矙娓氣偓瀹曟垿宕卞☉娆忓壒闂佸壊鍋侀崕鏌ユ偂閵夆晜鐓涢柛銉㈡櫅娴犳粓鏌嶈閸撴瑧绱炴繝鍥ф槬婵炴垯鍨圭粻锝夋煟濡櫣浠涢柨娑樼箰椤啴濡堕崱妯烘殫闂佺ǹ顑囬崑銈呯暦閹惰姤鎯為悷娆忓閺嬫垿姊虹涵鍛【闁挎洏鍊曠叅闁挎洖鍊搁悡鏇㈡煙閻戞﹩娈曢柣鎾存礋閺岋繝宕堕妷銉ヮ瀳婵炲瓨绮嶇划宥夊Φ閸曨喚鐤€闁挎繂鎳庣粻濠氭⒑闁偛鑻晶顖涖亜閺冣偓閻楃姴鐣烽弶璇炬棃宕ㄩ闂寸暗闂備浇娉曢崰鎾存叏瀹勬壆鏆ゅ〒姘e亾闁哄瞼鍠栭獮鎴﹀箛闂堟稒顔勭紓鍌欒兌婵儳鈻嶉弴鐘冲床婵犻潧顑嗛ˉ鍫熺箾閹寸偠澹樻い锝嗘そ濮婄儤娼幍顔煎闂佽鍠栭崐鎼侊綖韫囨拋娲敂閸涱厽顓奸梻渚€娼ч悧鍡涘箟濞戙埄鏁嗗ù锝堟椤旀洟姊洪崨濠勭煀闁哥喍鍗抽獮鍐偂楠炵喓鎳撻オ浼村礋椤掆偓閳ь剚鍔曢埞鎴﹀焺閸愨晛鈧劙鏌涢埞鎯у⒉闁瑰嘲鎳忕粭鐔碱敍濞磋翰鍎靛濠氬磼濞嗘帒鍘$紓渚囧櫘閸ㄤ即锝炶箛姘ヤ汗闁圭儤鍨归悾娲⒑閻撳孩鎲搁柡浣规倐閵嗗懘宕f径宀€鐦堟繝鐢靛Т閸婄粯鏅跺☉銏$厽闁规儳顕ú鎾煛鐏炲墽銆掑ù鐙呯畵瀹曟粏顦俊鎻掔墕椤啴濡堕崱妯碱槰缂備緡鍠楅幑鍥ь嚕鐠囨祴妲堥柕蹇曞瑜旈弻娑樷槈閸楃偞鐏堝銈忚吂閺呯姴顫忓ú顏呯劵婵炴垶鍩冮弫鈧梻浣告啞閺屻劎绮旈崼鏇炵闁靛繒濮弨浠嬫倵閿濆簼绨芥い锔哄姂濮婂搫鐣烽崶銊ユ畬闂侀潧娲﹂敃銏ゅ箹鐟欏嫭鍎熼柕蹇嬪灮閻﹀牏绱掗崜褍顣奸拑杈ㄣ亜椤愵澁韬柡灞剧〒閳ь剨缍嗘禍婊堫敂椤撶姭鍋撶憴鍕闁搞劌鐖奸妴渚€寮撮姀鈩冩珖闂侀€炲苯澧撮柟顕嗙節閸ㄩ箖骞囨担鍝勬暩闂佽崵濮惧銊ф媰閿曞倸纾块柟閭﹀枤绾剧晫鈧箍鍎遍幊蹇涘窗濮椻偓閺岋紕浠﹂悙顒傤槰缂備胶绮惄顖氱暦瑜版帩鏁婇柛娆嶅劤濡垶姊婚崒娆愮グ妞ゆ泦鍛床閻庯綆鍓氶鑺ユ叏濮楀棗澧绘繛鍏肩墪閳规垿鎮╃€圭姴顥濈紒鐐劤閸氬鎹㈠☉銏犲耿婵☆垵娅f禒瀛樼節绾版ǚ鍋撻懠顒傜厯濠殿喖锕ㄥ▍锝夊箯閻樿鐏抽柧蹇e亞娴滎亪姊绘担铏瑰笡闁绘绮撳畷銏n樄闁诡喗鍎抽悾锟犲箥閾忣偅鏉搁梻浣虹《閸撴繈鎮烽敃鈧埢鎾诲即閵忊檧鎷洪梻渚囧亞閸嬫盯鎳熼娑欐珷妞ゆ牗绮庣壕濂告煛閸愩劌鈧悂寮稿☉姘e亾濞堝灝鏋熼柟姝屾珪閹便劑鍩€椤掑嫭鐓冮柛婵嗗閳ь剛鎳撻埢宥咁吋婢跺鎷绘繛杈剧秬濞咃絿鏁☉銏″珔閺夊牃鏅滈崰鎰版煛婢跺﹦浠㈤柡鍡秮閺岀喖顢欑紓瀛樺灩閹广垹鈹戠€n亞鍊為梺闈浨归崹铏光偓姘偢濮婄粯鎷呴崨濠傛殘闂佺懓鎲″Σ鎺楀Φ閹版澘绀冮柍鍝勫枤濞叉悂姊虹紒妯哄闁稿簺鍊濋幃锟犲即閵忥紕鍘藉┑鈽嗗灠閹碱偆鐥閺岀喖鎯傞崫銉戠紓浣虹帛閻╊垰鐣烽柆宥呯疀妞ゆ帒鍊风槐娆撴⒒娴g瓔鍤冮柛鐘愁殜閹兘鍩¢崨顓犵暫濠电姴锕ら崥姗€鎮㈤崗鐓庝簵闁硅壈鎻槐鏇㈩敇婵傚憡鈷掗柛灞捐壘閳ь剚鎮傚畷鎰槹鎼淬埄鍋ㄩ梺璺ㄥ枔婵挳鎯屽Δ鍛彄闁搞儯鍔嶇粈鍫濃槈閹惧磭效闁哄瞼鍠愬ḿ蹇涘箚瑜滃ú顓㈡倵鐟欏嫭灏柣鎺炵畵楠炲牓濡搁妷顔藉瘜闁荤姴娲╁鎾寸珶閺囥垺鈷掑ù锝呮啞閹牓鏌¢崼顐㈠缂侇喗鐟╅獮瀣晲閸ワ箒鍩呴梻鍌氬€风欢姘缚閼姐倐鍋撻棃娑氱劯鐎规洏鍨洪妶锝夊礃閳轰椒绨甸梻浣告贡閸嬫捇寮告總绋跨哗闁兼亽鍎禍婊堟煛閸愩劌鈧爼鍩€椤掆偓椤戝鎮¢鍕垫晢闁稿本绮庨敍婵嬫⒑缁嬫寧婀扮紒瀣灴瀹曨偊宕崟銊︽杸闂佹寧绋戠€氼參寮抽渚囨闁绘劕寮堕崰妯尖偓娈垮枛婢у酣骞戦崟顖椻偓锕傚箣濠靛洦姣岄梻鍌氬€搁崐鐑芥嚄閸洖绠犻柟鍓х帛閸嬨倝鏌曟繛褍鍟悘濠囨倵閸忓浜鹃梺鍛婃处閸嬪嫰宕甸幋锔解拺闁告挻褰冩禍鏍煕鎼淬垻鍙€闁糕晜鐩獮鎺楀箠閵娿儳绉洪柡浣瑰姍瀹曘劑顢欓崗鍏肩暭闂傚倷鑳堕、濠勪焊濞嗘劗浠氶梻浣哥枃椤宕归崸妞尖偓浣糕枎閹炬潙鈧攱銇勯幒宥囧妽闁伙附鎹囧缁樼瑹閳ь剙岣胯铻炴俊銈呮噹閻ゎ喗銇勯弽銊х煁鐎规洖寮剁换婵嬫濞戝崬鍓扮紒鐐劤閸氬鎹㈠┑鍥╃瘈闁稿本鍑规禒鎯ь渻閵堝棙鈷愭繛鑼枎椤繒绱掑Ο璇差€撻梺闈╁瘜閸樹粙鎳i崶顒佲拺闁硅偐鍋涙俊璺ㄧ磼椤曞懎鐏﹂柟顔矫埢搴ㄥ箻缁瀚肩紓鍌氬€烽悞锕傛晪缂備焦顨嗙敮锟犲蓟閿濆牏鐤€闁哄倸鐏濋幗鍨節绾板纾块柡浣筋嚙閻g兘鎮㈢喊杈ㄦ櫖濠殿喗锕㈢涵鎼佸船濞差亝鈷掑ù锝囧劋閸も偓闂佸鏉垮闁瑰箍鍨归濂稿幢濞嗘ɑ绁┑掳鍊х徊浠嬪疮椤栫偛鐓曢柟杈鹃檮閻撴瑩鏌熼娑欑凡鐞氭岸姊烘潪鎵獢濞存粌鐖煎璇测槈閵忕姈鈺呮煏婢舵稓鐣卞ù鐘虫尦閹鈻撻崹顔界亪濡炪値鍘鹃崗姗€鐛崘顔碱潊闁靛牆鎳愰ˇ褔姊虹紒妯诲碍閻庢稈鏅犻幃鐐鐎涙ǚ鎷绘繛杈剧到閹芥粓寮搁崘鈺€绻嗘俊鐐靛帶婵″吋銇勯鍕殻妤犵偞甯″顒勫垂椤斿彞鍠婇梻鍌欑婢瑰﹪宕戦崨顒煎搫顫滈埀顒勫春濞戙垹绠i柨鏃囆掗幏鍝勵渻閵堝棗濮傞柛濠冩礃缁傛帒饪伴崼鐔哄幘濠电偠灏褔鎮橀敂閿亾鐟欏嫭纾搁柛銊ょ矙楠炲啯绂掔€n亜绐涙繝鐢靛Т鐎氼剟鐛崼婵冩斀闁绘ê鐏氶弳鈺佲攽椤旇姤灏︾€规洦鍨堕獮宥夘敊閸欍儳鐟濋梻浣烘嚀婢х晫鍒掗鐐村亗闁绘柨鍚嬮悡銉︾節闂堟稒顥為柟鍏煎姍閺屾稑螣閾忚鎲煎銈冨妸閸庣敻骞冨▎鎾宠摕闁靛鍎遍崣濠囨⒒娴g儤鍤€缁剧虎鍙冨畷鎴﹀Χ閸℃洜绠氶梺缁樺灱婵倝寮插⿰鍫熺厽闁挎繂鎳撶€氭壆绱掗埀顒佺瑹閳ь剙顫忔繝姘<婵﹩鍏橀崑鎾搭槹鎼达絿鐒兼繛鎾村焹閸嬫挻顨ラ悙宸█闁糕晛瀚板畷姗€顢旈崱妯烘疄濠电姴鐥夐弶搴撳亾閺囥垹绠犻幖娣妼閸ㄥ倿鏌涘畝鈧崑鐐烘偂閺囩喍绻嗛柕鍫濇噹閺嗘瑥霉濠婂啰绉洪柡宀嬬磿閳ь剨缍嗛崑鍛存偂閵夆晜鎳氶柡宥庡幗閻撱儲绻濋棃娑欘棡闁革絽缍婇弻锟犲幢濞嗗繋妲愰梺鍝勮嫰缁夊綊寮婚妸褉鍋撻敐搴濈敖濞寸厧鐭傚铏规嫚閳ヨ櫕鐏堢紓鍌氱Т閿曨亪鎮伴鐣岀懝闁逞屽墴閻涱噣骞掑Δ鈧粻锝嗙節閸偄濮夐柍褜鍓氭繛濠傤潖缂佹ɑ濯撮柛娑橈攻閸庢挸顪冮妶鍡楃仴婵☆偅绻傞锝嗙節濮橆儵鈺呮煃鏉炴媽鍏岄柛妯绘尦濮婅櫣娑甸崨顔兼锭闁诲酣娼ч惌鍌氼嚕椤愶絿绡€闁告洦鍘介敍蹇涙⒑閸濆嫷妲搁柣蹇旂箞閹虫粎鎲撮崟顓狀啎闂佸壊鍋呯换鍌炪€傚畷鍥╃<閺夊牄鍔嶇亸鎵磼濡ゅ啫鏋涚€规洘鍎奸ˇ鎶芥煟韫囨挾澧︽慨濠呮缁辨帒顫滈崱妯兼殾闂備胶鎳撻幉锟犲箖閸岀偛绠栭柟顖嗗懏娈濋梻渚囧弿闂勫嫬顕欏ú顏呪拺闂侇偆鍋涢懟顖涙櫠閹绢喗鐓忛柛鈩冩礈椤︼箓鏌嶇拠鏌ュ弰妤犵偞锕㈠鍫曞箣濠婂嫬浜濋梻鍌欐祰椤曆呮崲閹烘纾婚柣妯哄棘濞戙垹绀嬫い鎾跺С缁楀姊洪棃娑崇础闁告侗鍨界槐鎶芥⒒娴e懙褰掑嫉椤掑嫭鍤屽Δ锝呭暙閻掑灚銇勯幒宥囧妽闁稿﹥鍔楅埀顒冾潐濞叉﹢宕濆▎鎾崇畺婵犲﹤鐗婇崵宥夋煏婢跺牆鍔楅柛瀣崌瀹曠ǹ螖娴e搫寮抽梻浣告惈濞层劑宕戝☉銏犵劦妞ゆ巻鍋撶紓宥咃工椤曪綁寮婚妷顔芥櫆闂佺硶鍓濋悷褔鏁嶅┑瀣拺缂佸瀵у﹢浼存煟閻旀繂娲ょ粈澶屸偓骞垮劚椤︿即鎮¤箛娑欑厱闁靛绲芥俊鎸庣箾閹绘帩鍤熼柍褜鍓氶鏍窗濡ゅ嫨浜归柛鎰靛枔閸嬫垵霉閸忓吋缍戦梺鍗炴处缁绘繈濮€閳衡偓閹秶绱掗悩铏磳鐎殿喛顕ч埥澶愬閻樻彃绁梻渚€娼ф灙闁稿氦娅曠粋鎺楀煛娴e弶鏂€闂佸疇妫勫Λ妤佺濠靛瀚呴弶鍫氭櫇绾捐偐绱撴担璐細婵炴彃顕埀顒冾潐濞叉牕鐣烽鍕厺閹兼番鍊楅悿鈧柟鑲╄ˉ濡插懎螞濠婂牊鈷掗柛灞剧懅椤︼箓鏌i妶鍛枠妞ゃ垺淇洪ˇ褰掓煙椤斻劌娲ら獮銏$箾閹寸偍缂氶柛妯绘尦濮婅櫣娑甸崨顔兼锭闁诲酣娼ч惌鍌氼嚕椤愶絿绡€闁告洦鍘介敍蹇擃渻閵堝棙灏靛┑顔芥尦瀹曘垻鈧潧鎽滅壕濂告煠缁嬭法浠涚紓宥嗗灴閺屽秶鎲撮崟顐や紝闂佽鍠楅悷鈺佺暦閿濆棗绶炲┑鐘插缁茬晫绱撻崒姘偓鐑芥倿閿曚降浜归柛鎰╁妵缂傛岸鏌嶉妷銉э紞闁哄棴闄勯幈銊ノ熼幐搴c€愮紓浣哄У婵炲﹪寮婚悢琛″亾濞戞鎴﹀煕閹扮増鐓熼幖绮规閻撳吋鎱ㄦ繝鍐┿仢闁诡喚鍏橀弻鍥晝閳ь剙鈻撻崼鏇熲拺缂佸顑欓崕鎰磼鐎n偅灏扮紒鏃傚枛瀵挳濮€閳哄倹娅栭梻浣虹帛閸旀鎮伴妷鈺佺婵炲樊浜濋埛鎺楁煕鐏炵偓鐨戝褎绋戦埥澶愬箻閼搁潧娈岄梺瀹犳椤︻垶锝炲┑瀣垫晝闁挎繂鎳庨蹇涙⒒閸屾瑧顦﹂柛姘儐缁傚秵绂掔€n亞锛熼梺鍦帛瀹曞ジ骞掑Δ鈧獮銏$箾閸℃ê鐏╅柨娑欑箞濮婅櫣绮欓幐搴㈡嫳闂佺厧缍婄粻鏍春閳ь剚銇勯幒宥囧妽闁稿﹥鍔楅埀顒冾潐濞叉﹢宕濆▎鎾跺祦闁哄秲鍔嶆刊鎾煕濠靛嫬鍔电紒槌栧枛閳规垿鏁嶉崟顐$捕濡炪倖鍨甸幊搴ㄦ箒闂佺粯鍨兼慨銈夊磿濡ゅ懏鐓曢柍鈺佸暔娴犵娀鏌嶈閸撴氨鏁幒妤嬬稏婵犻潧顑嗛弲鏌ユ煕濞戝崬澧い銉﹀哺濮婄粯鎷呴挊澹捇鎷戞潏鈺冪<閻犲洩灏欐晶鏇熴亜椤愩垻绠伴悡銈嗐亜韫囨挾校闁哄懌鍨藉娲焻閻愯尪瀚板褎澹嗙槐鎺楊敊閼恒儮鎷婚梺閫炲苯澧存繛浣冲洤绠烘繝濠傜墛閸庢鏌涢埄鍐姇闁绘挻娲熼幃姗€鎮欓幓鎺嗘寖闂佸磭顑曢崕宕囨閹烘梹瀚氶柛娆忣樈濡繝姊洪棃娑欐悙閻庢碍婢橀锝嗙鐎n€晝鎲歌箛娑欏仼闁告繂瀚峰〒濠氭煏閸繃鍣界紒鐘插暱閳规垿鎮欓埡浣峰闂傚倷绀侀幖顐︽儗婢跺本宕叉繝闈涙閺嗭箓姊洪鈧粙渚€寮崶顒佺厽闁瑰瓨绻冮ˉ鐐烘煕閻樼鑰挎慨濠勭帛閹峰懘鎮滃Ο鐑樼暚闁诲孩顔栭崰鏍偉婵傚摜宓侀柛鎰靛枛绾惧ジ鏌i幇顖氱毢闁伙絾妞介幃宄扳堪閸曨剛鍙嗛梺浼欑悼閸忔﹢骞冮埄鍐╁劅婵☆垳绮弶鎼佹⒒娴gǹ顥忛柛瀣╃窔瀹曠懓煤椤忓嫰妫峰銈嗙墬缁海澹曟禒瀣厱閻忕偛澧介幊鍡涙煕韫囨挾鐒搁柡灞剧〒閳ь剨缍嗛崑鍛暦瀹€鈧埀顒冾潐濞叉ê煤閻旇偐宓侀幖娣妽鐎电姴顭跨捄鍝勭彁闁哄洢鍨洪悡鐔煎箹閹碱厼鐏g紒澶屾暬閺屾盯骞樼壕瀣棟闂佷紮绲块崗妯虹暦閿濆棗绶炵€光偓閳ь剟顢欓弴銏♀拺闁荤喐澹嗛幗鐘绘煟閻旀潙鍔﹂柟顔斤耿閸╋繝宕橀鍡床闂備胶绮悷銉╁箠閹邦喚鐭欓柤濮愬€楃壕鑲╃磽娴h疮缂氱紒鐘靛仦娣囧﹪顢曢姀鐘虫闂佸疇妫勯ˇ顖烇綖濠靛鏁勯柤鎭掑劚椤徰呯磽閸屾艾鈧悂宕愬畡鎳婂綊宕堕妸褜娲稿銈嗗笒鐎氼剛澹曟繝姘厪闁割偅绻冩刊鍏肩箾閸忚偐澧甸柡灞剧☉閳规垿宕卞缁樼亞闂備焦鍎崇换妤咃綖婢跺备鍋撳顓炲摵闁哄瞼鍠撶槐鎺懳熼搹璇″剬婵$偑鍊栧褰掑垂閼哥數鈹嶅┑鐘叉处閸婇攱銇勮箛鎾愁仱闁稿鎹囬獮瀣晝閳ь剛绮堟径灞稿亾閸忓浜鹃梺鍛婃处閸撴艾鈻嶉崶顒佲拺闂傚牊绋撴晶鏇熴亜瑜夐崑鎾剁磽閸屾氨校闁绘濞€閹繝顢曢敃鈧悙濠囨煏婵炑€鍋撳┑顔兼喘濮婅櫣鎷犻垾宕囦化闂佺ǹ顑冮崐婵嗩嚕婵犳碍鏅插璺侯儏娴滄粓姊洪崨濠勨槈闁挎洩绠撳畷娆撳灳閹颁焦瀵岄梺闈涚墕濡瑩鎳栭悩缁樼厱闁靛绲芥俊鐑芥煙闁垮銇濇慨濠冩そ瀹曘劍绻濋崟顓犳殼闂佽瀛╅崙褰掑储婵傚壊鏁婇煫鍥ㄦ尨閺€浠嬫倵閿濆骸浜為柛姗€浜堕弻锝嗘償椤栨粎校闂佺ǹ顑呭Λ妤冨弲闂佸湱铏庨崰妤呮偂閺囥垺鐓冮柛婵嗗閳ь剙顭烽崺濠囧即閻橆偄浜鹃柛顭戝亝缁舵煡鎮楀鐓庡箻闁瑰箍鍨归埞鎴﹀炊閵娿儱濡抽梻渚€娼х换鎺撴叏瀹勬嫈锝夋晲婢跺鎷婚梺绋挎湰閻熝呯玻閺冣偓缁绘稒鎷呴崘鍙夊闁稿顑夐弻娑㈠焺閸愵亖妲堥梺姹囧€ら崰妤呭Φ閸曨垰绠涢柛鎾茬椤曡京绱撴担绛嬪殭婵☆偅顨婇崺鐐哄箣閿曗偓绾惧吋鎱ㄥ鍡楀箹闁哄棗鐗撳铏圭磼濡闉嶉梺鑽ゅ暱閺呯姴顕i弰蹇f▉缂備胶濮甸惄顖炲极閹版澘宸濇い鎺戝€诲▔鎸庣節閻㈤潧校妞ゆ梹鐗犲畷浼村冀椤剝妞介弫鍐磼濮g》绠撻弻娑㈠即閵娿儳浠╅梺鍛婎殙濞呮洘绌辨繝鍥舵晬婵﹩鍘介崕鎾寸節濞堝灝鏋熸繛鍙夌矌濡叉劙骞樼€涙ê顎撻梺鎯х箳閹虫挾绮敍鍕=濞达絿鐡旈崵娆撴煟濡も偓濡繈骞冩ィ鍐╁€婚柦妯侯槺閻i箖姊绘笟鍥у伎闂傚嫬瀚伴崺銏犵暆閸曨兘鎷绘繛杈剧秬婵倝濡撮崘顔界厽闁硅櫣鍋涢々顒勬煕閹烘挸绗掗柣锝嗙箞瀹曠喖顢曢妶鍛闂傚倷鑳堕幊鎾活敋椤撱垹纾绘繛鎴炴皑娑撳秹鏌eΟ鑲╁笡闁抽攱鍨圭槐鎺斺偓锝庝簻閻繝鏌¢埀顒佺節濮橆厾鍘甸梺鑽ゅ枔婢ф宕板Ο娲绘闁绘劘顕滃銉╂懚閺嶎厽鐓曟繛鎴濆船瀵噣鏌涢悙鑼煟婵﹥妞藉畷顐﹀礋椤掆偓缁愭盯姊虹粙娆惧剱闁烩晩鍨伴悾鐑藉箣濠垫劕鎮戦梺绯曞墲閻熝囶敊閺囥垺鐓熼幖杈剧稻閺嗏晠寮搁鍡忓亾濞戞瑧绠撴い顏勫暣婵″爼宕卞Δ鍐ф樊婵犵妲呴崑鍛崲閸繄鏆﹂柛婵嗗濡插牓鏌曡箛鏇炐ユい鎾存そ濮婃椽骞愭惔銏╂⒖閻炴碍鐟╅弻鐔风暋闁妇鍚嬪┑顔硷攻濡炶棄鐣峰⿰鍫濈闁瑰搫绉堕弫鏍⒒娴e憡鎲稿┑顔炬暬楠炴垿宕堕妸銈囩畾闂佸湱铏庨崰鏍不閹惰姤鐓涢柛鎰╁妼閳ь剙顭烽弫宥呪堪閸啿鎷虹紓鍌欑劍閿曨偊鎳撻幐搴g濞达絽鍟跨€氼噣銆呴悜鑺モ拺妞ゆ巻鍋撶紒澶屾暬閹€斥槈閵忊€斥偓鍫曟煟閹邦厼绲婚柍閿嬫閺屽秹顢涘☉娆戭槶缂備浇椴哥敮鐐垫閹烘嚦鐔兼嚃閳哄啯婢栭梺璇叉唉椤煤濮椻偓閺佸啴濮€閵堝啠鍋撴笟鈧顕€宕煎┑鍫Ч闂備線娼ф灙闁稿孩鐓″畷鎰板即閵忊檧鎷婚梺绋挎湰閼归箖鍩€椤掑嫷妫戠紒顔肩墛缁楃喖鍩€椤掑嫬绠栭柛褎顨呴悙濠冦亜椤掑澧柣鈺婂灠閻g兘鎮㈢喊杈ㄦ櫖闂侀€炲苯澧寸€规洖鐖奸、妤呭焵椤掑倻涓嶆い鏇楀亾闁哄本鐩獮妯虹暦閸ワ箒妾告繝鐢靛仦缁佹挳寮查悩鍏呯箚闁汇垻枪缁犳盯鏌℃径搴㈢《妞ゆ柨锕铏规喆閸曨偆顦ㄥ┑鐐差槹閻╊垶鎮伴鈧獮鍥偋閸垹骞楅梺纭呭亹鐞涖儵鍩€椤掆偓閸熸寧娼忛崨瀛樷拺缂佸顑欓崕鎰版煙閻熺増鍠樻鐐插暙铻栭柛娑卞枟濞呮粓鏌熼懖鈺勊夐柍褜鍓氶崜姘缚妤e啯鐓熼柣鎰嚟閸熻尙绱掗悩铏碍妞ゎ偄绻掔槐鎺懳熺拠宸偓鎾绘⒑閹呯缂佺姴绉归崺鈧い鎺嗗亾闁挎洦浜濠氭晸閻樻彃绐涘銈嗘煣閸曟﹢鍩€椤掍礁娴柡灞界Х椤т線鏌涢幘瀛樼殤闁哥姴锕ら濂稿椽娴e搫鏁告繝娈垮枟閵囨盯宕戦幘缁樼厵妞ゆ棁妫勯崝銈夋煟閿濆繒绡€闁哄苯娲弫鍌炴寠婢跺瞼澶勯梻鍌氬€风欢姘跺焵椤掑倸浠滈柤娲诲灡閺呭爼骞橀鐣屽帾闂佺硶鍓濆ú婊呯玻閺冨倵鍋撳▓鍨珮闁革綇绲介悾鐑芥偂鎼存ɑ鏂€闂佺硶鍓濋悷褍鐣烽崫鍕ㄦ斀闁挎稑瀚禍濂告煕婵犲啰澧垫鐐村姈閵堬綁宕橀妸褏宕堕梻浣筋潐閸庡磭绮诲鍡欘洸鐟滅増甯楅悡娆戠磽娴i潧鐏╅柡瀣枛閺屽秹鏌ㄧ€n亝璇為梺鍝勬湰缁嬫挻绂掗敃鍌氱闁归偊鍓﹀Λ鐔兼⒒娓氣偓閳ь剛鍋涢懟顖涙櫠椤曗偓閺屾盯濮€閿涘嫬寮ㄥ┑鐘亾濞撴埃鍋撴慨濠冩そ楠炴牠鎮欓幓鎺懶ら梻浣告啞閹碱偆绮婚幘鎰佸殨妞ゆ劑鍊愰崑鎾绘晲鎼粹剝鐏嶉梺缁樻尰缁嬫捇鍩€椤掆偓缁犲秹宕曟潏顭戞闁归棿鑳跺畵渚€鏌″搴″箺闁绘挾鍠栭弻鏇㈠醇濠靛鈧鏌$€n剙鏋涢柡灞炬礋瀹曟儼顦叉い蹇e幗椤ㄣ儵鎮欓崣澶婃灎閻庤娲樼划宥夊箯閸涘瓨鍊绘俊顖涙た閸熷懘姊婚崒姘偓鐑芥嚄閸撲礁鍨濇い鏍仜缁€澶愭煛閸ャ儱鐏柡鍛箞閺屻劑寮撮悙娴嬪亾閸濄儳涓嶉柣鏂垮悑閻撴瑩姊婚崒姘煎殶妞わ讣濡囩槐鎺楊敃閵忊懣褔鏌$仦鍓ф创妞ゃ垺娲熼弫鎰板炊閳哄啯姣庨梻鍌欒兌绾爼寮插┑瀣;闁靛牆鎷嬪ḿ鏍ㄧ箾瀹割喕绨荤紒鈧崼銉︾厵缂備焦锚缁楀倻绱掗妸褍甯堕柍瑙勫灴閹瑩骞撻幒鏃堢崜闂備焦瀵уú蹇涘垂閽樺鏆﹂柛婵嗗濡插牓鏌曡箛鏇炐ユい鎾存そ濮婅櫣绱掑Ο鍓佺窗闂佽桨鐒﹂幃鍌炲极瀹ュ應鏀介柛銉㈡櫇椤旀洟鏌℃径濠勫濠⒀呮櫕缁棃顢楅崟顒傚幈闁诲函缍嗘禍婊堝焵椤掆偓濞硷繝鎮伴閿亾閿濆倹娅囩紒澶婄摠缁绘繈濮€閿濆懐鍘梺鍛婃⒐濞茬喖寮荤€n喖鐐婃い鎺嶈兌閸樹粙姊洪崫鍕殭闁稿﹨宕靛褔鍩€椤掑倻纾藉ù锝夋涧婵″吋銇勯鐐叉Щ妞ゎ偄绻愮叅妞ゅ繐鎷嬪Λ鍐ㄢ攽閻愭潙鐏卞瀛樻倐椤㈡捇宕卞☉娆屾嫽闂佺ǹ鏈懝楣冾敂閳哄懏鍊垫慨妯煎帶閺嬬喓绱掗崒姘毙ф鐐寸墬閹峰懘宕妷顔兼倯濠碉紕鍋戦崐鏍蓟閵婏附娅犲ù鐘差儐閺咁剚绻濇繝鍌滃闁抽攱鍨圭槐鎺斺偓锝庡亜椤曟粍绻濋埀顒勫箥椤斿墽锛滈柣搴秵閸嬪嫰鎮橀妷鈺傤梿濠㈣泛顑冩禍婊堟煛閸愩劌鈧骞楅崒娑氱闁割偅绮庨惌娆撴煛瀹€瀣М妤犵偛娲、妤呭焵椤掑倻妫憸鏃堝蓟濞戙垺鍋愮紒娑氼攰閳ь剙娼¢弻鈥崇暆閳ь剟宕伴弽顓溾偓浣糕枎閹炬緞鈺呮煏婢舵盯妾柟顔界懇濮婄粯鎷呯粙鑳煘濠电偛妯婇崣鍐嚕婵犳艾鍗抽柨娑樺閺夋悂姊洪崫鍕窛闁稿⿴鍋婃慨鈧柕蹇嬪灮閿涙粓姊虹紒妯撶懓鈻嶉弴銏犖︽繝闈涙处閸欏繐鈹戦悩鎻掝伀閻㈩垱鐩弻鐔风暋閻楀牆娅ょ紓浣诡殘閸犳牠銆佸☉妯锋婵炲棙鍔栭澶愭⒒閸屾艾鈧兘鎳楅懜鐢典粴婵$偑鍊栭崹闈浳涘┑鍡欐殾婵犻潧鏌堥弮鍫濆窛妞ゆ挾濮烽弳顐⑩攽閻愬瓨缍戦柛姘儏宀e灝鈻庤箛鏃€娈伴梻鍌氬€风粈渚€鎮块崶褜娴栭柕濞炬櫆閸ゅ嫰鏌涢锝嗙』闁搞儺鍓﹂弫鍥煟閹般劍娅嗛柡鍌楀亾闂傚倷鑳剁划顖氱幓鐠恒劌鍨濇い鏍ㄥ焹濡插牏鎲搁弮鍫濊摕闁挎繂鎲橀弮鍫濈劦妞ゆ帒瀚弲婵嬫煥閺囩偛鈧悂鎮為崹顐犱簻闁瑰搫绉电粊鏉款熆鐟欏媶鎴﹀Φ閸曨垼鏁囬柣妯诲絻楠炲鎮楀▓鍨灈妞ゎ參鏀辨穱濠囧箹娴e摜鍘搁梺绋挎湰閻喚鑺辨繝姘拻濞达絽鎲¢崯鐐电磼鐠囨彃鈧鍩€椤掍浇澹橀柟铏耿瀵偊骞囬鐐电獮闁诲函缍嗛崜娆撶嵁濡ゅ懏鈷掑ù锝囩摂濞兼劙鏌涙惔銏犫枙闁诡喗妞芥俊姝岊槾闁活厼妫濋幃妤呮晲鎼粹剝鐏嶉梺缁樻尰閻燂箓濡甸崟顖氱睄闁稿本绮嶉幉妯衡攽閻愯尙澧涚紒顔芥崌瀵鍩勯崘鈺侇€撻梺鑽ゅ枑濠㈡﹢锝炲澶嬧拺閻犲洠鈧磭浠┑鈽嗗亜閸熸潙鐣峰ú顏呮櫇闁稿本姘ㄩ崝锕€顪冮妶鍡楃瑨閻庢凹鍓涙竟鏇熺節濮橆厾鍘甸梺纭咁潐閸旀洟鎮¢幇顔瑰亾鐟欏嫭绀€妞わ妇鏁诲濠氬即閻旇櫣顔曢悷婊冪Ч楠炲繘骞嬮悩鎰佹綗闂佹儳娴氶崑鍡欏姬閳ь剙鈹戦悙鑼闁诲繑绻堝鎼佹偄閻撳骸鍤戝銈呯箰婵炲﹪鎮烽幍鍐茬墯闁硅偐琛ラ埀顒佸墯濞兼儳鈹戦悩顔肩伇妞ゎ偄顦叅婵☆垵鍋愮槐锕傛煟閿濆懐鐏遍柣顓熺懇閹綊骞侀幒鎴濐潎闂佺粯绋掗幑鍥ь潖缂佹ɑ濯寸紒瀣儥濡矂姊虹粙娆惧剰闁硅櫕鍔欏畷鐗堢節閸屻倕鎮戦梺鍛婁緱娴滄繈鎮楀ú顏呪拺闁告稑锕g欢閬嶆煕閺冣偓閸庡ジ濡甸幇鏉跨闁规儳鍘栧Ч妤佺節閻㈤潧浠滄俊顐n殘閹广垽骞嬮悙鑼獮闂佸憡娲﹂崹閬嶆偂閻斿吋鐓欓柟顖嗗啯姣愰梺鍝勬閸犳牠寮婚悢鍏煎殤妞ゆ垯鍨圭紞濠囧Χ椤忓懎顕遍柡澶嬪灴閸炶泛鈹戦悩缁樻锭闁绘绮屽嵄闁割偅娲橀埛鎺戙€掑锝呬壕濠电偘鍖犻崱妤侇仩闂傚倷绀侀幉鈩冪瑹濡ゅ懎鍨傞柣鎾冲閿濆绠瑰ù锝呭帨閹风粯绻涙潏鍓хК婵炲拑缍佹俊瀛樼節閸ャ劎鍘遍梺瑙勫劤椤曨厾绮诲Ο鑲╃<妞ゆ梻鏅幊鍥殽閻愬樊鍎旈柡浣稿€块幐濠冨緞閸℃ぞ澹曢梺绉嗗嫷娈曢柣鎾存礃閵囧嫰顢橀悢椋庝淮婵炲瓨绮嶉悧鏇㈡箒濠电姴锕ょ€氼噣鎯岄幒妤佺厸鐎光偓閳ь剟宕伴幘璇茬劦妞ゆ帒鍊归弳鈺呭几椤忓娊褰掓偐瀹曞洨鐓夐梺鍝勬湰閻╊垰顕i鍌涘珰婵炴潙顑呮禍鐐節闂堟侗鍎忛柦鍐枛閺屻劌鈹戦崱娆忊叡闂佹眹鍊愰崑鎾斥攽閻樺灚鏆╁┑顔芥尦瀹曨垶顢涢悙鏉戜户闂佸搫绋侀崑鍡欏閽樺褰掓晲閸曨厾鐓撻梺鍛婄箖濡炰粙寮婚悢鐓庡窛濠电姴鍟埀顒佸姈閵囧嫰濮€閳晜鍨圭紓鎾绘偩瀹€鈧惌娆撴煙缁嬭法鏄傚ù鐘灲濮婄粯鎷呴崨濠傛殘闂佸憡妫戠粻鎾崇暦閵忥紕闄勭紒瀣硶閻i箖姊洪崜鎻掍簴闁稿孩鐓¢幃锟犳偄閻撳海顔愬┑鐑囩秵閸撴瑩鎮炲ú顏呯厱闁绘棃顥撶粻濠氭煛鐏炲墽娲撮柟顔规櫅閻g兘宕惰閹蜂即姊绘担鍝勪缓闁稿氦宕电划濠氬箻鐠囪尪鎽曢梺闈浤涢埀顒勫磻閹剧粯鏅查柛灞剧⊕閻濇牜绱撴担鍝勑i柤褰掔畺閸╃偤骞嬮敂缁樻櫓闂佷紮绲介惉濂告偩閻㈠憡鈷戞繛鑼额嚙楠炴牠鏌eΔ鈧Λ妤€鐣甸崟顖涒拺缂備焦锚閻忓崬鈹戦鍝勨偓婵嬪春濞戙垹绠i柣妯兼暩閿涙粓鏌f惔顖滅У闁稿甯″畷鏇㈠Ψ閳哄倻鍘遍柟鍏肩暘閸ㄨ鎱ㄥ澶嬬厸鐎光偓閳ь剟宕伴弽顓炵畺闁绘垼濮ら崑瀣煕椤愶絿绠栭柣蹇撻叄閺岋絾鎯旈姀鈺佹櫛闂侀潻缍嗛崳锝呯暦閹寸偟绡€闁搞儮鏅涚粊锕傛⒑閹肩偛鍔撮柛鎿勭畵瀵偊宕堕浣哄幗闂佸搫鍊搁悘婵單g拠娴嬫斀闂勫洤鈻嶉弴鐘冲床婵犻潧鐗嗛弸鍫熶繆椤栨稒銇熸繛鍏煎灴濮婃椽骞栭悙鎻掝潎濠电偘鍖犻崶銉㈠亾閸涱喚闄勭紒瀣嚦閳哄懏鐓ラ柡鍌氱仢閳锋梻鎲告导瀵哥暫婵﹥妞藉畷顐﹀礋椤掆偓缁愭盯姊虹粙鍨劉闁告梹娲熸俊鎾箳閹惧墎鐦堝┑顔斤供閸橀箖宕㈤鍫熲拺闁告挻褰冩禍婵堢磼鐠囨彃鏆i挊鐔兼煟濡儤鈻曢柣鏂挎閹茬ǹ鈹戦崼顫瑝闂佽宕橀褔鎷戦悢鍝ョ闁瑰鍋熼幊鍛磼閳锯偓閸嬫捇姊绘担鍛婂暈闁告棑闄勭粋宥呪堪閸繄鍘遍梺鍓插亖閸庢煡鍩涢幋锔解拺妞ゆ劑鍊曟禒婊堟煠濞茶鐏¢柡鍛埣椤㈡盯鎮欑€电ǹ骞楅梻浣告惈閸燁垶宕归崹顐f珷閻庢稒锕╁▓浠嬫煟閹邦垰鐨虹紒鐘差煼閺屸剝鎷呯憴鍕3闂佽桨鐒﹂幑鍥极閹剧粯鏅搁柨鐕傛嫹>>  闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁绘劦鍓欓崝銈嗙節閳ь剟鏌嗗鍛姦濡炪倖甯掗崐褰掑吹閳ь剟鏌f惔銏犲毈闁告瑥鍟悾宄扮暦閸パ屾闁诲函绲婚崝瀣уΔ鍛拺闁革富鍘奸崝瀣煕閵娿儳绉虹€规洘鍔欓幃娆忣啅椤旇棄鐦滈梻渚€娼ч悧鍡椢涘Δ鍐當闁圭儤顨嗛悡銉╂煛閸ユ湹绨绘い鈺婂墰缁辨帡顢欓悾灞惧櫙缂備胶濮甸惄顖氼嚕椤曗偓瀹曟帒饪伴崨顕呮綋闂傚倸鍊风欢姘缚瑜庨〃銉ㄧ疀閺囩偟绛忛梺鍛婃寙閸曨偄骞戦梻浣虹帛閸旓箓宕滈敃鈧埢鎾绘偋閸稐绨婚棅顐㈡处閹稿宕抽搹鍦=鐎广儱妫楅悘鎾煛鐏炵偓绀嬬€规洖宕灒闁惧繐婀遍幊鏍磽閸屾瑨鍏岀紒顕呭灣閹广垽宕掗悜鍥╃◤濠电娀娼ч鎰板极閸ヮ剚鐓熸俊顖濐嚙缁茶崵绱掗悩闈涗槐婵﹥妞介幊锟犲Χ閸涱喚鈧墽绱撴笟鍥ф灈闁活厼鍊垮缁樼節閸ャ劍娅滄繝銏f硾璋╅柕澶嗘櫆閻撴洟鏌熸导瀛樻锭闁哄绋撻埀顒傛嚀閹诧紕鎹㈤崼銉ヨ摕闁斥晛鍟欢鐐烘倵閿濆簼绨藉ù鐘层偢濮婃椽骞愭惔锝傚缂備緡鍠楅幐鎼侊綖韫囨拋娲敂閸滀焦顥堟繝鐢靛仦閻n亪宕濆畝鈧槐鐐寸節閸屾粍娈鹃梺鍝勬川閸嬫劙寮告惔銊︾厵闁诡垎鍜冪礊闂佹椿鍋勭€氭澘顫忓ú顏勭闁圭粯甯婄花浠嬫⒑閸濄儱校闁告梹娲熼崺銏狀吋閸涱亜鐗氶梺鍓插亞閸熷潡骞忓ú顏呪拺闁告稑锕﹂埥澶愭煥閺囶亞鎮兼繛鍡愬灲閺屽棗顓奸崱娆忓箞婵犵妲呴崹鏉匡耿闁秵鍎楁繛鍡樻尰閻撴瑦銇勯弮鈧弸濠氭嚀鐠恒劉鍋撳▓鍨灍闁瑰憡濞婇獮鍐煛閸涱喖浠虹紒鐐緲椤﹂亶姊婚鐐粹拻闁稿本鐟ㄩ崗宀勫几椤忓牊鐓涢柛顐亜婢ь喗銇勯锝囩疄濠碘剝鎮傞弫鍌炲箚瑜夐崣鐐烘⒒閸屾艾鈧悂宕愰悜鑺ュ殑闁告挷绀侀崹婵囥亜閺嶎偄浜奸柍褜鍓欓崯鏉戠暦閸楃偐妲堥柡宥冨€曟禍楣冩煕閹伴潧鏋涢梺鍗炴喘閺屾洘寰勯崼婵嗗Б濡炪倖鏌ㄩˇ闈涱潖濞差亝顥堟繛鎴炴皑椤斿﹥绻濆▓鍨珮闁告瑥鍟锝夊Ω閿旂虎娴勯柣搴秵閸嬪嫰鍩€椤掑倹鏆柡灞诲妼閳规垿宕卞☉鎵佸亾濡も偓闇夋繝濠傛琚氭繛锝呮搐閿曨亪銆侀弴銏狀潊闁绘ǹ娅曢鍕⒒娴e摜鏋冩い顐㈩樀瀹曞綊宕稿Δ鈧粻鏍ㄧ箾閸℃ɑ灏紒鐙欏洦鐓欓悗鐢登瑰皬濠电儑缍嗛崳锝夊蓟閿濆棙鍎熼柕鍫濆缂嶅牆鈹戦悙棰濆殝缂佺姵鎸搁悾宄扳堪閸喎浜滄俊鐐差儏鐎涒晛鈻撻幆褉鏀介柣妯款嚋瀹搞儵鏌eΔ鈧Λ娑氬垝婵犳艾唯闁挎棁妗ㄧ花濠氭⒑閸濆嫬鈧悂鎮樺┑瀣厱闁哄啫鐗婇悡銉︾箾閹寸偟鎳呴柣顓炵灱缁辨帗娼忛妸锕€纾抽悗瑙勬礃鐢帡鍩㈡惔銊ョ闁圭⒈鍘搁崑鎾诲冀椤撶啿鎷洪梺纭呭亹閸嬫稒淇婇懖鈺冪=鐎广儱鎷戦煬顒勬煙椤旇宓嗘い銏″哺閸┾偓妞ゆ帒瀚畵渚€鏌涢妷顔煎闁稿顑夐弻娑㈩敃閻樿尙浠煎Δ鐘靛仜閻楁挸顫忛搹瑙勫珰闁圭粯甯掑В鎰磽閸屾氨孝婵☆偅绻傞悾鐑藉箣閿曗偓瀹告繃銇勯幘璺盒f繛鍫ョ畺閺岋綀绠涢弴鐐版埛闂佺ǹ顑嗛幑鍥х暦閿濆牏鐤€闁圭虎鍨遍弬鈧梻浣虹帛钃辩憸鏉垮暣椤㈡棃顢曢敂钘変缓濡炪倖鐗楃粙鎾趁洪幘顔界厸鐎光偓閳ь剟宕版惔銊﹀仼闁跨喓濮甸崑瀣煕椤愶絿绠栭柣锝咁煼閺岋絾鎯旈妶搴㈢秷濠电偞褰冪换妯虹暦濠靛棭鍚嬮柛銉e妼鎼村﹤鈹戦悩缁樻锭妞ゆ垵鎳愮划鍫ュ礃椤旂晫鍘繝鐢靛仜閻忔繈宕濆顓滀簻闁靛绠戠粭姘辩磼缂佹ḿ绠為柟顔荤矙濡啫霉闊彃鍔﹂柡灞稿墲閹峰懐鎲撮崟顐熷亾閹邦喒鍋撶憴鍕闁搞劎鏁婚崺銉﹀緞閹邦剦娼婇梺鐐藉劚閸熸寧绔熺€n亖鏀介柣鎰摠缂嶆垿鏌涘顒夊剰瀹€锝呯仢閳诲酣骞嬮悩鐢靛姸濠电姰鍨煎▔娑欏緞閸ヮ剙纾婚柟鎹愬吹瀹撲線鏌涢…鎴濇灈濠殿喖楠搁—鍐Χ韫囨挾妲i梺鎼炲妼绾绢參宕氶幒鎾剁瘈婵﹩鍘奸埀顒傚厴閺岋綁骞嬮悙銊х窗闂佸憡锕╂禍婵堟崲濠靛鍋ㄩ梻鍫熺◥閹寸兘姊虹粙娆惧剱闁瑰憡鎮傞崺銏狀吋婢跺﹤鑰垮┑鐐村灦閻熝囧储鏉堛劎绡€闁汇垽娼у瓭闂佺ǹ顑呭Λ婵嬪箖閳╁啰闄勯柛娑橈功閸樻悂鏌h箛鏇炰哗妞ゆ泦鍥х劦妞ゆ帊鑳剁粻鐐烘煟濞戝崬鏋熺紒妤冨枛閸┾偓妞ゆ帒瀚畵渚€鏌熼悜姗嗘當缂佺媴绲剧换婵嬫濞戞瑱绱炲┑鐐插悑閻╊垰顫忔繝姘<婵炲棙鍩堝Σ顕€姊虹涵鍜佸殝缂佺粯绻堥悰顕€骞囬弶澶哥炊闂侀潧锛忛崪浣剐︽繝鐢靛Х閺佸憡鎱ㄩ弶鎳ㄦ椽濡舵径瀣彅闂佺粯鏌ㄩ崥瀣偂閻斿吋鐓涢柛鎰╁妼閳ь剙鎽滈弫顕€宕滄担铏癸紲闂侀€炲苯澧寸€规洘甯¢幃娆戔偓鐢登归獮妯荤節閻㈤潧浠︽繛鍏肩懇椤㈡牠宕卞缁樼€洪梺绯曞墲宀h法绮绘ィ鍐╃厱妞ゆ劦鍋勬禍婊冾熆瑜嶉悺銊╁箞閵婏妇绡€闁告劏鏂傛禒銏ゆ倵鐟欏嫭纾搁柛鏂跨Ф閹广垹鈹戠€n亞顦ㄥ銈呯箰鐎氼剙效閼碱剛纾介柛灞捐壘閳ь剟顥撶划鍫熺瑹閳ь剝妫熷銈嗙墬缁海绮堟繝鍌楁斀闁绘ê寮跺婵堚偓瑙勬尫缁舵岸寮诲☉銏犵疀闂傚牊绋掗悘宥夋⒑閸濆嫭鍣洪柟顔煎€垮濠氭晲閸涘倻鍠栧畷顐﹀礋椤掍胶妲繝鐢靛仜閻°劎鍒掔仦鏂よ€块弶鍫氭櫆椤洟鏌熼悜姗嗘當缂佲偓閸垺鍠愮€广儱顦埀顒€鍊圭缓浠嬪川婵犲嫬寮虫繝娈垮枟閿曗晠宕曢鍫熷仭闁归潧鍟块悧姘舵⒑閸撴彃浜栭柛銊ヮ煼瀵娊顢曢敂瑙f嫼闁荤姴娲犻埀顒冩珪閻忓牓姊洪幖鐐茬仾闁绘搫绻濆畷娲閳╁啫鍔呴梺闈涚墕濞层劑寮堕幖浣光拺闁荤喐澹嗘禒銏ゆ煕閻斿弶娅婇柟顖楀亾濡炪倕绻愬Λ娑氬娴犲鐓曢悘鐐插⒔閹冲棙銇勯弬娆炬█闁哄本绋撻埀顒婄秵閸嬪懎鐣峰畝鍕厸閻忕偟鏅暩濡炪伇鍌滅獢闁哄本鐩獮妯尖偓闈涙啞閸d即姊虹化鏇熸珖闁稿鍊濋悰顔锯偓锝庡枟閺呮粓鏌﹀Ο渚Т闁稿鎹囬幃婊堟嚍閵壯冨箻缂備胶鍋撳妯虹暦椤掍焦娅犳い鏍仦閻撴洟鏌¢崶銉ョ伄闁伙絿鍎ら幈銊︾節閸涱噮浠╃紓渚囧枟閻熲晛鐣烽悩璇茬労闁告劏鏅滃В搴ㄦ⒒閸屾瑨鍏岀紒顕呭灦閵嗗啴宕卞▎蹇撶亰闁瑰吋鐣崝宀€绮堥崱娑欑厵闁绘垶蓱閻撴盯鏌涚€n偅宕岄柡浣瑰姈閹棃鍩勯崘顏冮偗缂傚倸鍊烽懗鑸垫叏閹€鏋嶉柡鍥╁枔閳瑰秴鈹戦悩鍙夋悙閸ユ挳姊洪崨濠冨闁告ê鍚嬫穱濠囨寠婢跺棙鏂€闂佺粯鍔曞鍫曞闯鐟欏嫪绻嗘い鎰剁悼缁犳挻銇勯銏㈢閻撱倖銇勮箛鎾愁仼缂佹劖绋掔换婵嬫偨闂堟刀銏ゆ煕閻曚礁浜伴柟顖欑窔閹粓鎳為妷銏″闂備礁鎲$粙鎴︽晝閿曞倹鍎楀┑鐘叉处閻撴洟鏌i弬鎸庢儓妞わ絽銈搁弻鐔碱敍濞戞瑢鎷圭紓浣虹帛缁诲牆鐣峰鈧、鏃堝幢濞嗘劦娼撻梻鍌氬€烽悞锕傛儑瑜版帒鍨傞柦妯侯槳缂傛氨鎲告惔锝囩焿闁圭儤顨呴悡娑㈡煕濞戝崬鏋ら柛姗€娼ч埞鎴︽倷鐠洪缚鏁垮銈嗘煥閿曪箓鎳為柆宥嗗仼閻忕偟枪娴滈箖鏌涢…鎴濅簼缂佽埖鐓¢弻銊╁即濡搫濮㈢紓渚囧枛椤戝鐛幒妤€妫橀柛婵嗗婢规洟姊洪幐搴g畵缂併劏鍋愰懞閬嶆嚍閵夛絼绨婚梺鍝勫暊閸嬫捇鏌涢妸褎鏆柛鈺冨仱楠炲鏁傞挊澶夋睏闂佽崵濮村▔褔宕樿閻姊婚崒娆掑厡缂侇噮鍨堕妴鍐川椤撳洦绋戦埥澶婎潩椤掆偓閻忓﹪鏌i悩鍙夌┛妞ゃ儱妫楃叅妞ゅ繐绉甸弲婊堟⒑閸涘﹣绶遍柛銊ゅ嵆閻涱喖螖娴h櫣鐦堢紒鍓у钃辨い顐躬閺屾盯濡歌閺嗩剛鈧娲橀崹鍧楃嵁閸ヮ剦鏁婇柤鎭掑劜椤斿洦绻濋悽闈涗沪闁割煈鍨跺畷鐟懊洪鍛簵闂佺粯鏌ㄩ崥瀣偂濞嗘挻鐓欐い鏍ф閼活垰鈻撻崼鏇熲拺闁荤喐婢橀弳閬嶆倵濮橆偄宓嗙€殿喖顭峰鎾閻橀潧鈧偤鎮峰⿰鍐фい銏℃椤㈡﹢鎮╅顫濠电偛鐗嗛悘婵嬪几濞嗘垹纾兼い鏃傛櫕閹冲嫬菐閸パ嶅伐妞ゎ偁鍨归悾婵囩節閸愬啨鍎遍埞鎴︽偐閹颁礁鏅遍梺鍝ュУ閻楁洜鍙呴梺闈涚墕椤︻偊鍩€椤掍焦顥堢€规洘锕㈤、娆撳床婢诡垰娲﹂悡鏇㈡煙閹佃櫕娅呭┑锛勫帶閳规垿顢欐總绋垮及濠殿喖锕ㄥ▍锝囨閹烘埈娼ㄩ柛鈩冡缚閺嗭箓姊绘担鍛婅础闁硅櫕鎸哥叅闁靛牆顦介弫瀣煥濠靛棙顥犵紒鈾€鍋撴繝娈垮枟閿曗晠宕滃☉銏犵闁圭虎鍠楅埛鎴︽煕濞戞﹫宸ュ┑顔瑰亾闂備礁鎼幊蹇涙儎椤栫偑鈧線骞樼拠鑼啋缂傚倷鐒﹀玻鍧楀储娴犲鈷戠紓浣股戦悡銉╂煙閼恒儳鐭掓鐐诧躬瀹曟﹢顢欓挊澶嗗亾閸偅鍙忔俊顖滃帶鐢泛顭胯濠㈡﹢鈥︾捄銊﹀枂闁告洦鍓涢ˇ鏉课旈悩闈涗粶闂佸府缍侀獮濠囨倷閸濆嫀銊╂煏韫囧ň鍋撻幇浣风椽闂傚倸鍊风粈渚€骞栭位鍥焼瀹ュ懐锛涢梺缁樺姇椤曨參鎮甸崼鏇熺厱闁斥晛鍟伴埥澶岀磼閳ь剚寰勭仦绋夸壕妤犵偛鐏濋崝姘亜閿斿灝宓嗛柟顔光偓鏂ユ瀻闁规儳顕崢浠嬫⒑缂佹ɑ鐓ラ柟纰卞亰閵嗗倹绺介崨濠勫幈闂佺粯岣跨换鈧紓鍌涘哺閺屽秷顧侀柛鎾村哺椤㈡瑩寮介鐐烘7濡炪倖娲嶉崑鎾垛偓瑙勬礃閸ㄥ墎鎹㈠┑瀣倞闁宠桨鑳堕妶锔界節绾版ɑ顫婇柛銊ф暬瀹曟垿骞囬纰辨闂佺ǹ绻樺Λ璺ㄦ崲閸℃ǜ浜滈柡宥冨妿閻矂鎮介娑氣姇闁靛洤瀚粻娑㈠即閻愬浜繝娈垮枛閿曪妇鍒掗鐐茬闁告稑鐡ㄩ崵宥夋煏婢诡垯璁查崑鎾寸節閸ャ劉鎷洪梻鍌氱墐閺呮繄绮旈崜浣虹<闁绘ǹ娅曞畷宀勬煟濞戝崬鏋︾紒鐘崇☉閳藉鈻庨幇顓т户闂傚倷娴囧▔鏇㈠闯閿曞倸绠柨鐕傛嫹-婵犵數濮烽弫鍛婃叏閻戣棄鏋侀柛娑橈攻閸欏繘鏌i幋锝嗩棄闁哄绶氶弻娑樷槈濮楀牊鏁鹃梺鍛婄懃缁绘﹢寮婚敐澶婄闁挎繂妫Λ鍕⒑閸濆嫷鍎庣紒鑸靛哺瀵鈽夊Ο閿嬵潔濠殿喗顨呴悧濠囧极妤e啯鈷戦柛娑橈功閹冲啰绱掔紒姗堣€跨€殿喖顭烽弫鎰緞婵犲嫷鍚呴梻浣瑰缁诲倸螞椤撶倣娑㈠礋椤栨稈鎷洪梺鍛婄箓鐎氱兘宕曟惔锝囩<闁兼悂娼ч崫铏光偓娈垮枛椤兘骞冮姀銈呯閻忓繑鐗楃€氫粙姊虹拠鏌ュ弰婵炰匠鍕彾濠电姴浼i敐澶樻晩闁告挆鍜冪床闂備胶绮崝锕傚礈濞嗘挸绀夐柕鍫濇缁犲墽鐥銏╂缂佲檧鍋撻柣搴㈩問閸犳牠鈥﹂悜钘夌畺闁靛繈鍨洪崑姗€鏌嶉妷銉ュ笭濠㈣娲熷鍝勑ч崶褏浼勫┑鐐叉噷閸庣敻骞冮悜钘夌妞ゆ棁濮ら崳褏绱撻崒姘偓鎼佸磹閹间礁纾圭€瑰嫭鍣磋ぐ鎺戠倞闁冲搫鍟伴ˇ鈺傜箾閺夋垵鎮戞繛鍏肩懅婢规洜鎲撮崟顓犵槇闂傚倸鐗婃笟妤呭磿韫囨稒鐓㈤柛鎰典簻閺嬫盯鏌$仦璇插鐎殿喗娼欒灃闁逞屽墯缁傚秵銈i崘鈺冨弰婵炴潙鍚嬮悷褔宕氭导瀛樼厪闁糕剝锚缁楁帗銇勯锝囩疄闁诡喒鍓濋幆鏃堟晲閸曨厽鏆板┑鐘茬棄閺夊簱鍋撻弽顬盯宕橀…鎴炵稁缂傚倷鐒﹁摫濠殿垱鎸抽弻娑樷槈濮楀牊鏁鹃梺绋垮閹告悂鍩為幋锕€鐓¢柛鈩冦仦缁ㄥジ姊洪崷顓€褰掑疮閸ф缍栭煫鍥ㄦ⒒椤╃兘鎮楅敐搴濈敖妞わ附婢橀—鍐Χ閸℃瑥顫у銈嗘礋娴滃爼寮崘顔肩<婵炴垶鑹鹃獮鍫ユ⒒娴e憡鎯堟繛灞傚灲瀹曟繂鐣濋崟顒€鈧爼鏌eΟ鍏兼毄缁炬儳銈搁弻锝呂熼崫鍕瘣闂佸磭绮ú鐔煎蓟閳ュ磭鏆嗛柍褜鍓熷畷浼村箻鐠囪尙鍔﹀銈嗗笂閼冲爼鍩婇弴鐐垫殕闁挎繂鐗婄涵鍓佺磼椤旂⒈鐓煎┑锛勫厴婵$兘宕橀妸褏楔闂佽鍠掗弲婵囩閿曞倸纾兼慨姗嗗亜閸ㄦ繂鈹戦悩鎰佸晱闁哥姵鐗犻弫鍐Χ婢跺﹦顔愬銈嗗姂閸婃洖顕i弻銉︹拺闁煎鍊曞瓭濠电偠顕滅粻鎺楀Φ閹版澘绀冩い蹇撴缁楀姊洪崨濠勭畵閻庢艾鍢查妴鎺撶節濮橆厾鍘梺鍓插亝缁诲倿寮冲▎蹇婃斀闁炽儳鍋ㄩ崑銏ゆ煛鐏炶濮傜€殿喗鎸虫俊鎼佸Χ閸モ晜鏅ㄥ┑锛勫亼閸婃牕煤閳哄啫绶ら柛褎顨呯粻顖炴煟濡姊块柛锔诲幐閸嬫捇鏁愭惔鈥茶埅濠电偛鍚嬪Λ鍐潖缂佹ḿ鐟归柍褜鍓欏玻鑳槾闁瑰箍鍨介獮鎺楀箻閺夋垵浼庨梻浣虹帛閸ㄧ厧螞閸曨厾鐭嗗鑸靛姈閻撴瑧绱撴担闈涚仼闁哄鍠栭弻宥夋煥鐎n亞浼岄梺鍝勬湰缁嬫垿鍩ユ径濠庢建闁割偅绻€缁憋絽鈹戦悩鎰佸晱闁哥噥鍋婂畷銊╊敍濠婃劗搴婇梻浣告惈椤︻垶鎮ч崟顖氱鐎广儱娲ㄩ惌鍡涙煕椤愩倕鏋嶇紒璇叉閺屾稑鈻庤箛锝喰︽繝娈垮枛缁夊爼鍩€椤掍緡鍟忛柛鐘崇☉閳绘柨鈽夐姀鐘靛幒闁瑰吋鐣崝宥夊磹闁垮浜滈柟鍝勬娴滈箖姊烘导娆撴缂侇喗鎸搁~蹇曠磼濡偐鎳濋梺閫炲苯澧畝锝堝劵椤﹀綊鏌熼銊ユ搐楠炪垺绻涢幋鐐ㄧ細闁挎稒鐟╁娲嚒閵堝懏鐎炬繝銏㈡嚀椤戝顕g粙娆惧悑濠㈣泛顑囬崢閬嶆⒑閺傘儲娅呴柛鐔跺嵆閸╁﹪寮撮姀锛勫幗闂佽宕樺▔娑㈠几濞戙垺鐓涚€光偓閳ь剟宕伴弽褏鏆︾憸鐗堝俯閺佸﹦鐥弶鍨秮缂佽鲸鍨圭槐鎾诲磼濞嗘帩鍞瑰┑锛勫珡閸パ咃紱闂佺懓澧界划顖炴偂閻旂厧绠规繛锝庡墮閻掓椽鏌涢悢椋庣闁哄本鐩幃鈺佺暦閸ャ劌鍨辨俊鐐€戦崹鐑樼┍濞差€洩銇愰幒鎾跺幈闂佸磭鎳撻悘婵嬪礉濠婂應鍋撻崹顐g凡閻庢矮鍗抽悰顕€宕堕澶嬫櫌婵犮垼娉涢鍥╃矓闁秵鈷掗柛灞剧懆閸忓瞼绱掗鍛仸闁轰礁鍟存慨鈧柣姗嗕簽缁变即鎮峰⿰鍐弰妤犵偛鐗撴俊鎼佸煛娓氣偓閸炲爼姊洪崫鍕窛闁哥喎娼¢獮蹇曠磼濡偐顔曢柡澶婄墕婢т粙宕氭导瀛樼厵閻犲泧鍛槇閻庤娲﹂崹鍫曞箖濞嗘挻鍊绘俊顖滃帶楠炲牓姊绘担鍛婃儓闁哥喓濞€瀹曟垿骞樼紒妯煎幗濠德板€曢崯顐㈢摥闂備椒绱徊鍧楀礂濡警鍤曢柟缁㈠枛椤懘鏌eΟ娲诲晱婵¤尙澧楃换婵嬫偨闂堟稐绮堕梺缁橆殔濡繈銆侀弽顓炲耿婵炲棙鍔栧▓浼存⒑鐠恒劌鏋斿┑顔芥尦瀵即濡烽埡鍌滃帗閻熸粍绮撳畷婊冾潩鐠轰綍锕傛煕閺囥劌鐏犵紒鐘冲▕閺岀喓鈧稒岣跨粻銉ッ归悩鑽ょ暫婵﹥妞介獮搴ㄦ嚍閵夛附娈搁梺姹囧焺閸ㄨ京鏁垾绛硅€垮〒姘e亾婵﹥妞介獮鎰償閿濆洨鏆ら梻浣烘嚀閸熻法鎹㈠Ο铏规殾妞ゆ牜鍋為崐鐑芥煟閹寸伝顏呯椤栫偞鈷戦悷娆忓缁舵彃顭胯濞村嘲顕h閸┾偓妞ゆ帒瀚埛鎴︽煕濠靛棗顏繝鈧幍顔剧<閻庯綆鍋勫ù顔筋殽閻愬弶顥㈢€殿噮鍓氶幆鏃堝箻閹碱厽缍屽┑鐘殿暯濡插懘宕规导鏉戝簥闁告瑥顦遍々鏌ユ煟閹伴潧澧扮紒鈾€鍋撻梻鍌氬€搁悧濠冪瑹濡ゅ懎纾块柟瀵稿Л閸嬫挾鎲撮崟顒€鐭紓浣藉煐瀹€绋款嚕婵犳碍鍋勯柛蹇氬亹閸旂兘姊洪幐搴㈢5闁稿鎹囬弻锛勨偓锝冨妼閳ь剚顨婇幆鈧い蹇撶墕缁犳氨鎲稿澶婄畺闁瑰瓨鍔叉惔銊ョ倞鐟滄繈鐓浣典簻闁靛骏绱曢埥澶愭煃閻熸澘鏆i柟顔界懇椤㈡鍩€椤掑嫭鍋熼弶鍫涘妿缁♀偓闂佹眹鍨藉ḿ褎绂掑⿰鍛亾濞堝灝鏋涢柣鏍с偢閻涱噣宕橀鑲╋紲濠殿喗锚閸氬绱炴惔鈾€鏀介柣鎰级閳绘洖霉濠婂嫮绠為挊鐔兼煕椤愩倕鏋旂紒鐘荤畺閺岀喓鈧數枪娴犫晛顭跨憴鍕嗘垿濡甸崟顖涙櫜闁告侗鍠楅崕鎾绘⒑鐎圭媭娼愰柛銊ユ健瀹曟椽濡烽埡浣歌€垮┑锛勫仜婢т粙宕欓崷顓犵=闁稿本鐟чˇ锔姐亜閹存繃顥㈡鐐村姈閵堬綁宕橀妸褜妲撮梻浣告贡閸庛倕顫忛懡銈咁棜闁稿繘妫跨换鍡樸亜閺嶃劎姘ㄩ悷娆忓椤╁弶绻濋棃娑卞剱闁抽攱鍨块弻娑樷槈濮楀牆浼愭繝娈垮枓閸嬫捇姊绘担鍛婃儓闁瑰啿绻掗幑銏ゅ醇濠靛牊娈鹃梺闈涚箞閸婃牠鎮為懖鈹惧亾楠炲灝鍔氭俊顐㈢焸楠炲繐煤椤忓應鎷洪梺鍛婄箓鐎氼剟鍩€椤掆偓閻栫厧鐣烽弴銏犵闁瑰搫妫欓悗娲⒑閸涘﹦鈽夐柣掳鍔戦幃锟犲即閻旇櫣顔曢梺绯曞墲閿氬┑顔兼搐閳规垿顢欓懖鈹絾銇勯妸锝呭姦闁诡喗鐟ラ蹇涱敊閻撳骸顥撻梻鍌欐祰椤曟牠宕伴幒妤€鐤炬繝濠傚暈缂傛岸鐓崶銊р槈闁绘挻绋戦湁闁挎繂娲ㄩ妴濠囨煙缁嬪灝顏紒缁樼箘閸犲﹥寰勫畝鈧敍鐔兼⒑缁嬫鍎愰柛銊ョ仢閻g兘骞囬弶鍨祮闂佺粯锚閸熸寧鎯旀繝鍥ㄢ拺閻熸瑥瀚ˉ瀣熆瑜庨〃濠傜暦閹寸姭鍋撻敐搴濈按闁衡偓娴犲鐓熸俊顖氭惈缁狙冾熆鐠哄搫顏柡灞剧〒閳ь剨缍嗘禍婊堝焵椤掆偓濞尖€愁嚕鐠囨祴妲堥柕蹇曞Х閻も偓闂備胶枪缁绘劙骞楀⿰鍫濈鐟滅増甯楅埛鎴︽煕濠靛嫬鍔氶弽锟犳⒑閸涘﹥鈷愰柣妤佺矒楠炴垿濮€閻橆偅鏂€闂佹悶鍎弲婵嬫儊閸儲鈷戠紒瀣濠€鎵磼椤旇偐鐒搁柕鍡楀€块幖褰掑捶椤撶媴绱冲┑鐐舵彧缁叉崘銇愰崘鈺冾洸濡わ絽鍟埛鎴︽煕閹炬潙绲诲ù婊呭仱閺屾盯鎮╅搹顐㈡殫缂備緡鍠氱划顖炲Χ閿濆绀冮柍鍝勫暙楠炲牓姊绘担瑙勭伇闁哄懏鐩畷銏°偅閸愮偓鏅滈梺鍓插亞閸犲酣鍩€椤掆偓閻栧ジ寮诲澶婁紶闁告洦鍓欏▍銈夋⒑缂佹ɑ灏甸柛鐘冲姍婵$敻宕熼姘鳖啋闁荤姾娅i崕銈夋倵妤e啯鍊甸悷娆忓缁€鈧梺娲诲幖閸婂灝顕f繝姘伋鐎规洖娲﹀▓鏇㈡⒑闁偛鑻晶瀵糕偓瑙勬磻閸楁娊鐛鈧幊婊冣枔閹稿海绋愰梻鍌欑濠€閬嶅磿閵堝鈧啴宕ㄦ潏鍓х◤闂佸憡绋戦悺銊╂偂閻旈晲绻嗘い鏍ㄧ箖椤忕娀鏌ㄥ☉妯夹ら柟鍙夋倐楠炲繒浠﹂悾灞绢嚄缂傚倷娴囨ご鎼佸箲閸パ呮殾闁圭儤鍩堝ḿ鈺傘亜閹达絾顥夊ù婊堢畺閺屾稑鈹戦崟顐㈠Б闂佹椿鍘介幑鍥蓟閿濆顫呴柣妯哄暱閺嗗牓姊虹粙娆惧剰妞ゆ垵顦靛濠氭晲閸涘倻鍠庨埢搴ㄥ箚瑜庨鍕⒒娴h姤顥夐柛鐔跺嵆瀹曚即寮介鐐舵憰闂佽法鍠撴慨鎾倷婵犲偆娓婚悗锝庝簼閹癸綁鏌ㄥ☉姘灈婵﹤鎼晥闁搞儜鈧崑鎾诲箛閺夎法锛涢梺鐟板⒔缁垶鍩涢幋锔藉仯闁搞儯鍔岀徊濠氭煕閵堝牅鍚紒杈ㄦ尭椤撳ジ宕ㄩ鍛紒缂傚倷绀侀崐鍝ョ矓閻熼偊鍤曞ù鐘差儛閺佸洭鏌i幇顕呮殰缂侀亶浜跺缁樻媴缁涘缍堥悗瑙勬礃閿曘垽銆佸鎰佹▌閻庤娲橀敃銏ゅ春閳ь剚銇勯幒鍡椾壕濡炪値浜滈崯瀛樹繆閸洖骞㈡俊顖滃劋濞堫偊姊绘担鍛靛綊顢栭崶顒€绐楅柡宓苯娈ㄩ梺鍝勫濞存艾螣閸曨偀鏀芥い鏃傘€嬮弨缁樹繆閻愯埖顥夐柣锝囧厴椤㈡洟鏁冮埀顒傜矆鐎n偁浜滈柡鍥╁仦閸f椽鏌﹂幋婵愭█婵﹦绮幏鍛村川闂堟稒璐¢柍褜鍓氱粙鍫ュ疾閻樿绠栭柨鐔哄У閺呮悂鏌eΟ鍨毢闁伙絾妞藉铏规崉閵娿儲鐏佹繝娈垮枟閹稿啿鐣烽敓鐘茬闁兼亽鍎抽崢浠嬫⒑閸濆嫬鏆欐繛璇х畵椤㈡棃鎮╅悙鎴掔盎闂佸搫鍟犻崑鎾寸箾閼碱剙鏋庢い顐㈢箰鐓ゆい蹇撴噹娴狀參姊虹憴鍕靛晱闁哥姵顨婇獮澶愭嚃閳哄啰锛濇繛杈剧悼閻℃棃宕靛▎鎾寸厱濠电姴鍊归崑銉︻殽閻愯宸ユ顏冨嵆瀹曢亶骞囬鍛綎闂傚倷绀佸﹢閬嶅磿閵堝绠板Δ锝呭暙閸屻劑鏌熼梻瀵稿妽闁绘挾鍠栭獮鏍箹椤撶偟浠梺鍛婂笚濠㈡﹢鈥﹂懗顖fЩ闂備礁搴滅紞渚€鐛崘鈹垮亝闁告劏鏅涙禒娲⒑閸涘﹦鈽夐柨鏇畵瀹曘垽骞栨担鍦幗闂婎偄娲﹀ú鏍ㄧ濠婂喚鐔嗙憸宀€鍒掑▎鎾虫槬闁靛绠戠欢鐐烘倵閿濆啫濡虹紒銊嚙椤啴濡堕崱妤€衼缂備浇灏▔鏇犲垝婵犳碍鍊烽柣鎴炨缚閸橀潧顪冮妶鍡樷拻闁硅櫕鎸婚弲鍫曞蓟閵夛妇鍘靛銈嗙墬缁嬫帡鎮¢妷鈺傜厓閻熸瑥瀚悘瀵糕偓瑙勬礀瀹曨剝鐏掗柣蹇撶箲閻楁洘绂嶆ィ鍐╃厱闁归偊鍘鹃妶鎾煛閳ь剚绂掔€n偆鍘藉┑鈽嗗灥椤曆勬櫠椤栫偞鐓曢柣鏃堫棑缁犲鏌$仦鍓ф创闁诡喒鏅涢悾鐑藉炊瑜夐幏浼存⒒娴h姤銆冪紒鈧笟鈧畷顖溾偓娑櫭肩换鍡涙煙闂傚顦﹂崬顖炴⒑闂堟盯鐛滅紒杈ㄦ礋閸┾偓妞ゆ帊鐒﹂妵婵囨叏婵犲啯銇濇鐐村姈閹棃鏁愰崶鈺傛濠碉紕鍋戦崐褏鈧潧鐭傚畷鐟扮暦閸パ冪亰婵犵數濮甸懝楣冨礃閳ь剙顪冮妶搴″幋闁逞屽墮绾绢厾绮旈搹鍏夊亾鐟欏嫭绀冩い銊ワ工閻e嘲螖閸涱喖娈愰梺鍐叉惈閸熺娀寮歌箛娑欌拻闁稿本鐟︾粊鐗堛亜閺囧棗鎳忓畷鏌ユ煙鐎电ǹ浠х紒鐘冲劤閳规垿鎮╅崣澶嬫倷闂佽棄鍟伴崰鎰崲濞戙垹绠i柣鎰暩閻撳倿姊哄Ч鍥р偓鎰板磻閹剧粯鈷掑ù锝呮啞鐠愶繝鏌涚€n偅灏畝锝呯仢閳诲氦绠涙繝鍐偓娲⒑閹稿海绠撻柟宄邦儏閵嗘帗绻濆顓犲帾闂佸壊鍋呯换鍌炲汲濞嗘挻鐓曢柡鍐e亾缂侇喖閰i崺鈧い鎺嗗亾闁告ɑ绮撳畷鎴﹀箻閸撲胶锛滈柣搴秵閸嬫帡宕曢妷锔剧闁稿繗鍋愭晶顏堟煃鐟欏嫬鐏撮柟顔规櫇閳ь剙婀辨慨鎾夊┑鍫㈢<闁绘劦鍓欓崝銈夋煕濮橆剦鍎戦柟骞垮灩閳藉濮€閻樿尪鈧灝鈹戦埥鍡楃仩闁圭⒈鍋婇敐鐐存償閵婏腹鎷洪梻鍌氱墛缁嬫挻鏅堕弮鍫熺厱婵°倓绀侀埢鏇燁殽閻愭彃鏆欓摶鏍煕閹般劍娅呴柡瀣€垮娲川婵犲啫顦╅梺鍛婃尰閻╊垵妫熷銈嗘尪閸ㄦ椽鍩涢幋锕€绾ч柣鎰版涧椤h偐绱掓担鍝勵暭闁靛洤瀚板鎾幢濡や礁顦╅梺绋款儌閺呯姴顫忓ú顏勫瀭妞ゆ洖鎳庨崜鏉款渻閵堝棙绀嬪ù婊冪埣瀵鍩勯崘銊х獮闁诲函缍嗘禍鐐寸婵傚憡鈷戞慨鐟版搐閳ь剚鍔欏畷鎴﹀箻閺傘儲鏂€闂佹寧绋戠€氼剚绂嶆總鍛婄厱濠电姴鍟版晶閬嶆煛娓氬洤娅嶆鐐村笒椤啫鈹戦崱妯烘灎闂佸搫鑻Λ妤咁敇婵傜ǹ宸濋柡澶庢硶閸樻挳姊婚崒姘偓鎼佸磹閹间焦鍋嬪┑鐘插閻瑩鏌涢鐘插姎缂備讲鏅涢湁闁绘ê妯婇崕鎰版煟閹惧啿鏆i柡宀嬬畱铻e〒姘煎灡鏁堟俊鐐€戦崕鑼垝閹捐钃熼柨婵嗙墢閻も偓闁诲函缍嗘禍婊勬叏閿曞倹鈷戦柛婵嗗濠€鎵磼鐎n偅宕岄柛鈹惧亾濡炪倖甯掗敃锔剧矓閻㈠憡鐓曢悗锝庝簻椤忣亪鏌熸笟鍨鐎垫澘瀚悾婵嬪焵椤掑倸顥氶柛蹇曨儠娴滄粓鏌¢崘銊︽悙濞存粎鎳撻…鑳槼缂佸鎸惧Σ鎰板箳閺冨倻锛滃┑鈽嗗灥閸嬫劙鎮块崟顖涘€甸悷娆忓缁€鍐偨椤栨稑绗╅柣蹇斿浮閹鎮烽弶娆句純濡炪倧缍囬梽鍕博閻旂厧鍗抽柕蹇婃閹锋椽姊洪棃鈺佺槣闁告ê銈稿畷婵堚偓锝庡枟閻撴洟鏌嶆潪鎷屽厡濠⒀勬礀閻f繈鏁愰崨顔间淮闂佺硶鏅换婵嗙暦閵娾晩鏁婇柟顖嗗啯杈堟繝鐢靛Х閺佸憡绻涢埀顒佺箾娴e啿鍚樺☉妯锋瀻闁圭偓濞婂Λ椋庣磽娴e壊鍎愭い鎴炵懇閹垽宕卞☉娆忎画濠电偛妫楃换鎰邦敂椤忓棛纾奸柍褜鍓涢埀顒婄秵閸嬪懘宕h箛鎾斀闁绘ɑ褰冮顐︽偨椤栨稓娲撮柡宀€鍠庨悾锟犳偋閸繃鐣婚柣搴ゎ潐濞插繘宕濆鍥ㄥ床婵犻潧顑呯粈鍐煏婵炲灝鍔氭い銉﹀浮濮婂宕掑顑藉亾閻戣姤鍊块柨鏇楀亾妞ゎ亜鍟村畷绋课旈埀顒傜矆閸喓绠鹃柛鈩兩戠亸顓㈠炊鐎靛摜纾藉ù锝呭閸庢挻绻涙径瀣鐎殿喗濞婇弫鍐焵椤掑嫭绠掗梻浣呵圭换鎰板触鐎n剛绀婇柟瀵稿Х绾惧ジ鏌eΟ鐑樷枙闁绘挸銈搁弻鐔碱敊閼测晝楔閻庤娲栭悥濂搞€侀弮鍫濈妞ゆ挾鍣ラ崵鍕⒒閸屾瑧顦﹂柟娴嬧偓婢勬盯骞嬮悩鍏哥瑝闂佺鎻懙褰掑焵椤掍焦顥堢€规洘锕㈤、娆撳床婢诡垰娲﹂悡鏇㈡煃閳轰礁鏋ゆ繛鍫燂耿閺岋綁鎮㈢粙鍨潚濠殿喖锕ュ浠嬪箖閳╁啯鍎熼柍鈺佸暞閻︼綁姊绘担铏瑰笡闁绘娲熸俊鍓佺矙鐠恒劍娈鹃梺缁樺灦宀h法寮ч埀顒勬⒑閹肩偛鍔€闁告劑鍔庨妶顕€姊婚崒娆戠獢婵炰匠鍕垫闊洦娲橀~鏇㈡煛閸ャ儱鐏╅柣顓燁殜閺屾盯鍩勯崘锔跨捕闂佽 鍋撻柤鎭掑劘娴滄粓鏌¢崘銊︾ォ婵炵》绱曢幉鎼佹偋閸繄鐟ㄩ梺鍝勫閸庣敻寮婚垾鎰佸悑閹肩补鈧磭顔戦梻浣呵归鍛村磹閸ф钃熼柨婵嗩槸缁秹鏌涢妷鎴濆€归惈蹇涙⒒娴e憡鍟為柣鐕傜畵楠炴垿宕堕鈧拑鐔哥箾閹存瑥鐏╅崬顖炴⒑閹稿海绠撻柟鍐插閹便劍鎯旈妸锔规嫼闂佸憡绋戦敃銉╂偂閻斿吋鐓曞┑鐘插枤濞堟ɑ淇婇崣澶婂妤犵偞甯″顒勫传閸曨亜顥氶梻浣瑰缁诲倹顨ラ幖浣哄祦闁哄稁鍘介悡鏇熸叏濮楀棗澧悹鎰剁磿缁辨帗娼忛妸銉х懖濠电偟鍘х换妯讳繆閹间礁唯鐟滄粓宕曞畝鈧槐鎾诲磼濞嗘劗銈版俊鐐存綑閹芥粓寮鈧獮鎺楀即閻樿精鍩呴梻鍌氬€风粈渚€宕ョ€n剛鐭堥柟缁㈠枛閻ょ偓绻濋棃娑卞剰婵懓寮堕妵鍕箛閳轰讲鍋撳Δ鍐棜濞寸姴顑嗛悡鏇㈡倶閻愭彃鈷旈柟鍐叉閺屾稖绠涢幘鍓佷紘缂備浇椴哥敮锟犮€佸璺哄窛妞ゆ挾濮抽崠鏍⒒娴g儤鍤€缂佺姴绉瑰畷褰掓寠婢跺本娈鹃梺缁樻尭缁ㄥ爼寮ㄦ禒瀣厱妞ゆ劑鍊曢弸鎴炪亜閺冣偓濞叉ḿ鎹㈠┑鍡忔灁闁割煈鍠楅悘宥夋⒑闂堟稒澶勯柣鈺婂灠閻g兘骞嬮敃鈧粻濠氭煛閸屾ê鍔滈柡鍌楀亾闂傚倷鐒﹂弸濂稿疾濞戙垹鐤ù鍏兼綑缁犳椽鏌涢幇銊︽澓濞存粍绮撻弻銊╁即濮樿京鐛㈤梺鍛婄箚濞咃絿妲愰幒鏃傜<婵☆垰鍚嬮崚娑㈡⒑鏉炴壆鍔嶉柛鏃€鐗犻獮鍡涘籍閸繄鍔撮梺鍛婂姦娴滄瑩骞夐悙顒傜瘈闁汇垽娼ч崜宕囩磼閼艰埖顥夐悡銈夋煏閸繍妲归柡鍛箖閵囧嫯绠涢幘璺侯暫缂備胶濮甸悧妤冩崲濞戙垹骞㈡俊顖滅帛閸庡酣姊烘潪鎵槮闁稿﹤娼″璇测槈閵忕姴宓嗗┑鈽嗗灠閹碱偊鈥栭崼鐔虹閻庢稒岣块惌鎺旂磼閻樺磭澧电€殿喖顭烽崹楣冨箛娴e憡鍊梺纭呭閹活亞寰婇悡骞兾旈埀顒勫煘閹达附鍊烽柛娆忣槴閺嬫瑦绻涚€涙ḿ鐭嬬紒顔芥崌楠炲啴鍨鹃弬銉︻潔闂侀潧楠忕槐鏇㈠储闁秵鈷戦悷娆忓缁舵煡鏌涘锝呬壕缂傚倷闄嶉崝蹇旀叏閵堝桅闁告洦鍨遍弲婊堟偣閸ヮ亜鐨哄ù鐙€鍘剧槐鎾存媴閾忕懓绗¢梺鐑╂櫓閸ㄥ爼鎮伴纰辨建闁逞屽墮椤曪綁宕奸弴鐐殿吅闂佺粯蓱瑜板啳鈪归梻鍌氬€搁崐鐑芥嚄閼哥數浠氭俊鐐€栭崹闈浳涘┑瀣祦闁归偊鍘归崑鍛存煕閹扳晛濡块柛鏃撶畱椤啴濡堕崱妤冪懆闂佸摜濮甸懝鎯х幓閸ф绠涙い鎾跺Х椤旀洟姊洪崨濠勬噧妞ゃ儯鍨介、鏃堝醇濮橈絽浜鹃柡鍐ㄧ墕缁€鍐煃閸濆嫬鏋ゆ繛鏉戝閺岋絾鎯旈婊呅f繛瀛樼矋缁诲倸宓勫銈嗗笒鐎氼參鍩涢幋锔解拺妞ゆ劑鍊曟禒婊堟煠濞茶鐏¢柡鍛埣椤㈡盯鎮欑€电ǹ甯鹃梻浣规偠閸庢粓宕橀崣銉х>濠德板€楁慨鐑藉磻閻愬灚鏆滈柟鐑橆殢閺佸洭鏌涜箛鏇炲付缂佸墎鍋ら幃妤呮晲閸ヨ埖姣岄梺绋款儐閹瑰洤顕f禒瀣╃憸蹇涱敊閺囥垺鐓熼幖娣灮閳洖鐣濋敐鍛仴闁诡垰鐬奸埀顒婄秵閸撴稓澹曢崗绗轰簻闁哄啫娲よ閻庤娲栭惉濂稿焵椤掍緡鍟忛柛鐘崇墵閳ワ箓鎮滈挊澶岀暫闂侀潧绻堥崐鏇犵矆閸岀偞鐓熼柟鎯х-瀹€鎼佹煕鐎n偅灏电紒杈ㄥ笒铻i柛锔诲幘閻g偓淇婇悙顏勨偓鏍偋濡ゅ啯宕查柛鎰靛櫘閺佸倿鏌eΟ娆炬⒖鐟滅増甯楅崑鎰版煣韫囷絽浜滈柛鐐差槸閳规垿顢欑涵閿嬫暰濠碉紕鍋樼划娆忣嚕婵犳艾宸濋悗娑櫭埀顒傚厴閺屻倝鎳濋悧鍫€€愬銈呮禋閸樼晫鎹㈠┑瀣厱闁逞屽墰娴狅箓鎳為妷褍缍嗛梻鍌欑閹碱偊寮甸鍕剮妞ゆ牗绋掗崣蹇涙煃瑜滈崜鐔煎蓟閵娿儮妲堟俊顖欒娴犲ジ鎮楀▓鍨灁闁告梹鍨甸~蹇涙惞閻熸澘顕ч梺鍝勬川閸犳劕顭块幘缁樷拺闁硅偐鍋涙慨鈧┑鐐叉嫅缁插潡宕氶幒鏂哄亾閿濆骸鏋涚紒鐘冲▕閺岋繝宕掑顓熷創婵炲瓨绮撶粻鏍蓟閵娿儮鏀介柛鈩兠▍褎绻涚€电ǹ校闁烩晩鍨跺濠氭晸閻樻彃绐涘銈嗘煥婢т粙鎮℃径濞炬斀妞ゆ梻銆嬮弨缁樹繆閻愯埖顥夐柣锝呭槻楗即宕煎┑鍫斀闂備胶鎳撻幖顐ょ矓閸洖鏋侀柡宥庡幗閳锋帒霉閿濆懏鍟為柟鑼归埞鎴︻敊閻愵剚姣堝Δ鐘靛仦閸ㄥ灝鐣烽幆閭︽Ь闂佸搫妫寸粻鎾诲蓟閺囷紕鐤€閻庯綆浜栭崑鎾诲即閻樺吀绗夐梺鑽ゅ枑閸g銇愰幒鎾存珳闂佸憡渚楅崢鍏兼綇閸涘瓨鈷戠憸鐗堝笚閺佽鲸淇婇悙鑸殿棄妞ゎ偄绻橀幖鍦喆閸曨偄骞戦梻浣告啞娓氭宕㈤崫鍕懷兾旈崨顔规嫼缂備礁顑嗛娆撳磿閹扮増鐓熼柍鍝勶工閻忕娀鏌i敐鍛Щ闁宠鍨垮畷浼搭敊閼恒儺妫冮悗瑙勬磸閸旀垿銆佸▎鎾崇畾鐟滃秶绮绘导瀛樷拻闁稿本鐟чˇ锕傛煙濞村澧茬紒妤冨枎铻栭柛娑卞幘閻涖儱鈹戦鏂や緵闁稿寒浜幖褰掑礂婢跺﹣澹曞┑鐐村灦椤忣喖饪伴崟顓ф锤濠电姴锕ら悧濠囨偂韫囨稓鍙撻柛銉戝秴浼愭繝鈷€鍕弨闁诡喗枪缁犳稑鈽夊▎鎰版暘闂傚倸娲らˇ鐢稿蓟閿濆應鏋庨煫鍥ㄦ煥濞呇囨⒑娴兼瑧鎮奸柡浣规倐閸┾偓妞ゆ帒鍠氬ḿ鎰箾閸欏缂氶柛鎺撳笩缁犳稑霉閺夋寧宸濋柍褜鍓氱粙鎺曞綘婵炲瓨绮嶇划鎾诲蓟閿熺姴绀冮柨婵嗘噸婢规洘绻濋悽闈涗哗閻忓繑鐟╁畷鐗堟償椤帞绋忛棅顐㈡处閹峰煤椤忓秵鏅滈梺鍛婃处閸欏骸危椤栫偞鈷掑ù锝嚽归幃鎴犵磼娴h灏︾€殿噮鍓熷畷鎺楁倷閼碱剨绱遍梻浣虹帛閸旀宕曢妶澶婄厱闁硅揪闄勯悡鏇熺節闂堟稒顥滄い蹇d邯閺屾盯鏁愰崱妯镐虎闂佸搫鐭夌紞渚€宕洪埄鍐瘈闁稿本绮堝鎾绘煟鎼淬値娼愭繛鍙壝—鍐嚍閵夛箑寮块梺閫炲苯澧撮柡灞炬礋瀹曠厧鈹戦崶褎鐣婚梻浣告憸閸嬫盯鎮ラ悡搴綎婵炲樊浜濋ˉ鍫熺箾閹达綁鍝烘い搴℃缁绘繄鍠婂Ο宄颁壕闁惧浚鍋勯弸鐘绘倵鐟欏嫭纾搁柛銊ㄦ铻為柛鎰╁妷濡插牓寮堕崼娑樺闁伙附绮撳缁樼瑹閳ь剙岣胯閹囧幢濡炪垺绋戦埢搴ㄥ箻瀹曞洤骞堥梻浣告贡閸庛倝銆冮崱娑欏亗闁绘柨鍚嬮悡鍐煃鏉炴壆顦﹂柡鍡欏仱閺岋綁骞橀崡鐐插Е闂佸搫鑻粔鍓佹閹烘嚦鐔烘嫚閼碱剨绱﹂梺璇插椤旀牠宕抽鈧畷鎶芥晲閸涱垱娈炬繝闈涘€搁幉锟犲磻閸曨垱鐓曟繝闈涙椤忊晝绱掑Δ浣稿摵婵﹤顭峰畷鎺戔枎閹邦喓鍋樺┑鐘愁問閸犳捇宕愬┑瀣瀬閻庯綆浜跺〒濠氭煏閸繄绠抽柣锝堟珪娣囧﹪顢曢姀鐙€浼傞梺璇茬箲鐢€愁潖濞差亝鐒婚柣鎰蔼鐎氭澘顭胯閹告娊寮婚悢纰辨晩缂佹稑顑嗛悾濂告⒑閻熸澘绾ч柟绋垮暱閻g兘鎮㈢喊杈ㄦ櫌闂佺ǹ琚崐鏍叿闂傚倸鍊搁崐鐑芥倿閿旈敮鍋撶粭娑樻噹閺嬪牏鈧箍鍎遍ˇ顖涱攰闂備礁鎲″ú锕傚垂閺夎娑橆潨閳ь剟骞冭ぐ鎺戠畳闁圭儤鍨甸‖瀣渻閵堝棙鈷愰悽顖涘浮閳ユ棃宕橀鍢壯囨煕閹扳晛濡垮ù鐘荤畺濮婃椽鎳¢妶鍛瘣闂佸搫鎳愭繛鈧柣娑卞櫍楠炲洭顢橀悩鐢垫闂備礁鎲¢崝鎴﹀礉鎼达絿鐜婚柣鎰劋閻撶喖骞栭幖顓炵仯缂佸鏁婚弻娑滅疀閺冨倹鍒涘Δ鐘靛仜閸燁偊顢橀崗鐓庣窞閻庯急鍕伜闂傚倷鑳舵灙闁哄牜鍓熼幊婵囥偅閸愩劎鍔﹀銈嗗笂閻掞箓宕愰幇顔瑰亾鐟欏嫭绀冮柛鏃€鐟╅悰顕€寮介妸锕€顎撻梺鍛婄缚閸庤崵妲愰鈧缁樻媴閾忕懓绗¢梺鎼炲妼閸氬骞堥妸鈺佄у璺猴工閹偤姊洪崨濠冨闁搞劑浜堕幃锟犲即閵忥紕鍘甸梺纭咁潐閸旀洟鎯冮悜妯镐簻闁挎棁鍋愰悾鐢告煛鐏炲墽娲村┑鈩冩倐閺佸倿宕滆閺嗩偊姊绘笟鈧ḿ褍煤閵堝洠鍋撳顓熺凡妞ゆ洩绲剧粋鎺斺偓锝呯仛閺呮繂顪冮妶搴′航闁告ü绮欏畷鐔煎礃椤旇В鎷绘繛杈剧到閹虫瑨銇愰幒婵囨櫈闂佸憡绋掗幆宀勫极閸曨偒鐔嗛柤鎼佹涧婵洭鏌﹂崘顏勬灈闁哄被鍔岄埞鎴﹀幢閳哄倐锔剧磽娴e搫校缂佸甯℃俊鐢稿礋椤栨氨顔掗柣鐘烘濞插懘鎮欓悜妯煎幈闁诲函缍嗛崜娆愮鏉堛劍鍙忓┑鐘插暞閵囨繄鈧娲﹂崑濠傜暦閻斿吋顥堟繛鎴灻ˉ宥囩磽閸屾艾鈧绮堟笟鈧棟妞ゆ牗绮庣粈濠傗攽閻樻彃浜為柛銈嗘礀閳规垿鎮╃€圭姴顥濋柟顖滃枛濮婃椽妫冨☉杈ㄐら梺鎼炲妽濡炶棄顕i鍕劦妞ゆ帒瀚埛鎺懨归敐鍫燁仩闁靛棗锕弻娑㈠箻鐎靛摜鐣鹃梺鍦摂閸嬪﹤顫忛搹瑙勫珰闁炽儴娅曢悘宥夋⒑閼姐倕鏆遍柡鍛洴閿濈偠绠涢幘浣规そ椤㈡棃宕熼褍鏅i梻鍌欒兌缁垶宕濋弽顑句汗闁告劦鍠掗埀顒佺墬瀵板嫬鐣濋埀顒傚閽樺褰掓晲閸モ晜鎲橀梺鎼炲€栭悷鈺呭蓟濞戙垺鍋勯柛娑橈工閸炲姊虹紒妯圭繁闁革綇绲介悾閿嬬附缁嬭銊╂煏婢跺﹦宀搁柡鍛█瀵寮撮悢椋庣獮婵犵數濮撮崯顖氱暦閹惰姤鈷戦柛婵勫劚鏍¢梺缁橆殘婵炩偓闁诡喕鍗抽、姘跺焵椤掑嫮宓侀柛銉墻閺佸洭鏌i弬鍨Щ濠碘剝濞婂缁樻媴閻熼偊鍤嬬紓浣筋嚙閸婂灝鐣烽鐐村亹閻犲洩灏欓敍娑㈡⒑鐟欏嫬绀冩い鏇嗗懐涓嶆繛鎴炵懀娴滄粓鏌¢崒姘变虎闁抽攱妫冮弻銊モ槈濞嗘垹鐣虹紓浣虹帛缁嬫帒岣胯箛娑樼鐟滃繗鎽梺鑽ゅ枑缁秴顭垮鈧畷顖烆敍濠婂懐鐒块悗骞垮劚濡酣宕戦崨瀛樼厱闁硅埇鍔嶉弶褰掓煙闁垮銇濇慨濠冩そ瀹曘劍绻濋崘銊╃€洪柣鐔哥矋濠㈡﹢宕婊呯焿鐎广儱鎳夐弨浠嬫煕椤愮姴鐏柨娑欑矒濮婃椽宕ㄦ繝鍐ㄧ煯闂佺粯甯粻鎾诲箖閻愬搫閿ゆ俊銈勮兌閸橆亪姊洪幖鐐插姌闁告柨鏈幈銊ヮ吋閸♀晜顔旈梺缁樺姈濞兼瑥霉椤旂瓔娈介柣鎰缂傛岸鏌嶈閸撴氨绮欓幒鎴犲箵闁兼剚鍨禍褰掓煙闂傚鍔嶉柍閿嬪浮閺屾稓浠﹂崜褎鍣銈忚缁犳捇寮婚悢璁垮湱鈧綆浜滈埛澶岀磽娴h娈橀柛鐘叉唉閻忓啴姊洪崨濠佺繁闁告﹢绠栭幃浼村Ψ閵夈垺鏂€闂佺粯鍔栧ḿ娆撴倶閿斿墽妫柡澶庢硶鏁堥悗瑙勬礃椤ㄥ懘銈导鏉戦唶闁绘柨鎼敮妤呮煟閻斿摜鐭嬬紒顔芥尭閻e嘲饪伴崼鐔蜂簻婵犻潧鍊搁ˇ鎵礊鎼达絿纾介柛灞剧懅閸斿秹鎷戦崡鐐╂斀妞ゆ牗绋掔亸锕傛煛鐏炲墽鈽夐柍钘夘槸椤粓宕奸悢鍛婃瘞闂傚倷鑳舵灙閻庢稈鏅犻獮鎰板箹娴e摜鍘撮梺纭呮彧缁犳垿鎮¢敓鐘崇厱闁斥晛鍟ㄦ禒锔剧磼閵娿劌浜圭紒杈ㄦ尰閹峰懘宕滈幓鎺戝闂佹眹鍩勯崹鎶藉磻閵堝宓侀柟杈剧畱椤懘鏌e鍡椾簼妞ゎ偄绉瑰娲濞戞氨顔婃繝娈垮枤閸忔ê鐣峰┑瀣櫇闁逞屽墴閳ユ棃宕橀鍢壯囨煕閳╁喚娈橀柣鐔稿姍濮婅櫣绱掑Ο娲殝缂備胶濮甸幐鎼佹偩閻戣姤鏅查柛顐犲灮閺夋悂姊洪崷顓℃闁搞劑浜跺顒勫焵椤掑嫭鈷掑ù锝堟鐢盯鎷戞潏鈺傚枑闁哄鐏濋弳锝団偓娈垮枟婵炲﹪骞冨▎鎾村€绘俊顖滃帶鐢箖姊绘担瑙勫仩闁稿寒鍨跺畷婵囨償閿濆洣绗夐梺缁樺姉閸庛倝鎮″☉姘e亾閸忓浜鹃梺閫炲苯澧寸€规洑鍗冲浠嬵敇濠ф儳浜惧ù锝囩《閺嬪酣鏌熼幆褏锛嶉柣锝夌畺閹嘲饪伴崘顎囨煟濞戝崬鏋ら柍褜鍓ㄧ紞鍡涘焵椤掑骞楁俊顐㈠暣楠炲啴鍩¢崨顕呮濠电偞鍨堕〃鍫ュ箲閺囩姷纾介柛灞剧懅椤︼附銇勯敂璇茬仯缂佽京鍋炵换婵嬪炊椤兙鍎遍湁闁挎繂娲ㄩ妴濠囨煛鐎n亪鍙勯柡宀€鍠栭弻鍥晝閳ь剟寮搁妶澶嬬厽闁挎洍鍋撻柣妤€妫濋崺鐐哄箣閿旂粯鏅╅梺鍝勫€堕崐鎾舵閻㈠憡鈷戠紒瀣硶缁犺尙绱掔€n偅宕岀€规洘宀搁獮鎺懳旀担瑙勭彸濠电姰鍨煎▔娑㈩敄閸岀偛绠┑鐘崇閳锋垹绱掔€n偄顕滄繝鈧导瀛樼厾鐟滅増甯為悾娲煕閳规儳浜炬俊鐐€栫敮鎺楀磹閹间礁鍌ㄩ柟缁㈠枟閻撴瑩鏌ц箛锝呬航婵炲牊绮撻弻鐔兼惞椤愩倗鐓夐梺璇″枙缁瑥鐣峰Δ鍛紶闁靛濡囪棟濠电姷鏁告慨鐑姐€傞鐐潟闁哄洢鍨圭壕濠氭煙鏉堝墽鐣辩痪鎯х秺閺屸€愁吋鎼粹€崇闂佹悶鍔岄崐鍨潖婵犳艾閱囬柣鏂垮槻楠炲繐鈹戦悙鏉戠仸閼裤倝鏌¢埀顒佺鐎n偄鈧敻鏌ㄥ┑鍡涱€楀褜鍠氱槐鎺撶瑹婵犲嫮鏆ゅ┑顔硷龚濞咃絽鈽夐悽绋垮窛妞ゆ柨鍚嬮柨顓犵磽閸屾瑨鍏屽┑顔炬暬瀹曞綊宕稿Δ鈧粻鏍ㄧ箾閸℃ê濮夌紒鈾€鍋撻梻浣告啞閸斞呯磽濮樿精濮冲┑鐘崇閳锋垿鏌i悢鍝勵暭闁诡垰鐗婃穱濠囶敃閿濆孩鐣风紓浣稿€哥粔鐢稿Χ閿濆绀冮柍鍦亾鐎氬ジ姊绘担钘壭撻柨姘亜閿旇鐏︾€殿喗濞婇幃銏ゅ礂閼测晛骞堥梻浣虹帛閿氱痪缁㈠幗閺呭爼鎮界喊妯轰壕婵炲牆鐏濋弸娑欍亜椤撱垺鏁卞ǎ鍥э躬楠炴牗鎷呴崫銉ュ箰闂備胶枪閺堫剟鎯岄鎹愬С濠电姵纰嶉埛鎺懨归敐鍛暈闁哥喓鍋熺槐鎺旀嫚閹绘巻鍋撴繝姘劦妞ゆ帊娴囨竟姗€鏌熼搹顐嗘垿骞堥妸鈺佺劦妞ゆ帒瀚悡蹇涙煕椤愶絿绠栨い銉﹀灴閺岀喖鏌ㄧ€n偁浠㈠┑顔硷攻濡炶棄鐣烽妸锔剧瘈閹兼番鍨婚弳顓㈡⒒娴e懙褰掝敄閸ヮ剙纾婚柣鎰▕閸ゆ鏌涢弴銊ョ仩缂佲偓鐎n偁浜滈柡宥冨妿閵嗘帡鏌涘鍡曢偗婵﹥妞介獮鏍倷閹绘帒螚闂備礁鎲¢崝鏇°亹閻愬灚顫曢柡鍐e亾濞e洤锕俊鍫曞炊椤喓鍎甸弻娑氣偓锝庡墮娴犙囨煛娓氬洤娅嶆鐐村笒铻栧┑鐘插暞濞呭秴鈹戦悩缁樻锭闁稿﹦绮悘娆撴⒑缂佹ê濮囬柨鏇ㄤ邯瀵濡舵径濠傜獩婵犵數濮撮崯顖炴偟椤忓嫧鏀介柣妯款嚋瀹搞儵鎮楀闂寸敖闁瑰箍鍨藉畷鍗炩槈濞嗘垵骞楅梻浣筋潐濠㈡﹢宕ラ埀顒傜磼閵娿儺鐓奸柡灞界Х椤т線鏌涢幘纾嬪閻撱倖鎱ㄥ璇蹭壕闂侀潧妫楅崯瀛樹繆閻戣棄惟鐟滃繘寮剁粙搴撴斀闁绘劖娼欓悘锕€鐣濋敐鍛仴妞ゃ垺鐟╁畷鍗炩槈濞嗗本瀚奸梺鑽ゅУ娴滀粙宕濈仦瑙f瀺闁规壆澧楅悡娆撴煕閹存瑥鈧牜鈧熬鎷�>>
闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁绘劦鍓欓崝銈嗙節閳ь剟鏌嗗鍛姦濡炪倖甯掗崐褰掑吹閳ь剟鏌f惔銏犲毈闁告瑥鍟悾宄扮暦閸パ屾闁诲函绲婚崝瀣уΔ鍛拺闁革富鍘奸崝瀣煕閵娿儳绉虹€规洘鍔欓幃娆忣啅椤旇棄鐦滈梻渚€娼ч悧鍡椢涘Δ鍐當闁圭儤顨嗛悡銉╂煛閸ユ湹绨绘い鈺婂墰缁辨帡顢欓悾灞惧櫙缂備胶濮甸惄顖氼嚕椤曗偓瀹曟帒饪伴崨顕呮綋闂傚倸鍊风欢姘缚瑜庨〃銉ㄧ疀閺囩偟绛忛梺鍛婃寙閸曨偄骞戦梻浣虹帛閸旓箓宕滈敃鈧埢鎾绘偋閸稐绨婚棅顐㈡处閹稿宕抽搹鍦=鐎广儱妫楅悘鎾煛鐏炵偓绀嬬€规洖宕灒闁惧繐婀遍幊鏍磽閸屾瑨鍏岀紒顕呭灣閹广垽宕掗悜鍥╃◤濠电娀娼ч鎰板极閸ヮ剚鐓熸俊顖濐嚙缁茶崵绱掗悩闈涗槐婵﹥妞介幊锟犲Χ閸涱喚鈧墽绱撴笟鍥ф灈闁活厼鍊垮缁樼節閸ャ劍娅滄繝銏f硾璋╅柕澶嗘櫆閻撴洟鏌熸导瀛樻锭闁哄绋撻埀顒傛嚀閹诧紕鎹㈤崼銉ヨ摕闁斥晛鍟欢鐐烘倵閿濆簼绨藉ù鐘层偢濮婃椽骞愭惔锝傚缂備緡鍠楅幐鎼侊綖韫囨拋娲敂閸滀焦顥堟繝鐢靛仦閻n亪宕濆畝鈧槐鐐寸節閸屾粍娈鹃梺鍝勬川閸嬫劙寮告惔銊︾厵闁诡垎鍜冪礊闂佹椿鍋勭€氭澘顫忓ú顏勭闁圭粯甯婄花浠嬫⒑閸濄儱校闁告梹娲熼崺銏狀吋閸涱亜鐗氶梺鍓插亞閸熷潡骞忓ú顏呪拺闁告稑锕﹂埥澶愭煥閺囶亞鎮兼繛鍡愬灲閺屽棗顓奸崱娆忓箞婵犵妲呴崹鏉匡耿闁秵鍎楁繛鍡樻尰閻撴瑦銇勯弮鈧弸濠氭嚀鐠恒劉鍋撳▓鍨灍闁瑰憡濞婇獮鍐煛閸涱喖浠虹紒鐐緲椤﹂亶姊婚鐐粹拻闁稿本鐟ㄩ崗宀勫几椤忓牊鐓涢柛顐亜婢ь喗銇勯锝囩疄濠碘剝鎮傞弫鍌炲箚瑜夐崣鐐烘⒒閸屾艾鈧悂宕愰悜鑺ュ殑闁告挷绀侀崹婵囥亜閺嶎偄浜奸柍褜鍓欓崯鏉戠暦閸楃偐妲堥柡宥冨€曟禍楣冩煕閹伴潧鏋涢梺鍗炴喘閺屾洘寰勯崼婵嗗Б濡炪倖鏌ㄩˇ闈涱潖濞差亝顥堟繛鎴炴皑椤斿﹥绻濆▓鍨珮闁告瑥鍟锝夊Ω閿旂虎娴勯柣搴秵閸嬪嫰鍩€椤掑倹鏆柡灞诲妼閳规垿宕卞☉鎵佸亾濡も偓闇夋繝濠傛琚氭繛锝呮搐閿曨亪銆侀弴銏狀潊闁绘ǹ娅曢鍕⒒娴e摜鏋冩い顐㈩樀瀹曞綊宕稿Δ鈧粻鏍ㄧ箾閸℃ɑ灏紒鐙欏洦鐓欓悗鐢登瑰皬濠电儑缍嗛崳锝夊蓟閿濆棙鍎熼柕鍫濆缂嶅牆鈹戦悙棰濆殝缂佺姵鎸搁悾宄扳堪閸喎浜滄俊鐐差儏鐎涒晛鈻撻幆褉鏀介柣妯款嚋瀹搞儵鏌eΔ鈧Λ娑氬垝婵犳艾唯闁挎棁妗ㄧ花濠氭⒑閸濆嫬鈧悂鎮樺┑瀣厱闁哄啫鐗婇悡銉︾箾閹寸偟鎳呴柣顓炵灱缁辨帗娼忛妸锕€纾抽悗瑙勬礃鐢帡鍩㈡惔銊ョ闁圭⒈鍘搁崑鎾诲冀椤撶啿鎷洪梺纭呭亹閸嬫稒淇婇懖鈺冪=鐎广儱鎷戦煬顒勬煙椤旇宓嗘い銏″哺閸┾偓妞ゆ帒瀚畵渚€鏌涢妷顔煎闁稿顑夐弻娑㈩敃閻樿尙浠煎Δ鐘靛仜閻楁挸顫忛搹瑙勫珰闁圭粯甯掑В鎰磽閸屾氨孝婵☆偅绻傞悾鐑藉箣閿曗偓瀹告繃銇勯幘璺盒f繛鍫ョ畺閺岋綀绠涢弴鐐版埛闂佺ǹ顑嗛幑鍥х暦閿濆牏鐤€闁圭虎鍨遍弬鈧梻浣虹帛钃辩憸鏉垮暣椤㈡棃顢曢敂钘変缓濡炪倖鐗楃粙鎾趁洪幘顔界厸鐎光偓閳ь剟宕版惔銊﹀仼闁跨喓濮甸崑瀣煕椤愶絿绠栭柣锝咁煼閺岋絾鎯旈妶搴㈢秷濠电偞褰冪换妯虹暦濠靛棭鍚嬮柛銉e妼鎼村﹤鈹戦悩缁樻锭妞ゆ垵鎳愮划鍫ュ礃椤旂晫鍘繝鐢靛仜閻忔繈宕濆顓滀簻闁靛绠戠粭姘辩磼缂佹ḿ绠為柟顔荤矙濡啫霉闊彃鍔﹂柡灞稿墲閹峰懐鎲撮崟顐熷亾閹邦喒鍋撶憴鍕闁搞劎鏁婚崺銉﹀緞閹邦剦娼婇梺鐐藉劚閸熸寧绔熺€n亖鏀介柣鎰摠缂嶆垿鏌涘顒夊剰瀹€锝呯仢閳诲酣骞嬮悩鐢靛姸濠电姰鍨煎▔娑欏緞閸ヮ剙纾婚柟鎹愬吹瀹撲線鏌涢…鎴濇灈濠殿喖楠搁—鍐Χ韫囨挾妲i梺鎼炲妼绾绢參宕氶幒鎾剁瘈婵﹩鍘奸埀顒傚厴閺岋綁骞嬮悙銊х窗闂佸憡锕╂禍婵堟崲濠靛鍋ㄩ梻鍫熺◥閹寸兘姊虹粙娆惧剱闁瑰憡鎮傞崺銏狀吋婢跺﹤鑰垮┑鐐村灦閻熝囧储鏉堛劎绡€闁汇垽娼у瓭闂佺ǹ顑呭Λ婵嬪箖閳╁啰闄勯柛娑橈功閸樻悂鏌h箛鏇炰哗妞ゆ泦鍥х劦妞ゆ帊鑳剁粻鐐烘煟濞戝崬鏋熺紒妤冨枛閸┾偓妞ゆ帒瀚畵渚€鏌熼悜姗嗘當缂佺媴绲剧换婵嬫濞戞瑱绱炲┑鐐插悑閻╊垰顫忔繝姘<婵炲棙鍩堝Σ顕€姊虹涵鍜佸殝缂佺粯绻堥悰顕€骞囬弶澶哥炊闂侀潧锛忛崪浣剐︽繝鐢靛Х閺佸憡鎱ㄩ弶鎳ㄦ椽濡舵径瀣彅闂佺粯鏌ㄩ崥瀣偂閻斿吋鐓涢柛鎰╁妼閳ь剙鎽滈弫顕€宕滄担铏癸紲闂侀€炲苯澧寸€规洘甯¢幃娆戔偓鐢登归獮妯荤節閻㈤潧浠︽繛鍏肩懇椤㈡牠宕卞缁樼€洪梺绯曞墲宀h法绮绘ィ鍐╃厱妞ゆ劦鍋勬禍婊冾熆瑜嶉悺銊╁箞閵婏妇绡€闁告劏鏂傛禒銏ゆ倵鐟欏嫭纾搁柛鏂跨Ф閹广垹鈹戠€n亞顦ㄥ銈呯箰鐎氼剙效閼碱剛纾介柛灞捐壘閳ь剟顥撶划鍫熺瑹閳ь剝妫熷銈嗙墬缁海绮堟繝鍌楁斀闁绘ê寮跺婵堚偓瑙勬尫缁舵岸寮诲☉銏犵疀闂傚牊绋掗悘宥夋⒑閸濆嫭鍣洪柟顔煎€垮濠氭晲閸涘倻鍠栧畷顐﹀礋椤掍胶妲繝鐢靛仜閻°劎鍒掔仦鏂よ€块弶鍫氭櫆椤洟鏌熼悜姗嗘當缂佲偓閸垺鍠愮€广儱顦埀顒€鍊圭缓浠嬪川婵犲嫬寮虫繝娈垮枟閿曗晠宕曢鍫熷仭闁归潧鍟块悧姘舵⒑閸撴彃浜栭柛銊ヮ煼瀵娊顢曢敂瑙f嫼闁荤姴娲犻埀顒冩珪閻忓牓姊洪幖鐐茬仾闁绘搫绻濆畷娲閳╁啫鍔呴梺闈涚墕濞层劑寮堕幖浣光拺闁荤喐澹嗘禒銏ゆ煕閻斿弶娅婇柟顖楀亾濡炪倕绻愬Λ娑氬娴犲鐓曢悘鐐插⒔閹冲棙銇勯弬娆炬█闁哄本绋撻埀顒婄秵閸嬪懎鐣峰畝鍕厸閻忕偟鏅暩濡炪伇鍌滅獢闁哄本鐩獮妯尖偓闈涙啞閸d即姊虹化鏇熸珖闁稿鍊濋悰顔锯偓锝庡枟閺呮粓鏌﹀Ο渚Т闁稿鎹囬幃婊堟嚍閵壯冨箻缂備胶鍋撳妯虹暦椤掍焦娅犳い鏍仦閻撴洟鏌¢崶銉ョ伄闁伙絿鍎ら幈銊︾節閸涱噮浠╃紓渚囧枟閻熲晛鐣烽悩璇茬労闁告劏鏅滃В搴ㄦ⒒閸屾瑨鍏岀紒顕呭灦閵嗗啴宕卞▎蹇撶亰闁瑰吋鐣崝宀€绮堥崱娑欑厵闁绘垶蓱閻撴盯鏌涚€n偅宕岄柡浣瑰姈閹棃鍩勯崘顏冮偗缂傚倸鍊烽懗鑸垫叏閹€鏋嶉柡鍥╁枔閳瑰秴鈹戦悩鍙夋悙閸ユ挳姊洪崨濠冨闁告ê鍚嬫穱濠囨寠婢跺棙鏂€闂佺粯鍔曞鍫曞闯鐟欏嫪绻嗘い鎰剁悼缁犳挻銇勯銏㈢閻撱倖銇勮箛鎾愁仼缂佹劖绋掔换婵嬫偨闂堟刀銏ゆ煕閻曚礁浜伴柟顖欑窔閹粓鎳為妷銏″闂備礁鎲$粙鎴︽晝閿曞倹鍎楀┑鐘叉处閻撴洟鏌i弬鎸庢儓妞わ絽銈搁弻鐔碱敍濞戞瑢鎷圭紓浣虹帛缁诲牆鐣峰鈧、鏃堝幢濞嗘劦娼撻梻鍌氬€烽悞锕傛儑瑜版帒鍨傞柦妯侯槳缂傛氨鎲告惔锝囩焿闁圭儤顨呴悡娑㈡煕濞戝崬鏋ら柛姗€娼ч埞鎴︽倷鐠洪缚鏁垮銈嗘煥閿曪箓鎳為柆宥嗗仼閻忕偟枪娴滈箖鏌涢…鎴濅簼缂佽埖鐓¢弻銊╁即濡搫濮㈢紓渚囧枛椤戝鐛幒妤€妫橀柛婵嗗婢规洟姊洪幐搴g畵缂併劏鍋愰懞閬嶆嚍閵夛絼绨婚梺鍝勫暊閸嬫捇鏌涢妸褎鏆柛鈺冨仱楠炲鏁傞挊澶夋睏闂佽崵濮村▔褔宕樿閻姊婚崒娆掑厡缂侇噮鍨堕妴鍐川椤撳洦绋戦埥澶婎潩椤掆偓閻忓﹪鏌i悩鍙夌┛妞ゃ儱妫楃叅妞ゅ繐绉甸弲婊堟⒑閸涘﹣绶遍柛銊ゅ嵆閻涱喖螖娴h櫣鐦堢紒鍓у钃辨い顐躬閺屾盯濡歌閺嗩剛鈧娲橀崹鍧楃嵁閸ヮ剦鏁婇柤鎭掑劜椤斿洦绻濋悽闈涗沪闁割煈鍨跺畷鐟懊洪鍛簵闂佺粯鏌ㄩ崥瀣偂濞嗘挻鐓欐い鏍ф閼活垰鈻撻崼鏇熲拺闁荤喐婢橀弳閬嶆倵濮橆偄宓嗙€殿喖顭峰鎾閻橀潧鈧偤鎮峰⿰鍐фい銏℃椤㈡﹢鎮╅顫濠电偛鐗嗛悘婵嬪几濞嗘垹纾兼い鏃傛櫕閹冲嫬菐閸パ嶅伐妞ゎ偁鍨归悾婵囩節閸愬啨鍎遍埞鎴︽偐閹颁礁鏅遍梺鍝ュУ閻楁洜鍙呴梺闈涚墕椤︻偊鍩€椤掍焦顥堢€规洘锕㈤、娆撳床婢诡垰娲﹂悡鏇㈡煙閹佃櫕娅呭┑锛勫帶閳规垿顢欐總绋垮及濠殿喖锕ㄥ▍锝囨閹烘埈娼ㄩ柛鈩冡缚閺嗭箓姊绘担鍛婅础闁硅櫕鎸哥叅闁靛牆顦介弫瀣煥濠靛棙顥犵紒鈾€鍋撴繝娈垮枟閿曗晠宕滃☉銏犵闁圭虎鍠楅埛鎴︽煕濞戞﹫宸ュ┑顔瑰亾闂備礁鎼幊蹇涙儎椤栫偑鈧線骞樼拠鑼啋缂傚倷鐒﹀玻鍧楀储娴犲鈷戠紓浣股戦悡銉╂煙閼恒儳鐭掓鐐诧躬瀹曟﹢顢欓挊澶嗗亾閸偅鍙忔俊顖滃帶鐢泛顭胯濠㈡﹢鈥︾捄銊﹀枂闁告洦鍓涢ˇ鏉课旈悩闈涗粶闂佸府缍侀獮濠囨倷閸濆嫀銊╂煏韫囧ň鍋撻幇浣风椽闂傚倸鍊风粈渚€骞栭位鍥焼瀹ュ懐锛涢梺缁樺姇椤曨參鎮甸崼鏇熺厱闁斥晛鍟伴埥澶岀磼閳ь剚寰勭仦绋夸壕妤犵偛鐏濋崝姘亜閿斿灝宓嗛柟顔光偓鏂ユ瀻闁规儳顕崢浠嬫⒑缂佹ɑ鐓ラ柟纰卞亰閵嗗倹绺介崨濠勫幈闂佺粯岣跨换鈧紓鍌涘哺閺屽秷顧侀柛鎾村哺椤㈡瑩寮介鐐烘7濡炪倖娲嶉崑鎾垛偓瑙勬礃閸ㄥ墎鎹㈠┑瀣倞闁宠桨鑳堕妶锔界節绾版ɑ顫婇柛銊ф暬瀹曟垿骞囬纰辨闂佺ǹ绻樺Λ璺ㄦ崲閸℃ǜ浜滈柡宥冨妿閻矂鎮介娑氣姇闁靛洤瀚粻娑㈠即閻愬浜繝娈垮枛閿曪妇鍒掗鐐茬闁告稑鐡ㄩ崵宥夋煏婢诡垯璁查崑鎾寸節閸ャ劉鎷洪梻鍌氱墐閺呮繄绮旈崜浣虹<闁绘ǹ娅曞畷宀勬煟濞戝崬鏋︾紒鐘崇☉閳藉鈻庨幇顓т户闂傚倷娴囧▔鏇㈠闯閿曞倸绠柨鐕傛嫹-婵犵數濮烽弫鍛婃叏閻戣棄鏋侀柛娑橈攻閸欏繘鏌i幋锝嗩棄闁哄绶氶弻娑樷槈濮楀牊鏁鹃梺鍛婄懃缁绘﹢寮婚敐澶婄闁挎繂妫Λ鍕⒑閸濆嫷鍎庣紒鑸靛哺瀵鈽夊Ο閿嬵潔濠殿喗顨呴悧濠囧极妤e啯鈷戦柛娑橈功閹冲啰绱掔紒姗堣€跨€殿喖顭烽弫鎰緞婵犲嫷鍚呴梻浣瑰缁诲倸螞椤撶倣娑㈠礋椤栨稈鎷洪梺鍛婄箓鐎氱兘宕曟惔锝囩<闁兼悂娼ч崫铏光偓娈垮枛椤兘骞冮姀銈呯閻忓繑鐗楃€氫粙姊虹拠鏌ュ弰婵炰匠鍕彾濠电姴浼i敐澶樻晩闁告挆鍜冪床闂備胶绮崝锕傚礈濞嗘挸绀夐柕鍫濇缁犲墽鐥銏╂缂佲檧鍋撻柣搴㈩問閸犳牠鈥﹂悜钘夌畺闁靛繈鍨洪崑姗€鏌嶉妷銉ュ笭濠㈣娲熷鍝勑ч崶褏浼勫┑鐐叉噷閸庣敻骞冮悜钘夌妞ゆ棁濮ら崳褏绱撻崒姘偓鎼佸磹閹间礁纾圭€瑰嫭鍣磋ぐ鎺戠倞闁冲搫鍟伴ˇ鈺傜箾閺夋垵鎮戞繛鍏肩懅婢规洜鎲撮崟顓犵槇闂傚倸鐗婃笟妤呭磿韫囨稒鐓㈤柛鎰典簻閺嬫盯鏌$仦璇插鐎殿喗娼欒灃闁逞屽墯缁傚秵銈i崘鈺冨弰婵炴潙鍚嬮悷褔宕氭导瀛樼厪闁糕剝锚缁楁帗銇勯锝囩疄闁诡喒鍓濋幆鏃堟晲閸曨厽鏆板┑鐘茬棄閺夊簱鍋撻弽顬盯宕橀…鎴炵稁缂傚倷鐒﹁摫濠殿垱鎸抽弻娑樷槈濮楀牊鏁鹃梺绋垮閹告悂鍩為幋锕€鐓¢柛鈩冦仦缁ㄥジ姊洪崷顓€褰掑疮閸ф缍栭煫鍥ㄦ⒒椤╃兘鎮楅敐搴濈敖妞わ附婢橀—鍐Χ閸℃瑥顫у銈嗘礋娴滃爼寮崘顔肩<婵炴垶鑹鹃獮鍫ユ⒒娴e憡鎯堟繛灞傚灲瀹曟繂鐣濋崟顒€鈧爼鏌eΟ鍏兼毄缁炬儳銈搁弻锝呂熼崫鍕瘣闂佸磭绮ú鐔煎蓟閳ュ磭鏆嗛柍褜鍓熷畷浼村箻鐠囪尙鍔﹀銈嗗笂閼冲爼鍩婇弴鐐垫殕闁挎繂鐗婄涵鍓佺磼椤旂⒈鐓煎┑锛勫厴婵$兘宕橀妸褏楔闂佽鍠掗弲婵囩閿曞倸纾兼慨姗嗗亜閸ㄦ繂鈹戦悩鎰佸晱闁哥姵鐗犻弫鍐Χ婢跺﹦顔愬銈嗗姂閸婃洖顕i弻銉︹拺闁煎鍊曞瓭濠电偠顕滅粻鎺楀Φ閹版澘绀冩い蹇撴缁楀姊洪崨濠勭畵閻庢艾鍢查妴鎺撶節濮橆厾鍘梺鍓插亝缁诲倿寮冲▎蹇婃斀闁炽儳鍋ㄩ崑銏ゆ煛鐏炶濮傜€殿喗鎸虫俊鎼佸Χ閸モ晜鏅ㄥ┑锛勫亼閸婃牕煤閳哄啫绶ら柛褎顨呯粻顖炴煟濡姊块柛锔诲幐閸嬫捇鏁愭惔鈥茶埅濠电偛鍚嬪Λ鍐潖缂佹ḿ鐟归柍褜鍓欏玻鑳槾闁瑰箍鍨介獮鎺楀箻閺夋垵浼庨梻浣虹帛閸ㄧ厧螞閸曨厾鐭嗗鑸靛姈閻撴瑧绱撴担闈涚仼闁哄鍠栭弻宥夋煥鐎n亞浼岄梺鍝勬湰缁嬫垿鍩ユ径濠庢建闁割偅绻€缁憋絽鈹戦悩鎰佸晱闁哥噥鍋婂畷銊╊敍濠婃劗搴婇梻浣告惈椤︻垶鎮ч崟顖氱鐎广儱娲ㄩ惌鍡涙煕椤愩倕鏋嶇紒璇叉閺屾稑鈻庤箛锝喰︽繝娈垮枛缁夊爼鍩€椤掍緡鍟忛柛鐘崇☉閳绘柨鈽夐姀鐘靛幒闁瑰吋鐣崝宥夊磹闁垮浜滈柟鍝勬娴滈箖姊烘导娆撴缂侇喗鎸搁~蹇曠磼濡偐鎳濋梺閫炲苯澧畝锝堝劵椤﹀綊鏌熼銊ユ搐楠炪垺绻涢幋鐐ㄧ細闁挎稒鐟╁娲嚒閵堝懏鐎炬繝銏㈡嚀椤戝顕g粙娆惧悑濠㈣泛顑囬崢閬嶆⒑閺傘儲娅呴柛鐔跺嵆閸╁﹪寮撮姀锛勫幗闂佽宕樺▔娑㈠几濞戙垺鐓涚€光偓閳ь剟宕伴弽褏鏆︾憸鐗堝俯閺佸﹦鐥弶鍨秮缂佽鲸鍨圭槐鎾诲磼濞嗘帩鍞瑰┑锛勫珡閸パ咃紱闂佺懓澧界划顖炴偂閻旂厧绠规繛锝庡墮閻掓椽鏌涢悢椋庣闁哄本鐩幃鈺佺暦閸ャ劌鍨辨俊鐐€戦崹鐑樼┍濞差€洩銇愰幒鎾跺幈闂佸磭鎳撻悘婵嬪礉濠婂應鍋撻崹顐g凡閻庢矮鍗抽悰顕€宕堕澶嬫櫌婵犮垼娉涢鍥╃矓闁秵鈷掗柛灞剧懆閸忓瞼绱掗鍛仸闁轰礁鍟存慨鈧柣姗嗕簽缁变即鎮峰⿰鍐弰妤犵偛鐗撴俊鎼佸煛娓氣偓閸炲爼姊洪崫鍕窛闁哥喎娼¢獮蹇曠磼濡偐顔曢柡澶婄墕婢т粙宕氭导瀛樼厵閻犲泧鍛槇閻庤娲﹂崹鍫曞箖濞嗘挻鍊绘俊顖滃帶楠炲牓姊绘担鍛婃儓闁哥喓濞€瀹曟垿骞樼紒妯煎幗濠德板€曢崯顐㈢摥闂備椒绱徊鍧楀礂濡警鍤曢柟缁㈠枛椤懘鏌eΟ娲诲晱婵¤尙澧楃换婵嬫偨闂堟稐绮堕梺缁橆殔濡繈銆侀弽顓炲耿婵炲棙鍔栧▓浼存⒑鐠恒劌鏋斿┑顔芥尦瀵即濡烽埡鍌滃帗閻熸粍绮撳畷婊冾潩鐠轰綍锕傛煕閺囥劌鐏犵紒鐘冲▕閺岀喓鈧稒岣跨粻銉ッ归悩鑽ょ暫婵﹥妞介獮搴ㄦ嚍閵夛附娈搁梺姹囧焺閸ㄨ京鏁垾绛硅€垮〒姘e亾婵﹥妞介獮鎰償閿濆洨鏆ら梻浣烘嚀閸熻法鎹㈠Ο铏规殾妞ゆ牜鍋為崐鐑芥煟閹寸伝顏呯椤栫偞鈷戦悷娆忓缁舵彃顭胯濞村嘲顕h閸┾偓妞ゆ帒瀚埛鎴︽煕濠靛棗顏繝鈧幍顔剧<閻庯綆鍋勫ù顔筋殽閻愬弶顥㈢€殿噮鍓氶幆鏃堝箻閹碱厽缍屽┑鐘殿暯濡插懘宕规导鏉戝簥闁告瑥顦遍々鏌ユ煟閹伴潧澧扮紒鈾€鍋撻梻鍌氬€搁悧濠冪瑹濡ゅ懎纾块柟瀵稿Л閸嬫挾鎲撮崟顒€鐭紓浣藉煐瀹€绋款嚕婵犳碍鍋勯柛蹇氬亹閸旂兘姊洪幐搴㈢5闁稿鎹囬弻锛勨偓锝冨妼閳ь剚顨婇幆鈧い蹇撶墕缁犳氨鎲稿澶婄畺闁瑰瓨鍔叉惔銊ョ倞鐟滄繈鐓浣典簻闁靛骏绱曢埥澶愭煃閻熸澘鏆i柟顔界懇椤㈡鍩€椤掑嫭鍋熼弶鍫涘妿缁♀偓闂佹眹鍨藉ḿ褎绂掑⿰鍛亾濞堝灝鏋涢柣鏍с偢閻涱噣宕橀鑲╋紲濠殿喗锚閸氬绱炴惔鈾€鏀介柣鎰级閳绘洖霉濠婂嫮绠為挊鐔兼煕椤愩倕鏋旂紒鐘荤畺閺岀喓鈧數枪娴犫晛顭跨憴鍕嗘垿濡甸崟顖涙櫜闁告侗鍠楅崕鎾绘⒑鐎圭媭娼愰柛銊ユ健瀹曟椽濡烽埡浣歌€垮┑锛勫仜婢т粙宕欓崷顓犵=闁稿本鐟чˇ锔姐亜閹存繃顥㈡鐐村姈閵堬綁宕橀妸褜妲撮梻浣告贡閸庛倕顫忛懡銈咁棜闁稿繘妫跨换鍡樸亜閺嶃劎姘ㄩ悷娆忓椤╁弶绻濋棃娑卞剱闁抽攱鍨块弻娑樷槈濮楀牆浼愭繝娈垮枓閸嬫捇姊绘担鍛婃儓闁瑰啿绻掗幑銏ゅ醇濠靛牊娈鹃梺闈涚箞閸婃牠鎮為懖鈹惧亾楠炲灝鍔氭俊顐㈢焸楠炲繐煤椤忓應鎷洪梺鍛婄箓鐎氼剟鍩€椤掆偓閻栫厧鐣烽弴銏犵闁瑰搫妫欓悗娲⒑閸涘﹦鈽夐柣掳鍔戦幃锟犲即閻旇櫣顔曢梺绯曞墲閿氬┑顔兼搐閳规垿顢欓懖鈹絾銇勯妸锝呭姦闁诡喗鐟ラ蹇涱敊閻撳骸顥撻梻鍌欐祰椤曟牠宕伴幒妤€鐤炬繝濠傚暈缂傛岸鐓崶銊р槈闁绘挻绋戦湁闁挎繂娲ㄩ妴濠囨煙缁嬪灝顏紒缁樼箘閸犲﹥寰勫畝鈧敍鐔兼⒑缁嬫鍎愰柛銊ョ仢閻g兘骞囬弶鍨祮闂佺粯锚閸熸寧鎯旀繝鍥ㄢ拺閻熸瑥瀚ˉ瀣熆瑜庨〃濠傜暦閹寸姭鍋撻敐搴濈按闁衡偓娴犲鐓熸俊顖氭惈缁狙冾熆鐠哄搫顏柡灞剧〒閳ь剨缍嗘禍婊堝焵椤掆偓濞尖€愁嚕鐠囨祴妲堥柕蹇曞Х閻も偓闂備胶枪缁绘劙骞楀⿰鍫濈鐟滅増甯楅埛鎴︽煕濠靛嫬鍔氶弽锟犳⒑閸涘﹥鈷愰柣妤佺矒楠炴垿濮€閻橆偅鏂€闂佹悶鍎弲婵嬫儊閸儲鈷戠紒瀣濠€鎵磼椤旇偐鐒搁柕鍡楀€块幖褰掑捶椤撶媴绱冲┑鐐舵彧缁叉崘銇愰崘鈺冾洸濡わ絽鍟埛鎴︽煕閹炬潙绲诲ù婊呭仱閺屾盯鎮╅搹顐㈡殫缂備緡鍠氱划顖炲Χ閿濆绀冮柍鍝勫暙楠炲牓姊绘担瑙勭伇闁哄懏鐩畷銏°偅閸愮偓鏅滈梺鍓插亞閸犲酣鍩€椤掆偓閻栧ジ寮诲澶婁紶闁告洦鍓欏▍銈夋⒑缂佹ɑ灏甸柛鐘冲姍婵$敻宕熼姘鳖啋闁荤姾娅i崕銈夋倵妤e啯鍊甸悷娆忓缁€鈧梺娲诲幖閸婂灝顕f繝姘伋鐎规洖娲﹀▓鏇㈡⒑闁偛鑻晶瀵糕偓瑙勬磻閸楁娊鐛鈧幊婊冣枔閹稿海绋愰梻鍌欑濠€閬嶅磿閵堝鈧啴宕ㄦ潏鍓х◤闂佸憡绋戦悺銊╂偂閻旈晲绻嗘い鏍ㄧ箖椤忕娀鏌ㄥ☉妯夹ら柟鍙夋倐楠炲繒浠﹂悾灞绢嚄缂傚倷娴囨ご鎼佸箲閸パ呮殾闁圭儤鍩堝ḿ鈺傘亜閹达絾顥夊ù婊堢畺閺屾稑鈹戦崟顐㈠Б闂佹椿鍘介幑鍥蓟閿濆顫呴柣妯哄暱閺嗗牓姊虹粙娆惧剰妞ゆ垵顦靛濠氭晲閸涘倻鍠庨埢搴ㄥ箚瑜庨鍕⒒娴h姤顥夐柛鐔跺嵆瀹曚即寮介鐐舵憰闂佽法鍠撴慨鎾倷婵犲偆娓婚悗锝庝簼閹癸綁鏌ㄥ☉姘灈婵﹤鎼晥闁搞儜鈧崑鎾诲箛閺夎法锛涢梺鐟板⒔缁垶鍩涢幋锔藉仯闁搞儯鍔岀徊濠氭煕閵堝牅鍚紒杈ㄦ尭椤撳ジ宕ㄩ鍛紒缂傚倷绀侀崐鍝ョ矓閻熼偊鍤曞ù鐘差儛閺佸洭鏌i幇顕呮殰缂侀亶浜跺缁樻媴缁涘缍堥悗瑙勬礃閿曘垽銆佸鎰佹▌閻庤娲橀敃銏ゅ春閳ь剚銇勯幒鍡椾壕濡炪値浜滈崯瀛樹繆閸洖骞㈡俊顖滃劋濞堫偊姊绘担鍛靛綊顢栭崶顒€绐楅柡宓苯娈ㄩ梺鍝勫濞存艾螣閸曨偀鏀芥い鏃傘€嬮弨缁樹繆閻愯埖顥夐柣锝囧厴椤㈡洟鏁冮埀顒傜矆鐎n偁浜滈柡鍥╁仦閸f椽鏌﹂幋婵愭█婵﹦绮幏鍛村川闂堟稒璐¢柍褜鍓氱粙鍫ュ疾閻樿绠栭柨鐔哄У閺呮悂鏌eΟ鍨毢闁伙絾妞藉铏规崉閵娿儲鐏佹繝娈垮枟閹稿啿鐣烽敓鐘茬闁兼亽鍎抽崢浠嬫⒑閸濆嫬鏆欐繛璇х畵椤㈡棃鎮╅悙鎴掔盎闂佸搫鍟犻崑鎾寸箾閼碱剙鏋庢い顐㈢箰鐓ゆい蹇撴噹娴狀參姊虹憴鍕靛晱闁哥姵顨婇獮澶愭嚃閳哄啰锛濇繛杈剧悼閻℃棃宕靛▎鎾寸厱濠电姴鍊归崑銉︻殽閻愯宸ユ顏冨嵆瀹曢亶骞囬鍛綎闂傚倷绀佸﹢閬嶅磿閵堝绠板Δ锝呭暙閸屻劑鏌熼梻瀵稿妽闁绘挾鍠栭獮鏍箹椤撶偟浠梺鍛婂笚濠㈡﹢鈥﹂懗顖fЩ闂備礁搴滅紞渚€鐛崘鈹垮亝闁告劏鏅涙禒娲⒑閸涘﹦鈽夐柨鏇畵瀹曘垽骞栨担鍦幗闂婎偄娲﹀ú鏍ㄧ濠婂喚鐔嗙憸宀€鍒掑▎鎾虫槬闁靛绠戠欢鐐烘倵閿濆啫濡虹紒銊嚙椤啴濡堕崱妤€衼缂備浇灏▔鏇犲垝婵犳碍鍊烽柣鎴炨缚閸橀潧顪冮妶鍡樷拻闁硅櫕鎸婚弲鍫曞蓟閵夛妇鍘靛銈嗙墬缁嬫帡鎮¢妷鈺傜厓閻熸瑥瀚悘瀵糕偓瑙勬礀瀹曨剝鐏掗柣蹇撶箲閻楁洘绂嶆ィ鍐╃厱闁归偊鍘鹃妶鎾煛閳ь剚绂掔€n偆鍘藉┑鈽嗗灥椤曆勬櫠椤栫偞鐓曢柣鏃堫棑缁犲鏌$仦鍓ф创闁诡喒鏅涢悾鐑藉炊瑜夐幏浼存⒒娴h姤銆冪紒鈧笟鈧畷顖溾偓娑櫭肩换鍡涙煙闂傚顦﹂崬顖炴⒑闂堟盯鐛滅紒杈ㄦ礋閸┾偓妞ゆ帊鐒﹂妵婵囨叏婵犲啯銇濇鐐村姈閹棃鏁愰崶鈺傛濠碉紕鍋戦崐褏鈧潧鐭傚畷鐟扮暦閸パ冪亰婵犵數濮甸懝楣冨礃閳ь剙顪冮妶搴″幋闁逞屽墮绾绢厾绮旈搹鍏夊亾鐟欏嫭绀冩い銊ワ工閻e嘲螖閸涱喖娈愰梺鍐叉惈閸熺娀寮歌箛娑欌拻闁稿本鐟︾粊鐗堛亜閺囧棗鎳忓畷鏌ユ煙鐎电ǹ浠х紒鐘冲劤閳规垿鎮╅崣澶嬫倷闂佽棄鍟伴崰鎰崲濞戙垹绠i柣鎰暩閻撳倿姊哄Ч鍥р偓鎰板磻閹剧粯鈷掑ù锝呮啞鐠愶繝鏌涚€n偅灏畝锝呯仢閳诲氦绠涙繝鍐偓娲⒑閹稿海绠撻柟宄邦儏閵嗘帗绻濆顓犲帾闂佸壊鍋呯换鍌炲汲濞嗘挻鐓曢柡鍐e亾缂侇喖閰i崺鈧い鎺嗗亾闁告ɑ绮撳畷鎴﹀箻閸撲胶锛滈柣搴秵閸嬫帡宕曢妷锔剧闁稿繗鍋愭晶顏堟煃鐟欏嫬鐏撮柟顔规櫇閳ь剙婀辨慨鎾夊┑鍫㈢<闁绘劦鍓欓崝銈夋煕濮橆剦鍎戦柟骞垮灩閳藉濮€閻樿尪鈧灝鈹戦埥鍡楃仩闁圭⒈鍋婇敐鐐存償閵婏腹鎷洪梻鍌氱墛缁嬫挻鏅堕弮鍫熺厱婵°倓绀侀埢鏇燁殽閻愭彃鏆欓摶鏍煕閹般劍娅呴柡瀣€垮娲川婵犲啫顦╅梺鍛婃尰閻╊垵妫熷銈嗘尪閸ㄦ椽鍩涢幋锕€绾ч柣鎰版涧椤h偐绱掓担鍝勵暭闁靛洤瀚板鎾幢濡や礁顦╅梺绋款儌閺呯姴顫忓ú顏勫瀭妞ゆ洖鎳庨崜鏉款渻閵堝棙绀嬪ù婊冪埣瀵鍩勯崘銊х獮闁诲函缍嗘禍鐐寸婵傚憡鈷戞慨鐟版搐閳ь剚鍔欏畷鎴﹀箻閺傘儲鏂€闂佹寧绋戠€氼剚绂嶆總鍛婄厱濠电姴鍟版晶閬嶆煛娓氬洤娅嶆鐐村笒椤啫鈹戦崱妯烘灎闂佸搫鑻Λ妤咁敇婵傜ǹ宸濋柡澶庢硶閸樻挳姊婚崒姘偓鎼佸磹閹间焦鍋嬪┑鐘插閻瑩鏌涢鐘插姎缂備讲鏅涢湁闁绘ê妯婇崕鎰版煟閹惧啿鏆i柡宀嬬畱铻e〒姘煎灡鏁堟俊鐐€戦崕鑼垝閹捐钃熼柨婵嗙墢閻も偓闁诲函缍嗘禍婊勬叏閿曞倹鈷戦柛婵嗗濠€鎵磼鐎n偅宕岄柛鈹惧亾濡炪倖甯掗敃锔剧矓閻㈠憡鐓曢悗锝庝簻椤忣亪鏌熸笟鍨鐎垫澘瀚悾婵嬪焵椤掑倸顥氶柛蹇曨儠娴滄粓鏌¢崘銊︽悙濞存粎鎳撻…鑳槼缂佸鎸惧Σ鎰板箳閺冨倻锛滃┑鈽嗗灥閸嬫劙鎮块崟顖涘€甸悷娆忓缁€鍐偨椤栨稑绗╅柣蹇斿浮閹鎮烽弶娆句純濡炪倧缍囬梽鍕博閻旂厧鍗抽柕蹇婃閹锋椽姊洪棃鈺佺槣闁告ê銈稿畷婵堚偓锝庡枟閻撴洟鏌嶆潪鎷屽厡濠⒀勬礀閻f繈鏁愰崨顔间淮闂佺硶鏅换婵嗙暦閵娾晩鏁婇柟顖嗗啯杈堟繝鐢靛Х閺佸憡绻涢埀顒佺箾娴e啿鍚樺☉妯锋瀻闁圭偓濞婂Λ椋庣磽娴e壊鍎愭い鎴炵懇閹垽宕卞☉娆忎画濠电偛妫楃换鎰邦敂椤忓棛纾奸柍褜鍓涢埀顒婄秵閸嬪懘宕h箛鎾斀闁绘ɑ褰冮顐︽偨椤栨稓娲撮柡宀€鍠庨悾锟犳偋閸繃鐣婚柣搴ゎ潐濞插繘宕濆鍥ㄥ床婵犻潧顑呯粈鍐煏婵炲灝鍔氭い銉﹀浮濮婂宕掑顑藉亾閻戣姤鍊块柨鏇楀亾妞ゎ亜鍟村畷绋课旈埀顒傜矆閸喓绠鹃柛鈩兩戠亸顓㈠炊鐎靛摜纾藉ù锝呭閸庢挻绻涙径瀣鐎殿喗濞婇弫鍐焵椤掑嫭绠掗梻浣呵圭换鎰板触鐎n剛绀婇柟瀵稿Х绾惧ジ鏌eΟ鐑樷枙闁绘挸銈搁弻鐔碱敊閼测晝楔閻庤娲栭悥濂搞€侀弮鍫濈妞ゆ挾鍣ラ崵鍕⒒閸屾瑧顦﹂柟娴嬧偓婢勬盯骞嬮悩鍏哥瑝闂佺鎻懙褰掑焵椤掍焦顥堢€规洘锕㈤、娆撳床婢诡垰娲﹂悡鏇㈡煃閳轰礁鏋ゆ繛鍫燂耿閺岋綁鎮㈢粙鍨潚濠殿喖锕ュ浠嬪箖閳╁啯鍎熼柍鈺佸暞閻︼綁姊绘担铏瑰笡闁绘娲熸俊鍓佺矙鐠恒劍娈鹃梺缁樺灦宀h法寮ч埀顒勬⒑閹肩偛鍔€闁告劑鍔庨妶顕€姊婚崒娆戠獢婵炰匠鍕垫闊洦娲橀~鏇㈡煛閸ャ儱鐏╅柣顓燁殜閺屾盯鍩勯崘锔跨捕闂佽 鍋撻柤鎭掑劘娴滄粓鏌¢崘銊︾ォ婵炵》绱曢幉鎼佹偋閸繄鐟ㄩ梺鍝勫閸庣敻寮婚垾鎰佸悑閹肩补鈧磭顔戦梻浣呵归鍛村磹閸ф钃熼柨婵嗩槸缁秹鏌涢妷鎴濆€归惈蹇涙⒒娴e憡鍟為柣鐕傜畵楠炴垿宕堕鈧拑鐔哥箾閹存瑥鐏╅崬顖炴⒑閹稿海绠撻柟鍐插閹便劍鎯旈妸锔规嫼闂佸憡绋戦敃銉╂偂閻斿吋鐓曞┑鐘插枤濞堟ɑ淇婇崣澶婂妤犵偞甯″顒勫传閸曨亜顥氶梻浣瑰缁诲倹顨ラ幖浣哄祦闁哄稁鍘介悡鏇熸叏濮楀棗澧悹鎰剁磿缁辨帗娼忛妸銉х懖濠电偟鍘х换妯讳繆閹间礁唯鐟滄粓宕曞畝鈧槐鎾诲磼濞嗘劗銈版俊鐐存綑閹芥粓寮鈧獮鎺楀即閻樿精鍩呴梻鍌氬€风粈渚€宕ョ€n剛鐭堥柟缁㈠枛閻ょ偓绻濋棃娑卞剰婵懓寮堕妵鍕箛閳轰讲鍋撳Δ鍐棜濞寸姴顑嗛悡鏇㈡倶閻愭彃鈷旈柟鍐叉閺屾稖绠涢幘鍓佷紘缂備浇椴哥敮锟犮€佸璺哄窛妞ゆ挾濮抽崠鏍⒒娴g儤鍤€缂佺姴绉瑰畷褰掓寠婢跺本娈鹃梺缁樻尭缁ㄥ爼寮ㄦ禒瀣厱妞ゆ劑鍊曢弸鎴炪亜閺冣偓濞叉ḿ鎹㈠┑鍡忔灁闁割煈鍠楅悘宥夋⒑闂堟稒澶勯柣鈺婂灠閻g兘骞嬮敃鈧粻濠氭煛閸屾ê鍔滈柡鍌楀亾闂傚倷鐒﹂弸濂稿疾濞戙垹鐤ù鍏兼綑缁犳椽鏌涢幇銊︽澓濞存粍绮撻弻銊╁即濮樿京鐛㈤梺鍛婄箚濞咃絿妲愰幒鏃傜<婵☆垰鍚嬮崚娑㈡⒑鏉炴壆鍔嶉柛鏃€鐗犻獮鍡涘籍閸繄鍔撮梺鍛婂姦娴滄瑩骞夐悙顒傜瘈闁汇垽娼ч崜宕囩磼閼艰埖顥夐悡銈夋煏閸繍妲归柡鍛箖閵囧嫯绠涢幘璺侯暫缂備胶濮甸悧妤冩崲濞戙垹骞㈡俊顖滅帛閸庡酣姊烘潪鎵槮闁稿﹤娼″璇测槈閵忕姴宓嗗┑鈽嗗灠閹碱偊鈥栭崼鐔虹閻庢稒岣块惌鎺旂磼閻樺磭澧电€殿喖顭烽崹楣冨箛娴e憡鍊梺纭呭閹活亞寰婇悡骞兾旈埀顒勫煘閹达附鍊烽柛娆忣槴閺嬫瑦绻涚€涙ḿ鐭嬬紒顔芥崌楠炲啴鍨鹃弬銉︻潔闂侀潧楠忕槐鏇㈠储闁秵鈷戦悷娆忓缁舵煡鏌涘锝呬壕缂傚倷闄嶉崝蹇旀叏閵堝桅闁告洦鍨遍弲婊堟偣閸ヮ亜鐨哄ù鐙€鍘剧槐鎾存媴閾忕懓绗¢梺鐑╂櫓閸ㄥ爼鎮伴纰辨建闁逞屽墮椤曪綁宕奸弴鐐殿吅闂佺粯蓱瑜板啳鈪归梻鍌氬€搁崐鐑芥嚄閼哥數浠氭俊鐐€栭崹闈浳涘┑瀣祦闁归偊鍘归崑鍛存煕閹扳晛濡块柛鏃撶畱椤啴濡堕崱妤冪懆闂佸摜濮甸懝鎯х幓閸ф绠涙い鎾跺Х椤旀洟姊洪崨濠勬噧妞ゃ儯鍨介、鏃堝醇濮橈絽浜鹃柡鍐ㄧ墕缁€鍐煃閸濆嫬鏋ゆ繛鏉戝閺岋絾鎯旈婊呅f繛瀛樼矋缁诲倸宓勫銈嗗笒鐎氼參鍩涢幋锔解拺妞ゆ劑鍊曟禒婊堟煠濞茶鐏¢柡鍛埣椤㈡盯鎮欑€电ǹ甯鹃梻浣规偠閸庢粓宕橀崣銉х>濠德板€楁慨鐑藉磻閻愬灚鏆滈柟鐑橆殢閺佸洭鏌涜箛鏇炲付缂佸墎鍋ら幃妤呮晲閸ヨ埖姣岄梺绋款儐閹瑰洤顕f禒瀣╃憸蹇涱敊閺囥垺鐓熼幖娣灮閳洖鐣濋敐鍛仴闁诡垰鐬奸埀顒婄秵閸撴稓澹曢崗绗轰簻闁哄啫娲よ閻庤娲栭惉濂稿焵椤掍緡鍟忛柛鐘崇墵閳ワ箓鎮滈挊澶岀暫闂侀潧绻堥崐鏇犵矆閸岀偞鐓熼柟鎯х-瀹€鎼佹煕鐎n偅灏电紒杈ㄥ笒铻i柛锔诲幘閻g偓淇婇悙顏勨偓鏍偋濡ゅ啯宕查柛鎰靛櫘閺佸倿鏌eΟ娆炬⒖鐟滅増甯楅崑鎰版煣韫囷絽浜滈柛鐐差槸閳规垿顢欑涵閿嬫暰濠碉紕鍋樼划娆忣嚕婵犳艾宸濋悗娑櫭埀顒傚厴閺屻倝鎳濋悧鍫€€愬銈呮禋閸樼晫鎹㈠┑瀣厱闁逞屽墰娴狅箓鎳為妷褍缍嗛梻鍌欑閹碱偊寮甸鍕剮妞ゆ牗绋掗崣蹇涙煃瑜滈崜鐔煎蓟閵娿儮妲堟俊顖欒娴犲ジ鎮楀▓鍨灁闁告梹鍨甸~蹇涙惞閻熸澘顕ч梺鍝勬川閸犳劕顭块幘缁樷拺闁硅偐鍋涙慨鈧┑鐐叉嫅缁插潡宕氶幒鏂哄亾閿濆骸鏋涚紒鐘冲▕閺岋繝宕掑顓熷創婵炲瓨绮撶粻鏍蓟閵娿儮鏀介柛鈩兠▍褎绻涚€电ǹ校闁烩晩鍨跺濠氭晸閻樻彃绐涘銈嗘煥婢т粙鎮℃径濞炬斀妞ゆ梻銆嬮弨缁樹繆閻愯埖顥夐柣锝呭槻楗即宕煎┑鍫斀闂備胶鎳撻幖顐ょ矓閸洖鏋侀柡宥庡幗閳锋帒霉閿濆懏鍟為柟鑼归埞鎴︻敊閻愵剚姣堝Δ鐘靛仦閸ㄥ灝鐣烽幆閭︽Ь闂佸搫妫寸粻鎾诲蓟閺囷紕鐤€閻庯綆浜栭崑鎾诲即閻樺吀绗夐梺鑽ゅ枑閸g銇愰幒鎾存珳闂佸憡渚楅崢鍏兼綇閸涘瓨鈷戠憸鐗堝笚閺佽鲸淇婇悙鑸殿棄妞ゎ偄绻橀幖鍦喆閸曨偄骞戦梻浣告啞娓氭宕㈤崫鍕懷兾旈崨顔规嫼缂備礁顑嗛娆撳磿閹扮増鐓熼柍鍝勶工閻忕娀鏌i敐鍛Щ闁宠鍨垮畷浼搭敊閼恒儺妫冮悗瑙勬磸閸旀垿銆佸▎鎾崇畾鐟滃秶绮绘导瀛樷拻闁稿本鐟чˇ锕傛煙濞村澧茬紒妤冨枎铻栭柛娑卞幘閻涖儱鈹戦鏂や緵闁稿寒浜幖褰掑礂婢跺﹣澹曞┑鐐村灦椤忣喖饪伴崟顓ф锤濠电姴锕ら悧濠囨偂韫囨稓鍙撻柛銉戝秴浼愭繝鈷€鍕弨闁诡喗枪缁犳稑鈽夊▎鎰版暘闂傚倸娲らˇ鐢稿蓟閿濆應鏋庨煫鍥ㄦ煥濞呇囨⒑娴兼瑧鎮奸柡浣规倐閸┾偓妞ゆ帒鍠氬ḿ鎰箾閸欏缂氶柛鎺撳笩缁犳稑霉閺夋寧宸濋柍褜鍓氱粙鎺曞綘婵炲瓨绮嶇划鎾诲蓟閿熺姴绀冮柨婵嗘噸婢规洘绻濋悽闈涗哗閻忓繑鐟╁畷鐗堟償椤帞绋忛棅顐㈡处閹峰煤椤忓秵鏅滈梺鍛婃处閸欏骸危椤栫偞鈷掑ù锝嚽归幃鎴犵磼娴h灏︾€殿噮鍓熷畷鎺楁倷閼碱剨绱遍梻浣虹帛閸旀宕曢妶澶婄厱闁硅揪闄勯悡鏇熺節闂堟稒顥滄い蹇d邯閺屾盯鏁愰崱妯镐虎闂佸搫鐭夌紞渚€宕洪埄鍐瘈闁稿本绮堝鎾绘煟鎼淬値娼愭繛鍙壝—鍐嚍閵夛箑寮块梺閫炲苯澧撮柡灞炬礋瀹曠厧鈹戦崶褎鐣婚梻浣告憸閸嬫盯鎮ラ悡搴綎婵炲樊浜濋ˉ鍫熺箾閹达綁鍝烘い搴℃缁绘繄鍠婂Ο宄颁壕闁惧浚鍋勯弸鐘绘倵鐟欏嫭纾搁柛銊ㄦ铻為柛鎰╁妷濡插牓寮堕崼娑樺闁伙附绮撳缁樼瑹閳ь剙岣胯閹囧幢濡炪垺绋戦埢搴ㄥ箻瀹曞洤骞堥梻浣告贡閸庛倝銆冮崱娑欏亗闁绘柨鍚嬮悡鍐煃鏉炴壆顦﹂柡鍡欏仱閺岋綁骞橀崡鐐插Е闂佸搫鑻粔鍓佹閹烘嚦鐔烘嫚閼碱剨绱﹂梺璇插椤旀牠宕抽鈧畷鎶芥晲閸涱垱娈炬繝闈涘€搁幉锟犲磻閸曨垱鐓曟繝闈涙椤忊晝绱掑Δ浣稿摵婵﹤顭峰畷鎺戔枎閹邦喓鍋樺┑鐘愁問閸犳捇宕愬┑瀣瀬閻庯綆浜跺〒濠氭煏閸繄绠抽柣锝堟珪娣囧﹪顢曢姀鐙€浼傞梺璇茬箲鐢€愁潖濞差亝鐒婚柣鎰蔼鐎氭澘顭胯閹告娊寮婚悢纰辨晩缂佹稑顑嗛悾濂告⒑閻熸澘绾ч柟绋垮暱閻g兘鎮㈢喊杈ㄦ櫌闂佺ǹ琚崐鏍叿闂傚倸鍊搁崐鐑芥倿閿旈敮鍋撶粭娑樻噹閺嬪牏鈧箍鍎遍ˇ顖涱攰闂備礁鎲″ú锕傚垂閺夎娑橆潨閳ь剟骞冭ぐ鎺戠畳闁圭儤鍨甸‖瀣渻閵堝棙鈷愰悽顖涘浮閳ユ棃宕橀鍢壯囨煕閹扳晛濡垮ù鐘荤畺濮婃椽鎳¢妶鍛瘣闂佸搫鎳愭繛鈧柣娑卞櫍楠炲洭顢橀悩鐢垫闂備礁鎲¢崝鎴﹀礉鎼达絿鐜婚柣鎰劋閻撶喖骞栭幖顓炵仯缂佸鏁婚弻娑滅疀閺冨倹鍒涘Δ鐘靛仜閸燁偊顢橀崗鐓庣窞閻庯急鍕伜闂傚倷鑳舵灙闁哄牜鍓熼幊婵囥偅閸愩劎鍔﹀銈嗗笂閻掞箓宕愰幇顔瑰亾鐟欏嫭绀冮柛鏃€鐟╅悰顕€寮介妸锕€顎撻梺鍛婄缚閸庤崵妲愰鈧缁樻媴閾忕懓绗¢梺鎼炲妼閸氬骞堥妸鈺佄у璺猴工閹偤姊洪崨濠冨闁搞劑浜堕幃锟犲即閵忥紕鍘甸梺纭咁潐閸旀洟鎯冮悜妯镐簻闁挎棁鍋愰悾鐢告煛鐏炲墽娲村┑鈩冩倐閺佸倿宕滆閺嗩偊姊绘笟鈧ḿ褍煤閵堝洠鍋撳顓熺凡妞ゆ洩绲剧粋鎺斺偓锝呯仛閺呮繂顪冮妶搴′航闁告ü绮欏畷鐔煎礃椤旇В鎷绘繛杈剧到閹虫瑨銇愰幒婵囨櫈闂佸憡绋掗幆宀勫极閸曨偒鐔嗛柤鎼佹涧婵洭鏌﹂崘顏勬灈闁哄被鍔岄埞鎴﹀幢閳哄倐锔剧磽娴e搫校缂佸甯℃俊鐢稿礋椤栨氨顔掗柣鐘烘濞插懘鎮欓悜妯煎幈闁诲函缍嗛崜娆愮鏉堛劍鍙忓┑鐘插暞閵囨繄鈧娲﹂崑濠傜暦閻斿吋顥堟繛鎴灻ˉ宥囩磽閸屾艾鈧绮堟笟鈧棟妞ゆ牗绮庣粈濠傗攽閻樻彃浜為柛銈嗘礀閳规垿鎮╃€圭姴顥濋柟顖滃枛濮婃椽妫冨☉杈ㄐら梺鎼炲妽濡炶棄顕i鍕劦妞ゆ帒瀚埛鎺懨归敐鍫燁仩闁靛棗锕弻娑㈠箻鐎靛摜鐣鹃梺鍦摂閸嬪﹤顫忛搹瑙勫珰闁炽儴娅曢悘宥夋⒑閼姐倕鏆遍柡鍛洴閿濈偠绠涢幘浣规そ椤㈡棃宕熼褍鏅i梻鍌欒兌缁垶宕濋弽顑句汗闁告劦鍠掗埀顒佺墬瀵板嫬鐣濋埀顒傚閽樺褰掓晲閸モ晜鎲橀梺鎼炲€栭悷鈺呭蓟濞戙垺鍋勯柛娑橈工閸炲姊虹紒妯圭繁闁革綇绲介悾閿嬬附缁嬭銊╂煏婢跺﹦宀搁柡鍛█瀵寮撮悢椋庣獮婵犵數濮撮崯顖氱暦閹惰姤鈷戦柛婵勫劚鏍¢梺缁橆殘婵炩偓闁诡喕鍗抽、姘跺焵椤掑嫮宓侀柛銉墻閺佸洭鏌i弬鍨Щ濠碘剝濞婂缁樻媴閻熼偊鍤嬬紓浣筋嚙閸婂灝鐣烽鐐村亹閻犲洩灏欓敍娑㈡⒑鐟欏嫬绀冩い鏇嗗懐涓嶆繛鎴炵懀娴滄粓鏌¢崒姘变虎闁抽攱妫冮弻銊モ槈濞嗘垹鐣虹紓浣虹帛缁嬫帒岣胯箛娑樼鐟滃繗鎽梺鑽ゅ枑缁秴顭垮鈧畷顖烆敍濠婂懐鐒块悗骞垮劚濡酣宕戦崨瀛樼厱闁硅埇鍔嶉弶褰掓煙闁垮銇濇慨濠冩そ瀹曘劍绻濋崘銊╃€洪柣鐔哥矋濠㈡﹢宕婊呯焿鐎广儱鎳夐弨浠嬫煕椤愮姴鐏柨娑欑矒濮婃椽宕ㄦ繝鍐ㄧ煯闂佺粯甯粻鎾诲箖閻愬搫閿ゆ俊銈勮兌閸橆亪姊洪幖鐐插姌闁告柨鏈幈銊ヮ吋閸♀晜顔旈梺缁樺姈濞兼瑥霉椤旂瓔娈介柣鎰缂傛岸鏌嶈閸撴氨绮欓幒鎴犲箵闁兼剚鍨禍褰掓煙闂傚鍔嶉柍閿嬪浮閺屾稓浠﹂崜褎鍣銈忚缁犳捇寮婚悢璁垮湱鈧綆浜滈埛澶岀磽娴h娈橀柛鐘叉唉閻忓啴姊洪崨濠佺繁闁告﹢绠栭幃浼村Ψ閵夈垺鏂€闂佺粯鍔栧ḿ娆撴倶閿斿墽妫柡澶庢硶鏁堥悗瑙勬礃椤ㄥ懘銈导鏉戦唶闁绘柨鎼敮妤呮煟閻斿摜鐭嬬紒顔芥尭閻e嘲饪伴崼鐔蜂簻婵犻潧鍊搁ˇ鎵礊鎼达絿纾介柛灞剧懅閸斿秹鎷戦崡鐐╂斀妞ゆ牗绋掔亸锕傛煛鐏炲墽鈽夐柍钘夘槸椤粓宕奸悢鍛婃瘞闂傚倷鑳舵灙閻庢稈鏅犻獮鎰板箹娴e摜鍘撮梺纭呮彧缁犳垿鎮¢敓鐘崇厱闁斥晛鍟ㄦ禒锔剧磼閵娿劌浜圭紒杈ㄦ尰閹峰懘宕滈幓鎺戝闂佹眹鍩勯崹鎶藉磻閵堝宓侀柟杈剧畱椤懘鏌e鍡椾簼妞ゎ偄绉瑰娲濞戞氨顔婃繝娈垮枤閸忔ê鐣峰┑瀣櫇闁逞屽墴閳ユ棃宕橀鍢壯囨煕閳╁喚娈橀柣鐔稿姍濮婅櫣绱掑Ο娲殝缂備胶濮甸幐鎼佹偩閻戣姤鏅查柛顐犲灮閺夋悂姊洪崷顓℃闁搞劑浜跺顒勫焵椤掑嫭鈷掑ù锝堟鐢盯鎷戞潏鈺傚枑闁哄鐏濋弳锝団偓娈垮枟婵炲﹪骞冨▎鎾村€绘俊顖滃帶鐢箖姊绘担瑙勫仩闁稿寒鍨跺畷婵囨償閿濆洣绗夐梺缁樺姉閸庛倝鎮″☉姘e亾閸忓浜鹃梺閫炲苯澧寸€规洑鍗冲浠嬵敇濠ф儳浜惧ù锝囩《閺嬪酣鏌熼幆褏锛嶉柣锝夌畺閹嘲饪伴崘顎囨煟濞戝崬鏋ら柍褜鍓ㄧ紞鍡涘焵椤掑骞楁俊顐㈠暣楠炲啴鍩¢崨顕呮濠电偞鍨堕〃鍫ュ箲閺囩姷纾介柛灞剧懅椤︼附銇勯敂璇茬仯缂佽京鍋炵换婵嬪炊椤兙鍎遍湁闁挎繂娲ㄩ妴濠囨煛鐎n亪鍙勯柡宀€鍠栭弻鍥晝閳ь剟寮搁妶澶嬬厽闁挎洍鍋撻柣妤€妫濋崺鐐哄箣閿旂粯鏅╅梺鍝勫€堕崐鎾舵閻㈠憡鈷戠紒瀣硶缁犺尙绱掔€n偅宕岀€规洘宀搁獮鎺懳旀担瑙勭彸濠电姰鍨煎▔娑㈩敄閸岀偛绠┑鐘崇閳锋垹绱掔€n偄顕滄繝鈧导瀛樼厾鐟滅増甯為悾娲煕閳规儳浜炬俊鐐€栫敮鎺楀磹閹间礁鍌ㄩ柟缁㈠枟閻撴瑩鏌ц箛锝呬航婵炲牊绮撻弻鐔兼惞椤愩倗鐓夐梺璇″枙缁瑥鐣峰Δ鍛紶闁靛濡囪棟濠电姷鏁告慨鐑姐€傞鐐潟闁哄洢鍨圭壕濠氭煙鏉堝墽鐣辩痪鎯х秺閺屸€愁吋鎼粹€崇闂佹悶鍔岄崐鍨潖婵犳艾閱囬柣鏂垮槻楠炲繐鈹戦悙鏉戠仸閼裤倝鏌¢埀顒佺鐎n偄鈧敻鏌ㄥ┑鍡涱€楀褜鍠氱槐鎺撶瑹婵犲嫮鏆ゅ┑顔硷龚濞咃絽鈽夐悽绋垮窛妞ゆ柨鍚嬮柨顓犵磽閸屾瑨鍏屽┑顔炬暬瀹曞綊宕稿Δ鈧粻鏍ㄧ箾閸℃ê濮夌紒鈾€鍋撻梻浣告啞閸斞呯磽濮樿精濮冲┑鐘崇閳锋垿鏌i悢鍝勵暭闁诡垰鐗婃穱濠囶敃閿濆孩鐣风紓浣稿€哥粔鐢稿Χ閿濆绀冮柍鍦亾鐎氬ジ姊绘担钘壭撻柨姘亜閿旇鐏︾€殿喗濞婇幃銏ゅ礂閼测晛骞堥梻浣虹帛閿氱痪缁㈠幗閺呭爼鎮界喊妯轰壕婵炲牆鐏濋弸娑欍亜椤撱垺鏁卞ǎ鍥э躬楠炴牗鎷呴崫銉ュ箰闂備胶枪閺堫剟鎯岄鎹愬С濠电姵纰嶉埛鎺懨归敐鍛暈闁哥喓鍋熺槐鎺旀嫚閹绘巻鍋撴繝姘劦妞ゆ帊娴囨竟姗€鏌熼搹顐嗘垿骞堥妸鈺佺劦妞ゆ帒瀚悡蹇涙煕椤愶絿绠栨い銉﹀灴閺岀喖鏌ㄧ€n偁浠㈠┑顔硷攻濡炶棄鐣烽妸锔剧瘈閹兼番鍨婚弳顓㈡⒒娴e懙褰掝敄閸ヮ剙纾婚柣鎰▕閸ゆ鏌涢弴銊ョ仩缂佲偓鐎n偁浜滈柡宥冨妿閵嗘帡鏌涘鍡曢偗婵﹥妞介獮鏍倷閹绘帒螚闂備礁鎲¢崝鏇°亹閻愬灚顫曢柡鍐e亾濞e洤锕俊鍫曞炊椤喓鍎甸弻娑氣偓锝庡墮娴犙囨煛娓氬洤娅嶆鐐村笒铻栧┑鐘插暞濞呭秴鈹戦悩缁樻锭闁稿﹦绮悘娆撴⒑缂佹ê濮囬柨鏇ㄤ邯瀵濡舵径濠傜獩婵犵數濮撮崯顖炴偟椤忓嫧鏀介柣妯款嚋瀹搞儵鎮楀闂寸敖闁瑰箍鍨藉畷鍗炩槈濞嗘垵骞楅梻浣筋潐濠㈡﹢宕ラ埀顒傜磼閵娿儺鐓奸柡灞界Х椤т線鏌涢幘纾嬪閻撱倖鎱ㄥ璇蹭壕闂侀潧妫楅崯瀛樹繆閻戣棄惟鐟滃繘寮剁粙搴撴斀闁绘劖娼欓悘锕€鐣濋敐鍛仴妞ゃ垺鐟╁畷鍗炩槈濞嗗本瀚奸梺鑽ゅУ娴滀粙宕濈仦瑙f瀺闁规壆澧楅悡娆撴煕閹存瑥鈧牜鈧熬鎷�>>  濠电姷鏁告慨鐑藉极閸涘﹥鍙忛柣鎴f閺嬩線鏌涘☉姗堟敾闁告瑥绻橀弻锝夊箣閿濆棭妫勯梺鍝勵儎缁舵岸寮诲☉妯锋婵鐗婇弫楣冩⒑閸涘﹦鎳冪紒缁橈耿瀵鏁愭径濠勵吅闂佹寧绻傚Λ顓炍涢崟顖涒拺闁告繂瀚烽崕搴g磼閼搁潧鍝虹€殿喖顭烽幃銏ゅ礂鐏忔牗瀚介梺璇查叄濞佳勭珶婵犲伣锝夘敊閸撗咃紲闂佺粯鍔﹂崜娆撳礉閵堝棎浜滄い鎾跺Т閸樺鈧鍠栭…鐑藉极閹邦厼绶炲┑鐘插閺夊憡淇婇悙顏勨偓鏍暜婵犲洦鍊块柨鏇炲€哥壕鍧楁煙閸撗呭笡闁抽攱鍨块弻鐔兼嚃閳轰椒绮舵繝纰樷偓鐐藉仮闁哄本绋掔换婵嬪磼濞戞ü娣柣搴㈩問閸犳盯顢氳閸┿儲寰勯幇顒夋綂闂佸啿鎼崐鐟扳枍閸ヮ剚鈷掑ù锝囨嚀椤曟粎绱掔拠鎻掆偓姝岀亱濠电偞鍨熼幊鐐哄炊椤掆偓鍞悷婊冪箳婢规洟鎸婃竟婵嗙秺閺佹劙宕ㄩ钘夊壍闂佸搫绉埀顒佹灱閺€浠嬫煟濮楀棗鏋涢柣蹇d邯閺屻劑寮村Ο铏逛紙閻庤娲樺浠嬪箖濞嗘挸浼犻柛鏇ㄥ弾閸氬懘姊绘担鐟邦嚋婵☆偂绀佽灋闁告洦鍓涢々鑼喐閻楀牆绗氶柛濠勬暬閹嘲鈻庤箛鎿冧痪缂備讲鍋撻柍褜鍓欓埞鎴︽倷鐎涙ḿ绋囬梺绋匡工閻忔繈顢氶敐澶婄闁兼亽鍎插▍銏ゆ⒑缂佹〞鎴﹀几婵傜ǹ绠柧蹇撴贡绾捐棄霉閿濆懎顥忛柛搴㈠姈閵囧嫰骞嬮悙鍨櫚閻庤娲樺ú婵堢不濞戙垹妫橀悹浣哥-閻╁酣姊绘担鐑樺殌闁宦板妿閹广垽宕橀銏狀樀閹晝绱掑Ο鐓庡箥婵°倗濮烽崑娑㈡倶濠靛鍊堕柍鍝勬噺閻撳啴鎮峰▎蹇擃仼闁诲繐顕埀顒冾潐濞叉牠鎮ユ總绋挎槬闁跨喓濮寸粈鍐┿亜韫囨挻濯兼繛鍏兼崌濮婂宕掑顑藉亾閻戣姤鍤勯柤鍝ユ暩娴犳岸姊绘担鍛婃儓闁绘绮撳畷婊冣槈閵忕姷顦梺鍦劋閸ㄥ綊寮抽崱娑欑厱闁哄洦顨嗛弶褰掓煕鐎n偅宕岀€规洘甯掕妞ゆ挾鍠愰妵婵囥亜閵忊剝顥堢€规洏鍔戦、鏃堝川椤撗傜椽濠电姷鏁告慨鐢割敊閺嶎厼绐楁慨妯挎硾缁犵娀鏌熼幑鎰滄繛宸簻鍥存繝銏f硾閿曪箓宕濋敃鈧—鍐Χ閸℃鐟愮紓浣哥亪閳ь剚鏋奸弸鏃€绻濇繝鍌涘櫝闁稿鎸鹃幉鎾礋椤掑偆妲伴梻浣规偠閸斿苯岣块敓鐘冲仒妞ゆ柨妲堥悢鐓庣闁绘挸娴疯ぐ鎾⒒娴e憡鍟為柣鐔村劦瀹曟垶绻濋崟顓濈瑝闂佽宕橀褔鎷戦悢鍝ョ闁瑰瓨鐟ラ悘鈺呮煕濡や礁鈻曢柡灞炬礃缁绘盯宕归鐓幮戝┑鐐差嚟婵參寮插┑鍫燁潟闁规儳鐡ㄦ刊鎾煕濠靛棗鐝旈柨婵嗩槹閻撶喖鏌嶉崫鍕跺伐闁诲骏濡囬埀顒侇問閸犳盯顢氳閸┿儲寰勯幇顒夋綂闂佸啿鎼崐鐟扳枍閸ヮ剚鈷掑ù锝囨嚀椤曟粎绱掔拠鎻掆偓姝岀亱濠电偞鍨熼幊鐐哄炊椤掆偓鎯熼梺闈涱樈閸犳鈧潧鐭傚娲濞戞艾顣洪梺纭呮珪閿曘垽銆侀幘婢勬棃宕橀鍡床濠电姰鍨煎▔娑㈠嫉椤掑嫬姹查柍鍝勬噺閻撴瑦顨ラ悙鑼虎闁诲繆鏅犻弻宥囨喆閸曨偆浼岄悗瑙勬礉缁墽绮诲☉銏犵睄闁稿本鐟ч幐澶愭⒒閸屾艾鈧绮堟担鍦彾濠电姴娲﹂崑鍌炴煕椤愮姴鍔氱紒鎰殕閹便劌顫滈崱妤€绠诲銈傛櫇閸忔﹢寮诲澶婁紶闁告洦鍓欏▍銈夋⒑閹惰姤鏁遍柛銊ユ健瀵鈽夊Ο閿嬵潔濠殿喗顨呴悧鎾舵鐎涙ḿ绡€闁靛骏缍嗗ḿ鎰版嫅闁秵鐓忛柛銉戝喚浼冨Δ鐘靛仜椤戝懘鍩為幋锕€鐐婇柤鍝ヮ暜妤犲繒绱撻崒姘偓椋庢閿熺姴绐楁俊銈呭暙閺嬪牏鈧箍鍎遍幊鍥╃磽濮樺墎鍙撻柛銉e妿閳藉骞嗛悢鍏煎仭婵犲﹤鍟扮粻濠氭煙椤栨瑧绐旂€规洖銈告俊鐑芥晜鐟欏嫬顏归梻鍌欒兌椤㈠﹪宕戦幇鏉跨;婵炴垯鍨圭粈澶愭煙缂併垹鏋熼柣鎾跺枛閻擃偊宕堕妸锔规嫽濡炪値鍓欓崥瀣Φ閸曨垱鏅濋柍褜鍓涚槐鐐寸節閸パ嗘憰闂佹寧绋戠€氼亜鈻介鍫熺厱闁圭偓銇炵拋鏌ュ磻閹捐绠抽柟鐐藉妼缂嶅﹪骞冮鍫濆窛妞ゆ牗绮嶅▓濂告煟鎼淬値娼愭繛鍙夅缚閸掓帟绠涘ù鏉挎喘楠炴﹢顢欓悾灞藉箞婵犵數鍋涘Λ娆撳礉濡ゅ啰涓嶉柡宥庡亞绾捐偐绱撴担璐細缂佺姷鍋涢埞鎴︻敊閻熼澹曢梻鍌欑劍鐎笛呮崲閸屾壕鍋撳☉鎺撴珖缂佽京鍋ゅ畷鐓庘攽閸愨晜鏉搁梻浣虹帛閸旀ê鈻斿☉銏″剭婵炲樊浜濋悡鏇㈡煟濡崵鍙€闁告瑥瀚伴弻銊モ攽閸繀鍝楃紓浣哄У閻╊垰顕i幘顔藉亹缁炬澘顦辨惔濠傗攽閻樻鏆俊鎻掓嚇瀹曞綊鎮介崜鍙夋櫔閻熸粍妫冮妴渚€骞樼拠鑼啋闂佸憡鎸烽懗鍫曟晬濠靛洨绠鹃弶鍫濆⒔閸掔増绻濋埀顒勬焼瀹ュ懐鍙€婵犮垼娉涢鍐╃濠婂牊鐓欓悗娑欋缚缁犳牠鏌涢敐鍛Ш闁哄苯绉剁槐鎺懳熺拠鑼紦婵°倗濮烽崑娑樏洪銏犵畺鐟滄柨鐣烽悡搴僵妞ゆ挾鍎愭导鏍⒒閸屾艾鈧绮堟笟鈧獮澶愭晬閸曨厾澶勯梺绉嗗嫷娈旂痪鎯ф健瀵爼宕煎☉妯侯瀷婵犫拃鈧埀顒佹灱閺€浠嬫煥濞戞ê顏╁ù婊冦偢閺屾稒绻濋崘銊т紝閻庤娲樼换鍌炴偩濠靛绀嬫い鎰╁€楅弸鍐⒑绾懎顥嶉柟娲讳簽濡叉劙寮撮姀鐘宠緢闂侀潧鐗嗛ˇ浼存偂閺囥垺鐓涢柛銉e劚婵″ジ鏌h箛銉х瘈闁哄苯绉归弻銊р偓锝庝簽娴煎矂姊洪崫鍕拱缂佸鍨块崺鐐哄箣閿曗偓楠炪垺淇婇妶鍜冩闁诡噯绲炬穱濠囨倷椤忓嫧鍋撻弴鐏荤懓顫濈捄铏癸紱婵犵數濮村ú銈夋嫅閻斿吋鐓ユ繝闈涙婢с垽鏌i妶鍌氫壕闂傚倷娴囬~澶愬磿閹惰棄鐤悹鎭掑妽閺嗘粎绱掔悰鈩冩 Fisher闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ゆ繝鈧柆宥呯劦妞ゆ帒鍊归崵鈧柣搴㈠嚬閸欏啫鐣峰畷鍥ь棜閻庯絻鍔嬪Ч妤呮⒑閸︻厼鍔嬮柛銊ョ秺瀹曟劙鎮欓悜妯轰画濠电姴锕ら崯鎵不閼姐倐鍋撳▓鍨灍濠电偛锕顐﹀礃椤旇偐锛滃┑鐐村灦閼归箖鐛崼鐔剁箚闁绘劦浜滈埀顑惧€濆畷銏$鐎n亜鐎梺鍓茬厛閸嬪棝銆呴崣澶岀瘈闂傚牊渚楅崕鎰版煟閹惧瓨绀冪紒缁樼洴瀹曞崬螖閸愵亶鍞虹紓鍌欒兌婵灚绻涙繝鍥ц摕鐎广儱鐗滃銊╂⒑閸涘﹥灏伴柣鐔濆懎鍨濋悹鍥ф▕閸氬顭跨捄鐚村姛闁挎稓鍠栧缁樼瑹閸パ冾潻闂佸憡顨嗗ú鐔风暦閸洦鏁嗗璺侯儐濞呮牗绻濋悽闈浶㈤柨鏇樺€濋獮濠囧箛閻楀牆鈧灝鈹戦崒姘暈闁绘挾鍠栭獮鏍箹椤撶偟浠紓浣割槺閺佸寮诲☉姘e亾閿濆倹娅囬柛鏂跨Ф缁辨帡宕掑姣欍垺顨滈鍐ㄥ祮鐎规洖銈搁幃銏ゅ传閸曨偆顓奸梻鍌氬€烽懗鍫曘€佹繝鍥风稏濠㈣埖鍔曠粈澶愭煛瀹ュ骸浜濋柛蹇旂矊铻栭柨婵嗘噹閺嗙偤鏌i幘瀵告创闁诡喗顨婇弫鎰償濠靛浠愰梻浣告啞閻熴儳鈧矮鍗冲濠氭晬閸曨亝鍕冮梺鍛婃寙閸曨偄鐏℃繝鐢靛Х椤d粙宕滃┑瀣畺闁稿本绋愮换鍡涙煙闂傚顦﹂崶鎾⒑閸涘﹣绶遍柛鐘崇墵瀹曟粓鎮介悽鐢碉紳闂佺ǹ鏈懝楣冨焵椤掆偓閸㈡煡婀侀梺鎼炲劘閸斿﹥绂掗崼銉︾厵闂傚倸顕ˇ锔剧磼閻樺磭鍙€闁哄本鐩俊鐑藉箣濠靛洤娅ゅ┑鐐茬墦缁犳牕顫忓ú顏勬嵍妞ゆ挾鍋涙俊娲⒑閹肩偛濡块柛鐘崇墪椤曪綁宕ㄦ繝鍐ㄥ妳闂侀潧饪垫俊鍥储閻㈠憡鐓涘璺猴功婢ф洖顭胯缁瑩鐛崘鈺冮檮闁告稑锕﹂崢钘夆攽閻愭潙鐏﹂柣妤佹礋瀹曟繈鏁傞懞銉ュ伎婵犵數濮寸€氼喚鏁☉姘辩<婵°倕鍟弸娑㈡煕閳规儳浜炬俊鐐€栧濠氬磻閹惧磭鏆嗛柨婵嗘噺閸嬨儵鏌熺粵鍦瘈濠碘€崇埣瀹曞爼鍩℃繝鍐冿箓姊婚崒娆掑厡缁绢厼鐖煎畷婊冣攽閸垻鐓撻梺纭呮彧闂勫嫰鍩涢幒鎾变簻闁哄稁鍋勬禒锕傛煟閹惧崬鍔滅紒缁樼箞濡啫鈽夊▎妯伙紒闂備線娼荤徊鑲╁垝濞嗘挸钃熼柨鐔哄Т楠炪垺銇勯幘璺哄壉婵炲樊鍙冨娲偡閺夎法楠囬梺璇″枛閸婂潡鐛崘顓ф▌閻庤娲滈崢褔鍩為幋锕€閱囬柕蹇娾偓铏暟闂傚倸鍊搁崐鐑芥嚄閸撲礁鍨濇い鏍ㄧ矋閺嗘粓鏌i弮鍌氬付缁炬儳顭烽弻鐔兼偋閸喓鍑¢梺缁樺笒閻忔岸濡甸崟顖氱闁瑰瓨绻冮悘鎾斥攽閻愭彃鎮戦柛鏃€鐟╁濠氭偄閾忓湱鐓撻柣鐘充航閸斿矂鎮¢悢鍏煎€甸悷娆忓缁€鍐╃箾閼碱剙鏋庨柣锝囧厴閺佹捇鎮╅崘娴嬪亾閸撲胶纾藉ù锝堝亗閹达箑桅婵犻潧顑嗛悡娑樏归敐鍤藉綊鍩€椤掆偓濞尖€愁嚕婵犳艾惟闁冲搫锕ラ弲顒€鈹戦鏂や緵闁稿瀚拌棢婵﹩鍏橀弨浠嬫煟閹邦垰鐓愮憸鎶婂懐纾奸棅顐幘閻瑧鈧娲﹂崹鍫曘€侀弴銏℃櫜闁搞儴鍩栭柨銈夋煟閻斿摜鐭屽褎顨堥弫顔嘉旈崨顔间簵闂佸憡鍔︽禍婵嬪窗閹邦厾绡€濠电姴鍊绘晶鏇犵磼閳ь剟宕奸悢绋垮伎濠碘槅鍨伴妵姗€宕ラ锔界厽妞ゆ挾鍠撻幊鍥煛瀹€鈧崰鏍箖濠婂喚娼ㄩ柛鈩冡缚閺嗭箓姊绘担鍛婃儓闁瑰嘲顑嗙粋宥夘敂閸曞灚缍庣紓鍌欑劍宀e潡鎮疯ぐ鎺撶厓鐟滄粓宕滈悢鐓庢槬闁逞屽墯閵囧嫰骞掗幋婵冨亾閸涘﹦顩锋繝濠傜墛閻撶姵绻涢懠棰濆殭闁诲骏绻濋弻锟犲川閺夎法鍘柣搴濈祷閸嬫劙鍩€椤掍胶鈯曞畝锝呮健瀹曘垽鏌嗗鍡╂濡炪倖鍔戦崹鐑樺緞閸曨兛绻嗘い鎰剁到閻忔挳鏌熼搹顐e暗闁圭懓瀚版俊鎼佸閻樺崬顥氭繝鐢靛仜閻楀棝鎮樺┑瀣嚑婵炴垶鐟f禍婊勩亜閹捐泛孝闁告ê鐡ㄩ〃銉╂倷閹绘帗娈绘繝娈垮枓閸嬫挸顪冮妶搴′航闁告﹢绠栧畷婊堝Ω閿斿墽顔曢柡澶婄墕婢т粙宕氶悧鍫㈢瘈闁逞屽墯濞煎繘濡歌濞叉悂姊洪崫鍕枆闁告ü绮欓崺娑㈠箳閹炽劌缍婇弫鎰板吹閽樺绉洪挊鐔肩叓閸ャ劎鈯曢柣鎾跺枛閺岀喖骞嗚閿涘秴顭胯婵″洭鍩€椤掑喚娼愭繛鍙壝…鍨熺捄銊ょ胺闂傚倷绀侀幉鈩冪瑹濡ゅ懎绐楅柡宥庡幖閻掑灚銇勯幒鍡椾壕闂佺粯鐗曢妶绋款嚕婵犳碍鍋勯柣鎾虫捣椤︻參鎮峰⿰鍐闁轰緡鍠栭埥澶愬閿涘嫬甯楅梻鍌欑閻忔繈顢栭崨瀛樺€堕柍鍝勬噺閻撶喖鏌曟径妯烘灆闂侇収鍨遍妵鍕閳藉懓鈧潡鏌熼鐣屾噰鐎殿喖鐖奸獮瀣倻閸℃洜鏁鹃梻鍌氬€搁崐鐑芥嚄閸撲礁鍨濇い鏍ㄧ矋瀹曡尙鈧箍鍎卞Λ娑€€呴崣澶堜簻闊洦鎸炬晶鏇㈡煢閸愵亜鏋戠紒缁樼洴楠炲鈻庤箛鏇氭偅缂傚倷绶¢崑鍕矓瑜版帒钃熺€广儱鐗滃銊╂⒑閸涘﹥灏甸柛鐘崇墵閻涱噣宕橀钘夆偓濠氭煢濡警妲洪柛妯烘啞缁绘盯骞樼壕瀣棟濠电偛鐪伴崐鏇㈠煝閹捐惟闁挎柨澧介惁鍫ユ⒑濮瑰洤鐏叉繛浣冲嫮澧$紓鍌欒兌閸嬫挸顭垮Ο鑲╃煋闁荤喖鍋婇崵鏇㈡煛鐏炶鍔氶柦鍐枛閺屾洘寰勫☉姗嗘喘闂佸憡锚瀹曨剟鈥旈崘顔嘉ч柛鈩冾殔椤孩绻濆▓鍨灍闁瑰憡濞婇獮鍐潨閳ь剟銆佸璺虹劦妞ゆ帒瀚拑鐔兼煃閳轰礁鏆欑紒鍓佸仱閹鏁愭惔鈥茬盎闂侀€炲苯澧柛鏃€鐗犻獮鍫ュΩ閿斿墽鐦堥梺鍛婁緱閸n喗绂掗埡鍛拺闁荤喐婢樼痪褔鏌熺粙鍨毐闁伙絿鍏橀幃銏㈠枈鏉堛劍娅囬梻渚€娼х换鎺撴叏瀹€鍕婵犻潧鍟弬鈧梻浣虹帛閿曗晠宕戦崨顔煎灁濞寸厧鐡ㄩ悡鏇㈡煙娴煎瓨娑ч柡瀣〒閳ь剚顔栭崰妤€顭垮鈧垾鏃堝礃椤斿槈褔鏌涢幇鈺佸濞寸娀绠栧娲嚒閵堝懏鐝㈢紓浣哄У閸ㄥ潡銆佸璺何ㄩ柍杞拌兌椤︽澘顪冮妶鍡楃瑨闁稿﹤顭烽、娆撳即閵忊檧鎷虹紓鍌欑劍閿氬┑顕嗙畵閺屾盯骞橀弶鎴濇懙閻庢鍠栭悥鐓庣暦閵婏妇绡€濞达綀娅i悾楣冩⒒娴h櫣甯涢柛鏃撻檮缁傚秴饪伴崼婵堝姦濡炪倖甯婇懗鑸垫櫠椤忓懌浜滄い鎰╁灮缁犺尙绱掔紒妯肩畵妞ゎ偅绻堥、鏍煘閸喖濮﹂梺璇″枟椤ㄥ﹪寮幇顓熷劅婵犻潧娲ら弸銈夋⒒娴e憡鎲搁柛鐘查叄楠炲﹤顫滈埀顒€顕f繝姘嵆闁绘棃顥撶粣鐐测攽閻愭潙鐏︾紒顔奸叄钘濋柣妤€鐗忕粻楣冩倵濞戞瑡缂氶柣顓烆儑缁辨帡顢欓懖鈹冣攽閿涘嫭鏆€规洜鍠栭、娑橆潩妲屾牕鏅梻浣藉吹婵儳鈻嶉敐鍚ゆ椽宕ㄩ弶鎴綂闂侀潧鐗嗗Λ娑㈠储閸楃偐鏀介柍钘夋閻忥絿绱掗鍛仯濞存粍鎮傞弫鍐磼濞戞艾骞愰梺璇茬箳閸嬬喐鐏欐繝鈷€鍕弨闁哄瞼鍠庨悾锟犳偋閸繃鐣婚梻浣筋嚃閸犳岸宕楀Ο渚殨閻犻缚銆€閺嬪酣鏌i幇闈涘缂佸鐗撳濠氬磼濮橆兘鍋撳畡鎳婂綊宕堕澶嬫櫔闂佸搫绋侀崢鑲╃玻濡や椒绻嗛柕鍫濇噺閸f椽鏌涚€e墎绡€闁哄苯绉靛ḿ顏堝箯鐏炶棄甯梻浣告惈濡挳姊介崟顖毼﹂柛鏇ㄥ灠缁犳盯鏌涢幘鑼跺厡闁哄棛濮风槐鎾存媴閹绘帊澹曢梺璇插嚱缂嶅棝宕戞担鍦洸婵犲﹤鐗婇悡娆撴煙娴e啯鐝繛鍛嚇閺岋綀绠涢敐鍕仐闂佸搫鐭夌换婵嗙暦閸楃倣鏃堝礃椤忓秴鏁归梻鍌欑閻ゅ洭锝炴径鎰瀭闁秆勵殔閺嬩胶鈧箍鍎遍ˇ顖滅矆鐎n偁浜滈柟鑸妼婢у弶绻濋埗鈺佷壕闂傚倸鍊搁崐鐑芥嚄閼哥數浠氶梻浣瑰濞插繘宕曢悽绋跨畺鐟滄棃骞冮埡鍛殥闁靛牆鎳愰妶锕傛⒒娴e摜绉洪柛瀣躬瀹曘垼銇愰幒鎴狅紱闂佸憡绋戦悺銊╂偂閺囥垺鐓欓柟浣冩珪濞呭懎鈹戦垾铏仴闁哄被鍔岄埥澶娾枎閹寸偛鍨辨繝娈垮枛閿曘劌鈻嶉敐鍥潟闁圭儤鍤﹂悢鍏煎€婚柍鍝勫€搁娲⒒閸屾瑧顦﹂柛鐔锋健瀹曟煡寮婚妷锕€浜遍梺鍦亾閸撴岸宕甸弴鐔翠簻闁规澘澧庨幃鑲╃磼閳锯偓閸嬫捇姊绘担瑙勫仩闁稿寒鍨跺畷婵囨償閵娿儱鍋嶉梺鍛婎殘閸嬫劙寮ㄦ禒瀣厽闁归偊鍘界紞鎴︽煟韫囥儳鐣遍柣锝嗙箞閺佹劙宕ㄩ闂存樊婵°倗濮烽崑鐐恒€冩繝鍥х畺闁冲搫鍟扮壕鍏间繆椤栨粌甯堕悽顖涱殜濮婂宕掑▎鎴М闂佽绻戠换鍫ャ€侀弽顓炲窛閻庢稒锚閳ь剙鐖奸幃妤€鈽夊▍铏灴瀹曪綀绠涢幘顖涙杸闂佺粯蓱瑜板啴寮抽悙鐑樼厪闁搞儯鍔庣粻鏍煏閸パ冾伃濠殿喒鍋撻梺鏂ユ櫅閸熶即藝閻楀牏绡€缁剧増菤閸嬫挸鐣烽崶褏鍘介柣搴ゎ潐濞插繘宕濋幋锔衡偓浣肝旈崨顓狅紲濠电偞鍨跺玻鍧椝囨导瀛樷拻闁稿本鑹鹃埀顒佹倐瀹曟劖顦版惔锝囩劶婵炴挻鍩冮崑鎾垛偓瑙勬磸閸庢娊鍩€椤掑﹦绉靛ù婊嗘硾閵嗘帗绻濆顓犲幈閻熸粌閰i妴鍐川閺夋垵鐎梺绋跨灱閸嬬偤鍩涢幋鐐簻闁瑰搫妫楁禍鍓х磽娴e壊妲归柟鍛婂▕楠炲啴骞愭惔娑樹簼闂佸憡鍔忛弲婵嬪储闁秵鈷戦悷娆忓缁€鍐倶韫囷絼閭い銏$懄瀵板嫰骞囬鐘插箞闂佽鍑界紞鍡涘磻閸涱垯鐒婃い鎾卞灪閻撳啴鏌﹀Ο渚▓婵″弶鎮傞弻宥囨嫚閺屻儺鈧鏌嶇拠鎻掝劉闁诡垱妫冮弫鎰板醇閵忋埄鍞规繝鐢靛Х閺佸憡鎱ㄩ悜钘夋瀬闁归棿绀佺壕缁樼箾閹存瑥鐏柛瀣儔閺屾稑鈽夐崡鐐典哗闂佹悶鍔嶇换鍐崲濞戙垹骞㈡俊顖濐嚙绾板秹姊洪挊澶婃殶闁哥姵鐗犲濠氬Ω閵夈垺鏂€闂佺硶妾ч弲婊呯懅缂傚倸鍊烽懗鑸垫叏閻㈢數鐭欓柟鐑橆殔妗呴梺鍛婃处閸ㄤ即宕橀埀顒勬⒑闂堟稈搴峰┑鈥虫搐閳绘捇濡堕崨顏呮杸濡炪倖娲栧Λ娑氱矈閻戣姤鐓曢柕濞垮妼閸氳淇婇崣澶婂妤犵偞岣块埀顒佺⊕閿氭い搴㈡崌濮婃椽宕ㄦ繝鍕暤闁诲孩鑹鹃幊姗€寮幘缁樺亹鐎规洖娲ら獮鍫熺節瀵伴攱婢橀埀顒佹尵缁牊绗熼埀顒勫春閵忋倕鍗抽柣姗嗗亜娴滅偓绻涢崼婵堜虎闁哄闄勯妵鍕即閸℃绁╅柡浣告喘閺屾稖绠涢弴鐐蹭粯缂備礁澧庨崑銈夊箖濡ゅ懏鏅查幖瀛樼箘閺佹牕鈹戦敍鍕闁哥姵鐗犻崺鐐哄箣閿旇棄浜瑰銈嗘閸嬫劖瀵奸崶顒佲拺缂侇垱娲樺▍鍡涙煟濡ゅ啫浠辨鐐搭殜椤㈡洟濡堕崶鈺嬬床婵犲痉鏉库偓鎾剁矆娓氣偓閹﹢鏁冮埀顒冨絹闂佹悶鍎滃鍫濇儓濠电姷顣介埀顒€纾崺锝団偓瑙勬礋娴滃爼宕洪敓鐘茬<闁靛牆鎳忛崐鏇炩攽閻樺灚鏆╅柛瀣洴閹椽濡歌閸ㄦ繄鈧箍鍎遍ˇ浼村磻閿熺姵鐓冮弶鐐村閸忓矂鏌¢崱顓犵暤闁哄被鍔戦幃銏ゅ传閸曟垯鍨荤槐鎺楁偑閳ь剟宕抽敐澶婅摕闁挎洍鍋撻摶锝呫€掑鐓庣仭閺佸牊绻濈喊妯峰亾閾忣偀鏋欓梺鍛婃尵閸犲酣锝炶箛鎾佹椽顢旈崨顖氬Х闂備胶绮崝妯间焊椤忓棌鍋撳顓熺凡妞ゎ叀鍎婚¨渚€鏌涢妸銉у煟鐎殿喖顭峰鎾閻橀潧鈧偤鎮峰⿰鍐фい銏℃椤㈡﹢鎮ゆ担璇″晬闂備胶绮崝鏍п缚濞嗗緷褰掝敊缁涘顔旈梺缁樺姇濡﹪宕曡箛娑欑厓閻熸瑥瀚悘瀵糕偓瑙勬礃閿曘垺淇婇幖浣肝ч柛婊€鐒﹂ˉ锟犳⒒閸屾艾鈧绮堟担铏圭濠电姴浼e☉姘磯闁靛ě鍛姸濠电偞鎸婚崺鍐磻閹惧灈鍋撶憴鍕缂傚秴锕ら悾鐑藉箳閹存梹顫嶅┑顔角规禍顒€危閸ヮ剚鈷掗柛灞捐壘閳ь剚鎮傞幃褎绻濋崟顓犵厯闂佸湱鍎ら〃鍛婵傚憡鐓忓┑鐐茬仢閸擃參鏌i悢绋款棎闁割偒浜弻娑㈠即閵娿儱绠婚梺缁樻尫缁舵艾顫忓ú顏咁棃婵炴垶鐟﹂幃娆撴煟鎼淬垹鍤柛銊ョ-閸掓帞鎷犲ù瀣潔闂侀潧绻掓慨鐑筋敊閹烘鈷戠憸鐗堝俯閺嗘帗淇婇悙鏉戠婵″弶鍔曢埞鎴犫偓锝庡亐閹风粯绻涙潏鍓у埌闁硅绻濆畷顖炴倷閻㈠灚锛忛梺鍝勵槼濞夋洘鏅ラ梻浣筋嚃閸犳洟宕¢崘宸殨闁靛ǹ鍎抽弳瀣煥閻曞倹瀚� Application Scientist闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁诡垎鍐f寖闂佺娅曢幑鍥灳閺冨牆绀冩い蹇庣娴滈箖鏌ㄥ┑鍡欏嚬缂併劎绮妵鍕箳鐎n亞浠鹃梺闈涙搐鐎氫即鐛崶顒夋晬婵絾瀵ч幑鍥蓟閻斿摜鐟归柛顭戝枛椤牆顪冮妶搴′簼缂侇喗鎸搁悾鐑藉础閻愬秵妫冮崺鈧い鎺戝瀹撲礁鈹戦悩鎻掝伀缁惧彞绮欓弻娑氫沪閹规劕顥濋梺閫炲苯澧伴柟铏崌閿濈偛鈹戠€n€晠鏌嶆潪鎷屽厡闁汇倕鎳愮槐鎾存媴閸撴彃鍓卞銈嗗灦閻熲晛鐣烽妷褉鍋撻敐搴℃灍闁绘挻娲橀妵鍕箛闂堟稐绨肩紓浣藉煐濮樸劎妲愰幘璇茬闁冲搫鍊婚ˇ鏉库攽椤旂》宸ユい顓炲槻閻g兘骞掗幋鏃€鐎婚梺瑙勬儗閸樺€熲叺闂傚倸鍊风粈浣革耿闁秴鐓曢柛顐犲劚绾捐鈹戦悩鎻掆偓濠氬汲閿斿浜滈柡宥庡亜娴狅箓鏌涚€n偄濮嶉柟顔肩秺瀹曞爼顢旈崟顓燁嚄闂備焦瀵х粙鎺楁儎椤栨凹娼栨繛宸簼閸嬶繝鏌℃径濠勬皑闁圭ǹ鍟扮槐鎾寸瑹閸パ勭彯闂佹悶鍔岄悥濂哥嵁閸愵喖鐏抽柡鍌樺劜閻庡姊虹憴鍕棎闁哄懏鐟ч懞杈ㄧ節濮橆厸鎷洪梺鍛婄箓鐎氼喛鈪归梻浣告啞閺屻劑鏌婇敐澶婃槬濠电姴娲ら崡鎶芥煏韫囥儳纾块柛妯圭矙濮婅櫣鎲撮崟顐㈠Б閻庤娲﹂崜鐔风暦濠靛鏅濋柛灞剧〒閸樻悂鏌h箛鏇炰户闁稿鎸剧划鍫⑩偓锝庡厴閸嬫挾鎲撮崟顒傤槬閻庤娲﹂崜婵嬫倶閹烘鈷戦柟顖嗗懐顔囧┑鐘亾闂侇剙绉寸粻鐘绘煛瀹ュ骸浜炵痪鍙ョ矙閺屾稓浠﹂崜褎鍣銈忚闂勫嫰濡甸崟顖氱婵犻潧娲ゅ▓妤呮⒑鏉炴壆顦﹂柛鐔告尦瀵偊宕橀鑲╋紲濠电偞鍨惰摫闁汇倕鎳樺娲传閸曞灚笑闂佺粯顨呯€氭澘鐣峰┑鍥ㄥ劅闁靛ǹ鍎抽崢娲⒑閸濆嫭鍌ㄩ柛銊︽そ閹繝鎮㈤崨濠傚伎濠碘槅鍨伴幖顐︽嚋閻熸噴鐟扳堪鎼淬埄娼ゞ Develop缂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁绘劦鍓欓崝銈囩磽瀹ュ拑韬€殿喖顭烽幃銏ゅ礂鐏忔牗瀚介梺璇查叄濞佳勭珶婵犲伣锝夘敊閸撗咃紲闂佺粯鍔﹂崜娆撳礉閵堝洨纾界€广儱鎷戦煬顒傗偓娈垮枛椤兘寮幇顓炵窞濠电姴瀚烽崥鍛存⒒娴g懓顕滅紒璇插€块獮澶娾槈閵忕姷顔掔紓鍌欑劍宀e潡宕㈡潏銊х瘈闁汇垽娼у瓭闂佺ǹ锕ょ紞濠傜暦閹达箑唯闁冲搫鍊婚崢鎼佹煟韫囨洖浠╂い鏇嗗嫭鍙忛柛灞惧閸嬫挸鈻撻崹顔界彯闂佸憡鎸鹃崰搴ㄦ偩閻ゎ垬浜归柟鐑樼箖閺呪晠鏌i悢鍝ユ噧閻庢凹鍓熼幆渚€鏌嗗鍡忔嫽闂佺ǹ鏈悷褔宕濆鍡曠箚闁绘劕寮堕崑銉р偓瑙勬磸閸ㄨ櫣绮嬮幒鏂哄亾閿濆骸浜滃ù鐙€鍙冨娲礃閸欏鍎撻梺鐟板暱闁帮綁骞忛幋锔藉亜闁稿繗鍋愰崢浠嬫⒑閸濆嫬鈧棄鈻旈弴鐐╂灁闂侇剙绉甸悡娑㈡倵閿濆簼閭柛娆忓閹便劍绻濇担铏圭厯閻庤娲栭悥濂搞€佸Δ浣哥窞閻庯綆鍋呴悵銊╂⒑閼姐倕鏋戠紒顔肩灱缁棃宕奸弴鐐电厬闂佸憡渚楅崣搴°€掓繝姘厪闁割偅绻冮ˉ鐐烘倶韫囷絼閭柡灞剧洴婵℃悂濡烽敃浣侯攨缂傚倷绶¢崰鏍€﹀畡鎵殾闁绘垹鐡旈弫鍥煟閺冨牊鏁遍柣搴ㄧ畺濮婄粯鎷呴搹鐟扮濡炪們鍔岄幊姗€骞冭瀹曞崬螣鐏忔牗鏁垫俊鐐€栭悧婊堝磻閻愮儤鍋傛繛鎴炩棨瑜版帗鏅查柛銈堟缂嶅﹤顕i幎鑺ユ櫜濠㈣泛顑囬崢鎼佹煟韫囨洖浠ч柛瀣尵缁牏鈧綆鍏橀崑鎾舵喆閸曨剛顦梺鍛婎焼閸パ呭幋闂佺鎻粻鎴︾嵁閵忋倖鐓冮弶鐐村椤︼箓宕鐐粹拻闁稿本鑹鹃埀顒佹倐瀹曟劕鐣¢幊濠傜秺瀹曞爼顢楁担瑙勵仧闂備線娼чˇ顐﹀疾濞戞艾顥氶悷娆忓缁♀偓闂傚倸鐗婄粙鎺楁晬瀹ュ棛绠鹃柛蹇氬亹婢х敻鏌$仦鐔锋閻も偓濠殿喗锚閸氬绱為崼銉︾厽閹兼番鍨婚。鑼偓鍏夊亾闁归棿绀侀拑鐔兼煟閺冨洦顏犵痪鎯у悑娣囧﹪顢涘┑鍥モ偓鍐煕閹烘埊韬慨濠冩そ瀹曘劍绻濋崘顏勫汲婵$偑鍊х粻鎺撶椤掆偓鍗遍柟鐗堟緲缁犲鎮楀☉娅亪顢撻幘缁樷拺闁告稑锕ョ亸鎵喐閺夊灝鏆g€规洘绮撻弻鍡楊吋閸℃瑥骞楅梻渚€娼х换鍡涘疾濞戙垺鍊堕柨婵嗩槹閻撴洟鏌eΟ铏癸紞濠⒀呮暬閺岋絽鈽夐崡鐐寸亪闁剧粯鐗犻弻娑樷堪閳ь剟鎮為敃鍌氱柧婵犻潧顑嗛埛鎴︽煙缁嬫寧鎹g紒鐘虫尰缁绘稓浠﹂崒姘潎闂佽鍨欢姘暦閻撳簶鏀介柛鎰ㄦ櫆閺夋悂姊绘担铏瑰笡闁告梹岣挎禍绋库枎閹邦厽鐝烽梺鍝勬储閸ㄦ椽鎮¢悢鑲╁彄闁搞儯鍔嶉埛鎺旂磼閻橀潧浠遍柡宀€鍠栭、娆撳棘閵堝牃鍋撻崸妤佺厵妞ゆ棁顫夊▍濠囨煙椤旂晫鎳囨鐐差儔楠炴帡寮崒娑欐珤闂傚倸鍊搁崐椋庣矆娓氣偓楠炴牠顢曢埛姘そ婵偓闁靛牆鎳愰ˇ顕€鏌h箛鏇炰户闁烩剝妫冨畷鐢稿即閻旂繝绨婚梺鍝勬处椤ㄥ懏绂嶆ィ鍐┾拺闁告繂瀚﹢浼存煟閳哄﹤鐏︾€规洘妞介幃娆撳传閸曨厾鏆伴柣鐔哥矊閺堫剛绮╅悢鐓庡嵆闁绘劏鏅滈弬鈧梻浣瑰缁嬫垹鈧凹鍓氱粋宥嗙附閸涘﹦鍘辨繝鐢靛Т閸熺増鏅堕鍛簻闁哄倽娉曠粻鑼磼缂佹ḿ绠撴い顐g箞椤㈡宕掗敂鎯ц€块梻鍌氬€峰ù鍥綖婢舵劕纾块柧蹇e亝濞呯娀骞栨潏鍓у埌妞ゃ儲鑹鹃埞鎴﹀磼濮橆厼鏆堥梺缁樻尵閸犳劖绌辨繝鍥舵晬婵ê褰夐搹搴ㄦ⒑濮瑰洤濡芥俊鐐舵椤曪綁顢曢敃鈧柋鍥煏婢舵稓鐣遍柍褜鍓涢弫濠氬箖瀹勬壋鏋庨煫鍥ㄦ惄娴犲墽绱撴担鎻掍壕闂佸憡鍔忛弲婵堢不妤e啯鐓曟繛鍡楁禋濡附銇勮箛鎾愁伀妤犵偞鎹囬弻銈夊箛娴e摜浠梺姹囧€愰崑鎾寸節閻㈤潧浠﹂柛銊ㄦ硾閻滃宕稿Δ鈧崒銊╂煙闂傚鍔嶉柍閿嬪灩缁辨帞鈧綆鍋勯婊勭節閳ь剚瀵肩€涙ḿ鍘鹃梺鑽ゅ枑濠㈡﹢鍩涢弮鍫熺厾婵炲樊浜欓幉鎯р攽閿涘嫬鍘撮柛鈺嬬節瀹曟帒螖娴e壊浼滃┑鐘垫暩閸嬬娀骞撻鍡楃筏濞寸姴顑呯粻鐔兼煥濞戞ê顏悗姘煼閺屻劑鎮㈤崫鍕戯綁鏌i幘瀛樼妤犵偞鐗滈埀顒佺⊕宀e潡鍩ユ径鎰厓鐟滄粓宕滃顑炴椽鎮㈤崗鍏兼珳闂佺粯鍔曟晶搴ㄦ偪閳ь剟姊洪崫鍕殭闁稿﹤顭烽幆渚€宕煎┑鍐╂杸濡炪倖姊归弸缁樼瑹濞戙垺鐓曟俊顖涗航閸嬨垻鈧娲樼划蹇涘Φ閹版澘绠抽柟缁㈠灡鐎氳偐绱撻崒娆戣窗闁搞劌宕叅闁哄秲鍔嶅▍鐘绘煕濞嗗浚妲跺ù婊勭矒閺屾洘绻涢崹顔煎Б缂備胶濮撮…鐑藉蓟閻旂⒈鏁婇柛婵嗗娴煎牓鎮楃憴鍕鐎规洦鍓熼崺銉﹀緞婵炵偓鐎婚梺鐟扮摠缁诲倻绮绘繝姘拻闁稿本鐟чˇ锔剧磽瀹ュ拑宸ラ摶鐐烘煕瑜庨〃鍡涘磹閸ф鐓ラ柡鍥殔娴滈箖姊虹€圭姵顥夋い锔藉▕钘濋柡灞诲劜閻撳啴鎮峰▎蹇擃仼闁诲繐鐡ㄩ妵鍕閿涘嫭鍣伴梺纭呮珪閻楃娀宕洪埄鍐╁闁圭粯甯掔欢褔姊婚崒姘偓椋庣矆娓氣偓楠炴牠顢曢敃鈧€氬銇勯幒鎴濃偓濠氭儗濞嗘挻鐓欓柟瑙勫姦閸ゆ瑩鏌i幒鎴犱粵闁靛洤瀚伴獮鎺楀箣椤栨艾顫犻梻浣告啞鐢顭垮鈧垾锕傛嚄椤栵絾些婵犵數鍋為幐鎶剿夐幘璇茬闁圭儤顨呯猾宥夋煕椤愵偄浜濋柡鍜佷邯濮婃椽鏌呴悙鑼跺濠⒀冾嚟閳ь剚顔栭崰鏍€﹂悜钘夋瀬鐎广儱顦粈瀣亜韫囨挻鍣瑰┑顖欏嵆濮婄粯鎷呴崨濠傛殘闂佸湱枪濡繂鐣烽悢纰辨晝闁靛浚婢€閻㈢粯绻濋悽闈浶ラ柡浣告啞閹便劑鎮滄慨鎰ㄥ亾閸岀儐鏁婇柣鎰靛墻濞肩喖姊洪崫鍕偍闁搞劌缍婇幏鎴︽偄婵傚鍞甸梺鍏兼倐濞佳勬櫠閺屻儲鐓曢柕澶樺枛婢ь噣鏌﹂崘顏勬灈闁哄本娲樺鍕槈濮楀棙鍠橀梻浣告啞閿氱€规洦鍓熼崺鐐哄箣閿曗偓閻擄繝鏌涢埄鍐炬畼濞寸姵娼欓埞鎴︽倷閸欏鐝旂紓鍌氱С缁舵岸鎮伴鍢夋棃宕ㄩ闂存睏闂備焦妞块崑鎺楀礈濞嗘挻鐓€闁挎繂鎳愰弳锕傛煙椤栫偛浜版俊缁邯濮婃椽宕ㄦ繝鍐f嫽闂佸摜濮甸幐鎯i幇鏉跨闁规儳顕粔鍫曟⒑闂堟胆褰掑磿閼碱剚瀚氶柣鎰嚟缁♀偓濠电偛鐗嗛悘婵嬪几閹剧粯鐓曢悗锝庡亝瀹曞本鎱ㄦ繝鍛仩缂佽鲸甯掕灒闊浄绲肩花钘夘熆鐟欏嫭绀嬫い銏∩戦獮濠偯瑰⿰鍐Ш妤犵偞鐗曡彁妞ゆ巻鍋撳┑鈥茬矙閺屽秹鏌ㄧ€n亞鐟ㄩ梻鍥ь樀閺屻劌鈹戦崱妯烘闂佸摜鍠撻崑銈夊蓟閻旂⒈鏁嶆慨妯哄船閳敻姊洪崫鍕効缂佺粯绻傞悾閿嬬附閸撳弶鏅濋梺闈涚箳婵厼岣块崜褏纾介柛灞剧懅鐠愪即鏌涢悩鎰佹疁闁诡喚鍏橀崺锟犲川椤栨氨銈﹂梻浣告贡閸庛倝宕甸敃鍌氱睄闁割偅绻勯崝锕€顪冮妶鍡楃瑨闁稿﹦绮粙澶婎吋閸℃ê寮垮┑鈽嗗灠閻忔繈鎮¢幇鐗堢厽闁规儳顕ú鎾煛鐏炲墽娲存鐐叉喘閸┾剝鎷呴崜鑼偓宄扳攽閻橆偅濯伴柛鏇ㄥ幗閸掓盯姊洪崫鍕効缂佺粯绻傞悾鐑筋敂閸涱喖顎撶紓浣割儏缁ㄩ亶骞忛锔解拻濞达絽鎲¢幆鍫ユ煛閸偄澧撮柟顖氬椤㈡稑顫濋悡搴㈩吙闂備礁婀遍搹搴ㄥ窗閺嶃劌鍔旈梻鍌欑窔濞佳囁囬銏犵?闂侇剙绋侀弫鍡樼節婵犲倻澧涢柍閿嬪笒闇夐柨婵嗘噺閸熺偤鏌熼崣澶嬪€愰柡灞剧〒閳ь剨缍嗛崜娆愮濠婂嫨浜滄い蹇撳閺嗭綁鏌熺粙鍖℃敾鐎垫澘瀚灒闁煎鍊楅埢澶岀磽閸屾艾鈧悂宕愰悜鑺ュ€块柨鏇氱劍閹冲苯鈹戦悩鎰佸晱闁搞劑浜堕獮鎰板箮閽樺鎽曞┑鐐村灦鑿ら柡鈧禒瀣厱闁哄洢鍔屾禍婊冣攽椤斿搫鐏ǎ鍥э躬婵″爼宕卞Ο閿嬪濠电儑绲藉ú銈夋晝椤忓牆绠栨繛鍡樻惄閺佸倿鏌涢弴妯哄濞存粓绠栭弻鐔告綇閸撗呮殸缂佺偓鍎冲ḿ锟犲蓟閿涘嫪娌悹鍥ㄥ絻婵海绱撴担鍝勑¢柛妤佸▕瀵濡堕崱妯哄伎闂佸綊鍋婇崗姗€宕戦幘璇插唨鐟滃繘寮抽敃鍌涚厱婵炲棗娴氬Σ铏圭磼閻樿崵鐣洪柡宀€鍠撻埀顒佺⊕宀e潡骞婇崘顔界厽闊洤锕ュ▍濠囨煛瀹€瀣М妤犵偞甯¢獮瀣偐鏉堚晠鈹忛梻鍌欑窔濞佳兠洪妶鍥e亾濮橆偄宓嗛柣娑卞櫍楠炴帒螖閳ь剛绮婚敐鍡欑瘈闁割煈鍋勬慨鍐煟閵夘喕閭慨濠勭帛閹峰懘鎼归悷鎵偧闂備礁婀辨灙妞ゎ厾鍏橀獮鍡涘礋椤栵絾鏅梺缁樺姌鐏忔瑩鎮鹃崫鍕ㄦ斀妞ゆ柨顫曟禒婊堟煕鐎n偅宕岄柡宀€鍠栭、娆撴偩鐏炴儳娅楅梻浣瑰缁嬫帡宕濋弴銏犵厴闁硅揪绠戦獮銏℃叏濡も偓濡寮崘娴嬫斀闁绘ê鐏氶弳鈺佲攽椤旀儳鍘撮柕鍡楀€圭粋鎺斺偓锝庝簽閸旓箑顪冮妶鍡楃瑨闁哥噥鍨堕幃鐢割敂閸喓鍘遍柣搴祷閸斿矂宕濋敃鍌涚厸鐎光偓鐎n剛锛熸繛瀵稿缁犳捇骞冮崜褌娌繝闈涘閸旀粓鏌曢崶褍顏い锕佷含缁辨帡鎳滈棃娑樻懙閻庢鍠涢褔鍩ユ径鎰潊闁绘ɑ顔栭崯瀣⒒娴e憡鍟炴い銊ョ墦瀹曟垵鈽夐埗鈹惧亾閺嶎偀鍋撻敐搴″缁炬崘妫勯湁闁挎繂妫楅悘濠囨煕濮樼厧浜伴柡灞剧〒閳ь剨绲婚崝宀勫焵椤掍焦绀嬮柟顕€绠栭幃婊堟寠婢跺矈鏀ㄩ梻浣虹帛閸斿繘寮插⿰鍫稏鐎广儱鎳夐弨浠嬫煃閽樺顥滈柣蹇ョ秮閺屽秴鐣¢幍顔碱暫闁告浜堕弻銈夊传閵夛附姣勭紓浣叉閸嬫捇姊绘担鍦菇闁搞劏妫勫玻鑳槼缂佸倹甯掗オ浼村礋椤忓棛鐣炬俊鐐€栭崝褏绱為崱妞绘灁闁哄啫鐗婇ˉ鍡楊熆鐠轰警鍎愰柛娆忕箲娣囧﹪顢涘☉姗嗗殝缂佺虎鍙冪粻鏍蓟濞戞﹩娼╂い鎺戝€绘闂備礁鎼惌澶屾崲濠靛棛鏆﹂柛顐f礀鍞梺闈涳紡閸屾粍锛忛梻鍌氬€烽懗鍓佸垝椤栫偛绠伴柛婵勫劜瀹曟煡鏌熼悧鍫熺凡闁绘挻锕㈤弻鐔告綇妤e啯顎嶉梺绋匡功閸忔ê顫忔繝姘唶闁绘棁銆€濡晜绻濋姀锝庢綈婵炲弶鐗犻崺鐐哄箣閿旇棄鈧兘鏌涘▎蹇fЦ婵炲拑绲介埞鎴﹀煡閸℃ぞ绨肩紓浣筋嚙閻楀棝顢氶敐鍥ㄥ珰鐎瑰壊鍠栭幃鎴炵節閵忥絾纭炬い鎴濇喘瀹曪綁宕卞☉娆戝幗闁瑰吋鎯岄崹宕囩矓闂堟耽鐟扳堪閸涱厺娌紓浣稿€圭敮鈥崇暦椤愶箑唯鐟滃繘鏁嶅┑鍥╃閺夊牆澧界粔顒佺箾閸滃啰鎮奸柡渚囧枛閳藉濮€閿涘嫬骞楅梻浣稿暱閹碱偊鏁冮妶澶嬪€堕柨鏃傜摂濞堜粙鏌i幇顖e殝闂婎剦鍓熼弻鐔碱敊鐟欏嫭鐝栫紓渚囧枤閺佽鐣烽悜绛嬫晣闁绘﹢娼ч獮鈧┑鐘垫暩婵兘寮崨濠勭闁逞屽墯缁绘稒鎷呴崘鎻掓偐婵炴垶菤閺嬪酣鏌熼幑鎰彧閺夊牆鐗嗛—鍐Χ閸℃瑥顫х紓渚囧枛濞撮攱绔熼弴鐔侯浄閻庯綆鍋嗛崢閬嶆煟韫囨洖浠滃褌绮欓獮濠囧炊閵娿倗绠氶梺鍛婃寙閸愩劌绠i梻浣告惈閺堫剟鎯勯姘煎殨妞ゆ帒瀚粻浼村箹濞n剙鐏╅梻鍌ゅ灦濮婄粯鎷呴崨濠傛殘闁汇埄鍨遍〃鍫ュ极椤曗偓閺佹捇鎮╅鐟颁壕濞达絿纭跺Σ鍫ユ煏韫囧ň鍋撻弬銉ヤ壕闁绘垼濮ら悡鏇熺箾閸℃绠板ù婊勫缁辨帡鎮╅搹顐㈢3閻庢鍠涢褔鍩ユ径鎰潊闁绘ɑ褰冪粊顕€姊绘笟鈧ḿ褎鐏欓梺绋挎唉濞呮洜绮嬮幒妤€鐓涢柛鎰典簽閿涙繃绻涙潏鍓у埌闁圭⒈鍋婇、鎾诲箻閸撲胶锛滈梺鍦帛鐢帡鍩涢弮鍫熺厵妤犵偛鐏濋悘鈺呮煃鐟欏嫬鐏╅柍褜鍓ㄧ紞鍡涘磻閹烘嚦娑㈠礃閵娿垺鏂€闂佺粯鍔栧ḿ娆撴倶閿曞倹鐓熼柣鏇炲€婚悾鍨殽閻愭彃鏆欓柍璇查叄楠炴ḿ鍒掔憴鍕伖闂傚倷绀侀幉锛勬崲閸屾壕鍋撳鍗炲幋鐎规洘娲熼獮瀣攽閸愨晜鏉搁梻浣虹帛閸斿繘寮插☉娆戭洸濡わ絽鍟埛鎺懨归敐鍥╂憘闁搞倕鍟撮弻娑㈡偐閹颁焦鐤侀梺闈涙閸熸潙鐣烽妸鈺佺骇闁瑰濮撮獮鎺楁⒒娴g瓔娼愮€规洘锕㈤、姘愁樄鐎规洖缍婂畷鎺戔槈閺嶏妇鐩庨梻浣告惈閸燁偊宕愰悷鎵虫瀺闁哄洨濮甸崰鎰版⒑椤撱劎鐣遍柣蹇ラ檮閹便劍绻濋崟顓炵闂佺懓鍢查幊妯虹暦閵娾晜顥堟繛鎴炴皑妤旀俊鐐€戦崹娲偋閻樿尙鏆﹂柕濞р偓閸嬫挸鈽夊▍铏灥閳诲秹宕惰濞撳鏌曢崼婵囧櫧缂佺姳鍗抽弻锝呂旈埀顒勬晝椤忓嫮鏆﹂柟瀛樻儕閻旀哺褔宕堕敂鍓ф晨闂傚倷绀侀幖顐﹀磹閸︻厸鍋撶粭娑樻祫缂嶆牜鈧箍鍎遍ˇ浼存偂閻斿吋鐓涢柛灞炬皑娴犮垽鏌熼钘夌伌闁哄本鐩俊鍫曞川椤撶喐顔掗梻浣告惈閼活垳绮旈悷鎵殾妞ゆ劧绠戠粈瀣亜閹板墎鎮煎ù鐘茬灱缁辨捇宕掑▎鎴М閻庤娲﹂崜娆擃敋閿濆绀堝ù锝囨嚀鎼村﹤鈹戦悩缁樻锭闁绘妫濆鎼佸醇閻斿墎绠氬銈嗙墬缁嬫帡濡甸悢鍝ョ闁稿繒鍘ч悘瀛樻叏婵犲啯銇濇鐐寸墵閹瑩骞撻幒婵囩秵濠电姷鏁搁崑姗€宕犻悩璇茬倞闁靛鍨规禍楣冩煕濞戝崬鏋ら梻鍕缁辨帞鈧綆鍙庨崵锕傛煃閸濆嫬鏆為柛鐘冲姍閻擃偊宕堕妸锔绢槬濡炪們鍎查懝鎹愮亙闂佹寧绻傞幊搴ㄥ汲閻愮儤鐓熼柟鎯ь嚟濞叉挳鏌$仦鍓ф创濠碉紕鍏橀弫鎰板川椤撶儐娼涢梻鍌欐祰椤曆兠瑰顓狀洸妞ゅ繐鐗嗛拑鐔衡偓骞垮劚椤︿即鎮¢妷鈺傚€甸柨婵嗙凹缁ㄤ粙鏌i悢鏉戝婵﹤顭峰畷鎯邦檨婵☆垪鍋撻梻浣告惈鐞氼偊宕濆畝鍕厴闁硅揪绠戦獮銏℃叏濡も偓濡鈻撳▎鎾寸厽闁绘柨鎽滈惌灞筋熆瑜庨〃鍫ュ极椤曗偓楠炴帡骞婇崼鍡楁搐閽冪喖鏌曟径娑滃悅闁瑰嘲鎼—鍐Χ閸℃娼戦梺绋款儐閹稿墽妲愰幒鎾崇窞閻忕偟鍋撳В鍫ユ⒑鐠団€虫灀闁逞屽墯閺嬪ジ寮告惔銊︾厵閻庣數枪鏍¢梺鎸庣☉缁绘ê顫忓ú顏勪紶闁告洖鐏氱瑧闂備浇顕х换鎴犳崲閸儱绠犳繝濠傜墛閸嬶繝鏌熼崘璇у姛闁硅櫕鎹囬妶顏呭閺夋垵绐涘銈嗘寙閸曨剛妲樻繝纰夌磿閸嬫垿宕愰幋锕€绀夊┑鐘叉搐绾惧潡鏌i姀鈶跺湱绮婚弽銊х闁糕剝锚閻忥箓鎮楀顓熺殤闁规彃鎲¢幆鏃堝Ω閵夛妇鈧剚淇婇妶蹇曞埌闁哥噥鍨跺畷鎰版偨閸涘﹦鍘卞銈庡幗閸ㄥ灚绂嶅┑鍫㈢<闁煎摜鏁搁崣鈧梺璇″枟椤ㄥ懘锝炲┑瀣垫晝闁靛繒濮烽妶顕€姊绘担铏瑰笡濞撴碍顨婂畷鎶芥晲閸涱垱娈鹃梺鍓插亝濞诧箓寮崱妤婄唵閻犺桨璀﹂崕鎰箾閸涱厾鐒告慨濠勭帛閹峰懘宕ㄩ棃娑氱Ш闁诡垰鏈鍕偓锝傛櫇缁犳岸姊洪幖鐐插姶闁告挻绋戦悾鍨瑹閳ь剟寮婚弴锛勭杸閻庯綆浜栭崑鎾诲冀椤撶偟鍘遍梺鍦劋椤ㄥ棝鎮¢弴銏″€堕柣鎰絻閳锋棃鏌熼崘鍙夊櫤闁靛洤瀚伴弫鍌涚附閸涘⿴鈧秶绱撴担铏瑰笡缂佽鐗撳畷娲焵椤掍降浜滈柟鐑樺灥椤忣亪鏌i幒鏇炰汗闁逞屽墮缁犲秹宕曢柆宥呯疇闁规壆澧楅弲顒佺箾閹存瑥鐏柍閿嬪灴閹嘲鈻庤箛鎿冧患缂備讲鍋撻柛鎰ㄦ杺娴滄粓鏌¢崶褎顥滈柟铏姍閹矂宕卞☉娆戝幈濡炪倖鍔戦崐鏇㈠几閹达附鐓曟繛鍡楃箳缁犳煡鏌熸笟鍨閾绘牠鏌嶈閸撴瑨鐏嬪┑掳鍊曢幊搴ㄥ磼閵娧€鍋撶憴鍕婵炲眰鍔庢竟鏇熺鐎n偆鍘遍柣蹇曞仜婢т粙鍩ユ径鎰厱婵犻潧娲﹂妵婵嬫煛瀹€瀣?濞寸媴绠撻幃鍓т沪濠㈩厼鎳夐崑鎾舵喆閸曨剙顦╅梺绋款儏閿曘倝鎮鹃悜鑺ュ亜缁炬媽椴搁弲婵嬫⒑缂佹ɑ顥嗘繛鎾诡潐缁旂喖寮撮姀鈾€鎷洪梺缁樻尭鐎涒晠骞夐幖浣圭厸濞达綀顫夐崐鎰版煏閸℃鍤囩€规洩绲惧鍕暆閳ь剟鎯侀崼鐔虹瘈闁汇垽娼у瓭闂佺ǹ锕︾划顖炲疾鐠鸿 妲堥柕蹇ョ磿閸樹粙姊虹憴鍕姢妞ゆ洦鍙冮獮濠囧炊椤掍胶鍘搁柣蹇曞仧鏋褑灏欓埀顒€鐏氬妯尖偓姘煎幘閹广垹鈹戠€n亞顦板銈呯箰濞诧箓顢撳Δ鈧埞鎴︽晬閸曨偂鏉梺绋磕涢崨顓犵瓘闂佺粯鍔﹂崜娑氱不閹€鏀介柣妯哄级閹兼劙鏌﹂崘顏勬灈闁哄矉缍佸顕€宕掑Δ浣哥彵闂備浇妗ㄧ粈渚€鏁冮鍫濊摕闁挎繂顦粻濠氭煕閹邦剚鈻曢柛鏂款樀濮婅櫣绮欐惔鎾舵箙闂佹悶鍔岀壕顓炍i幇鏉跨閻庢稒锚椤庢捇姊洪幆褏绠抽柟铏尵缁參鏁嶉崟顓狅紳婵炶揪绲块悺鏃堝吹濞嗘劒绻嗘い鎰剁悼缁犳碍淇婇銈呮灈婵﹥妞藉畷顐﹀礋椤曞懏钑夐梻浣呵圭€涒晠鎮¢垾宕囨殾闁圭増婢橀崹鍌涖亜閹板墎鍒扮€殿喖鐏濋埞鎴︻敊缁涘鐣跺┑鈽嗗亝椤ㄥ﹪鎮伴鍢夋棃宕橀鍡床闂佽崵濮撮幖顐﹀箹椤愩倗妫憸鏃堝蓟閺囥垹鐐婄憸宥夘敂椤撶喆浜滈柕蹇婂墲缁€瀣攽椤旂懓浜鹃梻渚€娼х换鍫ュ春閸曨垰鑸圭憸鐗堝笚閳锋帒銆掑锝呬壕濠电偘鍖犻崶銊ヤ罕闂佺粯鍔楃换婵堟崲閸℃稒鐓曢柕澶樺枛婢ь喚绱掗悩闈涙瀾濞e洤锕俊鍫曞川椤斿吋顏犻梺鎼炲劜閹稿啿顫忓ú顏勫窛濠电姴鍟ˇ鈺呮⒑閸涘﹥灏扮紒瀣灥閻滃宕稿Δ鈧崘鈧銈嗘尵閸熷潡骞忔繝姘拺缂佸瀵у﹢浼存煟閻旀繂娉氶崶顒佹櫆闁伙絽鐬奸惁鍫ユ⒑闁偛鑻晶鎾煛鐏炶姤顥滄い鎾炽偢瀹曘劑顢涢妶鍥ф優闂傚倸鍊风欢姘缚瑜旈幃褔宕卞ù鏉挎喘椤㈡稑饪伴崨顒傜憹闂備礁鎼ˇ顖滆姳闁秴缁╁ù鐘差儐閻撶喐淇婇婵囶仩闁挎稑绉甸妵鍕晲閸℃瑥寮ㄩ梺鍝勭焿缂嶄線鐛鈧畷锟犳倷閹绘帩娼ラ梻鍌欑窔濞佳兠洪妶鍥e亾濮橆偄宓嗛柣娑卞枛铻i柛蹇曞帶绾绢垶姊洪悜鈺傛珕閻㈩垰娲畷鏇㈠箮閼恒儱鍓﹀銈呯箰閻楀棛绮婚弻銉︾厵闂侇叏绠戝鐐繆椤愩垹顏慨濠傤煼瀹曟儼顧佹俊顖楀亾闂備礁鎼悮顐﹀礉瀹€鍕厴闁硅揪绠戦獮銏′繆椤栨粌鍔嬫い蹇曞У娣囧﹪鎮欓鍕ㄥ亾閹达箑纾块弶鍫氭櫆瀹曟煡鏌熺€电ǹ浠ч柍鐟扮Т閳规垿鎮╅崣澶嬫倷缂備胶濮烽弫濠氬蓟閻斿吋鍊绘俊顖濐嚙绾板秹姊洪崫鍕棞闁绘鎸搁~蹇撁洪鍜佹濠电偞鍨堕悷锕傚箖濞嗘挻鐓熼幖娣灮椤e弶绻濋姀鈽呰€挎い銏″哺閺佹劖寰勬繝鍕靛晪婵$偑鍊栭弻銊ノi崼銉ョ厸闁告侗鍠氶崢顏呯節閵忥絾纭鹃柣妤€妫濆畷婵嬪Χ閸℃劒绨婚梺鍝勫暊閸嬫捇鎮介妞诲亾閹颁焦缍庣紓鍌欑劍钃卞┑顖涙尦閺屾稑鈽夊鍫濅紣闂佸搫妫楅悧鎾诲蓟閿濆顫呴柍杞拌兌娴狀厼顪冮妶鍐ㄥ闁绘鎸搁锝夘敃閿旂粯鏅梺閫炲苯澧寸€殿噮鍋婇獮妯肩磼濡桨姹楅梻浣告啞閻熴儵藝閹峰备鍙㈤梻鍌氬€搁崐宄懊归崶褉鏋栭柡鍥ュ灩缁愭鏌熼幆褏鎽犻柛娆忕箻閺屸剝寰勭€n亞鍔搁梺鍝ュ枎閹冲繒鎹㈠┑瀣棃婵炴垶鐟ラ崑宥嗙箾鐎涙ḿ鐭嬬紒顔芥崌瀵鎮㈤悡搴g暰閻熸粌绉归幊婊嗐亹閹烘挾鍘介棅顐㈡搐閿曘儱鈻嶆繝鍥ㄧ厸閻忕偟枪婢ф煡鏌熷畡鐗堝殗鐎规洦鍋婃俊鐑解€栭鍝勫闁宠鍨块、娆戞兜瀹勬澘顫犵紓鍌欑贰閸n噣宕归崼鏇犲祦闊洦绋戝婵嬫煛婢跺鐏ョ紒鎰⊕缁绘繈鎮介棃娴躲垽鏌涢悤浣镐喊鐎规洘绮撳畷褰掝敃閵堝洨妲囬梻浣圭湽閸ㄨ棄岣胯缁傛帒饪伴崼鐔哄幗濡炪倕绻愰崯顐㈢暤閸℃瑢鍋撶憴鍕缂佽鐗撻悰顔锯偓锝庝簴閺€浠嬫煕椤愩倕鏋戞い鏃€娲熷缁樻媴娓氼垱鏁梺瑙勬た娴滎亜顫忔禒瀣妞ゆ牗姘ㄩ敍娆撴⒑缂佹ê鐏卞┑顔哄€濋幃锟犳偐閻㈠灚锛忛梺鍝勵槸閻忔繈鎳滈悷閭︾唵鐟滄粓宕规潏鈺傚床婵炴垯鍨归柋鍥ㄧ節闂堟稑顏╁ù鐙€鍣e铏规嫚閳ヨ櫕鐏嶅銈冨妼閿曨亪骞冩导鎼晪闁逞屽墮閻g柉銇愰幒婵囨櫓闂佺粯鎸哥€垫帒岣垮☉妯锋斀闁挎稑瀚禍濂告煕婵炑冩噽绾捐姤鎱ㄥΟ鎸庣【缁绢厸鍋撻梻浣筋潐閸庣厧螞閸曨垰鍙婇柕澶涘缁犻箖鏌熺€涙ḿ鎳冮柣蹇婃櫇缁辨帡鎮崨顖溞滈梺鍝勭焿缁插€熺亽闂佺ǹ绻愰崥瀣掗崟顖涒拺闁圭ǹ娴烽埊鏇犵磼鐠囨彃鏆熼柟骞垮灩閳藉鈻庨幇顔拘ら梻浣告啞閹稿棝宕橀妸褍甯撴繝纰夌磿閸嬫垿宕愰妶澶婄;闁告稑鐡ㄩ崑瀣煟濡崵婀介柍褜鍏涚欢姘嚕椤曗偓瀹曠厧鈹戠€n亝鏆梻鍌欒兌缁垶寮婚妸鈺傚剭婵犻潧顑呯壕濠氭煙閹规劦鍤欓梺鍗炴喘閺岋繝宕堕埡浣圭亖闂佸憡鐟ュΛ婵嗩潖濞差亜浼犻柛鏇ㄥ墮椤︹晛顪冮妶鍐ㄥ闁瑰啿绻掔划瀣吋閸℃劕浜濋梺鍛婂姀閺備線骞忛悜妯肩闁哄鍨甸幃鎴︽煟閻旀繂鎳愰惌娆撴煠婵劕鈧澹曟總鍛婂仯闁搞儺浜滈惃鍝勵熆瑜濇俊鍥焵椤掍緡鍟忛柛锝庡櫍瀹曟垶绻濋崶鈺佺ウ闂佹悶鍎洪崜娆戠棯瑜旈弻娑⑩€﹂幋婵囩亾闂佺粯绋堥弲婊勭┍婵犲洦鍊锋い蹇撳閸嬫捇寮介‖顒佺洴瀹曟﹢濡告惔銏㈡创鐎规洖缍婇、娆撴倷閺屻儱寮板銈冨灪瀹€鎼佸春閳ь剚銇勯幒鎴濐仼闁藉啰鍠栭弻銊モ攽閸℃﹩妫¢梺绋挎捣閸犳牠寮婚弴銏犻唶婵犻潧妫崝澶岀磽閸屾氨孝闁绘妫濋崺鐐哄箣閿旇棄鈧兘鏌熺紒妯虹濡ょ姴娲ㄧ槐鎾寸瑹閸パ勭亶闂佺懓鎲¢幃鍌炲箖妤e啯鍊婚柦妯侯槸瀹撳棝姊洪棃娑氱濠殿喖鐗愰ˇ褰掓煛鐏炲墽鈽夋顏冨嵆閸┾偓妞ゆ帒鍊婚惌鍡椕归敐鍥┿€婇柡瀣⒐閵囧嫰骞囬崼鏇燁€嶉梺鎶芥敱閸ㄥ潡寮诲☉妯锋婵鐗婇弫鐐節閵忥絾纭鹃悗姘嵆瀵鈽夐姀鐘栤晠鏌ㄩ弴妤€浜惧銈冨劚椤戝洨妲愰幒妤婃晩婵炲棙鍎冲▓顓㈡⒑鐎圭姵顥夋い锔诲灦閸┿垺鎯旈埥鍡楁倯闂佸憡娲﹂崢鎯р枖閸ф鈷掗柛灞剧懄缁佺増銇勯銏╂Ц闁伙絽鍢茶灒閻炴稈鍓濋悘鍐ㄢ攽閻愭潙鐏﹀畝锝呮健楠炴濡烽妷銏℃杸闁圭儤濞婂畷鎰旀担鐟板伎闂佺粯鍨煎Λ鍕婵犳碍鐓熼柟閭﹀幒閼割亪鏌嶈閸撴瑩宕婊勫床婵犻潧顑呯壕濂告煏閸繃顥犵紒瀣╄兌缁辨捇宕掑顑藉亾閻戣姤鍊块柨鏇氱劍閹冲苯鈹戦悩鎰佸晱闁搞劋鍗抽、姘额敇閻樻剚娼熼梺鍦劋閺岋繝宕戦幘缁樻櫜閹肩补鈧尙鐩庢俊鐐€栧ú妯煎垝瀹ュ绠為柕濞炬櫆閺呮煡鏌涢埄鍐炬當妞ゎ偅甯掗埞鎴︻敊绾攱鏁惧┑锛勫仩濡嫰鎮鹃悜鑺ュ€荤紒娑橆儐閺咃絽鈹戦悙鏉戠仸闁荤喆鍎甸幃鐢告焼瀹ュ棌鎷绘繛杈剧到閹虫瑨銇愰幒婵囨櫈闂佸憡绋戦悺銊╁疾濠靛洢浜滈煫鍥ㄦ尭椤忔挳鏌涢妶鍡樼闁靛洤瀚伴獮鍥礈娴g儤娈哥紓鍌欒閸嬫捇鏌涢幇銊︽澓濞存粍绮撻弻锟犲磼濞戞﹩鍤嬪銈庡亜缁夊爼骞夐幖浣哥睄闁割偅绻嗛幗鏇炩攽閻愭潙鐏﹂懣銈嗕繆閹绘帞澧﹂柡灞剧☉閳诲酣骞囬妷褏绐楅梻浣告啞閸ㄧ數绱炴繝鍌ゆ綎闁惧繗顫夌€氭岸鏌$仦璇插姶闁逞屽墯椤ㄥ﹪寮婚悢鍝勬瀳闁告鍋橀崰濠囨⒑缁洘娅囬柛瀣ㄥ€濋悰顔锯偓锝庡枟閺呮粓鏌﹀Ο渚Т闁稿鎹囬幃婊堟嚍閵壯冨箞婵犵數鍋涘Λ妤€霉濮橆儵鐔煎醇閻斿墎绠氬銈嗗姦閸撴稓寮ч埀顒€鈹戦纭锋敾婵$偘绮欓悰顕€寮介鐔封偓鐑芥煙缂佹ê淇柣搴ゆ珪缁绘繈鎮介棃娴舵盯鏌涚€n偅宕岀€殿喖鐖煎畷鐓庘槈濡警鐎烽梻浣虹帛缁诲倿鎮ユ總绋胯摕闁跨喓濮撮悙濠囨煃鏉炴壆鍔嶉柣蹇庣窔濮婂宕掑顒変患闁诲孩鐭崡鍐差嚕鐠囨祴妲堟俊顖炴敱椤秴鈹戦绛嬫當闁绘妫欓幈銊モ槈閵忊檧鎷洪梺鍛婄☉鑹呯紓鍌涘哺閺屸剝鎷呯粵瀣濡炪値鍋勭换鎰弲濡炪倕绻愮€氼厼鐣靛鍜佹富闁靛牆妫欑亸闈涒攽椤旂⒈鍤熺紒顕呭弮閺佹捇鎮╁畷鍥у箺闂備線娼х换鍡涘疾濞戙垺鍊舵繛鍡樻尰閻撴盯鏌涘☉鍗炵仩鐎涙繈姊烘导娆戞偧闁稿繑锚椤曪綁骞橀纰辨綂闂佺粯岣块弫鎼佸级閹间焦鈷掑ù锝堟鐢稒銇勯妸銉﹀殗闁诡啫鍥у耿婵炴垶岣块崝锕€顪冮妶鍡楀潑闁稿鎹囬弻锝堢疀閺傚灝鎽靛Δ鐘靛仜閻楁挻淇婇幖浣肝ㄩ幖杈剧到閺嬫盯鏌熼鐟板⒉闁诡垱鏌ㄩ埞鎴﹀幢閳哄偆妫ラ梻鍌氬€峰ù鍥敋瑜忛埀顒佺▓閺呯娀骞冮姀銈庢晢闁告洦鍋嗛鍡涙⒑鐠恒劌娅愰柟鍑ゆ嫹>>
濠电姷鏁告慨鐑藉极閸涘﹥鍙忛柣鎴f閺嬩線鏌涘☉姗堟敾闁告瑥绻橀弻锝夊箣閿濆棭妫勯梺鍝勵儎缁舵岸寮诲☉妯锋婵鐗婇弫楣冩⒑閸涘﹦鎳冪紒缁橈耿瀵鏁愭径濠勵吅闂佹寧绻傚Λ顓炍涢崟顖涒拺闁告繂瀚烽崕搴g磼閼搁潧鍝虹€殿喖顭烽幃銏ゅ礂鐏忔牗瀚介梺璇查叄濞佳勭珶婵犲伣锝夘敊閸撗咃紲闂佺粯鍔﹂崜娆撳礉閵堝棎浜滄い鎾跺Т閸樺鈧鍠栭…鐑藉极閹邦厼绶炲┑鐘插閺夊憡淇婇悙顏勨偓鏍暜婵犲洦鍊块柨鏇炲€哥壕鍧楁煙閸撗呭笡闁抽攱鍨块弻鐔兼嚃閳轰椒绮舵繝纰樷偓鐐藉仮闁哄本绋掔换婵嬪磼濞戞ü娣柣搴㈩問閸犳盯顢氳閸┿儲寰勯幇顒夋綂闂佸啿鎼崐鐟扳枍閸ヮ剚鈷掑ù锝囨嚀椤曟粎绱掔拠鎻掆偓姝岀亱濠电偞鍨熼幊鐐哄炊椤掆偓鍞悷婊冪箳婢规洟鎸婃竟婵嗙秺閺佹劙宕ㄩ钘夊壍闂佸搫绉埀顒佹灱閺€浠嬫煟濮楀棗鏋涢柣蹇d邯閺屻劑寮村Ο铏逛紙閻庤娲樺浠嬪箖濞嗘挸浼犻柛鏇ㄥ弾閸氬懘姊绘担鐟邦嚋婵☆偂绀佽灋闁告洦鍓涢々鑼喐閻楀牆绗氶柛濠勬暬閹嘲鈻庤箛鎿冧痪缂備讲鍋撻柍褜鍓欓埞鎴︽倷鐎涙ḿ绋囬梺绋匡工閻忔繈顢氶敐澶婄闁兼亽鍎插▍銏ゆ⒑缂佹〞鎴﹀几婵傜ǹ绠柧蹇撴贡绾捐棄霉閿濆懎顥忛柛搴㈠姈閵囧嫰骞嬮悙鍨櫚閻庤娲樺ú婵堢不濞戙垹妫橀悹浣哥-閻╁酣姊绘担鐑樺殌闁宦板妿閹广垽宕橀銏狀樀閹晝绱掑Ο鐓庡箥婵°倗濮烽崑娑㈡倶濠靛鍊堕柍鍝勬噺閻撳啴鎮峰▎蹇擃仼闁诲繐顕埀顒冾潐濞叉牠鎮ユ總绋挎槬闁跨喓濮寸粈鍐┿亜韫囨挻濯兼繛鍏兼崌濮婂宕掑顑藉亾閻戣姤鍤勯柤鍝ユ暩娴犳岸姊绘担鍛婃儓闁绘绮撳畷婊冣槈閵忕姷顦梺鍦劋閸ㄥ綊寮抽崱娑欑厱闁哄洦顨嗛弶褰掓煕鐎n偅宕岀€规洘甯掕妞ゆ挾鍠愰妵婵囥亜閵忊剝顥堢€规洏鍔戦、鏃堝川椤撗傜椽濠电姷鏁告慨鐢割敊閺嶎厼绐楁慨妯挎硾缁犵娀鏌熼幑鎰滄繛宸簻鍥存繝銏f硾閿曪箓宕濋敃鈧—鍐Χ閸℃鐟愮紓浣哥亪閳ь剚鏋奸弸鏃€绻濇繝鍌涘櫝闁稿鎸鹃幉鎾礋椤掑偆妲伴梻浣规偠閸斿苯岣块敓鐘冲仒妞ゆ柨妲堥悢鐓庣闁绘挸娴疯ぐ鎾⒒娴e憡鍟為柣鐔村劦瀹曟垶绻濋崟顓濈瑝闂佽宕橀褔鎷戦悢鍝ョ闁瑰瓨鐟ラ悘鈺呮煕濡や礁鈻曢柡灞炬礃缁绘盯宕归鐓幮戝┑鐐差嚟婵參寮插┑鍫燁潟闁规儳鐡ㄦ刊鎾煕濠靛棗鐝旈柨婵嗩槹閻撶喖鏌嶉崫鍕跺伐闁诲骏濡囬埀顒侇問閸犳盯顢氳閸┿儲寰勯幇顒夋綂闂佸啿鎼崐鐟扳枍閸ヮ剚鈷掑ù锝囨嚀椤曟粎绱掔拠鎻掆偓姝岀亱濠电偞鍨熼幊鐐哄炊椤掆偓鎯熼梺闈涱樈閸犳鈧潧鐭傚娲濞戞艾顣洪梺纭呮珪閿曘垽銆侀幘婢勬棃宕橀鍡床濠电姰鍨煎▔娑㈠嫉椤掑嫬姹查柍鍝勬噺閻撴瑦顨ラ悙鑼虎闁诲繆鏅犻弻宥囨喆閸曨偆浼岄悗瑙勬礉缁墽绮诲☉銏犵睄闁稿本鐟ч幐澶愭⒒閸屾艾鈧绮堟担鍦彾濠电姴娲﹂崑鍌炴煕椤愮姴鍔氱紒鎰殕閹便劌顫滈崱妤€绠诲銈傛櫇閸忔﹢寮诲澶婁紶闁告洦鍓欏▍銈夋⒑閹惰姤鏁遍柛銊ユ健瀵鈽夊Ο閿嬵潔濠殿喗顨呴悧鎾舵鐎涙ḿ绡€闁靛骏缍嗗ḿ鎰版嫅闁秵鐓忛柛銉戝喚浼冨Δ鐘靛仜椤戝懘鍩為幋锕€鐐婇柤鍝ヮ暜妤犲繒绱撻崒姘偓椋庢閿熺姴绐楁俊銈呭暙閺嬪牏鈧箍鍎遍幊鍥╃磽濮樺墎鍙撻柛銉e妿閳藉骞嗛悢鍏煎仭婵犲﹤鍟扮粻濠氭煙椤栨瑧绐旂€规洖銈告俊鐑芥晜鐟欏嫬顏归梻鍌欒兌椤㈠﹪宕戦幇鏉跨;婵炴垯鍨圭粈澶愭煙缂併垹鏋熼柣鎾跺枛閻擃偊宕堕妸锔规嫽濡炪値鍓欓崥瀣Φ閸曨垱鏅濋柍褜鍓涚槐鐐寸節閸パ嗘憰闂佹寧绋戠€氼亜鈻介鍫熺厱闁圭偓銇炵拋鏌ュ磻閹捐绠抽柟鐐藉妼缂嶅﹪骞冮鍫濆窛妞ゆ牗绮嶅▓濂告煟鎼淬値娼愭繛鍙夅缚閸掓帟绠涘ù鏉挎喘楠炴﹢顢欓悾灞藉箞婵犵數鍋涘Λ娆撳礉濡ゅ啰涓嶉柡宥庡亞绾捐偐绱撴担璐細缂佺姷鍋涢埞鎴︻敊閻熼澹曢梻鍌欑劍鐎笛呮崲閸屾壕鍋撳☉鎺撴珖缂佽京鍋ゅ畷鐓庘攽閸愨晜鏉搁梻浣虹帛閸旀ê鈻斿☉銏″剭婵炲樊浜濋悡鏇㈡煟濡崵鍙€闁告瑥瀚伴弻銊モ攽閸繀鍝楃紓浣哄У閻╊垰顕i幘顔藉亹缁炬澘顦辨惔濠傗攽閻樻鏆俊鎻掓嚇瀹曞綊鎮介崜鍙夋櫔閻熸粍妫冮妴渚€骞樼拠鑼啋闂佸憡鎸烽懗鍫曟晬濠靛洨绠鹃弶鍫濆⒔閸掔増绻濋埀顒勬焼瀹ュ懐鍙€婵犮垼娉涢鍐╃濠婂牊鐓欓悗娑欋缚缁犳牠鏌涢敐鍛Ш闁哄苯绉剁槐鎺懳熺拠鑼紦婵°倗濮烽崑娑樏洪銏犵畺鐟滄柨鐣烽悡搴僵妞ゆ挾鍎愭导鏍⒒閸屾艾鈧绮堟笟鈧獮澶愭晬閸曨厾澶勯梺绉嗗嫷娈旂痪鎯ф健瀵爼宕煎☉妯侯瀷婵犫拃鈧埀顒佹灱閺€浠嬫煥濞戞ê顏╁ù婊冦偢閺屾稒绻濋崘銊т紝閻庤娲樼换鍌炴偩濠靛绀嬫い鎰╁€楅弸鍐⒑绾懎顥嶉柟娲讳簽濡叉劙寮撮姀鐘宠緢闂侀潧鐗嗛ˇ浼存偂閺囥垺鐓涢柛銉e劚婵″ジ鏌h箛銉х瘈闁哄苯绉归弻銊р偓锝庝簽娴煎矂姊洪崫鍕拱缂佸鍨块崺鐐哄箣閿曗偓楠炪垺淇婇妶鍜冩闁诡噯绲炬穱濠囨倷椤忓嫧鍋撻弴鐏荤懓顫濈捄铏癸紱婵犵數濮村ú銈夋嫅閻斿吋鐓ユ繝闈涙婢с垽鏌i妶鍌氫壕闂傚倷娴囬~澶愬磿閹惰棄鐤悹鎭掑妽閺嗘粎绱掔悰鈩冩 Fisher闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ゆ繝鈧柆宥呯劦妞ゆ帒鍊归崵鈧柣搴㈠嚬閸欏啫鐣峰畷鍥ь棜閻庯絻鍔嬪Ч妤呮⒑閸︻厼鍔嬮柛銊ョ秺瀹曟劙鎮欓悜妯轰画濠电姴锕ら崯鎵不閼姐倐鍋撳▓鍨灍濠电偛锕顐﹀礃椤旇偐锛滃┑鐐村灦閼归箖鐛崼鐔剁箚闁绘劦浜滈埀顑惧€濆畷銏$鐎n亜鐎梺鍓茬厛閸嬪棝銆呴崣澶岀瘈闂傚牊渚楅崕鎰版煟閹惧瓨绀冪紒缁樼洴瀹曞崬螖閸愵亶鍞虹紓鍌欒兌婵灚绻涙繝鍥ц摕鐎广儱鐗滃銊╂⒑閸涘﹥灏伴柣鐔濆懎鍨濋悹鍥ф▕閸氬顭跨捄鐚村姛闁挎稓鍠栧缁樼瑹閸パ冾潻闂佸憡顨嗗ú鐔风暦閸洦鏁嗗璺侯儐濞呮牗绻濋悽闈浶㈤柨鏇樺€濋獮濠囧箛閻楀牆鈧灝鈹戦崒姘暈闁绘挾鍠栭獮鏍箹椤撶偟浠紓浣割槺閺佸寮诲☉姘e亾閿濆倹娅囬柛鏂跨Ф缁辨帡宕掑姣欍垺顨滈鍐ㄥ祮鐎规洖銈搁幃銏ゅ传閸曨偆顓奸梻鍌氬€烽懗鍫曘€佹繝鍥风稏濠㈣埖鍔曠粈澶愭煛瀹ュ骸浜濋柛蹇旂矊铻栭柨婵嗘噹閺嗙偤鏌i幘瀵告创闁诡喗顨婇弫鎰償濠靛浠愰梻浣告啞閻熴儳鈧矮鍗冲濠氭晬閸曨亝鍕冮梺鍛婃寙閸曨偄鐏℃繝鐢靛Х椤d粙宕滃┑瀣畺闁稿本绋愮换鍡涙煙闂傚顦﹂崶鎾⒑閸涘﹣绶遍柛鐘崇墵瀹曟粓鎮介悽鐢碉紳闂佺ǹ鏈懝楣冨焵椤掆偓閸㈡煡婀侀梺鎼炲劘閸斿﹥绂掗崼銉︾厵闂傚倸顕ˇ锔剧磼閻樺磭鍙€闁哄本鐩俊鐑藉箣濠靛洤娅ゅ┑鐐茬墦缁犳牕顫忓ú顏勬嵍妞ゆ挾鍋涙俊娲⒑閹肩偛濡块柛鐘崇墪椤曪綁宕ㄦ繝鍐ㄥ妳闂侀潧饪垫俊鍥储閻㈠憡鐓涘璺猴功婢ф洖顭胯缁瑩鐛崘鈺冮檮闁告稑锕﹂崢钘夆攽閻愭潙鐏﹂柣妤佹礋瀹曟繈鏁傞懞銉ュ伎婵犵數濮寸€氼喚鏁☉姘辩<婵°倕鍟弸娑㈡煕閳规儳浜炬俊鐐€栧濠氬磻閹惧磭鏆嗛柨婵嗘噺閸嬨儵鏌熺粵鍦瘈濠碘€崇埣瀹曞爼鍩℃繝鍐冿箓姊婚崒娆掑厡缁绢厼鐖煎畷婊冣攽閸垻鐓撻梺纭呮彧闂勫嫰鍩涢幒鎾变簻闁哄稁鍋勬禒锕傛煟閹惧崬鍔滅紒缁樼箞濡啫鈽夊▎妯伙紒闂備線娼荤徊鑲╁垝濞嗘挸钃熼柨鐔哄Т楠炪垺銇勯幘璺哄壉婵炲樊鍙冨娲偡閺夎法楠囬梺璇″枛閸婂潡鐛崘顓ф▌閻庤娲滈崢褔鍩為幋锕€閱囬柕蹇娾偓铏暟闂傚倸鍊搁崐鐑芥嚄閸撲礁鍨濇い鏍ㄧ矋閺嗘粓鏌i弮鍌氬付缁炬儳顭烽弻鐔兼偋閸喓鍑¢梺缁樺笒閻忔岸濡甸崟顖氱闁瑰瓨绻冮悘鎾斥攽閻愭彃鎮戦柛鏃€鐟╁濠氭偄閾忓湱鐓撻柣鐘充航閸斿矂鎮¢悢鍏煎€甸悷娆忓缁€鍐╃箾閼碱剙鏋庨柣锝囧厴閺佹捇鎮╅崘娴嬪亾閸撲胶纾藉ù锝堝亗閹达箑桅婵犻潧顑嗛悡娑樏归敐鍤藉綊鍩€椤掆偓濞尖€愁嚕婵犳艾惟闁冲搫锕ラ弲顒€鈹戦鏂や緵闁稿瀚拌棢婵﹩鍏橀弨浠嬫煟閹邦垰鐓愮憸鎶婂懐纾奸棅顐幘閻瑧鈧娲﹂崹鍫曘€侀弴銏℃櫜闁搞儴鍩栭柨銈夋煟閻斿摜鐭屽褎顨堥弫顔嘉旈崨顔间簵闂佸憡鍔︽禍婵嬪窗閹邦厾绡€濠电姴鍊绘晶鏇犵磼閳ь剟宕奸悢绋垮伎濠碘槅鍨伴妵姗€宕ラ锔界厽妞ゆ挾鍠撻幊鍥煛瀹€鈧崰鏍箖濠婂喚娼ㄩ柛鈩冡缚閺嗭箓姊绘担鍛婃儓闁瑰嘲顑嗙粋宥夘敂閸曞灚缍庣紓鍌欑劍宀e潡鎮疯ぐ鎺撶厓鐟滄粓宕滈悢鐓庢槬闁逞屽墯閵囧嫰骞掗幋婵冨亾閸涘﹦顩锋繝濠傜墛閻撶姵绻涢懠棰濆殭闁诲骏绻濋弻锟犲川閺夎法鍘柣搴濈祷閸嬫劙鍩€椤掍胶鈯曞畝锝呮健瀹曘垽鏌嗗鍡╂濡炪倖鍔戦崹鐑樺緞閸曨兛绻嗘い鎰剁到閻忔挳鏌熼搹顐e暗闁圭懓瀚版俊鎼佸閻樺崬顥氭繝鐢靛仜閻楀棝鎮樺┑瀣嚑婵炴垶鐟f禍婊勩亜閹捐泛孝闁告ê鐡ㄩ〃銉╂倷閹绘帗娈绘繝娈垮枓閸嬫挸顪冮妶搴′航闁告﹢绠栧畷婊堝Ω閿斿墽顔曢柡澶婄墕婢т粙宕氶悧鍫㈢瘈闁逞屽墯濞煎繘濡歌濞叉悂姊洪崫鍕枆闁告ü绮欓崺娑㈠箳閹炽劌缍婇弫鎰板吹閽樺绉洪挊鐔肩叓閸ャ劎鈯曢柣鎾跺枛閺岀喖骞嗚閿涘秴顭胯婵″洭鍩€椤掑喚娼愭繛鍙壝…鍨熺捄銊ょ胺闂傚倷绀侀幉鈩冪瑹濡ゅ懎绐楅柡宥庡幖閻掑灚銇勯幒鍡椾壕闂佺粯鐗曢妶绋款嚕婵犳碍鍋勯柣鎾虫捣椤︻參鎮峰⿰鍐闁轰緡鍠栭埥澶愬閿涘嫬甯楅梻鍌欑閻忔繈顢栭崨瀛樺€堕柍鍝勬噺閻撶喖鏌曟径妯烘灆闂侇収鍨遍妵鍕閳藉懓鈧潡鏌熼鐣屾噰鐎殿喖鐖奸獮瀣倻閸℃洜鏁鹃梻鍌氬€搁崐鐑芥嚄閸撲礁鍨濇い鏍ㄧ矋瀹曡尙鈧箍鍎卞Λ娑€€呴崣澶堜簻闊洦鎸炬晶鏇㈡煢閸愵亜鏋戠紒缁樼洴楠炲鈻庤箛鏇氭偅缂傚倷绶¢崑鍕矓瑜版帒钃熺€广儱鐗滃銊╂⒑閸涘﹥灏甸柛鐘崇墵閻涱噣宕橀钘夆偓濠氭煢濡警妲洪柛妯烘啞缁绘盯骞樼壕瀣棟濠电偛鐪伴崐鏇㈠煝閹捐惟闁挎柨澧介惁鍫ユ⒑濮瑰洤鐏叉繛浣冲嫮澧$紓鍌欒兌閸嬫挸顭垮Ο鑲╃煋闁荤喖鍋婇崵鏇㈡煛鐏炶鍔氶柦鍐枛閺屾洘寰勫☉姗嗘喘闂佸憡锚瀹曨剟鈥旈崘顔嘉ч柛鈩冾殔椤孩绻濆▓鍨灍闁瑰憡濞婇獮鍐潨閳ь剟銆佸璺虹劦妞ゆ帒瀚拑鐔兼煃閳轰礁鏆欑紒鍓佸仱閹鏁愭惔鈥茬盎闂侀€炲苯澧柛鏃€鐗犻獮鍫ュΩ閿斿墽鐦堥梺鍛婁緱閸n喗绂掗埡鍛拺闁荤喐婢樼痪褔鏌熺粙鍨毐闁伙絿鍏橀幃銏㈠枈鏉堛劍娅囬梻渚€娼х换鎺撴叏瀹€鍕婵犻潧鍟弬鈧梻浣虹帛閿曗晠宕戦崨顔煎灁濞寸厧鐡ㄩ悡鏇㈡煙娴煎瓨娑ч柡瀣〒閳ь剚顔栭崰妤€顭垮鈧垾鏃堝礃椤斿槈褔鏌涢幇鈺佸濞寸娀绠栧娲嚒閵堝懏鐝㈢紓浣哄У閸ㄥ潡銆佸璺何ㄩ柍杞拌兌椤︽澘顪冮妶鍡楃瑨闁稿﹤顭烽、娆撳即閵忊檧鎷虹紓鍌欑劍閿氬┑顕嗙畵閺屾盯骞橀弶鎴濇懙閻庢鍠栭悥鐓庣暦閵婏妇绡€濞达綀娅i悾楣冩⒒娴h櫣甯涢柛鏃撻檮缁傚秴饪伴崼婵堝姦濡炪倖甯婇懗鑸垫櫠椤忓懌浜滄い鎰╁灮缁犺尙绱掔紒妯肩畵妞ゎ偅绻堥、鏍煘閸喖濮﹂梺璇″枟椤ㄥ﹪寮幇顓熷劅婵犻潧娲ら弸銈夋⒒娴e憡鎲搁柛鐘查叄楠炲﹤顫滈埀顒€顕f繝姘嵆闁绘棃顥撶粣鐐测攽閻愭潙鐏︾紒顔奸叄钘濋柣妤€鐗忕粻楣冩倵濞戞瑡缂氶柣顓烆儑缁辨帡顢欓懖鈹冣攽閿涘嫭鏆€规洜鍠栭、娑橆潩妲屾牕鏅梻浣藉吹婵儳鈻嶉敐鍚ゆ椽宕ㄩ弶鎴綂闂侀潧鐗嗗Λ娑㈠储閸楃偐鏀介柍钘夋閻忥絿绱掗鍛仯濞存粍鎮傞弫鍐磼濞戞艾骞愰梺璇茬箳閸嬬喐鐏欐繝鈷€鍕弨闁哄瞼鍠庨悾锟犳偋閸繃鐣婚梻浣筋嚃閸犳岸宕楀Ο渚殨閻犻缚銆€閺嬪酣鏌i幇闈涘缂佸鐗撳濠氬磼濮橆兘鍋撳畡鎳婂綊宕堕澶嬫櫔闂佸搫绋侀崢鑲╃玻濡や椒绻嗛柕鍫濇噺閸f椽鏌涚€e墎绡€闁哄苯绉靛ḿ顏堝箯鐏炶棄甯梻浣告惈濡挳姊介崟顖毼﹂柛鏇ㄥ灠缁犳盯鏌涢幘鑼跺厡闁哄棛濮风槐鎾存媴閹绘帊澹曢梺璇插嚱缂嶅棝宕戞担鍦洸婵犲﹤鐗婇悡娆撴煙娴e啯鐝繛鍛嚇閺岋綀绠涢敐鍕仐闂佸搫鐭夌换婵嗙暦閸楃倣鏃堝礃椤忓秴鏁归梻鍌欑閻ゅ洭锝炴径鎰瀭闁秆勵殔閺嬩胶鈧箍鍎遍ˇ顖滅矆鐎n偁浜滈柟鑸妼婢у弶绻濋埗鈺佷壕闂傚倸鍊搁崐鐑芥嚄閼哥數浠氶梻浣瑰濞插繘宕曢悽绋跨畺鐟滄棃骞冮埡鍛殥闁靛牆鎳愰妶锕傛⒒娴e摜绉洪柛瀣躬瀹曘垼銇愰幒鎴狅紱闂佸憡绋戦悺銊╂偂閺囥垺鐓欓柟浣冩珪濞呭懎鈹戦垾铏仴闁哄被鍔岄埥澶娾枎閹寸偛鍨辨繝娈垮枛閿曘劌鈻嶉敐鍥潟闁圭儤鍤﹂悢鍏煎€婚柍鍝勫€搁娲⒒閸屾瑧顦﹂柛鐔锋健瀹曟煡寮婚妷锕€浜遍梺鍦亾閸撴岸宕甸弴鐔翠簻闁规澘澧庨幃鑲╃磼閳锯偓閸嬫捇姊绘担瑙勫仩闁稿寒鍨跺畷婵囨償閵娿儱鍋嶉梺鍛婎殘閸嬫劙寮ㄦ禒瀣厽闁归偊鍘界紞鎴︽煟韫囥儳鐣遍柣锝嗙箞閺佹劙宕ㄩ闂存樊婵°倗濮烽崑鐐恒€冩繝鍥х畺闁冲搫鍟扮壕鍏间繆椤栨粌甯堕悽顖涱殜濮婂宕掑▎鎴М闂佽绻戠换鍫ャ€侀弽顓炲窛閻庢稒锚閳ь剙鐖奸幃妤€鈽夊▍铏灴瀹曪綀绠涢幘顖涙杸闂佺粯蓱瑜板啴寮抽悙鐑樼厪闁搞儯鍔庣粻鏍煏閸パ冾伃濠殿喒鍋撻梺鏂ユ櫅閸熶即藝閻楀牏绡€缁剧増菤閸嬫挸鐣烽崶褏鍘介柣搴ゎ潐濞插繘宕濋幋锔衡偓浣肝旈崨顓狅紲濠电偞鍨跺玻鍧椝囨导瀛樷拻闁稿本鑹鹃埀顒佹倐瀹曟劖顦版惔锝囩劶婵炴挻鍩冮崑鎾垛偓瑙勬磸閸庢娊鍩€椤掑﹦绉靛ù婊嗘硾閵嗘帗绻濆顓犲幈閻熸粌閰i妴鍐川閺夋垵鐎梺绋跨灱閸嬬偤鍩涢幋鐐簻闁瑰搫妫楁禍鍓х磽娴e壊妲归柟鍛婂▕楠炲啴骞愭惔娑樹簼闂佸憡鍔忛弲婵嬪储闁秵鈷戦悷娆忓缁€鍐倶韫囷絼閭い銏$懄瀵板嫰骞囬鐘插箞闂佽鍑界紞鍡涘磻閸涱垯鐒婃い鎾卞灪閻撳啴鏌﹀Ο渚▓婵″弶鎮傞弻宥囨嫚閺屻儺鈧鏌嶇拠鎻掝劉闁诡垱妫冮弫鎰板醇閵忋埄鍞规繝鐢靛Х閺佸憡鎱ㄩ悜钘夋瀬闁归棿绀佺壕缁樼箾閹存瑥鐏柛瀣儔閺屾稑鈽夐崡鐐典哗闂佹悶鍔嶇换鍐崲濞戙垹骞㈡俊顖濐嚙绾板秹姊洪挊澶婃殶闁哥姵鐗犲濠氬Ω閵夈垺鏂€闂佺硶妾ч弲婊呯懅缂傚倸鍊烽懗鑸垫叏閻㈢數鐭欓柟鐑橆殔妗呴梺鍛婃处閸ㄤ即宕橀埀顒勬⒑闂堟稈搴峰┑鈥虫搐閳绘捇濡堕崨顏呮杸濡炪倖娲栧Λ娑氱矈閻戣姤鐓曢柕濞垮妼閸氳淇婇崣澶婂妤犵偞岣块埀顒佺⊕閿氭い搴㈡崌濮婃椽宕ㄦ繝鍕暤闁诲孩鑹鹃幊姗€寮幘缁樺亹鐎规洖娲ら獮鍫熺節瀵伴攱婢橀埀顒佹尵缁牊绗熼埀顒勫春閵忋倕鍗抽柣姗嗗亜娴滅偓绻涢崼婵堜虎闁哄闄勯妵鍕即閸℃绁╅柡浣告喘閺屾稖绠涢弴鐐蹭粯缂備礁澧庨崑銈夊箖濡ゅ懏鏅查幖瀛樼箘閺佹牕鈹戦敍鍕闁哥姵鐗犻崺鐐哄箣閿旇棄浜瑰銈嗘閸嬫劖瀵奸崶顒佲拺缂侇垱娲樺▍鍡涙煟濡ゅ啫浠辨鐐搭殜椤㈡洟濡堕崶鈺嬬床婵犲痉鏉库偓鎾剁矆娓氣偓閹﹢鏁冮埀顒冨絹闂佹悶鍎滃鍫濇儓濠电姷顣介埀顒€纾崺锝団偓瑙勬礋娴滃爼宕洪敓鐘茬<闁靛牆鎳忛崐鏇炩攽閻樺灚鏆╅柛瀣洴閹椽濡歌閸ㄦ繄鈧箍鍎遍ˇ浼村磻閿熺姵鐓冮弶鐐村閸忓矂鏌¢崱顓犵暤闁哄被鍔戦幃銏ゅ传閸曟垯鍨荤槐鎺楁偑閳ь剟宕抽敐澶婅摕闁挎洍鍋撻摶锝呫€掑鐓庣仭閺佸牊绻濈喊妯峰亾閾忣偀鏋欓梺鍛婃尵閸犲酣锝炶箛鎾佹椽顢旈崨顖氬Х闂備胶绮崝妯间焊椤忓棌鍋撳顓熺凡妞ゎ叀鍎婚¨渚€鏌涢妸銉у煟鐎殿喖顭峰鎾閻橀潧鈧偤鎮峰⿰鍐фい銏℃椤㈡﹢鎮ゆ担璇″晬闂備胶绮崝鏍п缚濞嗗緷褰掝敊缁涘顔旈梺缁樺姇濡﹪宕曡箛娑欑厓閻熸瑥瀚悘瀵糕偓瑙勬礃閿曘垺淇婇幖浣肝ч柛婊€鐒﹂ˉ锟犳⒒閸屾艾鈧绮堟担铏圭濠电姴浼e☉姘磯闁靛ě鍛姸濠电偞鎸婚崺鍐磻閹惧灈鍋撶憴鍕缂傚秴锕ら悾鐑藉箳閹存梹顫嶅┑顔角规禍顒€危閸ヮ剚鈷掗柛灞捐壘閳ь剚鎮傞幃褎绻濋崟顓犵厯闂佸湱鍎ら〃鍛婵傚憡鐓忓┑鐐茬仢閸擃參鏌i悢绋款棎闁割偒浜弻娑㈠即閵娿儱绠婚梺缁樻尫缁舵艾顫忓ú顏咁棃婵炴垶鐟﹂幃娆撴煟鎼淬垹鍤柛銊ョ-閸掓帞鎷犲ù瀣潔闂侀潧绻掓慨鐑筋敊閹烘鈷戠憸鐗堝俯閺嗘帗淇婇悙鏉戠婵″弶鍔曢埞鎴犫偓锝庡亐閹风粯绻涙潏鍓у埌闁硅绻濆畷顖炴倷閻㈠灚锛忛梺鍝勵槼濞夋洘鏅ラ梻浣筋嚃閸犳洟宕¢崘宸殨闁靛ǹ鍎抽弳瀣煥閻曞倹瀚� Application Scientist闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁诡垎鍐f寖闂佺娅曢幑鍥灳閺冨牆绀冩い蹇庣娴滈箖鏌ㄥ┑鍡欏嚬缂併劎绮妵鍕箳鐎n亞浠鹃梺闈涙搐鐎氫即鐛崶顒夋晬婵絾瀵ч幑鍥蓟閻斿摜鐟归柛顭戝枛椤牆顪冮妶搴′簼缂侇喗鎸搁悾鐑藉础閻愬秵妫冮崺鈧い鎺戝瀹撲礁鈹戦悩鎻掝伀缁惧彞绮欓弻娑氫沪閹规劕顥濋梺閫炲苯澧伴柟铏崌閿濈偛鈹戠€n€晠鏌嶆潪鎷屽厡闁汇倕鎳愮槐鎾存媴閸撴彃鍓卞銈嗗灦閻熲晛鐣烽妷褉鍋撻敐搴℃灍闁绘挻娲橀妵鍕箛闂堟稐绨肩紓浣藉煐濮樸劎妲愰幘璇茬闁冲搫鍊婚ˇ鏉库攽椤旂》宸ユい顓炲槻閻g兘骞掗幋鏃€鐎婚梺瑙勬儗閸樺€熲叺闂傚倸鍊风粈浣革耿闁秴鐓曢柛顐犲劚绾捐鈹戦悩鎻掆偓濠氬汲閿斿浜滈柡宥庡亜娴狅箓鏌涚€n偄濮嶉柟顔肩秺瀹曞爼顢旈崟顓燁嚄闂備焦瀵х粙鎺楁儎椤栨凹娼栨繛宸簼閸嬶繝鏌℃径濠勬皑闁圭ǹ鍟扮槐鎾寸瑹閸パ勭彯闂佹悶鍔岄悥濂哥嵁閸愵喖鐏抽柡鍌樺劜閻庡姊虹憴鍕棎闁哄懏鐟ч懞杈ㄧ節濮橆厸鎷洪梺鍛婄箓鐎氼喛鈪归梻浣告啞閺屻劑鏌婇敐澶婃槬濠电姴娲ら崡鎶芥煏韫囥儳纾块柛妯圭矙濮婅櫣鎲撮崟顐㈠Б閻庤娲﹂崜鐔风暦濠靛鏅濋柛灞剧〒閸樻悂鏌h箛鏇炰户闁稿鎸剧划鍫⑩偓锝庡厴閸嬫挾鎲撮崟顒傤槬閻庤娲﹂崜婵嬫倶閹烘鈷戦柟顖嗗懐顔囧┑鐘亾闂侇剙绉寸粻鐘绘煛瀹ュ骸浜炵痪鍙ョ矙閺屾稓浠﹂崜褎鍣銈忚闂勫嫰濡甸崟顖氱婵犻潧娲ゅ▓妤呮⒑鏉炴壆顦﹂柛鐔告尦瀵偊宕橀鑲╋紲濠电偞鍨惰摫闁汇倕鎳樺娲传閸曞灚笑闂佺粯顨呯€氭澘鐣峰┑鍥ㄥ劅闁靛ǹ鍎抽崢娲⒑閸濆嫭鍌ㄩ柛銊︽そ閹繝鎮㈤崨濠傚伎濠碘槅鍨伴幖顐︽嚋閻熸噴鐟扳堪鎼淬埄娼ゞ Develop缂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁绘劦鍓欓崝銈囩磽瀹ュ拑韬€殿喖顭烽幃銏ゅ礂鐏忔牗瀚介梺璇查叄濞佳勭珶婵犲伣锝夘敊閸撗咃紲闂佺粯鍔﹂崜娆撳礉閵堝洨纾界€广儱鎷戦煬顒傗偓娈垮枛椤兘寮幇顓炵窞濠电姴瀚烽崥鍛存⒒娴g懓顕滅紒璇插€块獮澶娾槈閵忕姷顔掔紓鍌欑劍宀e潡宕㈡潏銊х瘈闁汇垽娼у瓭闂佺ǹ锕ょ紞濠傜暦閹达箑唯闁冲搫鍊婚崢鎼佹煟韫囨洖浠╂い鏇嗗嫭鍙忛柛灞惧閸嬫挸鈻撻崹顔界彯闂佸憡鎸鹃崰搴ㄦ偩閻ゎ垬浜归柟鐑樼箖閺呪晠鏌i悢鍝ユ噧閻庢凹鍓熼幆渚€鏌嗗鍡忔嫽闂佺ǹ鏈悷褔宕濆鍡曠箚闁绘劕寮堕崑銉р偓瑙勬磸閸ㄨ櫣绮嬮幒鏂哄亾閿濆骸浜滃ù鐙€鍙冨娲礃閸欏鍎撻梺鐟板暱闁帮綁骞忛幋锔藉亜闁稿繗鍋愰崢浠嬫⒑閸濆嫬鈧棄鈻旈弴鐐╂灁闂侇剙绉甸悡娑㈡倵閿濆簼閭柛娆忓閹便劍绻濇担铏圭厯閻庤娲栭悥濂搞€佸Δ浣哥窞閻庯綆鍋呴悵銊╂⒑閼姐倕鏋戠紒顔肩灱缁棃宕奸弴鐐电厬闂佸憡渚楅崣搴°€掓繝姘厪闁割偅绻冮ˉ鐐烘倶韫囷絼閭柡灞剧洴婵℃悂濡烽敃浣侯攨缂傚倷绶¢崰鏍€﹀畡鎵殾闁绘垹鐡旈弫鍥煟閺冨牊鏁遍柣搴ㄧ畺濮婄粯鎷呴搹鐟扮濡炪們鍔岄幊姗€骞冭瀹曞崬螣鐏忔牗鏁垫俊鐐€栭悧婊堝磻閻愮儤鍋傛繛鎴炩棨瑜版帗鏅查柛銈堟缂嶅﹤顕i幎鑺ユ櫜濠㈣泛顑囬崢鎼佹煟韫囨洖浠ч柛瀣尵缁牏鈧綆鍏橀崑鎾舵喆閸曨剛顦梺鍛婎焼閸パ呭幋闂佺鎻粻鎴︾嵁閵忋倖鐓冮弶鐐村椤︼箓宕鐐粹拻闁稿本鑹鹃埀顒佹倐瀹曟劕鐣¢幊濠傜秺瀹曞爼顢楁担瑙勵仧闂備線娼чˇ顐﹀疾濞戞艾顥氶悷娆忓缁♀偓闂傚倸鐗婄粙鎺楁晬瀹ュ棛绠鹃柛蹇氬亹婢х敻鏌$仦鐔锋閻も偓濠殿喗锚閸氬绱為崼銉︾厽閹兼番鍨婚。鑼偓鍏夊亾闁归棿绀侀拑鐔兼煟閺冨洦顏犵痪鎯у悑娣囧﹪顢涘┑鍥モ偓鍐煕閹烘埊韬慨濠冩そ瀹曘劍绻濋崘顏勫汲婵$偑鍊х粻鎺撶椤掆偓鍗遍柟鐗堟緲缁犲鎮楀☉娅亪顢撻幘缁樷拺闁告稑锕ョ亸鎵喐閺夊灝鏆g€规洘绮撻弻鍡楊吋閸℃瑥骞楅梻渚€娼х换鍡涘疾濞戙垺鍊堕柨婵嗩槹閻撴洟鏌eΟ铏癸紞濠⒀呮暬閺岋絽鈽夐崡鐐寸亪闁剧粯鐗犻弻娑樷堪閳ь剟鎮為敃鍌氱柧婵犻潧顑嗛埛鎴︽煙缁嬫寧鎹g紒鐘虫尰缁绘稓浠﹂崒姘潎闂佽鍨欢姘暦閻撳簶鏀介柛鎰ㄦ櫆閺夋悂姊绘担铏瑰笡闁告梹岣挎禍绋库枎閹邦厽鐝烽梺鍝勬储閸ㄦ椽鎮¢悢鑲╁彄闁搞儯鍔嶉埛鎺旂磼閻橀潧浠遍柡宀€鍠栭、娆撳棘閵堝牃鍋撻崸妤佺厵妞ゆ棁顫夊▍濠囨煙椤旂晫鎳囨鐐差儔楠炴帡寮崒娑欐珤闂傚倸鍊搁崐椋庣矆娓氣偓楠炴牠顢曢埛姘そ婵偓闁靛牆鎳愰ˇ顕€鏌h箛鏇炰户闁烩剝妫冨畷鐢稿即閻旂繝绨婚梺鍝勬处椤ㄥ懏绂嶆ィ鍐┾拺闁告繂瀚﹢浼存煟閳哄﹤鐏︾€规洘妞介幃娆撳传閸曨厾鏆伴柣鐔哥矊閺堫剛绮╅悢鐓庡嵆闁绘劏鏅滈弬鈧梻浣瑰缁嬫垹鈧凹鍓氱粋宥嗙附閸涘﹦鍘辨繝鐢靛Т閸熺増鏅堕鍛簻闁哄倽娉曠粻鑼磼缂佹ḿ绠撴い顐g箞椤㈡宕掗敂鎯ц€块梻鍌氬€峰ù鍥綖婢舵劕纾块柧蹇e亝濞呯娀骞栨潏鍓у埌妞ゃ儲鑹鹃埞鎴﹀磼濮橆厼鏆堥梺缁樻尵閸犳劖绌辨繝鍥舵晬婵ê褰夐搹搴ㄦ⒑濮瑰洤濡芥俊鐐舵椤曪綁顢曢敃鈧柋鍥煏婢舵稓鐣遍柍褜鍓涢弫濠氬箖瀹勬壋鏋庨煫鍥ㄦ惄娴犲墽绱撴担鎻掍壕闂佸憡鍔忛弲婵堢不妤e啯鐓曟繛鍡楁禋濡附銇勮箛鎾愁伀妤犵偞鎹囬弻銈夊箛娴e摜浠梺姹囧€愰崑鎾寸節閻㈤潧浠﹂柛銊ㄦ硾閻滃宕稿Δ鈧崒銊╂煙闂傚鍔嶉柍閿嬪灩缁辨帞鈧綆鍋勯婊勭節閳ь剚瀵肩€涙ḿ鍘鹃梺鑽ゅ枑濠㈡﹢鍩涢弮鍫熺厾婵炲樊浜欓幉鎯р攽閿涘嫬鍘撮柛鈺嬬節瀹曟帒螖娴e壊浼滃┑鐘垫暩閸嬬娀骞撻鍡楃筏濞寸姴顑呯粻鐔兼煥濞戞ê顏悗姘煼閺屻劑鎮㈤崫鍕戯綁鏌i幘瀛樼妤犵偞鐗滈埀顒佺⊕宀e潡鍩ユ径鎰厓鐟滄粓宕滃顑炴椽鎮㈤崗鍏兼珳闂佺粯鍔曟晶搴ㄦ偪閳ь剟姊洪崫鍕殭闁稿﹤顭烽幆渚€宕煎┑鍐╂杸濡炪倖姊归弸缁樼瑹濞戙垺鐓曟俊顖涗航閸嬨垻鈧娲樼划蹇涘Φ閹版澘绠抽柟缁㈠灡鐎氳偐绱撻崒娆戣窗闁搞劌宕叅闁哄秲鍔嶅▍鐘绘煕濞嗗浚妲跺ù婊勭矒閺屾洘绻涢崹顔煎Б缂備胶濮撮…鐑藉蓟閻旂⒈鏁婇柛婵嗗娴煎牓鎮楃憴鍕鐎规洦鍓熼崺銉﹀緞婵炵偓鐎婚梺鐟扮摠缁诲倻绮绘繝姘拻闁稿本鐟чˇ锔剧磽瀹ュ拑宸ラ摶鐐烘煕瑜庨〃鍡涘磹閸ф鐓ラ柡鍥殔娴滈箖姊虹€圭姵顥夋い锔藉▕钘濋柡灞诲劜閻撳啴鎮峰▎蹇擃仼闁诲繐鐡ㄩ妵鍕閿涘嫭鍣伴梺纭呮珪閻楃娀宕洪埄鍐╁闁圭粯甯掔欢褔姊婚崒姘偓椋庣矆娓氣偓楠炴牠顢曢敃鈧€氬銇勯幒鎴濃偓濠氭儗濞嗘挻鐓欓柟瑙勫姦閸ゆ瑩鏌i幒鎴犱粵闁靛洤瀚伴獮鎺楀箣椤栨艾顫犻梻浣告啞鐢顭垮鈧垾锕傛嚄椤栵絾些婵犵數鍋為幐鎶剿夐幘璇茬闁圭儤顨呯猾宥夋煕椤愵偄浜濋柡鍜佷邯濮婃椽鏌呴悙鑼跺濠⒀冾嚟閳ь剚顔栭崰鏍€﹂悜钘夋瀬鐎广儱顦粈瀣亜韫囨挻鍣瑰┑顖欏嵆濮婄粯鎷呴崨濠傛殘闂佸湱枪濡繂鐣烽悢纰辨晝闁靛浚婢€閻㈢粯绻濋悽闈浶ラ柡浣告啞閹便劑鎮滄慨鎰ㄥ亾閸岀儐鏁婇柣鎰靛墻濞肩喖姊洪崫鍕偍闁搞劌缍婇幏鎴︽偄婵傚鍞甸梺鍏兼倐濞佳勬櫠閺屻儲鐓曢柕澶樺枛婢ь噣鏌﹂崘顏勬灈闁哄本娲樺鍕槈濮楀棙鍠橀梻浣告啞閿氱€规洦鍓熼崺鐐哄箣閿曗偓閻擄繝鏌涢埄鍐炬畼濞寸姵娼欓埞鎴︽倷閸欏鐝旂紓鍌氱С缁舵岸鎮伴鍢夋棃宕ㄩ闂存睏闂備焦妞块崑鎺楀礈濞嗘挻鐓€闁挎繂鎳愰弳锕傛煙椤栫偛浜版俊缁邯濮婃椽宕ㄦ繝鍐f嫽闂佸摜濮甸幐鎯i幇鏉跨闁规儳顕粔鍫曟⒑闂堟胆褰掑磿閼碱剚瀚氶柣鎰嚟缁♀偓濠电偛鐗嗛悘婵嬪几閹剧粯鐓曢悗锝庡亝瀹曞本鎱ㄦ繝鍛仩缂佽鲸甯掕灒闊浄绲肩花钘夘熆鐟欏嫭绀嬫い銏∩戦獮濠偯瑰⿰鍐Ш妤犵偞鐗曡彁妞ゆ巻鍋撳┑鈥茬矙閺屽秹鏌ㄧ€n亞鐟ㄩ梻鍥ь樀閺屻劌鈹戦崱妯烘闂佸摜鍠撻崑銈夊蓟閻旂⒈鏁嶆慨妯哄船閳敻姊洪崫鍕効缂佺粯绻傞悾閿嬬附閸撳弶鏅濋梺闈涚箳婵厼岣块崜褏纾介柛灞剧懅鐠愪即鏌涢悩鎰佹疁闁诡喚鍏橀崺锟犲川椤栨氨銈﹂梻浣告贡閸庛倝宕甸敃鍌氱睄闁割偅绻勯崝锕€顪冮妶鍡楃瑨闁稿﹦绮粙澶婎吋閸℃ê寮垮┑鈽嗗灠閻忔繈鎮¢幇鐗堢厽闁规儳顕ú鎾煛鐏炲墽娲存鐐叉喘閸┾剝鎷呴崜鑼偓宄扳攽閻橆偅濯伴柛鏇ㄥ幗閸掓盯姊洪崫鍕効缂佺粯绻傞悾鐑筋敂閸涱喖顎撶紓浣割儏缁ㄩ亶骞忛锔解拻濞达絽鎲¢幆鍫ユ煛閸偄澧撮柟顖氬椤㈡稑顫濋悡搴㈩吙闂備礁婀遍搹搴ㄥ窗閺嶃劌鍔旈梻鍌欑窔濞佳囁囬銏犵?闂侇剙绋侀弫鍡樼節婵犲倻澧涢柍閿嬪笒闇夐柨婵嗘噺閸熺偤鏌熼崣澶嬪€愰柡灞剧〒閳ь剨缍嗛崜娆愮濠婂嫨浜滄い蹇撳閺嗭綁鏌熺粙鍖℃敾鐎垫澘瀚灒闁煎鍊楅埢澶岀磽閸屾艾鈧悂宕愰悜鑺ュ€块柨鏇氱劍閹冲苯鈹戦悩鎰佸晱闁搞劑浜堕獮鎰板箮閽樺鎽曞┑鐐村灦鑿ら柡鈧禒瀣厱闁哄洢鍔屾禍婊冣攽椤斿搫鐏ǎ鍥э躬婵″爼宕卞Ο閿嬪濠电儑绲藉ú銈夋晝椤忓牆绠栨繛鍡樻惄閺佸倿鏌涢弴妯哄濞存粓绠栭弻鐔告綇閸撗呮殸缂佺偓鍎冲ḿ锟犲蓟閿涘嫪娌悹鍥ㄥ絻婵海绱撴担鍝勑¢柛妤佸▕瀵濡堕崱妯哄伎闂佸綊鍋婇崗姗€宕戦幘璇插唨鐟滃繘寮抽敃鍌涚厱婵炲棗娴氬Σ铏圭磼閻樿崵鐣洪柡宀€鍠撻埀顒佺⊕宀e潡骞婇崘顔界厽闊洤锕ュ▍濠囨煛瀹€瀣М妤犵偞甯¢獮瀣偐鏉堚晠鈹忛梻鍌欑窔濞佳兠洪妶鍥e亾濮橆偄宓嗛柣娑卞櫍楠炴帒螖閳ь剛绮婚敐鍡欑瘈闁割煈鍋勬慨鍐煟閵夘喕閭慨濠勭帛閹峰懘鎼归悷鎵偧闂備礁婀辨灙妞ゎ厾鍏橀獮鍡涘礋椤栵絾鏅梺缁樺姌鐏忔瑩鎮鹃崫鍕ㄦ斀妞ゆ柨顫曟禒婊堟煕鐎n偅宕岄柡宀€鍠栭、娆撴偩鐏炴儳娅楅梻浣瑰缁嬫帡宕濋弴銏犵厴闁硅揪绠戦獮銏℃叏濡も偓濡寮崘娴嬫斀闁绘ê鐏氶弳鈺佲攽椤旀儳鍘撮柕鍡楀€圭粋鎺斺偓锝庝簽閸旓箑顪冮妶鍡楃瑨闁哥噥鍨堕幃鐢割敂閸喓鍘遍柣搴祷閸斿矂宕濋敃鍌涚厸鐎光偓鐎n剛锛熸繛瀵稿缁犳捇骞冮崜褌娌繝闈涘閸旀粓鏌曢崶褍顏い锕佷含缁辨帡鎳滈棃娑樻懙閻庢鍠涢褔鍩ユ径鎰潊闁绘ɑ顔栭崯瀣⒒娴e憡鍟炴い銊ョ墦瀹曟垵鈽夐埗鈹惧亾閺嶎偀鍋撻敐搴″缁炬崘妫勯湁闁挎繂妫楅悘濠囨煕濮樼厧浜伴柡灞剧〒閳ь剨绲婚崝宀勫焵椤掍焦绀嬮柟顕€绠栭幃婊堟寠婢跺矈鏀ㄩ梻浣虹帛閸斿繘寮插⿰鍫稏鐎广儱鎳夐弨浠嬫煃閽樺顥滈柣蹇ョ秮閺屽秴鐣¢幍顔碱暫闁告浜堕弻銈夊传閵夛附姣勭紓浣叉閸嬫捇姊绘担鍦菇闁搞劏妫勫玻鑳槼缂佸倹甯掗オ浼村礋椤忓棛鐣炬俊鐐€栭崝褏绱為崱妞绘灁闁哄啫鐗婇ˉ鍡楊熆鐠轰警鍎愰柛娆忕箲娣囧﹪顢涘☉姗嗗殝缂佺虎鍙冪粻鏍蓟濞戞﹩娼╂い鎺戝€绘闂備礁鎼惌澶屾崲濠靛棛鏆﹂柛顐f礀鍞梺闈涳紡閸屾粍锛忛梻鍌氬€烽懗鍓佸垝椤栫偛绠伴柛婵勫劜瀹曟煡鏌熼悧鍫熺凡闁绘挻锕㈤弻鐔告綇妤e啯顎嶉梺绋匡功閸忔ê顫忔繝姘唶闁绘棁銆€濡晜绻濋姀锝庢綈婵炲弶鐗犻崺鐐哄箣閿旇棄鈧兘鏌涘▎蹇fЦ婵炲拑绲介埞鎴﹀煡閸℃ぞ绨肩紓浣筋嚙閻楀棝顢氶敐鍥ㄥ珰鐎瑰壊鍠栭幃鎴炵節閵忥絾纭炬い鎴濇喘瀹曪綁宕卞☉娆戝幗闁瑰吋鎯岄崹宕囩矓闂堟耽鐟扳堪閸涱厺娌紓浣稿€圭敮鈥崇暦椤愶箑唯鐟滃繘鏁嶅┑鍥╃閺夊牆澧界粔顒佺箾閸滃啰鎮奸柡渚囧枛閳藉濮€閿涘嫬骞楅梻浣稿暱閹碱偊鏁冮妶澶嬪€堕柨鏃傜摂濞堜粙鏌i幇顖e殝闂婎剦鍓熼弻鐔碱敊鐟欏嫭鐝栫紓渚囧枤閺佽鐣烽悜绛嬫晣闁绘﹢娼ч獮鈧┑鐘垫暩婵兘寮崨濠勭闁逞屽墯缁绘稒鎷呴崘鎻掓偐婵炴垶菤閺嬪酣鏌熼幑鎰彧閺夊牆鐗嗛—鍐Χ閸℃瑥顫х紓渚囧枛濞撮攱绔熼弴鐔侯浄閻庯綆鍋嗛崢閬嶆煟韫囨洖浠滃褌绮欓獮濠囧炊閵娿倗绠氶梺鍛婃寙閸愩劌绠i梻浣告惈閺堫剟鎯勯姘煎殨妞ゆ帒瀚粻浼村箹濞n剙鐏╅梻鍌ゅ灦濮婄粯鎷呴崨濠傛殘闁汇埄鍨遍〃鍫ュ极椤曗偓閺佹捇鎮╅鐟颁壕濞达絿纭跺Σ鍫ユ煏韫囧ň鍋撻弬銉ヤ壕闁绘垼濮ら悡鏇熺箾閸℃绠板ù婊勫缁辨帡鎮╅搹顐㈢3閻庢鍠涢褔鍩ユ径鎰潊闁绘ɑ褰冪粊顕€姊绘笟鈧ḿ褎鐏欓梺绋挎唉濞呮洜绮嬮幒妤€鐓涢柛鎰典簽閿涙繃绻涙潏鍓у埌闁圭⒈鍋婇、鎾诲箻閸撲胶锛滈梺鍦帛鐢帡鍩涢弮鍫熺厵妤犵偛鐏濋悘鈺呮煃鐟欏嫬鐏╅柍褜鍓ㄧ紞鍡涘磻閹烘嚦娑㈠礃閵娿垺鏂€闂佺粯鍔栧ḿ娆撴倶閿曞倹鐓熼柣鏇炲€婚悾鍨殽閻愭彃鏆欓柍璇查叄楠炴ḿ鍒掔憴鍕伖闂傚倷绀侀幉锛勬崲閸屾壕鍋撳鍗炲幋鐎规洘娲熼獮瀣攽閸愨晜鏉搁梻浣虹帛閸斿繘寮插☉娆戭洸濡わ絽鍟埛鎺懨归敐鍥╂憘闁搞倕鍟撮弻娑㈡偐閹颁焦鐤侀梺闈涙閸熸潙鐣烽妸鈺佺骇闁瑰濮撮獮鎺楁⒒娴g瓔娼愮€规洘锕㈤、姘愁樄鐎规洖缍婂畷鎺戔槈閺嶏妇鐩庨梻浣告惈閸燁偊宕愰悷鎵虫瀺闁哄洨濮甸崰鎰版⒑椤撱劎鐣遍柣蹇ラ檮閹便劍绻濋崟顓炵闂佺懓鍢查幊妯虹暦閵娾晜顥堟繛鎴炴皑妤旀俊鐐€戦崹娲偋閻樿尙鏆﹂柕濞р偓閸嬫挸鈽夊▍铏灥閳诲秹宕惰濞撳鏌曢崼婵囧櫧缂佺姳鍗抽弻锝呂旈埀顒勬晝椤忓嫮鏆﹂柟瀛樻儕閻旀哺褔宕堕敂鍓ф晨闂傚倷绀侀幖顐﹀磹閸︻厸鍋撶粭娑樻祫缂嶆牜鈧箍鍎遍ˇ浼存偂閻斿吋鐓涢柛灞炬皑娴犮垽鏌熼钘夌伌闁哄本鐩俊鍫曞川椤撶喐顔掗梻浣告惈閼活垳绮旈悷鎵殾妞ゆ劧绠戠粈瀣亜閹板墎鎮煎ù鐘茬灱缁辨捇宕掑▎鎴М閻庤娲﹂崜娆擃敋閿濆绀堝ù锝囨嚀鎼村﹤鈹戦悩缁樻锭闁绘妫濆鎼佸醇閻斿墎绠氬銈嗙墬缁嬫帡濡甸悢鍝ョ闁稿繒鍘ч悘瀛樻叏婵犲啯銇濇鐐寸墵閹瑩骞撻幒婵囩秵濠电姷鏁搁崑姗€宕犻悩璇茬倞闁靛鍨规禍楣冩煕濞戝崬鏋ら梻鍕缁辨帞鈧綆鍙庨崵锕傛煃閸濆嫬鏆為柛鐘冲姍閻擃偊宕堕妸锔绢槬濡炪們鍎查懝鎹愮亙闂佹寧绻傞幊搴ㄥ汲閻愮儤鐓熼柟鎯ь嚟濞叉挳鏌$仦鍓ф创濠碉紕鍏橀弫鎰板川椤撶儐娼涢梻鍌欐祰椤曆兠瑰顓狀洸妞ゅ繐鐗嗛拑鐔衡偓骞垮劚椤︿即鎮¢妷鈺傚€甸柨婵嗙凹缁ㄤ粙鏌i悢鏉戝婵﹤顭峰畷鎯邦檨婵☆垪鍋撻梻浣告惈鐞氼偊宕濆畝鍕厴闁硅揪绠戦獮銏℃叏濡も偓濡鈻撳▎鎾寸厽闁绘柨鎽滈惌灞筋熆瑜庨〃鍫ュ极椤曗偓楠炴帡骞婇崼鍡楁搐閽冪喖鏌曟径娑滃悅闁瑰嘲鎼—鍐Χ閸℃娼戦梺绋款儐閹稿墽妲愰幒鎾崇窞閻忕偟鍋撳В鍫ユ⒑鐠団€虫灀闁逞屽墯閺嬪ジ寮告惔銊︾厵閻庣數枪鏍¢梺鎸庣☉缁绘ê顫忓ú顏勪紶闁告洖鐏氱瑧闂備浇顕х换鎴犳崲閸儱绠犳繝濠傜墛閸嬶繝鏌熼崘璇у姛闁硅櫕鎹囬妶顏呭閺夋垵绐涘銈嗘寙閸曨剛妲樻繝纰夌磿閸嬫垿宕愰幋锕€绀夊┑鐘叉搐绾惧潡鏌i姀鈶跺湱绮婚弽銊х闁糕剝锚閻忥箓鎮楀顓熺殤闁规彃鎲¢幆鏃堝Ω閵夛妇鈧剚淇婇妶蹇曞埌闁哥噥鍨跺畷鎰版偨閸涘﹦鍘卞銈庡幗閸ㄥ灚绂嶅┑鍫㈢<闁煎摜鏁搁崣鈧梺璇″枟椤ㄥ懘锝炲┑瀣垫晝闁靛繒濮烽妶顕€姊绘担铏瑰笡濞撴碍顨婂畷鎶芥晲閸涱垱娈鹃梺鍓插亝濞诧箓寮崱妤婄唵閻犺桨璀﹂崕鎰箾閸涱厾鐒告慨濠勭帛閹峰懘宕ㄩ棃娑氱Ш闁诡垰鏈鍕偓锝傛櫇缁犳岸姊洪幖鐐插姶闁告挻绋戦悾鍨瑹閳ь剟寮婚弴锛勭杸閻庯綆浜栭崑鎾诲冀椤撶偟鍘遍梺鍦劋椤ㄥ棝鎮¢弴銏″€堕柣鎰絻閳锋棃鏌熼崘鍙夊櫤闁靛洤瀚伴弫鍌涚附閸涘⿴鈧秶绱撴担铏瑰笡缂佽鐗撳畷娲焵椤掍降浜滈柟鐑樺灥椤忣亪鏌i幒鏇炰汗闁逞屽墮缁犲秹宕曢柆宥呯疇闁规壆澧楅弲顒佺箾閹存瑥鐏柍閿嬪灴閹嘲鈻庤箛鎿冧患缂備讲鍋撻柛鎰ㄦ杺娴滄粓鏌¢崶褎顥滈柟铏姍閹矂宕卞☉娆戝幈濡炪倖鍔戦崐鏇㈠几閹达附鐓曟繛鍡楃箳缁犳煡鏌熸笟鍨閾绘牠鏌嶈閸撴瑨鐏嬪┑掳鍊曢幊搴ㄥ磼閵娧€鍋撶憴鍕婵炲眰鍔庢竟鏇熺鐎n偆鍘遍柣蹇曞仜婢т粙鍩ユ径鎰厱婵犻潧娲﹂妵婵嬫煛瀹€瀣?濞寸媴绠撻幃鍓т沪濠㈩厼鎳夐崑鎾舵喆閸曨剙顦╅梺绋款儏閿曘倝鎮鹃悜鑺ュ亜缁炬媽椴搁弲婵嬫⒑缂佹ɑ顥嗘繛鎾诡潐缁旂喖寮撮姀鈾€鎷洪梺缁樻尭鐎涒晠骞夐幖浣圭厸濞达綀顫夐崐鎰版煏閸℃鍤囩€规洩绲惧鍕暆閳ь剟鎯侀崼鐔虹瘈闁汇垽娼у瓭闂佺ǹ锕︾划顖炲疾鐠鸿 妲堥柕蹇ョ磿閸樹粙姊虹憴鍕姢妞ゆ洦鍙冮獮濠囧炊椤掍胶鍘搁柣蹇曞仧鏋褑灏欓埀顒€鐏氬妯尖偓姘煎幘閹广垹鈹戠€n亞顦板銈呯箰濞诧箓顢撳Δ鈧埞鎴︽晬閸曨偂鏉梺绋磕涢崨顓犵瓘闂佺粯鍔﹂崜娑氱不閹€鏀介柣妯哄级閹兼劙鏌﹂崘顏勬灈闁哄矉缍佸顕€宕掑Δ浣哥彵闂備浇妗ㄧ粈渚€鏁冮鍫濊摕闁挎繂顦粻濠氭煕閹邦剚鈻曢柛鏂款樀濮婅櫣绮欐惔鎾舵箙闂佹悶鍔岀壕顓炍i幇鏉跨閻庢稒锚椤庢捇姊洪幆褏绠抽柟铏尵缁參鏁嶉崟顓狅紳婵炶揪绲块悺鏃堝吹濞嗘劒绻嗘い鎰剁悼缁犳碍淇婇銈呮灈婵﹥妞藉畷顐﹀礋椤曞懏钑夐梻浣呵圭€涒晠鎮¢垾宕囨殾闁圭増婢橀崹鍌涖亜閹板墎鍒扮€殿喖鐏濋埞鎴︻敊缁涘鐣跺┑鈽嗗亝椤ㄥ﹪鎮伴鍢夋棃宕橀鍡床闂佽崵濮撮幖顐﹀箹椤愩倗妫憸鏃堝蓟閺囥垹鐐婄憸宥夘敂椤撶喆浜滈柕蹇婂墲缁€瀣攽椤旂懓浜鹃梻渚€娼х换鍫ュ春閸曨垰鑸圭憸鐗堝笚閳锋帒銆掑锝呬壕濠电偘鍖犻崶銊ヤ罕闂佺粯鍔楃换婵堟崲閸℃稒鐓曢柕澶樺枛婢ь喚绱掗悩闈涙瀾濞e洤锕俊鍫曞川椤斿吋顏犻梺鎼炲劜閹稿啿顫忓ú顏勫窛濠电姴鍟ˇ鈺呮⒑閸涘﹥灏扮紒瀣灥閻滃宕稿Δ鈧崘鈧銈嗘尵閸熷潡骞忔繝姘拺缂佸瀵у﹢浼存煟閻旀繂娉氶崶顒佹櫆闁伙絽鐬奸惁鍫ユ⒑闁偛鑻晶鎾煛鐏炶姤顥滄い鎾炽偢瀹曘劑顢涢妶鍥ф優闂傚倸鍊风欢姘缚瑜旈幃褔宕卞ù鏉挎喘椤㈡稑饪伴崨顒傜憹闂備礁鎼ˇ顖滆姳闁秴缁╁ù鐘差儐閻撶喐淇婇婵囶仩闁挎稑绉甸妵鍕晲閸℃瑥寮ㄩ梺鍝勭焿缂嶄線鐛鈧畷锟犳倷閹绘帩娼ラ梻鍌欑窔濞佳兠洪妶鍥e亾濮橆偄宓嗛柣娑卞枛铻i柛蹇曞帶绾绢垶姊洪悜鈺傛珕閻㈩垰娲畷鏇㈠箮閼恒儱鍓﹀銈呯箰閻楀棛绮婚弻銉︾厵闂侇叏绠戝鐐繆椤愩垹顏慨濠傤煼瀹曟儼顧佹俊顖楀亾闂備礁鎼悮顐﹀礉瀹€鍕厴闁硅揪绠戦獮銏′繆椤栨粌鍔嬫い蹇曞У娣囧﹪鎮欓鍕ㄥ亾閹达箑纾块弶鍫氭櫆瀹曟煡鏌熺€电ǹ浠ч柍鐟扮Т閳规垿鎮╅崣澶嬫倷缂備胶濮烽弫濠氬蓟閻斿吋鍊绘俊顖濐嚙绾板秹姊洪崫鍕棞闁绘鎸搁~蹇撁洪鍜佹濠电偞鍨堕悷锕傚箖濞嗘挻鐓熼幖娣灮椤e弶绻濋姀鈽呰€挎い銏″哺閺佹劖寰勬繝鍕靛晪婵$偑鍊栭弻銊ノi崼銉ョ厸闁告侗鍠氶崢顏呯節閵忥絾纭鹃柣妤€妫濆畷婵嬪Χ閸℃劒绨婚梺鍝勫暊閸嬫捇鎮介妞诲亾閹颁焦缍庣紓鍌欑劍钃卞┑顖涙尦閺屾稑鈽夊鍫濅紣闂佸搫妫楅悧鎾诲蓟閿濆顫呴柍杞拌兌娴狀厼顪冮妶鍐ㄥ闁绘鎸搁锝夘敃閿旂粯鏅梺閫炲苯澧寸€殿噮鍋婇獮妯肩磼濡桨姹楅梻浣告啞閻熴儵藝閹峰备鍙㈤梻鍌氬€搁崐宄懊归崶褉鏋栭柡鍥ュ灩缁愭鏌熼幆褏鎽犻柛娆忕箻閺屸剝寰勭€n亞鍔搁梺鍝ュ枎閹冲繒鎹㈠┑瀣棃婵炴垶鐟ラ崑宥嗙箾鐎涙ḿ鐭嬬紒顔芥崌瀵鎮㈤悡搴g暰閻熸粌绉归幊婊嗐亹閹烘挾鍘介棅顐㈡搐閿曘儱鈻嶆繝鍥ㄧ厸閻忕偟枪婢ф煡鏌熷畡鐗堝殗鐎规洦鍋婃俊鐑解€栭鍝勫闁宠鍨块、娆戞兜瀹勬澘顫犵紓鍌欑贰閸n噣宕归崼鏇犲祦闊洦绋戝婵嬫煛婢跺鐏ョ紒鎰⊕缁绘繈鎮介棃娴躲垽鏌涢悤浣镐喊鐎规洘绮撳畷褰掝敃閵堝洨妲囬梻浣圭湽閸ㄨ棄岣胯缁傛帒饪伴崼鐔哄幗濡炪倕绻愰崯顐㈢暤閸℃瑢鍋撶憴鍕缂佽鐗撻悰顔锯偓锝庝簴閺€浠嬫煕椤愩倕鏋戞い鏃€娲熷缁樻媴娓氼垱鏁梺瑙勬た娴滎亜顫忔禒瀣妞ゆ牗姘ㄩ敍娆撴⒑缂佹ê鐏卞┑顔哄€濋幃锟犳偐閻㈠灚锛忛梺鍝勵槸閻忔繈鎳滈悷閭︾唵鐟滄粓宕规潏鈺傚床婵炴垯鍨归柋鍥ㄧ節闂堟稑顏╁ù鐙€鍣e铏规嫚閳ヨ櫕鐏嶅銈冨妼閿曨亪骞冩导鎼晪闁逞屽墮閻g柉銇愰幒婵囨櫓闂佺粯鎸哥€垫帒岣垮☉妯锋斀闁挎稑瀚禍濂告煕婵炑冩噽绾捐姤鎱ㄥΟ鎸庣【缁绢厸鍋撻梻浣筋潐閸庣厧螞閸曨垰鍙婇柕澶涘缁犻箖鏌熺€涙ḿ鎳冮柣蹇婃櫇缁辨帡鎮崨顖溞滈梺鍝勭焿缁插€熺亽闂佺ǹ绻愰崥瀣掗崟顖涒拺闁圭ǹ娴烽埊鏇犵磼鐠囨彃鏆熼柟骞垮灩閳藉鈻庨幇顔拘ら梻浣告啞閹稿棝宕橀妸褍甯撴繝纰夌磿閸嬫垿宕愰妶澶婄;闁告稑鐡ㄩ崑瀣煟濡崵婀介柍褜鍏涚欢姘嚕椤曗偓瀹曠厧鈹戠€n亝鏆梻鍌欒兌缁垶寮婚妸鈺傚剭婵犻潧顑呯壕濠氭煙閹规劦鍤欓梺鍗炴喘閺岋繝宕堕埡浣圭亖闂佸憡鐟ュΛ婵嗩潖濞差亜浼犻柛鏇ㄥ墮椤︹晛顪冮妶鍐ㄥ闁瑰啿绻掔划瀣吋閸℃劕浜濋梺鍛婂姀閺備線骞忛悜妯肩闁哄鍨甸幃鎴︽煟閻旀繂鎳愰惌娆撴煠婵劕鈧澹曟總鍛婂仯闁搞儺浜滈惃鍝勵熆瑜濇俊鍥焵椤掍緡鍟忛柛锝庡櫍瀹曟垶绻濋崶鈺佺ウ闂佹悶鍎洪崜娆戠棯瑜旈弻娑⑩€﹂幋婵囩亾闂佺粯绋堥弲婊勭┍婵犲洦鍊锋い蹇撳閸嬫捇寮介‖顒佺洴瀹曟﹢濡告惔銏㈡创鐎规洖缍婇、娆撴倷閺屻儱寮板銈冨灪瀹€鎼佸春閳ь剚銇勯幒鎴濐仼闁藉啰鍠栭弻銊モ攽閸℃﹩妫¢梺绋挎捣閸犳牠寮婚弴銏犻唶婵犻潧妫崝澶岀磽閸屾氨孝闁绘妫濋崺鐐哄箣閿旇棄鈧兘鏌熺紒妯虹濡ょ姴娲ㄧ槐鎾寸瑹閸パ勭亶闂佺懓鎲¢幃鍌炲箖妤e啯鍊婚柦妯侯槸瀹撳棝姊洪棃娑氱濠殿喖鐗愰ˇ褰掓煛鐏炲墽鈽夋顏冨嵆閸┾偓妞ゆ帒鍊婚惌鍡椕归敐鍥┿€婇柡瀣⒐閵囧嫰骞囬崼鏇燁€嶉梺鎶芥敱閸ㄥ潡寮诲☉妯锋婵鐗婇弫鐐節閵忥絾纭鹃悗姘嵆瀵鈽夐姀鐘栤晠鏌ㄩ弴妤€浜惧銈冨劚椤戝洨妲愰幒妤婃晩婵炲棙鍎冲▓顓㈡⒑鐎圭姵顥夋い锔诲灦閸┿垺鎯旈埥鍡楁倯闂佸憡娲﹂崢鎯р枖閸ф鈷掗柛灞剧懄缁佺増銇勯銏╂Ц闁伙絽鍢茶灒閻炴稈鍓濋悘鍐ㄢ攽閻愭潙鐏﹀畝锝呮健楠炴濡烽妷銏℃杸闁圭儤濞婂畷鎰旀担鐟板伎闂佺粯鍨煎Λ鍕婵犳碍鐓熼柟閭﹀幒閼割亪鏌嶈閸撴瑩宕婊勫床婵犻潧顑呯壕濂告煏閸繃顥犵紒瀣╄兌缁辨捇宕掑顑藉亾閻戣姤鍊块柨鏇氱劍閹冲苯鈹戦悩鎰佸晱闁搞劋鍗抽、姘额敇閻樻剚娼熼梺鍦劋閺岋繝宕戦幘缁樻櫜閹肩补鈧尙鐩庢俊鐐€栧ú妯煎垝瀹ュ绠為柕濞炬櫆閺呮煡鏌涢埄鍐炬當妞ゎ偅甯掗埞鎴︻敊绾攱鏁惧┑锛勫仩濡嫰鎮鹃悜鑺ュ€荤紒娑橆儐閺咃絽鈹戦悙鏉戠仸闁荤喆鍎甸幃鐢告焼瀹ュ棌鎷绘繛杈剧到閹虫瑨銇愰幒婵囨櫈闂佸憡绋戦悺銊╁疾濠靛洢浜滈煫鍥ㄦ尭椤忔挳鏌涢妶鍡樼闁靛洤瀚伴獮鍥礈娴g儤娈哥紓鍌欒閸嬫捇鏌涢幇銊︽澓濞存粍绮撻弻锟犲磼濞戞﹩鍤嬪銈庡亜缁夊爼骞夐幖浣哥睄闁割偅绻嗛幗鏇炩攽閻愭潙鐏﹂懣銈嗕繆閹绘帞澧﹂柡灞剧☉閳诲酣骞囬妷褏绐楅梻浣告啞閸ㄧ數绱炴繝鍌ゆ綎闁惧繗顫夌€氭岸鏌$仦璇插姶闁逞屽墯椤ㄥ﹪寮婚悢鍝勬瀳闁告鍋橀崰濠囨⒑缁洘娅囬柛瀣ㄥ€濋悰顔锯偓锝庡枟閺呮粓鏌﹀Ο渚Т闁稿鎹囬幃婊堟嚍閵壯冨箞婵犵數鍋涘Λ妤€霉濮橆儵鐔煎醇閻斿墎绠氬銈嗗姦閸撴稓寮ч埀顒€鈹戦纭锋敾婵$偘绮欓悰顕€寮介鐔封偓鐑芥煙缂佹ê淇柣搴ゆ珪缁绘繈鎮介棃娴舵盯鏌涚€n偅宕岀€殿喖鐖煎畷鐓庘槈濡警鐎烽梻浣虹帛缁诲倿鎮ユ總绋胯摕闁跨喓濮撮悙濠囨煃鏉炴壆鍔嶉柣蹇庣窔濮婂宕掑顒変患闁诲孩鐭崡鍐差嚕鐠囨祴妲堟俊顖炴敱椤秴鈹戦绛嬫當闁绘妫欓幈銊モ槈閵忊檧鎷洪梺鍛婄☉鑹呯紓鍌涘哺閺屸剝鎷呯粵瀣濡炪値鍋勭换鎰弲濡炪倕绻愮€氼厼鐣靛鍜佹富闁靛牆妫欑亸闈涒攽椤旂⒈鍤熺紒顕呭弮閺佹捇鎮╁畷鍥у箺闂備線娼х换鍡涘疾濞戙垺鍊舵繛鍡樻尰閻撴盯鏌涘☉鍗炵仩鐎涙繈姊烘导娆戞偧闁稿繑锚椤曪綁骞橀纰辨綂闂佺粯岣块弫鎼佸级閹间焦鈷掑ù锝堟鐢稒銇勯妸銉﹀殗闁诡啫鍥у耿婵炴垶岣块崝锕€顪冮妶鍡楀潑闁稿鎹囬弻锝堢疀閺傚灝鎽靛Δ鐘靛仜閻楁挻淇婇幖浣肝ㄩ幖杈剧到閺嬫盯鏌熼鐟板⒉闁诡垱鏌ㄩ埞鎴﹀幢閳哄偆妫ラ梻鍌氬€峰ù鍥敋瑜忛埀顒佺▓閺呯娀骞冮姀銈庢晢闁告洦鍋嗛鍡涙⒑鐠恒劌娅愰柟鍑ゆ嫹>>  闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁诡垎鍐f寖闂佺娅曢幑鍥灳閺冨牆绀冩い蹇庣娴滈箖鏌ㄥ┑鍡欏嚬缂併劌銈搁弻鐔兼儌閸濄儳袦闂佸搫鐭夌紞渚€銆佸鈧幃娆撳箹椤撶噥妫ч梻鍌欑窔濞佳兾涘▎鎴炴殰闁圭儤顨愮紞鏍ㄧ節闂堟侗鍎愰柡鍛叀閺屾稑鈽夐崡鐐差潻濡炪們鍎查懝楣冨煘閹寸偛绠犻梺绋匡攻椤ㄥ棝骞堥妸鈺傚€婚柦妯侯槺閿涙稑鈹戦悙鏉戠亶闁瑰磭鍋ゅ畷鍫曨敆娴i晲缂撶紓鍌欑椤戝棛鈧瑳鍥ㄥ€垫い鎺戝閳锋垿鏌i悢鍛婄凡闁抽攱姊荤槐鎺楊敋閸涱厾浠搁悗瑙勬礃閸ㄥ潡鐛崶顒佸亱闁割偁鍨归獮妯肩磽娴e搫浜炬繝銏∶悾鐑筋敆娴h鐝风紓鍌欑劍鐪夌紒璇叉閺岋紕浠︾拠鎻掑闂佽鐓$粻鏍蓟閳ュ磭鏆嗛悗锝庡墰琚﹂梻浣筋嚃閸犳捇宕归挊澶屾殾妞ゆ劧绠戝敮閻熸粌绻樺畷銏ゅ箳閹存梹鏂€闂佺粯锕╅崑鍛垔娴煎瓨鐓曢柡鍥╁仧娴犳盯鏌i敐鍛仮婵﹦鍎ゅḿ顏堝箥椤旇法鐛ラ梻渚€娼荤紞鍥╃礊娓氣偓閹即顢氶埀顒勭嵁閹烘嚦鏃堝焵椤掑倻灏电€广儱顦伴悡鏇㈡倶閻愭彃鈷旈柣顓炵焸閺屾盯寮捄銊ョ厽濠殿喖锕︾划顖炲箯閸涱垳鐭欐繛鍡欏亾椤ユ垿姊绘担鍛靛綊顢栭崨顓囨稑鈹戦崱娆愭婵炴潙鍚嬪ḿ娆戠不婵犳碍鍋i柛婵嗗閹牏鎮敐澶嬧拻濞撴埃鍋撻柍褜鍓涢崑娑㈡嚐椤栨稒娅犻悗娑櫳戦崣蹇撯攽閻樻彃浜為柣鎾瑰亹閳ь剝顫夊ú妯兼暜閹烘缍栨繝闈涱儏绾偓闂佺粯鍨靛Λ娆忣熆閹寸偟绡€闁汇垽娼ф禒锕傛煙濮濆苯鍚归柛鐘诧工椤撳吋寰勯崼姘壕闁告劏鏅濈弧鈧梺绋挎湰缁秴鈻撴ィ鍐┾拺闁告繂瀚婵嬫煕鐎n偄濮囬崡閬嶆煕椤愮姴鍔滈柣鎾崇箻閻擃偊宕堕妷銉ュБ缂佺偓鍎冲ḿ锟犲蓟濞戞鐔兼倻濡儤娈樼紓鍌欒兌缁垳绮欓幒鎴撶細闊洦绋戠粈鍫㈡喐瀹ュ鏄ラ悘鐐插⒔缁♀偓闂侀潧绻堥崹娲吹閳ь剟姊洪幐搴㈠濞存粍绮撻幃楣冩倻閽樺宓嗛梺闈涚箳婵兘鎯堥崟顖涒拺闁告挻褰冩禍鐐烘煕閻樿櫕宕岀€规洏鍨介獮鏍ㄦ媴閸︻厼骞楅梻濠庡亜濞诧箑煤閺嶃劎顩风憸鏃堝蓟閿熺姴妞藉ù锝夋櫜缁ㄥジ姊洪崫鍕櫡闁稿海鏁诲濠氭晲閸℃ê鍔呴梺闈涚墕鐎涒晝绱為崼婵冩斀闁绘劙顤傞崵瀣磼閻樿櫕灏柣锝囧厴楠炲鎮欓悽鐢垫闂備胶枪閺堫剛鍒掑鍛灁濡わ絽鍟埛鎴犵磽娴h偂鎴﹀煕閹烘鐓冪€瑰嫭澹嗘晶锔锯偓娈垮櫘閸嬪﹤鐣峰鈧、娆撴偩鐏炶棄绠洪梻鍌欑閹碱偊宕鈷氭椽鏁冮崒娑樻畼闂佽崵鍠栭崑濠囨偄閸℃稒鍋℃繛鍡楃箰椤忣亞绱掗埀顒傗偓锝庡枟閻撴稓鈧厜鍋撻悗锝庡墰琚﹂梻浣筋嚃閸犳捇宕归挊澶屾殾妞ゆ劧绠戝敮闂佹寧娲嶉崑鎾寸箾閸涱喖鐏存慨濠呮閹风娀骞撻幒婵嗗Ψ闂備礁鎲¢崹鐢电礊婵犲倻鏆﹂柟鎯板Г閺呮彃顭跨捄濂斤繝濡烽埡鍌滃幈濠电偞鍨堕悷锔剧礊閹达附鐓㈤柛鎰典簻閺嬫盯鏌$仦鐐鐎垫澘瀚埥澶婎潨閸℃ê鏋犻梻鍌欑閹诧繝鏁冮埡鍌滎洸妞ゅ繐瀚峰ḿ鏍ㄧ箾瀹割喕绨荤紒鈧崼銉︾厵缂備焦锚缁楀倻绱掗妸銊ヤ汗缂佽鲸鎸婚幏鍛驳鐎n亝顔勭紓鍌欑椤︽澘岣垮▎蹇曟殼闁告洦鍨遍崑鈩冪節婵犲倹鍣规い锝呫偢閹粙顢涘☉杈ㄧ杹闂佽鍣换婵嬪箖閵忋倕绀傞柤娴嬫櫅楠炲秹姊绘担绛嬪殐闁搞劌閰e畷銊╊敊閽樺鐏堢紓鍌氬€搁崐椋庢媼閺屻儱纾婚柟鍓х帛閸婄敻鏌ㄥ┑鍡涱€楅柡瀣枛閺岋綁骞樼€靛憡鍒涢梺璇″枟閿曘垽骞冨▎鎾搭棃婵炴垶顨呴ˉ姘辩磽閸屾瑨顔夐柛瀣崌閺屾盯骞囬崗鍝ユ寜闂佺ǹ顑嗛幑鍥х暦瑜版帩鏁冮柨婵嗘搐閸ゆ帡姊虹拠鎻掝劉闁告垵缍婂畷鎶芥晲婢跺﹥妲梺閫炲苯澧柕鍥у楠炴帡骞嬮姘潬缂傚倷绀侀ˇ闈涐缚瑜斿﹢浣糕攽閻樿宸ラ柟鍐插缁傛帡鏁傞崜褏锛滈梺绋挎湰缁嬫垵霉椤旂瓔娈介柣鎰彧閼版寧銇勯姀锛勬噰闁诡喖澧芥禒锕傛寠婢跺矈鍟堥梻鍌氬€烽懗鍫曞箠閹捐瑙﹂悗锝庡枟閸嬧晜銇勮箛鎾跺闁搞劌鍊婚幉鎼佹偋閸繄鐟ㄩ梺鍛婁亢椤濡甸崟顖氱闁瑰瓨绻嶆禒楣冩⒑缂佹ɑ灏版繛鑼枛瀵鎮㈤悡搴g暰閻熸粌绻橀獮妤呮偐缂佹ḿ鍘介梺闈涒康缁犳垿鎮橀埡鍐<閺夊牄鍔屽ù顔姐亜閵忥紕鎳呴柛鐘诧躬瀹曪繝鎮欓幓鎺濇婵犵绱曢崑鎴﹀磹閺嶎厼绠伴柟闂寸鐟欙箓鎮楅敐搴濇喚闁搞倖顨婇弻娑㈠即閵娿儱绠伴梺绋款儐閹瑰洭寮幇顓熷劅闁炽儲鍓氬ḿ璇测攽閻樻剚鍟忛柛鐘愁殜楠炲啴宕掗悙鑼舵憰闂佹寧绻傚Λ娆撳磿閻斿吋鐓ユ繛鎴灻顐︽煛閸℃ḿ娲存慨濠呮缁瑩宕稿Δ濞惧亾濡ゅ啠鍋撶憴鍕闁告挻绻堥幃妯尖偓锝庡枟閸婄敻鏌涜箛鎿冩Ц濞存粓绠栧娲川婵犲啫顦╅梺绋款儏濡繈銆佸▎鎾冲耿婵$偟绮弬鈧梻浣虹帛閸旀洖顕i崼鏇炵厺闁哄洨浼濋悷鎵冲牚闁告洦鍘鹃悿鍕⒑缁洘娅嗛柣鈺婂灦閻涱喚鈧綆鍠楅弲婊堟煟閿濆懓瀚版鐐茬墦濮婄粯鎷呴悷閭﹀殝濠碘槅鍋傜欢姘躲€佸鎰佹Ь闂佽桨绶¢崰妤呭箚閺冨牆惟闁挎梹鍎抽獮妤呮⒒娴h櫣甯涙慨濠勭帛閻忔瑥鈹戦悙鍙夊櫧闁稿鍠栭獮澶愬箹娴g懓浜遍梺鍓插亝缁诲嫰鎮烽弻銉︹拺缂佸灏呭銉︺亜椤撶姴鍘寸€殿喖顭烽弫鍐焵椤掑啰浜介梻浣虹帛閼归箖顢氶鐘电焼闁糕剝绋掗埛鎴︽⒒閸喍绶辨俊鍙夋尦閺岋繝宕ㄩ鍓х厜闂佽鍠掗埀顒佹灱閺嬪酣鏌熼幆褜鍤熼柛妯圭矙濮婃椽鎮烽柇锕€娈堕梺绋垮閸ㄥ墎绮悢灏佹婵炲棙鍨归鏇㈡⒑閸撴彃浜為柛鐘冲姉缁牏鈧綆鍠楅悡娑氣偓鍏夊亾閻庯綆鍓涜ⅵ婵°倗濮烽崑鐐茬幓閸ф鐒垫い鎺嶈兌閳洖鐣濋敐鍛仴閽樻繂霉閻撳海鎽犻柍閿嬪灴閺屾稑鈹戦崱妤婁紑闂佺粯甯熷▔鏇犳閹烘绠甸柟鍝勬娴滈箖鏌i弮鍥ㄣ€冮柤鍓蹭邯濮婂宕掑▎鎴М濠电姭鍋撻弶鍫涘妿娴犳碍绻濋悽闈涗粶妞ゆ洦鍙冨缁樺緞閹邦儵锕傛煙闁箑鐏辨俊鎻掑⒔缁辨挻鎷呮禒瀣懙闂佸湱枪椤兘鐛箛娑樺窛闁哄鍨归宀勬⒑閻熺増鎯堢紒澶嬫尦钘熸慨妯垮煐閳锋帡鏌涚仦鍓ф噮妞わ讣绠戦…鍧楁偡鐢喛鍚悗瑙勬礃閸ㄥ墎绮悢鐓庣劦妞ゆ巻鍋撻柣锝囨焿閵囨劙骞掗幘铏吋闂備線娼ч悧鍡涘箯鐎n€稑饪伴崼鐔叉嫼缂備礁顑堝▔鏇犵不閾忣偁浜滈柟瀵稿仦缁€鍐磼閸屾氨孝妤楊亙鍗冲畷濂告偄閸濆嫬绠伴梻鍌欑閹诧繝宕濋幋锕€绀夌€广儱顦粻褰掓煙闁箑鏋熼柛瀣墬閹便劌螣閸喚鍘梺鎶芥敱閸ㄥ潡寮婚悢鐓庣畾闁哄鏅濋幘缁樼厸濞撴埃鍋撳ù婊冪埣楠炲啯绂掔€e灚鏅梺闈涚墕濞层劑鎯侀崼銉﹀€垫繛鍫濈仢閺嬶附銇勯弴鍡楁祩閺佸洤鈹戦崒婧撳綊鏌嬮崶銊d簻闁规澘澧庣粔鐢告煃瑜滈崜娆徝洪鐑嗘綎缂備焦蓱婵挳鏌涘☉姗堝伐闁哄棗鐗撳铏规喆閸曨厽鎲欏銈嗘肠閸ラ绋忓┑鐘绘涧椤戝懏鍎柣鐔哥矊缁夌懓鐣烽悷鎵虫斀闁搞儮鏅濋鏇㈡⒑缁洖澧查拑閬嶆倶韫囷絽骞樼紒杈ㄥ浮閹晠宕樺ù瀣亞闂備礁鎼惌澶屾崲濠靛棛鏆﹂柛顐f礀閻撴稑霉閿濆懏璐¢柍褜鍓熺粻鏍ь潖濞差亝顥堥柍鍝勫暟琚﹂梻浣姐€€閸嬫捇寮堕崼姘珕鐎规洖寮剁换婵嬫濞戝崬鍓遍梺绋款儍閸旀垵顫忔繝姘唶闁绘棁銆€濡晝绱撴笟鍥ф灈闁绘牜鍘ч~蹇涙惞閸忓浜鹃柣褎鎮傚顔界節閵忊埄鎴﹀箞閵娾晛纾兼繝褎鍎虫禍楣冩偡濞嗗繐顏紒鈧埀顒勬⒑鐠囪尙绠茬€光偓閹间胶宓侀柛鈩冪☉缁秹鏌涢锝嗗剷闁冲搫鎳忛悡蹇擃熆鐠団€崇仩缂佸鍩栫粙澶愬箵閹哄棙鏂€闂佺粯锚閻忔岸寮抽埡浣叉斀闁绘劏鏅涙禍鐐節閻㈤潧浠掗柛鏍█瀹曞爼鎳滈崹顐g彈闂傚倷绀侀幉锛勭矙閹达附鍋ら柕濞р偓閸嬫挸顫濋浣告畻闂佸搫鐭夌紞浣割嚕椤掑嫬鍨傛い鏃囨閳ь剦鍨跺铏圭磼濡纰嶇紓浣虹帛閸旀瑩宕洪悙鍝勭闁挎棁妫勯埀顒傚厴濮婂宕奸悢琛℃)婵犮垼顫夊ú鏍煘閹达附鍊烽柛娆忣槸濞咃絽鈹戦埥鍡椾簼缂佽鐗嗛锝囨嫚濞村顫嶅┑顔斤公缁茶姤绂嶆ィ鍐╃叆婵犻潧妫涢崙鍦磼閵娿儱鎮戦柕鍥у婵$兘鏁愰崨顖欑礄闂備礁鎼惌澶屾閺囩喓顩烽柨鏇炲€哥粈鍫㈡喐鐎n喖鐒垫い鎺嶇缁楁帡妫佹径鎰厽婵炲棗绻戦崳浠嬫煟閿濆洦鏆╅柍褜鍓濋~澶娒哄Ο鐓庡灊闊洦铔嬮崶顒夋晩闁瑰瓨甯炵粻姘舵⒑閸︻厾甯涢悽顖滃仦閺呭爼寮撮悢缈犵盎濡炪倕绻愮€氼剟寮抽敐鍛斀闁炽儱纾崺锝団偓瑙勬磸閸斿酣鍩€椤掑倹鏆╅弸顏呬繆閻愭壆鐭欐慨濠勭帛閹峰懘鎮滃Ο鐑樼暚闂備焦鎮堕崐鏍偋閻樿崵宓侀煫鍥ㄧ⊕閺呮悂鏌ㄩ悤鍌涘14濠电姷鏁告慨鐑藉极閸涘﹥鍙忛柣鎴f閺嬩線鏌涘☉姗堟敾闁告瑥绻橀弻锝夊箣閿濆棭妫勯梺鍝勵儎缁舵岸寮诲☉妯锋婵鐗婇弫楣冩⒑閸涘﹦鎳冪紒缁橈耿瀵鏁愭径濠勵吅闂佹寧绻傚Λ顓炍涢崟顖涒拺闁告繂瀚烽崕搴g磼閼搁潧鍝虹€殿喛顕ч埥澶娢熼柨瀣垫綌婵犳鍠楅〃鍛存偋婵犲洤鏋佸Δ锝呭暞閳锋垿鏌涘☉姗堝姛闁瑰啿鍟扮槐鎺旂磼濡搫顫掑┑鐘亾濞撴埃鍋撴慨濠呮缁瑧鎹勯妸褜鍞堕梻浣告啞閼归箖顢栭崶鈺傤潟闁绘劕鎼粻锝夋煥閺冨倹娅曢柛姗€浜跺娲濞淬劌缍婂畷鏇㈡焼瀹ュ懐鍔﹀銈嗗坊閸嬫挻銇勯鐘插幋闁绘侗鍠楀鍕箛椤掑偆鍟囧┑鐐舵彧缁插潡骞婇幘瀵割洸闂侇剙绉甸埛鎴︽煕閹炬潙绲诲ù婊勭箘缁辨帞鎷犻幓鎺濅純闂佽鍠氶崗妯侯嚕婵犳艾唯闁挎棁顫夌€氳偐绱撻崒娆戭槮妞ゆ垵鎳愭禍鎼佸川椤撗冩櫊闂侀潧顦弲婊堟偂閻斿吋鐓涚€规搩鍠曠粈浣圭椤曗偓閹鈻撻崹顔界仌濡炪倖娉﹂崶褏鍙€婵犮垼鍩栭崝鏇綖閸涘瓨鐓冮柛婵嗗閳ь剛鎳撻埢宥夊炊椤掍讲鎷绘繛杈剧秬濞咃絿鏁☉銏″珔閺夊牃鏅滈崰鎰版煛婢跺﹦浠㈤柡鍡欏仱閺岀喐绗熼崹顔碱瀴闂佽鍨卞Λ鍐╀繆閹间焦鏅滈悷娆忓椤忕懓鈹戦悩鎰佸晱闁哥姵宀搁獮濠囧箻鐡掍焦妞芥俊鑸靛緞婵犲嫬濮︽俊鐐€栫敮濠勬閳ユ枼鏋旀繝濠傛噳閸嬫挾鎲撮崟顒傤槰闂佹悶鍔屽ḿ锟犳偘椤旂⒈娼ㄩ柍褜鍓熼獮濠傗堪閸噥妫冨┑鐐村灦宀e潡宕惔鈾€鏀介柣妯虹仛閺嗏晠鏌涚€n剙浠辩€规洖缍婇、娑㈡倷閹绘帞鈧參姊洪棃鈺佺槣闁告ḿ鍋撶粙澶婎吋婢跺鍙嗗┑鐘绘涧濡瑩藟閻樼數纾奸柣妯垮吹閻f椽鏌$仦鍓ф创闁糕晛瀚板畷姗€鎮欓鍌涙瘔缂傚倸鍊烽懗鑸垫叏閹绢喖鐤柛褎顨嗙粻鎺楁⒒娴h櫣甯涢弸顏嗏偓瑙勬礈閺佸骞冩ィ鍐╁€绘俊顖濐嚙瀵寧绻濋悽闈浶㈤柟鍐茬箻椤㈡棃鎮╅悽鐢碉紲濡炪倖姊婚弲顐﹀箠閸愵喗鐓冮悹鍥ㄧ叀閸欏嫭顨ラ悙鍙夘棥妞わ附褰冮…璺ㄦ喆閸旂瓔浜崺鐐哄箣閿旇棄鈧兘鏌ょ喊鍗炲闁硅尪鍋愮槐鎾寸瑹閸パ勭亾婵犳鍠氶弫鍝ュ垝鐎n亶鍚嬪鑸瞪戦弲婊堟⒑閸涘﹥绀嬫繛浣冲啠鏋旈柕濞炬櫆閻撶喖鏌eΟ鍝勭骇濠㈣泛瀚槐鎺撴媴鐟欏嫮绋囬柛妤呬憾閺屾盯顢曢悩鎻掑闂佺粯鎸哥换姗€鎮¢锕€鐐婇柕濠忓椤︺儵鎮楀☉娆戠疄闁诡喗顨堥幉鎾礋椤掆偓绾板秴鈹戦埥鍡椾簼缂佽鍊块敐鐐剁疀閹句焦妞介、鏃堝椽娴h妫冨┑鐘垫暩閸嬬偤鎮鹃鍫濈鐎光偓閳ь剛妲愰悙瀵哥瘈闁稿本绮嶅▓楣冩⒑閸濆嫭鍌ㄩ柛銊︽そ閹偤鎳栭埞鎯т壕妤犵偛鐏濋崝姘舵煙閾忣偄濮嶇€规洏鍨介弻鍡楊吋閸″繑瀚奸梻渚€娼荤€靛矂宕㈡總绋跨閻庯綆鍠楅悡鏇㈡煏婵炑冨暞閻忓牓鎮楀▓鍨灁闁告柨绉剁划瀣箳閺傚搫浜鹃柨婵嗛娴滅偤鏌涘Ο鍦煓婵﹪缂氶妵鎰板箳閹存粌鏋堥梻浣规偠閸斿宕¢幎钘夌畾闁告劦鍠栨导鐘绘煕閺囩姵鏆╅柛鐐垫暬閹嘲饪伴崘鎯у壎閻庤娲濋~澶岀矉閹烘柡鍋撻敐搴濇捣闁硅姤娲熷铏规崉閵娿儲鐏佹繝娈垮枟濞兼瑩鈥旈崘顔藉癄濠㈣绻傜紞濠囧极閹邦厼绶為悗锝庡亞瑜版悂姊绘担鍛婃喐濠殿喗鎸抽弫鍐敂閸曞灚缍庨梺鎯х箳閹虫挾鈧灚鐓¢弻锟犲炊閳轰焦鐎惧┑鐘灪鐢€愁潖閾忓湱鐭欐繛鍡樺劤閸撻亶姊洪悷鐗堝暈闁诡喖鍊块崹楣冨籍閸繄顦ㄥ銈嗘煥濡插牐顦归柡灞剧洴閸╁嫰宕橀悙顒傛殽婵犵數鍋涢崥瀣垂閸噮娼栭柧蹇撴贡閻瑦绻涢崱妯哄姢闁告捇浜跺娲捶椤撶喎娈屽┑鐐叉▕閸樺ジ顢氶敐鍥ㄥ珰婵炴潙顑嗛~宥呪攽閳藉棗鐏$紒顔奸叄瀹曚即寮介鐐电枃闂佽法鍠撴慨鏉戞纯闂備焦鎮堕崕顕€寮插☉姘殰闁靛ň鏅滈埛鎴︽偣閸パ冪骇闁哥偛顦伴妵鍕敃閵忊晜笑闁绘挶鍊栭幈銊ヮ渻鐠囪弓澹曢柣搴ゎ潐濞叉牜绱炴繝鍌滄殾缂佸顕抽弮鍫濈闁靛ě浣镐喊婵犵數濮烽。钘壩i崨鏉戝瀭闁汇垻枪绾惧鏌熼柇锕€鏋涙い銉﹀哺閺屾稖绠涘☉娆欑吹缂備浇顕уΛ娆撳Φ閸曨垰鍐€闁靛ě鍛帎闂佹眹鍩勯崹浼存偉婵傜ǹ绠栧ù鐘差儛閺佸秵绻涢幋锝夊摵闁汇倓绶氬娲传閸曨厾鍔圭紓鍌氱С缁舵岸鐛崘顔碱潊闁靛牆鎳嶇槐鍫曟⒑闂堟冻绱¢柛娑卞幖缁楁帞绱撻崒姘偓鎼佸磹妞嬪孩顐介柨鐔哄Т缁愭淇婇妶鍛櫣缂佺姳鍗抽弻鐔兼⒒鐎电ǹ濡介梺绋款儌閺呮繈鍩€椤掑倹鍤€閻庢凹鍘界粩鐔衡偓锝庡枛闁卞洦銇勮箛鎾跺闁绘挻娲橀妵鍕箛閳轰讲鍋撻弴銏犲嚑閹肩补鍩楅悷鎵冲牚闁告洦鍘鹃悡澶娾攽椤旂》榫氭繛鍜冪悼濡叉劙骞掗幊宕囧枔閹风娀鎳犻澶嬫婵犵數濮烽弫鎼佸磻濞戙埄鏁嬫い鎾卞灩缁€鍌涙叏濡炶浜惧Δ鐘靛仜閸燁垶濡堕敐澶婄闁宠桨璁查崑鎾剁磼濡湱绠氬銈嗙墬缁诲倹绂嶇憴鍕╀簻闁哄啠鍋撴繛鑼枎椤繐煤椤忓嫪绱堕梺鍛婃礀閻忔碍鏅ラ梻鍌欑劍閹爼宕濇惔銊ユ瀬濠电姵姘ㄥ畵渚€鏌涢幇闈涙灈缂佺媴缍侀弻锝夊箛椤旇姤姣勫銈嗘⒐濞茬喎顫忛搹鍦煓閻犳亽鍔庨鎴︽⒑缁嬫鍎愰柛鏃€鐟╅悰顔界節閸パ咁槰濡炪倖姊婚弲顐﹀储閸涘﹦绠鹃柟鍓ь棎婢规ɑ绻涚仦鍌氣偓鏇㈠煝瀹ュ拋鍚嬮柛鈩兠鎸庣節閻㈤潧孝閻庢凹鍠氶弫顔尖槈閵忥紕鍘甸悗鐟板婢ф宕甸崶鈹惧亾鐟欏嫭澶勯柛瀣攻娣囧﹪鎮滈懞銉︽珕闂備焦顑欓崹鐗堢閻愵兙浜滈柡鍌濇硶濮g偤鏌¢埀顒佺鐎n偆鍘撻梺瀹犳〃缁€渚€寮抽弬妫靛綊鎮╅棃娑掓瀰闂佸搫鏈惄顖氼嚕椤曗偓閸┾偓妞ゆ帒瀚崹鍌炴煕瑜庨〃鍫濈暤娴g硶鏀介柣妯垮紦鏉╁綊鏌¢崘銊у鐎瑰憡绻冮妵鍕箻閸楃偟浠奸梺杞扮缂嶅﹤顫忕紒妯诲闁告稑锕ラ崕鎾斥攽閻愯尙婀撮柛鏃€鍨甸悾鐑芥偋閸喎鍔呴梺闈涚箞閸╁嫬煤缁嬪簱鏀介幒鎶藉磹閺囥垹绠犻煫鍥ㄧ☉閻撴洟鏌熺€电ǹ啸婵☆偒鍨遍妵鍕箻鐠鸿桨娌梺闈╃秬濞咃綁骞夐幖浣哥濠电姴鍊规径鍕煃闁垮娴柡灞剧洴瀵挳濡搁妷銈囩泿婵$偑鍊曞ù姘跺矗閸愵喖钃熸繛鎴欏灩閻撴盯鏌涚仦鍓х煁闁告帗绋戣灃闁绘﹢娼ф禒婊勩亜閹存繍妯€鐎殿噮鍋婂畷鎺楁倷閺夋垳鎮i梺璇茬箳閸嬬姴螞閸曨厾涓嶉柕澹懐锛濋梺绋挎湰閼归箖鍩€椤掑嫷妫戠紒顔肩墛缁楃喖鍩€椤掑嫨鈧線寮介鐐茶€垮┑鐐叉閼活垱绂嶉崜褏纾兼俊銈勮兌閳藉绻涚仦鍌氣偓妤冨垝婵犳艾钃熼柕澶涘閸欏棗鈹戦悩缁樻锭婵☆偅鐟ラ蹇撯攽閸垺锛忛梺璇″瀻娴i晲鍒掗梻浣告惈閻寰婇崐鐔轰航闂備礁婀辨灙婵炲鏌夐妵鎰樄闁哄矉缍€缁犳盯骞橀崜渚囧敼濠电姰鍨婚幊鎾澄涘☉妯滐綁骞囬弶璺唺闂佸搫鍟崐濠氭晬濠婂啠鏀介柍钘夋閻忥絾銇勯幋鐐寸闁糕斁鍋撳銈嗗笂缁€浣该归鈧弻鈥崇暆閳ь剟宕伴幇鍏洭鎮ч崼鐔峰妳闂佸疇椴哥敮鈺呭礈濮樿泛桅闁告洦鍨遍弲婊堟煠閹帒鍔氶柛鐐差樀濮婃椽宕崟顓犲姽缂傚倸绉崇欢姘嚕椤愶箑绠涢柡澶庢硶閸婄偤姊洪棃娑掑悍闂傚嫬瀚伴幆渚€骞樼紒妯锋嫽婵炶揪绲介幉锟犲箚閸儲鐓熸い鎺嗗亾闁靛牏枪閻i攱瀵奸弶鎴濆敤濡炪倖鎸绘竟鏇㈠磻閹惧瓨濯撮柛鎾冲级閸嶇敻鏌i悩鑽ょ窗婵炲拑缍佸畷婵嬫晝閳ь剟鈥旈崘顔嘉ч柛鈩冾殘閻熴劑姊虹粙鍖″姛缂侇噮鍨崇划娆愬緞婵犲骸鎮戞繝銏f硾椤戝洭宕㈤幖浣瑰€垫鐐茬仢閸旀艾螖閻樿櫕鍊愰柣娑卞櫍瀵粙顢橀悢鍝勫籍闂備礁鎲¢崝锔界濠婂牆鍑犳繛鎴欏灪閻撴盯鎮橀悙鎻掆挃婵炲弶鎸抽弻娑㈠煛娴e壊浼冮悗瑙勬礃閿曘垽骞冨▎鎿冩晢濠㈣泛锕ラ崐鏇㈡⒒閸屾艾鈧绮堟笟鈧獮澶愭晸閻樺啿娈炴俊銈忕到閸犳岸寮崟顐唵闁兼悂娼ф慨鍥煢閸愵亜鏋戠紒缁樼洴楠炲鈻庤箛鏇氭偅闂備胶绮敮妤€顪冩禒瀣摕婵炴垯鍨圭粻娑㈡煕韫囨挻鎲搁柛鎴濈秺濮婃椽妫冮埡鍌楀亾閵夆晛绀傞柣鎰靛墯椤ュ牓鏌熼瑙勬珚婵☆偄鍟埥澶娢旀担绋款€忛梻鍌氬€烽悞锔锯偓绗涘厾楦跨疀濞戞ê鐎悷婊呭鐢亞绱為弽顓犲彄闁搞儯鍔嶇粈鍫㈢棯閹冩倯濞e洤锕、娑樷攽閹邦剚顔勬俊鐐€曠€涒晠骞戦崶褜娼栨繛宸簻瀹告繂鈹戦悩鎻掝仱婵℃彃鐗撳娲箰鎼淬垻锛橀梺绋匡攻缁诲倿顢氶敐澶婄闁芥ê顦甸崬鍫曟⒑闂堟侗妾ч柤闈涚秺楠炲繐煤椤忓應鎷洪梺缁樻尭鐎垫帒岣块悢鍏肩厱濠电姴鍟粈瀣偓娈垮枟閹倸鐣烽幒妤佸€烽悗鐢登归獮鍫ユ⒑閸︻厼甯堕柣掳鍔庨幑銏ゅ礋椤撶姷鐒鹃梻浣哥仢椤戝嫮鎹㈤崱妯镐簻闁规壋鏅涢埀顒佹礋瀵ǹ鈽夐姀锛勫幐闁诲繒鍋熸灙濠⒀嗗皺閳ь剙鐏氬妯尖偓姘煎幘閹广垹鈹戠€n亞顦板銈嗗姦閸嬪懎鈻撴總鍛娾拻闁稿本鐟чˇ锕傛煙绾板崬浜版鐐诧龚缁犳盯寮撮悢宄扮哎闂備礁鎲¢崝锔界閻愮儤鍎楁繛鍡楁禋閻斿棝鎮规ウ瑁も偓鈧柣顏勵儔閺屾稑顫濋澶婂壎闂佸搫鏈惄顖炲春閸曨垰绀傞柣娆屽亾濞存粍绮撻、姘舵晲婢跺﹤鐎銈嗘椤寮埀顒勬⒒娴e摜鏋冩俊顐㈠铻炴俊銈呮噺閸婂爼鏌eΟ鑲╁笡闁绘挾鍠栭悡顐﹀炊閵婏腹鎷荤紓浣哄Х閸嬨倝寮婚悢纰辨晪闁糕剝鐟ч惁鍫澪旈悩闈涗粶婵炲樊鍙冮獮鍐樄鐎规洖銈告慨鈧柣妯垮皺椤旀垿姊婚崒姘偓宄懊归崶顒婄稏濠㈣埖鍔曠壕鍧楁煙閹澘袚闁稿鍊濋弻鏇熺箾瑜嶉幊鎰版倿婵傚憡鐓熼幖鎼灣缁夌敻鏌涢悩鎰佹疁闁诡喒鈧枼妲堟慨姗堢到娴滈箖鏌涜箛鎿冩Ц濞存粓绠栧娲焻閻愯尪瀚板褍顕埀顒冾潐濞叉垿宕¢崘宸殨濞寸姴顑愰弫鍥煟閹邦喗鏆╅柡鍡╁亝缁绘繈鎮介棃娑楃捕濠碘槅鍋呴悷鈺呯嵁閺嶎厼鐓涢柛娑卞幗閻庮剟姊虹化鏇炲⒉妞わ箓缂氶妵鎰板箳閹惧瓨鐝抽梻浣稿閸嬪棝宕抽妷锔绢浄闁冲搫鎳忛埛鎴︽倵閸︻厼顎岄柛銈嗙懅缁辨帞绱掑Ο铏逛桓缂備礁鐭佹ご鍝ユ崲濠靛鐐婇柕濞垮劗閸嬫捇鏌ㄧ€c劋绨婚棅顐㈡处閹告悂顢旈妶澶嬬厱閻庯綆鍋呭畷灞绢殽閻愬樊鍎旈柡浣稿暣閸┾偓妞ゆ帒鍊搁ˉ姘舵煕瑜庨〃鍡涘煕閹寸偑浜滈柟鍝勬娴滃墽绱撴担鍓插剮缂佽埖鑹鹃锝夘敃閿曗偓缁€瀣亜閺嶃劎銆掗柛姗€浜跺娲濞戣鲸肖闂佹悶鍔岄幖顐﹀煝瀹ュ骞㈡俊顖炴櫜缁ㄨ顪冮妶鍡楀Ё缂佹彃澧界划鍫⑩偓锝庡枟閻撴稓鈧厜鍋撻柍褜鍓熷畷浼村冀椤撶偟鐣哄┑鐘诧工閸氭﹢鎮㈤悜妯虹彴闂佸搫琚崕鎶藉焵椤掑啯顏犵紒杈ㄦ崌瀹曟帒顫濋钘変壕闁告縿鍎抽惌鎾绘煛婢跺娈繛宸憾閺佸洭鏌曡箛鏇炐柟鑺ユ礋濮婃椽宕崟顒€绐涢梺鍝ュУ閹稿墽鍒掔紒妯稿亝闁告劏鏅濋崢鍗烆渻閵堝骸骞楅柛銊ф暬瀵ǹ鈽夊Ο閿嬫杸濡炪倖妫佹慨銈囩矆鐎n喗鐓涚€光偓鐎n剛袦闂佽鍠掗弲鐘茬暦閿濆棗绶炲┑鐘插瀹曟椽姊婚崒娆掑厡閺嬵亝銇勯幋婵嗘殻鐎规洘鍔曢埞鎴犫偓锝庡墮缁侊箓姊洪崨濠傚闁告搩鍣e顕€宕煎┑鍫О闂備礁鐤囧銊╂倿閿曞倹鍊垫い鎾卞灪閳锋帒霉閿濆懏鍟為柛鐔哄仦缁绘稓鎷犺閻g數鈧娲樼划宀勫煡婢舵劕鐓戦柛婵嗗閸犳ê鈹戦敍鍕幋闁糕晪绻濆畷鎺戭潩閿濆懍澹曢梺姹囧灩閹诧繝宕戦埄鍐闁糕剝顨堢粻鐗堛亜韫囷絼绨绘い顓℃硶閹瑰嫰宕崟鍏哥磾闂備礁鎼張顒勬儎椤栫偟宓佹俊顖氬悑瀹曞鏌i幋鐐ㄧ細濞存粠浜缁樻媴閼恒儯鈧啴鏌i幒鐐电暤鐎规洘绻傞埢搴ㄥ箻瀹曞洨鏆繝鐢靛仜濡娆㈤悜钘夋嵍妞ゆ挻绋戞禍楣冩煥濠靛棝顎楀ù婊勭箞閺屸剝寰勭€n偄鈧劖鎱ㄦ繝鍛仩闁归濞€楠炴捇骞掗幋鐐垫И缂傚倸鍊峰ù鍥ь嚕閹捐泛鍨濇繛鍡樻尭缁犳牗淇婇娆掝劅婵炲皷鏅犻幃瑙勩偊閹稿寒浠╅梺鍝勭潤閸ャ劉鎷洪梻鍌氱墛缁嬫挾绮婚悙鐑樼厱濠电姴鍟版晶鐢告煕閳哄倻娲存鐐差儔閺佸倻鎲撮敐鍡楊伖濠碉紕鍋戦崐鏍礉閹达箑纾归柡鍥╁枔椤╅攱绻濇繝鍌滃闁绘挾濮电换娑㈡嚑妫版繂娈梺璇查獜缁绘繈寮婚敓鐘插窛妞ゆ挾濮撮悡鐔奉渻閵堝啫鐏柣鈺婂灦楠炲啫鈻庨幋鏂夸壕闁汇垻娅ヨぐ鎺斿祦鐎广儱鎳夐弨浠嬫煟閹邦剛鎽犻悘蹇庡嵆閺屻倛銇愰幒鏃傛毇闂佽鍠楅敋闁宠鍨垮畷鍫曞Ω閵夈儰绱熼梻鍌欒兌鏋柡鍫墯缁旂喖寮撮姀鐘碉紱闂佽宕橀崺鏍窗閸℃稒鐓曢柡鍥ュ妼婢х増銇勯敂鍝勫婵﹥妞介獮鎰償閵忣澁绱梻浣规偠閸斿鍒掑▎鎰箚閻庢稒蓱婵绱掗娑欑闁诲骸顭峰娲偡闁箑娈堕梺绋款儐閻╊垰顕i幖浣哥<闁绘劗琛ラ幏娲⒑閸︻厐鐟懊规搴d笉闁瑰墽绻濈换鍡樸亜閹板墎绉垫繛鍫熺矋閵囧嫰濮€閳╁喚姊块梺闈涙处閸旀瑩鐛幒妤€绠绘い鏍ㄧ☉椤忔椽姊婚崒娆掑厡閺嬵亪鏌¢崼顐㈠⒋闁诡喚鏌夐ˇ褰掓寠濠靛鐓ラ柡鍐ㄥ€瑰▍鏇犵磼閳锯偓閸嬫捇姊绘笟鈧埀顒傚仜閼活垱鏅堕娑氱闁绘挸娴风粻璇测攽閳╁啰鎽冩い锕佷含缁辨帡顢欓懖鈺傛喖缂備胶绮换鍌烆敋閵夆晜鐓ラ悗锝庡亞閸戯繝姊洪柅鐐茶嫰婢ь垱銇勯妸銉︻棦妤犵偛鐗撴俊鎼佸煛閸屾矮缂撶紓鍌欑椤戝牆鈻旈弴銏″仼婵炲樊浜濋埛鎴犵磼鐎n偄顕滄繝鈧悧鍫熷弿婵☆垳枪婵倻鈧鍠楁繛濠囧极閸愵喖鐒垫い鎺戝缁犳帡姊绘担鍛靛湱鎹㈤幇鏉胯Е閻庯綆鍓涚粈濠囨煙鏉堥箖妾柣鎾存礃娣囧﹪濡堕崟顓фМ闂佸磭绮ú鐔煎蓟閿涘嫪娌柣鎰靛墰椤︻喚绱撴担鍝勑i柣鈺婂灡娣囧﹪鎮块锝喰梻浣瑰缁嬫捇宕伴弽褜娼栨繛宸簻瀹告繂鈹戦悙鍨珪缂佸彉鍗冲鐑樻姜閻楀牏銈板銈嗘肠閸ラ绋忛棅顐㈡处閹峰煤椤忓秵鏅滈梺鍛婃处閸嬪棝鎮伴埡浣叉斀闁绘ê鐏氶弳鈺佲攽椤旇姤灏︾€规洘鍔楃槐鎺懳熺喊杈ㄧカ闁荤喐绮嶉弻銊╋綖韫囨稒鎯為柛锔诲幘閻撴捇姊洪崨濠勫ⅳ闁告挻绻堝顐c偅閸愨斁鎷虹紓鍌欑劍閿曗晛鈻撻弴鐘电<妞ゆ棁濮ゅ畷宀€鈧娲樺浠嬪春閳ь剚銇勯幒宥夋濞存粍绮撻弻鐔煎传閸曨厜銉╂煕韫囨挾鐒搁柡灞剧洴閹垽宕妷銉ョ哗闂備礁鎼惉濂稿窗閺嵮呮殾婵炲棙鎸稿洿闂佺硶鍓濋〃蹇斿閿燂拷>>
闂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌熼梻瀵割槮缁炬儳缍婇弻鐔兼⒒鐎靛壊妲紒鐐劤缂嶅﹪寮婚悢鍏尖拻閻庨潧澹婂Σ顔剧磼閻愵剙鍔ょ紓宥咃躬瀵鎮㈤崗灏栨嫽闁诲酣娼ф竟濠偽i鍓х<闁诡垎鍐f寖闂佺娅曢幑鍥灳閺冨牆绀冩い蹇庣娴滈箖鏌ㄥ┑鍡欏嚬缂併劌銈搁弻鐔兼儌閸濄儳袦闂佸搫鐭夌紞渚€銆佸鈧幃娆撳箹椤撶噥妫ч梻鍌欑窔濞佳兾涘▎鎴炴殰闁圭儤顨愮紞鏍ㄧ節闂堟侗鍎愰柡鍛叀閺屾稑鈽夐崡鐐差潻濡炪們鍎查懝楣冨煘閹寸偛绠犻梺绋匡攻椤ㄥ棝骞堥妸鈺傚€婚柦妯侯槺閿涙稑鈹戦悙鏉戠亶闁瑰磭鍋ゅ畷鍫曨敆娴i晲缂撶紓鍌欑椤戝棛鈧瑳鍥ㄥ€垫い鎺戝閳锋垿鏌i悢鍛婄凡闁抽攱姊荤槐鎺楊敋閸涱厾浠搁悗瑙勬礃閸ㄥ潡鐛崶顒佸亱闁割偁鍨归獮妯肩磽娴e搫浜炬繝銏∶悾鐑筋敆娴h鐝风紓鍌欑劍鐪夌紒璇叉閺岋紕浠︾拠鎻掑闂佽鐓$粻鏍蓟閳ュ磭鏆嗛悗锝庡墰琚﹂梻浣筋嚃閸犳捇宕归挊澶屾殾妞ゆ劧绠戝敮閻熸粌绻樺畷銏ゅ箳閹存梹鏂€闂佺粯锕╅崑鍛垔娴煎瓨鐓曢柡鍥╁仧娴犳盯鏌i敐鍛仮婵﹦鍎ゅḿ顏堝箥椤旇法鐛ラ梻渚€娼荤紞鍥╃礊娓氣偓閹即顢氶埀顒勭嵁閹烘嚦鏃堝焵椤掑倻灏电€广儱顦伴悡鏇㈡倶閻愭彃鈷旈柣顓炵焸閺屾盯寮捄銊ョ厽濠殿喖锕︾划顖炲箯閸涱垳鐭欐繛鍡欏亾椤ユ垿姊绘担鍛靛綊顢栭崨顓囨稑鈹戦崱娆愭婵炴潙鍚嬪ḿ娆戠不婵犳碍鍋i柛婵嗗閹牏鎮敐澶嬧拻濞撴埃鍋撻柍褜鍓涢崑娑㈡嚐椤栨稒娅犻悗娑櫳戦崣蹇撯攽閻樻彃浜為柣鎾瑰亹閳ь剝顫夊ú妯兼暜閹烘缍栨繝闈涱儏绾偓闂佺粯鍨靛Λ娆忣熆閹寸偟绡€闁汇垽娼ф禒锕傛煙濮濆苯鍚归柛鐘诧工椤撳吋寰勯崼姘壕闁告劏鏅濈弧鈧梺绋挎湰缁秴鈻撴ィ鍐┾拺闁告繂瀚婵嬫煕鐎n偄濮囬崡閬嶆煕椤愮姴鍔滈柣鎾崇箻閻擃偊宕堕妷銉ュБ缂佺偓鍎冲ḿ锟犲蓟濞戞鐔兼倻濡儤娈樼紓鍌欒兌缁垳绮欓幒鎴撶細闊洦绋戠粈鍫㈡喐瀹ュ鏄ラ悘鐐插⒔缁♀偓闂侀潧绻堥崹娲吹閳ь剟姊洪幐搴㈠濞存粍绮撻幃楣冩倻閽樺宓嗛梺闈涚箳婵兘鎯堥崟顖涒拺闁告挻褰冩禍鐐烘煕閻樿櫕宕岀€规洏鍨介獮鏍ㄦ媴閸︻厼骞楅梻濠庡亜濞诧箑煤閺嶃劎顩风憸鏃堝蓟閿熺姴妞藉ù锝夋櫜缁ㄥジ姊洪崫鍕櫡闁稿海鏁诲濠氭晲閸℃ê鍔呴梺闈涚墕鐎涒晝绱為崼婵冩斀闁绘劙顤傞崵瀣磼閻樿櫕灏柣锝囧厴楠炲鎮欓悽鐢垫闂備胶枪閺堫剛鍒掑鍛灁濡わ絽鍟埛鎴犵磽娴h偂鎴﹀煕閹烘鐓冪€瑰嫭澹嗘晶锔锯偓娈垮櫘閸嬪﹤鐣峰鈧、娆撴偩鐏炶棄绠洪梻鍌欑閹碱偊宕鈷氭椽鏁冮崒娑樻畼闂佽崵鍠栭崑濠囨偄閸℃稒鍋℃繛鍡楃箰椤忣亞绱掗埀顒傗偓锝庡枟閻撴稓鈧厜鍋撻悗锝庡墰琚﹂梻浣筋嚃閸犳捇宕归挊澶屾殾妞ゆ劧绠戝敮闂佹寧娲嶉崑鎾寸箾閸涱喖鐏存慨濠呮閹风娀骞撻幒婵嗗Ψ闂備礁鎲¢崹鐢电礊婵犲倻鏆﹂柟鎯板Г閺呮彃顭跨捄濂斤繝濡烽埡鍌滃幈濠电偞鍨堕悷锔剧礊閹达附鐓㈤柛鎰典簻閺嬫盯鏌$仦鐐鐎垫澘瀚埥澶婎潨閸℃ê鏋犻梻鍌欑閹诧繝鏁冮埡鍌滎洸妞ゅ繐瀚峰ḿ鏍ㄧ箾瀹割喕绨荤紒鈧崼銉︾厵缂備焦锚缁楀倻绱掗妸銊ヤ汗缂佽鲸鎸婚幏鍛驳鐎n亝顔勭紓鍌欑椤︽澘岣垮▎蹇曟殼闁告洦鍨遍崑鈩冪節婵犲倹鍣规い锝呫偢閹粙顢涘☉杈ㄧ杹闂佽鍣换婵嬪箖閵忋倕绀傞柤娴嬫櫅楠炲秹姊绘担绛嬪殐闁搞劌閰e畷銊╊敊閽樺鐏堢紓鍌氬€搁崐椋庢媼閺屻儱纾婚柟鍓х帛閸婄敻鏌ㄥ┑鍡涱€楅柡瀣枛閺岋綁骞樼€靛憡鍒涢梺璇″枟閿曘垽骞冨▎鎾搭棃婵炴垶顨呴ˉ姘辩磽閸屾瑨顔夐柛瀣崌閺屾盯骞囬崗鍝ユ寜闂佺ǹ顑嗛幑鍥х暦瑜版帩鏁冮柨婵嗘搐閸ゆ帡姊虹拠鎻掝劉闁告垵缍婂畷鎶芥晲婢跺﹥妲梺閫炲苯澧柕鍥у楠炴帡骞嬮姘潬缂傚倷绀侀ˇ闈涐缚瑜斿﹢浣糕攽閻樿宸ラ柟鍐插缁傛帡鏁傞崜褏锛滈梺绋挎湰缁嬫垵霉椤旂瓔娈介柣鎰彧閼版寧銇勯姀锛勬噰闁诡喖澧芥禒锕傛寠婢跺矈鍟堥梻鍌氬€烽懗鍫曞箠閹捐瑙﹂悗锝庡枟閸嬧晜銇勮箛鎾跺闁搞劌鍊婚幉鎼佹偋閸繄鐟ㄩ梺鍛婁亢椤濡甸崟顖氱闁瑰瓨绻嶆禒楣冩⒑缂佹ɑ灏版繛鑼枛瀵鎮㈤悡搴g暰閻熸粌绻橀獮妤呮偐缂佹ḿ鍘介梺闈涒康缁犳垿鎮橀埡鍐<閺夊牄鍔屽ù顔姐亜閵忥紕鎳呴柛鐘诧躬瀹曪繝鎮欓幓鎺濇婵犵绱曢崑鎴﹀磹閺嶎厼绠伴柟闂寸鐟欙箓鎮楅敐搴濇喚闁搞倖顨婇弻娑㈠即閵娿儱绠伴梺绋款儐閹瑰洭寮幇顓熷劅闁炽儲鍓氬ḿ璇测攽閻樻剚鍟忛柛鐘愁殜楠炲啴宕掗悙鑼舵憰闂佹寧绻傚Λ娆撳磿閻斿吋鐓ユ繛鎴灻顐︽煛閸℃ḿ娲存慨濠呮缁瑩宕稿Δ濞惧亾濡ゅ啠鍋撶憴鍕闁告挻绻堥幃妯尖偓锝庡枟閸婄敻鏌涜箛鎿冩Ц濞存粓绠栧娲川婵犲啫顦╅梺绋款儏濡繈銆佸▎鎾冲耿婵$偟绮弬鈧梻浣虹帛閸旀洖顕i崼鏇炵厺闁哄洨浼濋悷鎵冲牚闁告洦鍘鹃悿鍕⒑缁洘娅嗛柣鈺婂灦閻涱喚鈧綆鍠楅弲婊堟煟閿濆懓瀚版鐐茬墦濮婄粯鎷呴悷閭﹀殝濠碘槅鍋傜欢姘躲€佸鎰佹Ь闂佽桨绶¢崰妤呭箚閺冨牆惟闁挎梹鍎抽獮妤呮⒒娴h櫣甯涙慨濠勭帛閻忔瑥鈹戦悙鍙夊櫧闁稿鍠栭獮澶愬箹娴g懓浜遍梺鍓插亝缁诲嫰鎮烽弻銉︹拺缂佸灏呭銉︺亜椤撶姴鍘寸€殿喖顭烽弫鍐焵椤掑啰浜介梻浣虹帛閼归箖顢氶鐘电焼闁糕剝绋掗埛鎴︽⒒閸喍绶辨俊鍙夋尦閺岋繝宕ㄩ鍓х厜闂佽鍠掗埀顒佹灱閺嬪酣鏌熼幆褜鍤熼柛妯圭矙濮婃椽鎮烽柇锕€娈堕梺绋垮閸ㄥ墎绮悢灏佹婵炲棙鍨归鏇㈡⒑閸撴彃浜為柛鐘冲姉缁牏鈧綆鍠楅悡娑氣偓鍏夊亾閻庯綆鍓涜ⅵ婵°倗濮烽崑鐐茬幓閸ф鐒垫い鎺嶈兌閳洖鐣濋敐鍛仴閽樻繂霉閻撳海鎽犻柍閿嬪灴閺屾稑鈹戦崱妤婁紑闂佺粯甯熷▔鏇犳閹烘绠甸柟鍝勬娴滈箖鏌i弮鍥ㄣ€冮柤鍓蹭邯濮婂宕掑▎鎴М濠电姭鍋撻弶鍫涘妿娴犳碍绻濋悽闈涗粶妞ゆ洦鍙冨缁樺緞閹邦儵锕傛煙闁箑鐏辨俊鎻掑⒔缁辨挻鎷呮禒瀣懙闂佸湱枪椤兘鐛箛娑樺窛闁哄鍨归宀勬⒑閻熺増鎯堢紒澶嬫尦钘熸慨妯垮煐閳锋帡鏌涚仦鍓ф噮妞わ讣绠戦…鍧楁偡鐢喛鍚悗瑙勬礃閸ㄥ墎绮悢鐓庣劦妞ゆ巻鍋撻柣锝囨焿閵囨劙骞掗幘铏吋闂備線娼ч悧鍡涘箯鐎n€稑饪伴崼鐔叉嫼缂備礁顑堝▔鏇犵不閾忣偁浜滈柟瀵稿仦缁€鍐磼閸屾氨孝妤楊亙鍗冲畷濂告偄閸濆嫬绠伴梻鍌欑閹诧繝宕濋幋锕€绀夌€广儱顦粻褰掓煙闁箑鏋熼柛瀣墬閹便劌螣閸喚鍘梺鎶芥敱閸ㄥ潡寮婚悢鐓庣畾闁哄鏅濋幘缁樼厸濞撴埃鍋撳ù婊冪埣楠炲啯绂掔€e灚鏅梺闈涚墕濞层劑鎯侀崼銉﹀€垫繛鍫濈仢閺嬶附銇勯弴鍡楁祩閺佸洤鈹戦崒婧撳綊鏌嬮崶銊d簻闁规澘澧庣粔鐢告煃瑜滈崜娆徝洪鐑嗘綎缂備焦蓱婵挳鏌涘☉姗堝伐闁哄棗鐗撳铏规喆閸曨厽鎲欏銈嗘肠閸ラ绋忓┑鐘绘涧椤戝懏鍎柣鐔哥矊缁夌懓鐣烽悷鎵虫斀闁搞儮鏅濋鏇㈡⒑缁洖澧查拑閬嶆倶韫囷絽骞樼紒杈ㄥ浮閹晠宕樺ù瀣亞闂備礁鎼惌澶屾崲濠靛棛鏆﹂柛顐f礀閻撴稑霉閿濆懏璐¢柍褜鍓熺粻鏍ь潖濞差亝顥堥柍鍝勫暟琚﹂梻浣姐€€閸嬫捇寮堕崼姘珕鐎规洖寮剁换婵嬫濞戝崬鍓遍梺绋款儍閸旀垵顫忔繝姘唶闁绘棁銆€濡晝绱撴笟鍥ф灈闁绘牜鍘ч~蹇涙惞閸忓浜鹃柣褎鎮傚顔界節閵忊埄鎴﹀箞閵娾晛纾兼繝褎鍎虫禍楣冩偡濞嗗繐顏紒鈧埀顒勬⒑鐠囪尙绠茬€光偓閹间胶宓侀柛鈩冪☉缁秹鏌涢锝嗗剷闁冲搫鎳忛悡蹇擃熆鐠団€崇仩缂佸鍩栫粙澶愬箵閹哄棙鏂€闂佺粯锚閻忔岸寮抽埡浣叉斀闁绘劏鏅涙禍鐐節閻㈤潧浠掗柛鏍█瀹曞爼鎳滈崹顐g彈闂傚倷绀侀幉锛勭矙閹达附鍋ら柕濞р偓閸嬫挸顫濋浣告畻闂佸搫鐭夌紞浣割嚕椤掑嫬鍨傛い鏃囨閳ь剦鍨跺铏圭磼濡纰嶇紓浣虹帛閸旀瑩宕洪悙鍝勭闁挎棁妫勯埀顒傚厴濮婂宕奸悢琛℃)婵犮垼顫夊ú鏍煘閹达附鍊烽柛娆忣槸濞咃絽鈹戦埥鍡椾簼缂佽鐗嗛锝囨嫚濞村顫嶅┑顔斤公缁茶姤绂嶆ィ鍐╃叆婵犻潧妫涢崙鍦磼閵娿儱鎮戦柕鍥у婵$兘鏁愰崨顖欑礄闂備礁鎼惌澶屾閺囩喓顩烽柨鏇炲€哥粈鍫㈡喐鐎n喖鐒垫い鎺嶇缁楁帡妫佹径鎰厽婵炲棗绻戦崳浠嬫煟閿濆洦鏆╅柍褜鍓濋~澶娒哄Ο鐓庡灊闊洦铔嬮崶顒夋晩闁瑰瓨甯炵粻姘舵⒑閸︻厾甯涢悽顖滃仦閺呭爼寮撮悢缈犵盎濡炪倕绻愮€氼剟寮抽敐鍛斀闁炽儱纾崺锝団偓瑙勬磸閸斿酣鍩€椤掑倹鏆╅弸顏呬繆閻愭壆鐭欐慨濠勭帛閹峰懘鎮滃Ο鐑樼暚闂備焦鎮堕崐鏍偋閻樿崵宓侀煫鍥ㄧ⊕閺呮悂鏌ㄩ悤鍌涘14濠电姷鏁告慨鐑藉极閸涘﹥鍙忛柣鎴f閺嬩線鏌涘☉姗堟敾闁告瑥绻橀弻锝夊箣閿濆棭妫勯梺鍝勵儎缁舵岸寮诲☉妯锋婵鐗婇弫楣冩⒑閸涘﹦鎳冪紒缁橈耿瀵鏁愭径濠勵吅闂佹寧绻傚Λ顓炍涢崟顖涒拺闁告繂瀚烽崕搴g磼閼搁潧鍝虹€殿喛顕ч埥澶娢熼柨瀣垫綌婵犳鍠楅〃鍛存偋婵犲洤鏋佸Δ锝呭暞閳锋垿鏌涘☉姗堝姛闁瑰啿鍟扮槐鎺旂磼濡搫顫掑┑鐘亾濞撴埃鍋撴慨濠呮缁瑧鎹勯妸褜鍞堕梻浣告啞閼归箖顢栭崶鈺傤潟闁绘劕鎼粻锝夋煥閺冨倹娅曢柛姗€浜跺娲濞淬劌缍婂畷鏇㈡焼瀹ュ懐鍔﹀銈嗗坊閸嬫挻銇勯鐘插幋闁绘侗鍠楀鍕箛椤掑偆鍟囧┑鐐舵彧缁插潡骞婇幘瀵割洸闂侇剙绉甸埛鎴︽煕閹炬潙绲诲ù婊勭箘缁辨帞鎷犻幓鎺濅純闂佽鍠氶崗妯侯嚕婵犳艾唯闁挎棁顫夌€氳偐绱撻崒娆戭槮妞ゆ垵鎳愭禍鎼佸川椤撗冩櫊闂侀潧顦弲婊堟偂閻斿吋鐓涚€规搩鍠曠粈浣圭椤曗偓閹鈻撻崹顔界仌濡炪倖娉﹂崶褏鍙€婵犮垼鍩栭崝鏇綖閸涘瓨鐓冮柛婵嗗閳ь剛鎳撻埢宥夊炊椤掍讲鎷绘繛杈剧秬濞咃絿鏁☉銏″珔閺夊牃鏅滈崰鎰版煛婢跺﹦浠㈤柡鍡欏仱閺岀喐绗熼崹顔碱瀴闂佽鍨卞Λ鍐╀繆閹间焦鏅滈悷娆忓椤忕懓鈹戦悩鎰佸晱闁哥姵宀搁獮濠囧箻鐡掍焦妞芥俊鑸靛緞婵犲嫬濮︽俊鐐€栫敮濠勬閳ユ枼鏋旀繝濠傛噳閸嬫挾鎲撮崟顒傤槰闂佹悶鍔屽ḿ锟犳偘椤旂⒈娼ㄩ柍褜鍓熼獮濠傗堪閸噥妫冨┑鐐村灦宀e潡宕惔鈾€鏀介柣妯虹仛閺嗏晠鏌涚€n剙浠辩€规洖缍婇、娑㈡倷閹绘帞鈧參姊洪棃鈺佺槣闁告ḿ鍋撶粙澶婎吋婢跺鍙嗗┑鐘绘涧濡瑩藟閻樼數纾奸柣妯垮吹閻f椽鏌$仦鍓ф创闁糕晛瀚板畷姗€鎮欓鍌涙瘔缂傚倸鍊烽懗鑸垫叏閹绢喖鐤柛褎顨嗙粻鎺楁⒒娴h櫣甯涢弸顏嗏偓瑙勬礈閺佸骞冩ィ鍐╁€绘俊顖濐嚙瀵寧绻濋悽闈浶㈤柟鍐茬箻椤㈡棃鎮╅悽鐢碉紲濡炪倖姊婚弲顐﹀箠閸愵喗鐓冮悹鍥ㄧ叀閸欏嫭顨ラ悙鍙夘棥妞わ附褰冮…璺ㄦ喆閸旂瓔浜崺鐐哄箣閿旇棄鈧兘鏌ょ喊鍗炲闁硅尪鍋愮槐鎾寸瑹閸パ勭亾婵犳鍠氶弫鍝ュ垝鐎n亶鍚嬪鑸瞪戦弲婊堟⒑閸涘﹥绀嬫繛浣冲啠鏋旈柕濞炬櫆閻撶喖鏌eΟ鍝勭骇濠㈣泛瀚槐鎺撴媴鐟欏嫮绋囬柛妤呬憾閺屾盯顢曢悩鎻掑闂佺粯鎸哥换姗€鎮¢锕€鐐婇柕濠忓椤︺儵鎮楀☉娆戠疄闁诡喗顨堥幉鎾礋椤掆偓绾板秴鈹戦埥鍡椾簼缂佽鍊块敐鐐剁疀閹句焦妞介、鏃堝椽娴h妫冨┑鐘垫暩閸嬬偤鎮鹃鍫濈鐎光偓閳ь剛妲愰悙瀵哥瘈闁稿本绮嶅▓楣冩⒑閸濆嫭鍌ㄩ柛銊︽そ閹偤鎳栭埞鎯т壕妤犵偛鐏濋崝姘舵煙閾忣偄濮嶇€规洏鍨介弻鍡楊吋閸″繑瀚奸梻渚€娼荤€靛矂宕㈡總绋跨閻庯綆鍠楅悡鏇㈡煏婵炑冨暞閻忓牓鎮楀▓鍨灁闁告柨绉剁划瀣箳閺傚搫浜鹃柨婵嗛娴滅偤鏌涘Ο鍦煓婵﹪缂氶妵鎰板箳閹存粌鏋堥梻浣规偠閸斿宕¢幎钘夌畾闁告劦鍠栨导鐘绘煕閺囩姵鏆╅柛鐐垫暬閹嘲饪伴崘鎯у壎閻庤娲濋~澶岀矉閹烘柡鍋撻敐搴濇捣闁硅姤娲熷铏规崉閵娿儲鐏佹繝娈垮枟濞兼瑩鈥旈崘顔藉癄濠㈣绻傜紞濠囧极閹邦厼绶為悗锝庡亞瑜版悂姊绘担鍛婃喐濠殿喗鎸抽弫鍐敂閸曞灚缍庨梺鎯х箳閹虫挾鈧灚鐓¢弻锟犲炊閳轰焦鐎惧┑鐘灪鐢€愁潖閾忓湱鐭欐繛鍡樺劤閸撻亶姊洪悷鐗堝暈闁诡喖鍊块崹楣冨籍閸繄顦ㄥ銈嗘煥濡插牐顦归柡灞剧洴閸╁嫰宕橀悙顒傛殽婵犵數鍋涢崥瀣垂閸噮娼栭柧蹇撴贡閻瑦绻涢崱妯哄姢闁告捇浜跺娲捶椤撶喎娈屽┑鐐叉▕閸樺ジ顢氶敐鍥ㄥ珰婵炴潙顑嗛~宥呪攽閳藉棗鐏$紒顔奸叄瀹曚即寮介鐐电枃闂佽法鍠撴慨鏉戞纯闂備焦鎮堕崕顕€寮插☉姘殰闁靛ň鏅滈埛鎴︽偣閸パ冪骇闁哥偛顦伴妵鍕敃閵忊晜笑闁绘挶鍊栭幈銊ヮ渻鐠囪弓澹曢柣搴ゎ潐濞叉牜绱炴繝鍌滄殾缂佸顕抽弮鍫濈闁靛ě浣镐喊婵犵數濮烽。钘壩i崨鏉戝瀭闁汇垻枪绾惧鏌熼柇锕€鏋涙い銉﹀哺閺屾稖绠涘☉娆欑吹缂備浇顕уΛ娆撳Φ閸曨垰鍐€闁靛ě鍛帎闂佹眹鍩勯崹浼存偉婵傜ǹ绠栧ù鐘差儛閺佸秵绻涢幋锝夊摵闁汇倓绶氬娲传閸曨厾鍔圭紓鍌氱С缁舵岸鐛崘顔碱潊闁靛牆鎳嶇槐鍫曟⒑闂堟冻绱¢柛娑卞幖缁楁帞绱撻崒姘偓鎼佸磹妞嬪孩顐介柨鐔哄Т缁愭淇婇妶鍛櫣缂佺姳鍗抽弻鐔兼⒒鐎电ǹ濡介梺绋款儌閺呮繈鍩€椤掑倹鍤€閻庢凹鍘界粩鐔衡偓锝庡枛闁卞洦銇勮箛鎾跺闁绘挻娲橀妵鍕箛閳轰讲鍋撻弴銏犲嚑閹肩补鍩楅悷鎵冲牚闁告洦鍘鹃悡澶娾攽椤旂》榫氭繛鍜冪悼濡叉劙骞掗幊宕囧枔閹风娀鎳犻澶嬫婵犵數濮烽弫鎼佸磻濞戙埄鏁嬫い鎾卞灩缁€鍌涙叏濡炶浜惧Δ鐘靛仜閸燁垶濡堕敐澶婄闁宠桨璁查崑鎾剁磼濡湱绠氬銈嗙墬缁诲倹绂嶇憴鍕╀簻闁哄啠鍋撴繛鑼枎椤繐煤椤忓嫪绱堕梺鍛婃礀閻忔碍鏅ラ梻鍌欑劍閹爼宕濇惔銊ユ瀬濠电姵姘ㄥ畵渚€鏌涢幇闈涙灈缂佺媴缍侀弻锝夊箛椤旇姤姣勫銈嗘⒐濞茬喎顫忛搹鍦煓閻犳亽鍔庨鎴︽⒑缁嬫鍎愰柛鏃€鐟╅悰顔界節閸パ咁槰濡炪倖姊婚弲顐﹀储閸涘﹦绠鹃柟鍓ь棎婢规ɑ绻涚仦鍌氣偓鏇㈠煝瀹ュ拋鍚嬮柛鈩兠鎸庣節閻㈤潧孝閻庢凹鍠氶弫顔尖槈閵忥紕鍘甸悗鐟板婢ф宕甸崶鈹惧亾鐟欏嫭澶勯柛瀣攻娣囧﹪鎮滈懞銉︽珕闂備焦顑欓崹鐗堢閻愵兙浜滈柡鍌濇硶濮g偤鏌¢埀顒佺鐎n偆鍘撻梺瀹犳〃缁€渚€寮抽弬妫靛綊鎮╅棃娑掓瀰闂佸搫鏈惄顖氼嚕椤曗偓閸┾偓妞ゆ帒瀚崹鍌炴煕瑜庨〃鍫濈暤娴g硶鏀介柣妯垮紦鏉╁綊鏌¢崘銊у鐎瑰憡绻冮妵鍕箻閸楃偟浠奸梺杞扮缂嶅﹤顫忕紒妯诲闁告稑锕ラ崕鎾斥攽閻愯尙婀撮柛鏃€鍨甸悾鐑芥偋閸喎鍔呴梺闈涚箞閸╁嫬煤缁嬪簱鏀介幒鎶藉磹閺囥垹绠犻煫鍥ㄧ☉閻撴洟鏌熺€电ǹ啸婵☆偒鍨遍妵鍕箻鐠鸿桨娌梺闈╃秬濞咃綁骞夐幖浣哥濠电姴鍊规径鍕煃闁垮娴柡灞剧洴瀵挳濡搁妷銈囩泿婵$偑鍊曞ù姘跺矗閸愵喖钃熸繛鎴欏灩閻撴盯鏌涚仦鍓х煁闁告帗绋戣灃闁绘﹢娼ф禒婊勩亜閹存繍妯€鐎殿噮鍋婂畷鎺楁倷閺夋垳鎮i梺璇茬箳閸嬬姴螞閸曨厾涓嶉柕澹懐锛濋梺绋挎湰閼归箖鍩€椤掑嫷妫戠紒顔肩墛缁楃喖鍩€椤掑嫨鈧線寮介鐐茶€垮┑鐐叉閼活垱绂嶉崜褏纾兼俊銈勮兌閳藉绻涚仦鍌氣偓妤冨垝婵犳艾钃熼柕澶涘閸欏棗鈹戦悩缁樻锭婵☆偅鐟ラ蹇撯攽閸垺锛忛梺璇″瀻娴i晲鍒掗梻浣告惈閻寰婇崐鐔轰航闂備礁婀辨灙婵炲鏌夐妵鎰樄闁哄矉缍€缁犳盯骞橀崜渚囧敼濠电姰鍨婚幊鎾澄涘☉妯滐綁骞囬弶璺唺闂佸搫鍟崐濠氭晬濠婂啠鏀介柍钘夋閻忥絾銇勯幋鐐寸闁糕斁鍋撳銈嗗笂缁€浣该归鈧弻鈥崇暆閳ь剟宕伴幇鍏洭鎮ч崼鐔峰妳闂佸疇椴哥敮鈺呭礈濮樿泛桅闁告洦鍨遍弲婊堟煠閹帒鍔氶柛鐐差樀濮婃椽宕崟顓犲姽缂傚倸绉崇欢姘嚕椤愶箑绠涢柡澶庢硶閸婄偤姊洪棃娑掑悍闂傚嫬瀚伴幆渚€骞樼紒妯锋嫽婵炶揪绲介幉锟犲箚閸儲鐓熸い鎺嗗亾闁靛牏枪閻i攱瀵奸弶鎴濆敤濡炪倖鎸绘竟鏇㈠磻閹惧瓨濯撮柛鎾冲级閸嶇敻鏌i悩鑽ょ窗婵炲拑缍佸畷婵嬫晝閳ь剟鈥旈崘顔嘉ч柛鈩冾殘閻熴劑姊虹粙鍖″姛缂侇噮鍨崇划娆愬緞婵犲骸鎮戞繝銏f硾椤戝洭宕㈤幖浣瑰€垫鐐茬仢閸旀艾螖閻樿櫕鍊愰柣娑卞櫍瀵粙顢橀悢鍝勫籍闂備礁鎲¢崝锔界濠婂牆鍑犳繛鎴欏灪閻撴盯鎮橀悙鎻掆挃婵炲弶鎸抽弻娑㈠煛娴e壊浼冮悗瑙勬礃閿曘垽骞冨▎鎿冩晢濠㈣泛锕ラ崐鏇㈡⒒閸屾艾鈧绮堟笟鈧獮澶愭晸閻樺啿娈炴俊銈忕到閸犳岸寮崟顐唵闁兼悂娼ф慨鍥煢閸愵亜鏋戠紒缁樼洴楠炲鈻庤箛鏇氭偅闂備胶绮敮妤€顪冩禒瀣摕婵炴垯鍨圭粻娑㈡煕韫囨挻鎲搁柛鎴濈秺濮婃椽妫冮埡鍌楀亾閵夆晛绀傞柣鎰靛墯椤ュ牓鏌熼瑙勬珚婵☆偄鍟埥澶娢旀担绋款€忛梻鍌氬€烽悞锔锯偓绗涘厾楦跨疀濞戞ê鐎悷婊呭鐢亞绱為弽顓犲彄闁搞儯鍔嶇粈鍫㈢棯閹冩倯濞e洤锕、娑樷攽閹邦剚顔勬俊鐐€曠€涒晠骞戦崶褜娼栨繛宸簻瀹告繂鈹戦悩鎻掝仱婵℃彃鐗撳娲箰鎼淬垻锛橀梺绋匡攻缁诲倿顢氶敐澶婄闁芥ê顦甸崬鍫曟⒑闂堟侗妾ч柤闈涚秺楠炲繐煤椤忓應鎷洪梺缁樻尭鐎垫帒岣块悢鍏肩厱濠电姴鍟粈瀣偓娈垮枟閹倸鐣烽幒妤佸€烽悗鐢登归獮鍫ユ⒑閸︻厼甯堕柣掳鍔庨幑銏ゅ礋椤撶姷鐒鹃梻浣哥仢椤戝嫮鎹㈤崱妯镐簻闁规壋鏅涢埀顒佹礋瀵ǹ鈽夐姀锛勫幐闁诲繒鍋熸灙濠⒀嗗皺閳ь剙鐏氬妯尖偓姘煎幘閹广垹鈹戠€n亞顦板銈嗗姦閸嬪懎鈻撴總鍛娾拻闁稿本鐟чˇ锕傛煙绾板崬浜版鐐诧龚缁犳盯寮撮悢宄扮哎闂備礁鎲¢崝锔界閻愮儤鍎楁繛鍡楁禋閻斿棝鎮规ウ瑁も偓鈧柣顏勵儔閺屾稑顫濋澶婂壎闂佸搫鏈惄顖炲春閸曨垰绀傞柣娆屽亾濞存粍绮撻、姘舵晲婢跺﹤鐎銈嗘椤寮埀顒勬⒒娴e摜鏋冩俊顐㈠铻炴俊銈呮噺閸婂爼鏌eΟ鑲╁笡闁绘挾鍠栭悡顐﹀炊閵婏腹鎷荤紓浣哄Х閸嬨倝寮婚悢纰辨晪闁糕剝鐟ч惁鍫澪旈悩闈涗粶婵炲樊鍙冮獮鍐樄鐎规洖銈告慨鈧柣妯垮皺椤旀垿姊婚崒姘偓宄懊归崶顒婄稏濠㈣埖鍔曠壕鍧楁煙閹澘袚闁稿鍊濋弻鏇熺箾瑜嶉幊鎰版倿婵傚憡鐓熼幖鎼灣缁夌敻鏌涢悩鎰佹疁闁诡喒鈧枼妲堟慨姗堢到娴滈箖鏌涜箛鎿冩Ц濞存粓绠栧娲焻閻愯尪瀚板褍顕埀顒冾潐濞叉垿宕¢崘宸殨濞寸姴顑愰弫鍥煟閹邦喗鏆╅柡鍡╁亝缁绘繈鎮介棃娑楃捕濠碘槅鍋呴悷鈺呯嵁閺嶎厼鐓涢柛娑卞幗閻庮剟姊虹化鏇炲⒉妞わ箓缂氶妵鎰板箳閹惧瓨鐝抽梻浣稿閸嬪棝宕抽妷锔绢浄闁冲搫鎳忛埛鎴︽倵閸︻厼顎岄柛銈嗙懅缁辨帞绱掑Ο铏逛桓缂備礁鐭佹ご鍝ユ崲濠靛鐐婇柕濞垮劗閸嬫捇鏌ㄧ€c劋绨婚棅顐㈡处閹告悂顢旈妶澶嬬厱閻庯綆鍋呭畷灞绢殽閻愬樊鍎旈柡浣稿暣閸┾偓妞ゆ帒鍊搁ˉ姘舵煕瑜庨〃鍡涘煕閹寸偑浜滈柟鍝勬娴滃墽绱撴担鍓插剮缂佽埖鑹鹃锝夘敃閿曗偓缁€瀣亜閺嶃劎銆掗柛姗€浜跺娲濞戣鲸肖闂佹悶鍔岄幖顐﹀煝瀹ュ骞㈡俊顖炴櫜缁ㄨ顪冮妶鍡楀Ё缂佹彃澧界划鍫⑩偓锝庡枟閻撴稓鈧厜鍋撻柍褜鍓熷畷浼村冀椤撶偟鐣哄┑鐘诧工閸氭﹢鎮㈤悜妯虹彴闂佸搫琚崕鎶藉焵椤掑啯顏犵紒杈ㄦ崌瀹曟帒顫濋钘変壕闁告縿鍎抽惌鎾绘煛婢跺娈繛宸憾閺佸洭鏌曡箛鏇炐柟鑺ユ礋濮婃椽宕崟顒€绐涢梺鍝ュУ閹稿墽鍒掔紒妯稿亝闁告劏鏅濋崢鍗烆渻閵堝骸骞楅柛銊ф暬瀵ǹ鈽夊Ο閿嬫杸濡炪倖妫佹慨銈囩矆鐎n喗鐓涚€光偓鐎n剛袦闂佽鍠掗弲鐘茬暦閿濆棗绶炲┑鐘插瀹曟椽姊婚崒娆掑厡閺嬵亝銇勯幋婵嗘殻鐎规洘鍔曢埞鎴犫偓锝庡墮缁侊箓姊洪崨濠傚闁告搩鍣e顕€宕煎┑鍫О闂備礁鐤囧銊╂倿閿曞倹鍊垫い鎾卞灪閳锋帒霉閿濆懏鍟為柛鐔哄仦缁绘稓鎷犺閻g數鈧娲樼划宀勫煡婢舵劕鐓戦柛婵嗗閸犳ê鈹戦敍鍕幋闁糕晪绻濆畷鎺戭潩閿濆懍澹曢梺姹囧灩閹诧繝宕戦埄鍐闁糕剝顨堢粻鐗堛亜韫囷絼绨绘い顓℃硶閹瑰嫰宕崟鍏哥磾闂備礁鎼張顒勬儎椤栫偟宓佹俊顖氬悑瀹曞鏌i幋鐐ㄧ細濞存粠浜缁樻媴閼恒儯鈧啴鏌i幒鐐电暤鐎规洘绻傞埢搴ㄥ箻瀹曞洨鏆繝鐢靛仜濡娆㈤悜钘夋嵍妞ゆ挻绋戞禍楣冩煥濠靛棝顎楀ù婊勭箞閺屸剝寰勭€n偄鈧劖鎱ㄦ繝鍛仩闁归濞€楠炴捇骞掗幋鐐垫И缂傚倸鍊峰ù鍥ь嚕閹捐泛鍨濇繛鍡樻尭缁犳牗淇婇娆掝劅婵炲皷鏅犻幃瑙勩偊閹稿寒浠╅梺鍝勭潤閸ャ劉鎷洪梻鍌氱墛缁嬫挾绮婚悙鐑樼厱濠电姴鍟版晶鐢告煕閳哄倻娲存鐐差儔閺佸倻鎲撮敐鍡楊伖濠碉紕鍋戦崐鏍礉閹达箑纾归柡鍥╁枔椤╅攱绻濇繝鍌滃闁绘挾濮电换娑㈡嚑妫版繂娈梺璇查獜缁绘繈寮婚敓鐘插窛妞ゆ挾濮撮悡鐔奉渻閵堝啫鐏柣鈺婂灦楠炲啫鈻庨幋鏂夸壕闁汇垻娅ヨぐ鎺斿祦鐎广儱鎳夐弨浠嬫煟閹邦剛鎽犻悘蹇庡嵆閺屻倛銇愰幒鏃傛毇闂佽鍠楅敋闁宠鍨垮畷鍫曞Ω閵夈儰绱熼梻鍌欒兌鏋柡鍫墯缁旂喖寮撮姀鐘碉紱闂佽宕橀崺鏍窗閸℃稒鐓曢柡鍥ュ妼婢х増銇勯敂鍝勫婵﹥妞介獮鎰償閵忣澁绱梻浣规偠閸斿鍒掑▎鎰箚閻庢稒蓱婵绱掗娑欑闁诲骸顭峰娲偡闁箑娈堕梺绋款儐閻╊垰顕i幖浣哥<闁绘劗琛ラ幏娲⒑閸︻厐鐟懊规搴d笉闁瑰墽绻濈换鍡樸亜閹板墎绉垫繛鍫熺矋閵囧嫰濮€閳╁喚姊块梺闈涙处閸旀瑩鐛幒妤€绠绘い鏍ㄧ☉椤忔椽姊婚崒娆掑厡閺嬵亪鏌¢崼顐㈠⒋闁诡喚鏌夐ˇ褰掓寠濠靛鐓ラ柡鍐ㄥ€瑰▍鏇犵磼閳锯偓閸嬫捇姊绘笟鈧埀顒傚仜閼活垱鏅堕娑氱闁绘挸娴风粻璇测攽閳╁啰鎽冩い锕佷含缁辨帡顢欓懖鈺傛喖缂備胶绮换鍌烆敋閵夆晜鐓ラ悗锝庡亞閸戯繝姊洪柅鐐茶嫰婢ь垱銇勯妸銉︻棦妤犵偛鐗撴俊鎼佸煛閸屾矮缂撶紓鍌欑椤戝牆鈻旈弴銏″仼婵炲樊浜濋埛鎴犵磼鐎n偄顕滄繝鈧悧鍫熷弿婵☆垳枪婵倻鈧鍠楁繛濠囧极閸愵喖鐒垫い鎺戝缁犳帡姊绘担鍛靛湱鎹㈤幇鏉胯Е閻庯綆鍓涚粈濠囨煙鏉堥箖妾柣鎾存礃娣囧﹪濡堕崟顓фМ闂佸磭绮ú鐔煎蓟閿涘嫪娌柣鎰靛墰椤︻喚绱撴担鍝勑i柣鈺婂灡娣囧﹪鎮块锝喰梻浣瑰缁嬫捇宕伴弽褜娼栨繛宸簻瀹告繂鈹戦悙鍨珪缂佸彉鍗冲鐑樻姜閻楀牏銈板銈嗘肠閸ラ绋忛棅顐㈡处閹峰煤椤忓秵鏅滈梺鍛婃处閸嬪棝鎮伴埡浣叉斀闁绘ê鐏氶弳鈺佲攽椤旇姤灏︾€规洘鍔楃槐鎺懳熺喊杈ㄧカ闁荤喐绮嶉弻銊╋綖韫囨稒鎯為柛锔诲幘閻撴捇姊洪崨濠勫ⅳ闁告挻绻堝顐c偅閸愨斁鎷虹紓鍌欑劍閿曗晛鈻撻弴鐘电<妞ゆ棁濮ゅ畷宀€鈧娲樺浠嬪春閳ь剚銇勯幒宥夋濞存粍绮撻弻鐔煎传閸曨厜銉╂煕韫囨挾鐒搁柡灞剧洴閹垽宕妷銉ョ哗闂備礁鎼惉濂稿窗閺嵮呮殾婵炲棙鎸稿洿闂佺硶鍓濋〃蹇斿閿燂拷>>  生物通微信公众号
生物通微信公众号
知名企业招聘
今日动态 | 人才市场 | 新技术专栏 | 中国科学人 | 云展台 | BioHot | 云讲堂直播 | 会展中心 | 特价专栏 | 技术快讯 | 免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号
