
-

生物通官微
陪你抓住生命科技
跳动的脉搏
微生物所揭示固有淋巴细胞在肺-肠轴黏膜系统中的成熟和功能建立机制
【字体: 大 中 小 】 时间:2022年12月13日 来源:中国科学院微生物研究所
编辑推荐:
近日,微生物研究所王硕研究组在国际学术期刊《 Nature Communications 》在线发表题目为 “ Maturation and specialization of group 2 innate lymphoid cells through the lung-gut axis ” 的研究论文,揭示了肺和肠道黏膜组织的固有淋巴细胞类型及其组织特异性,并研究了 II 类固有淋巴细胞( ILC2 )的在肺 - 肠轴黏膜系统中的迁移和成熟过程,阐述了其在稳态及炎性状态下沿肺 - 肠轴成熟和功能建立的机制

膜免疫系统中数量众多的固有淋巴细胞(Innate lymphoid cell, ILC)既是免疫信号活化的起始者,也是联系固有免疫与适应性免疫的重要桥梁。近日,微生物研究所王硕研究组在国际学术期刊《Nature Communications》在线发表题目为“Maturation and specialization of group 2 innate lymphoid cells through the lung-gut axis”的研究论文,揭示了肺和肠道黏膜组织的固有淋巴细胞类型及其组织特异性,并研究了II类固有淋巴细胞(ILC2)的在肺-肠轴黏膜系统中的迁移和成熟过程,阐述了其在稳态及炎性状态下沿肺-肠轴成熟和功能建立的机制。
固有淋巴样细胞(ILC)在黏膜抗感染和维持组织稳态中发挥重要作用。然而,对于黏膜中ILC细胞的异质性以及成熟过程的研究甚少。研究团队通过单细胞测序对小鼠肺脏和小肠组织固有层中的ILC进行分析,鉴定了肺脏和肠道的十一类ILC亚群,并进一步鉴定了肺脏和肠道ILC的组织特异性分子。通过对肺和肠道ILC2表达的分子进行分析后发现,ILC2从肺脏到肠道逐渐成熟,驻留在肺脏中的ILC2高表达CCR2,而驻留在小肠中的ILC2高表达CCR4。研究人员构建了CCR2-mNeonGreen和CCR2-mNeonGreen的报告基因小鼠,通过报告基因小鼠模型揭示了在IL-33的处理下,ILC2存在肺-肠轴迁移过程。另一方面,研究团队通过移植实验和谱系示踪实验揭示了在IL-33诱导以及初生小鼠ILC2的成熟和功能建立过程中也存在肺-肠轴调控。过敏诱导的肺脏ILC2功能异常也会影响小肠ILC2的稳态。综上,本项研究揭示了ILC在肺脏和肠道中的组织特异性,研究了ILC2在成熟和功能建立过程中的肺-肠轴调控机制。
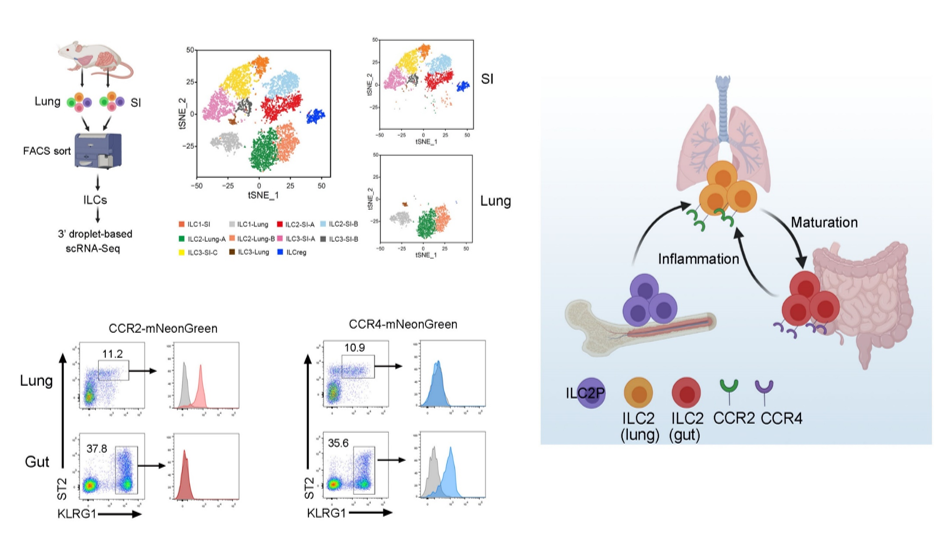
图1. 肺和肠组织固有淋巴细胞鉴定和ILC2的肺-肠轴迁移调控机制
中国科学院微生物研究所王硕研究组助理研究员赵敏、博士生邵菲和博士生於逗为本文共同第一作者,中国科学院微生物研究所王硕研究员及北京大学基础医学院夏朋延研究员为本文的共同通讯作者。本项研究得到了中国科学院战略性先导科技专项(B类)、国家重点研发计划、国家自然科学基金和中国科学院青年创新促进会等基金项目的资助。
 缂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌i幋锝呅撻柛濠傛健閺屻劑寮崒娑欑彧婵炲濮电喊宥囨崲濠靛棌鏋旈柛顭戝枟閻忓秹鏌ら崹锕€娲﹂悡鏇㈡煛閸屾碍鍋ラ柛娆忓閺屾盯鍩為幆褌澹曞┑锛勫亼閸婃牜鏁繝鍕焼濞撴埃鍋撶€规洑鍗冲鎾偐閻㈢绱查梻浣虹帛閿氶柛鐔锋健閹﹢骞橀鐣屽幍濡炪倖鏌ㄩ幖顐﹀礉閿曞倹鐓涘ù锝堫潐瀹曞矂鏌℃担瑙勫磳闁轰焦鎹囬弫鎾绘晸閿燂拷 | 闂傚倸鍊搁崐鎼佸磹瀹勬噴褰掑炊閵娧呭骄闂佸壊鍋掑鈧柣鎺戯攻缁绘盯宕卞Ο鍝勵潔闂佸憡鐟ョ换姗€寮婚悢纰辨晬闁糕剝顨夌€氱増绻涢崼娑樺缂佺粯绻堥幃浠嬫濞磋缍侀弻銈堛亹閹烘梻鏆悗瑙勬穿缁插墽鎹㈠┑瀣倞鐟滃繘顢欓幇顑芥斀闁绘垵娲ㄧ粔鐢告煕閹惧鎳囬柟顔斤耿椤㈡棃宕卞Ο杞扮病婵犵數濞€濞佳囶敄閸℃稑鐓曢柟杈鹃檮閻撴洘绻涢幋鐑囧叕鐎规悶鍎崇槐鎺懳旀担鍝ョ懖婵烇絽娲ら敃顏堛€侀弴銏℃櫜閹兼番鍨婚弶褰掓⒒娴g瓔鍤冮柛鐘崇墵楠炴牠顢曢敂鑲╃◤濠电姴锕ら悧濠囧磻閵堝洨纾奸柍褜鍓熷鎵驳濞差亝鈷掗柛灞捐壘閳ь剛鍏橀幃鐐烘晜闁款垰浜剧紒妤佺☉閹虫劙鎯屽▎鎾寸厵闁绘垶锕╁▓鏇㈡煕閵堝懓瀚伴摶鏍煥濠靛棙鍣归柡瀣ㄥ€濋弻鈩冩媴闂堚晞鍚梺鍝勫閳ь剚鍓氶崥瀣煕閹扳晛濡兼い顒€顑夊鍝勭暦閸モ晛绗″┑鈽嗗亜閸熸潙顕f繝姘ч柛鈩兠鍧楁⒑瑜版帒浜伴柛蹇旓耿瀹曟垿骞樺鍕瀹曘劑顢欓悡搴☆棗闂備胶鎳撻崥瀣偩椤忓牆绀夌€广儱顦伴崑鍌炴煟濡⒈鏆柛瀣尵閹叉挳宕熼鍌ゆК婵犵數鍋涢惇浼村磹閺嶎偆鐭夐柟鐑橆殔閻撴盯鏌涘☉鍗炴灓闁告ɑ鎹囧娲濞戣鲸顎嗘繝纰樷偓铏枠闁诡垰鐭傞獮鎺懳旀担鍝勫箥闂備焦鍎冲ù姘跺磻閸涱垯鐒婂ù鐓庣摠閻撴瑧鈧懓瀚晶妤呭吹閸ヮ剚鐓欐い鏃傛櫕閻﹪鎽堕敐澶嬬厱闊洦鎸搁幃鎴炪亜閺傝法绠绘慨濠傤煼瀹曟帒鈻庨幒鎴濆腐闂備胶枪椤戝啴宕濋幋婵堟殾闁哄洢鍨洪崵鎴炪亜閹哄棗浜鹃梺鎼炲妽缁诲牓骞冨鈧幃娆撴濞戞顥氶梻浣告啞閻熴儳鎹㈠鈧濠氭晲婢跺﹦鐤€濡炪倖姊婚崢褎淇婂ú顏呪拺缂備焦锚缁楁帗銇勯鐘插幋鐎殿喖顭烽弫鎰緞婵犲喚妫熼梻浣稿閻撳牓宕板Δ鍛9妞ゆ牜鍋為埛鎴︽煕濠靛棗顏い銉у仱閺岋綁鍩℃繝鍌滀桓閻庢鍠涢褔顢橀崗鐓庣窞濠电偐鍋撻崝鎴﹀蓟閵娾晛妫橀柛顭戝枓閹稿啫顪冮妶鍡樼叆婵炲眰鍔庡Σ鎰板箻鐎涙ê顎撻梺鑽ゅ枔婢ф寮虫导瀛樷拺闁荤喐婢樺▓鈺呮煙閸戙倖瀚�>>
缂傚倸鍊搁崐鎼佸磹閹间礁纾归柟闂寸绾惧綊鏌i幋锝呅撻柛濠傛健閺屻劑寮崒娑欑彧婵炲濮电喊宥囨崲濠靛棌鏋旈柛顭戝枟閻忓秹鏌ら崹锕€娲﹂悡鏇㈡煛閸屾碍鍋ラ柛娆忓閺屾盯鍩為幆褌澹曞┑锛勫亼閸婃牜鏁繝鍕焼濞撴埃鍋撶€规洑鍗冲鎾偐閻㈢绱查梻浣虹帛閿氶柛鐔锋健閹﹢骞橀鐣屽幍濡炪倖鏌ㄩ幖顐﹀礉閿曞倹鐓涘ù锝堫潐瀹曞矂鏌℃担瑙勫磳闁轰焦鎹囬弫鎾绘晸閿燂拷 | 闂傚倸鍊搁崐鎼佸磹瀹勬噴褰掑炊閵娧呭骄闂佸壊鍋掑鈧柣鎺戯攻缁绘盯宕卞Ο鍝勵潔闂佸憡鐟ョ换姗€寮婚悢纰辨晬闁糕剝顨夌€氱増绻涢崼娑樺缂佺粯绻堥幃浠嬫濞磋缍侀弻銈堛亹閹烘梻鏆悗瑙勬穿缁插墽鎹㈠┑瀣倞鐟滃繘顢欓幇顑芥斀闁绘垵娲ㄧ粔鐢告煕閹惧鎳囬柟顔斤耿椤㈡棃宕卞Ο杞扮病婵犵數濞€濞佳囶敄閸℃稑鐓曢柟杈鹃檮閻撴洘绻涢幋鐑囧叕鐎规悶鍎崇槐鎺懳旀担鍝ョ懖婵烇絽娲ら敃顏堛€侀弴銏℃櫜閹兼番鍨婚弶褰掓⒒娴g瓔鍤冮柛鐘崇墵楠炴牠顢曢敂鑲╃◤濠电姴锕ら悧濠囧磻閵堝洨纾奸柍褜鍓熷鎵驳濞差亝鈷掗柛灞捐壘閳ь剛鍏橀幃鐐烘晜闁款垰浜剧紒妤佺☉閹虫劙鎯屽▎鎾寸厵闁绘垶锕╁▓鏇㈡煕閵堝懓瀚伴摶鏍煥濠靛棙鍣归柡瀣ㄥ€濋弻鈩冩媴闂堚晞鍚梺鍝勫閳ь剚鍓氶崥瀣煕閹扳晛濡兼い顒€顑夊鍝勭暦閸モ晛绗″┑鈽嗗亜閸熸潙顕f繝姘ч柛鈩兠鍧楁⒑瑜版帒浜伴柛蹇旓耿瀹曟垿骞樺鍕瀹曘劑顢欓悡搴☆棗闂備胶鎳撻崥瀣偩椤忓牆绀夌€广儱顦伴崑鍌炴煟濡⒈鏆柛瀣尵閹叉挳宕熼鍌ゆК婵犵數鍋涢惇浼村磹閺嶎偆鐭夐柟鐑橆殔閻撴盯鏌涘☉鍗炴灓闁告ɑ鎹囧娲濞戣鲸顎嗘繝纰樷偓铏枠闁诡垰鐭傞獮鎺懳旀担鍝勫箥闂備焦鍎冲ù姘跺磻閸涱垯鐒婂ù鐓庣摠閻撴瑧鈧懓瀚晶妤呭吹閸ヮ剚鐓欐い鏃傛櫕閻﹪鎽堕敐澶嬬厱闊洦鎸搁幃鎴炪亜閺傝法绠绘慨濠傤煼瀹曟帒鈻庨幒鎴濆腐闂備胶枪椤戝啴宕濋幋婵堟殾闁哄洢鍨洪崵鎴炪亜閹哄棗浜鹃梺鎼炲妽缁诲牓骞冨鈧幃娆撴濞戞顥氶梻浣告啞閻熴儳鎹㈠鈧濠氭晲婢跺﹦鐤€濡炪倖姊婚崢褎淇婂ú顏呪拺缂備焦锚缁楁帗銇勯鐘插幋鐎殿喖顭烽弫鎰緞婵犲喚妫熼梻浣稿閻撳牓宕板Δ鍛9妞ゆ牜鍋為埛鎴︽煕濠靛棗顏い銉у仱閺岋綁鍩℃繝鍌滀桓閻庢鍠涢褔顢橀崗鐓庣窞濠电偐鍋撻崝鎴﹀蓟閵娾晛妫橀柛顭戝枓閹稿啫顪冮妶鍡樼叆婵炲眰鍔庡Σ鎰板箻鐎涙ê顎撻梺鑽ゅ枔婢ф寮虫导瀛樷拺闁荤喐婢樺▓鈺呮煙閸戙倖瀚�>>  闂傚倸鍊搁崐鎼佸磹妞嬪孩顐芥慨姗嗗厳缂傛氨鎲稿鍫罕婵犲痉鏉库偓鏇㈠箠韫囨稑鍚归柟閭﹀幑娴滄粓鏌″搴′簻濞寸姵绮岄々濂稿川鐎涙ǚ鎷洪梺纭呭亹閸嬫盯宕濆Δ鍛厸闁告侗鍠氶幊鍥煙椤旀儳浠︾紒缁樼箞瀹曞爼鍩℃担鍝ュ闂傚倷鐒﹂幃鍫曞磿椤栫偛绀夐幖娣妼杩濋梺鍦劋椤ㄥ棝鎮¢悢鍏肩厵闂侇叏绠戞晶楣冩煕閺冨倸鏋旂紒杈ㄥ笚濞煎繘濡搁妷褜鍎岄梻浣烘嚀閸㈡煡顢栨径鎰鐟滅増甯╅弫鍐煏閸繂鏆欏ù鐘冲浮濮婂宕掑▎鎺戝帯闁哄浜濋妵鍕箣濠靛浂妫ょ紓渚囧枟閻熲晠鐛幒妤€绫嶉柛灞剧矌閸橆垰鈹戦悩顔肩伇婵炲鐩、鏍幢濞戞ḿ锛熼梺缁樻煥閸氬鎮¢崘顔界厪濠㈣泛鐗嗛崝姘辩磼閻欐瑥瀚换鍡樸亜閺嶃劎鍟查棅顒夊墴閺屸€崇暆閳ь剟宕伴弽褏鏆︽俊銈呮噹缁€鍌炴煟閹炬娊顎楅柡鈧鐔剁箚闁绘劦浜滈埀顒佸灴瀹曟洟寮婚妷銉ь唹闂佹悶鍎洪崗娆撳焵椤戣法顦︽い顐g矒閸┾偓妞ゆ帒瀚畵渚€鏌″鍐ㄥ濠殿垱鎸抽弻锝夋偄绾拌鲸娈ラ梺鍛婄箖椤ㄥ﹤顫忕紒妯诲闁惧繐绠嶉埀顒€锕弻娑㈠箻鐎靛摜鐤勯悗瑙勬礃缁诲棛绮诲☉妯锋婵☆垳銆嬬槐閬嶆⒒娴e憡璐¢柛瀣崌瀹曟粌顫濈捄楦啃曢柣搴秵閸犳鎮¢弴銏$厓闁宠桨绀侀弸銈嗙箾閸啋鎴炵┍婵犲浂鏁嶆慨姗嗗墻娴煎啴姊洪崫鍕効缂佹煡绠栭獮鍡涘籍閸惊鈺呮煥閺傚墽鐭欓柡渚囦邯濮婄粯鎷呴崨濠傛殘闂佺厧缍婄粻鏍€侀弽銊ョ窞闁归偊鍠栫粊锕傛⒑绾懏褰ч梻鍕瀵煡骞撻幒婵堝數闁荤姾娅g亸銊╁礉閻旀悶浜滈柡鍌涘閸ゅ洦鎱ㄦ繝鍐┿仢婵☆偄鍟埥澶嬫綇閵娿垺鐏侀梻鍌欑劍閹爼宕濆畝鈧竟鏇㈩敇閻樻彃鐏婇梺鍓插亞閸犲海娆㈤悙鐑樼厵闂侇叏绠戦獮姗€鏌涘Ο鍦煓婵﹪缂氶妵鎰板箳閹存粌鏋堥梻浣告憸婵敻銆冩繝鍌滄殾闁汇垻枪閻掑灚銇勯幒鎴濐仾闁抽攱鍨块弻鐔兼嚃閳轰椒绮堕梺閫炲苯鍘甸柛濠冪箓閻g兘骞庨懞銉︽珳闂佸憡渚楅崹鍗炩枔妤e啯鈷戦悹鎭掑妼閺嬫柨鈹戦纰卞殶缂侇喖鐗撳畷姗€顢欓悾灞藉箥缂傚倸鍊烽悞锕傛晪缂備焦銇涢弲婊堝Φ閸曨垰妫樻繛鍡欏亾閳诲牆鈹戦纭烽練婵炲拑绲块崚鎺戔枎閹寸偛纾梺闈浤涚仦鑺ユ毆缂傚倸鍊搁崐椋庣矆娓氣偓钘濋梺顒€绉寸粈鍌涗繆椤栨繃顏犻柡鍡閹叉悂鎮ч崼婵堢懆缂佺偓鍎抽崥瀣崲濞戙垹绠f繝闈涚墳缁辩偤姊哄ú璇插箺妞ゃ劌锕ら~蹇涙惞閻熸澘顕ч梺鍝勬川閸嬫盯鍩涙径濠庢富闁靛牆鍟俊濂告煙閾忣偄濮囨い鏇樺劜缁绘繈宕惰閺佹粌鈹戞幊閸婃捇鎳楅崼鏇炲偍濞寸姴顑嗛埛鎴︽⒒閸喓銆掔紒鐘靛仱閺屾稒绻濋崘顏勨吂闂佸疇妫勯ˇ鎶剿囪ぐ鎺撶厸鐎光偓鐎n剛袦闂佺硶鏅涚€氭澘鐣峰鈧、鏃堝川椤撶喓褰撮梻鍌氬€峰ù鍥敋閺嶎厼鐤い鎰剁畱閻愬﹦鎲搁弮鍫濊埞闁割偅娲橀埛鎴犵磽娴h偂鎴λ夐崼鐔翠簻闁靛闄勭亸鎵磼閸屾稑娴鐐叉喘閹囧醇閵忕姴绠洪梻浣侯攰閸嬫劗鎮伴妷鈺佺婵犻潧鐗婄€氬鏌ㄩ悢鍝勑i柣鎾存礋閹鏁愭惔鈾€鍋撶捄銊х=婵ǹ浜壕濂稿级閸碍娅呭ù鐘欏洦鐓冪憸婊堝礈閵娧呯闁糕剝绋戦悞鍨亜閹寸偛鍔ら柣蹇婃櫇缁辨挸顓奸崪鍐惈閻庢鍠栭…閿嬩繆濮濆矈妲烽梺绋款儐閹瑰洭寮幇顓熷劅婵☆垵妗ㄦ竟鏇烆渻閵堝棛澧﹂柛濠冪墱閳ь剚鐔幏锟�>>
闂傚倸鍊搁崐鎼佸磹妞嬪孩顐芥慨姗嗗厳缂傛氨鎲稿鍫罕婵犲痉鏉库偓鏇㈠箠韫囨稑鍚归柟閭﹀幑娴滄粓鏌″搴′簻濞寸姵绮岄々濂稿川鐎涙ǚ鎷洪梺纭呭亹閸嬫盯宕濆Δ鍛厸闁告侗鍠氶幊鍥煙椤旀儳浠︾紒缁樼箞瀹曞爼鍩℃担鍝ュ闂傚倷鐒﹂幃鍫曞磿椤栫偛绀夐幖娣妼杩濋梺鍦劋椤ㄥ棝鎮¢悢鍏肩厵闂侇叏绠戞晶楣冩煕閺冨倸鏋旂紒杈ㄥ笚濞煎繘濡搁妷褜鍎岄梻浣烘嚀閸㈡煡顢栨径鎰鐟滅増甯╅弫鍐煏閸繂鏆欏ù鐘冲浮濮婂宕掑▎鎺戝帯闁哄浜濋妵鍕箣濠靛浂妫ょ紓渚囧枟閻熲晠鐛幒妤€绫嶉柛灞剧矌閸橆垰鈹戦悩顔肩伇婵炲鐩、鏍幢濞戞ḿ锛熼梺缁樻煥閸氬鎮¢崘顔界厪濠㈣泛鐗嗛崝姘辩磼閻欐瑥瀚换鍡樸亜閺嶃劎鍟查棅顒夊墴閺屸€崇暆閳ь剟宕伴弽褏鏆︽俊銈呮噹缁€鍌炴煟閹炬娊顎楅柡鈧鐔剁箚闁绘劦浜滈埀顒佸灴瀹曟洟寮婚妷銉ь唹闂佹悶鍎洪崗娆撳焵椤戣法顦︽い顐g矒閸┾偓妞ゆ帒瀚畵渚€鏌″鍐ㄥ濠殿垱鎸抽弻锝夋偄绾拌鲸娈ラ梺鍛婄箖椤ㄥ﹤顫忕紒妯诲闁惧繐绠嶉埀顒€锕弻娑㈠箻鐎靛摜鐤勯悗瑙勬礃缁诲棛绮诲☉妯锋婵☆垳銆嬬槐閬嶆⒒娴e憡璐¢柛瀣崌瀹曟粌顫濈捄楦啃曢柣搴秵閸犳鎮¢弴銏$厓闁宠桨绀侀弸銈嗙箾閸啋鎴炵┍婵犲浂鏁嶆慨姗嗗墻娴煎啴姊洪崫鍕効缂佹煡绠栭獮鍡涘籍閸惊鈺呮煥閺傚墽鐭欓柡渚囦邯濮婄粯鎷呴崨濠傛殘闂佺厧缍婄粻鏍€侀弽銊ョ窞闁归偊鍠栫粊锕傛⒑绾懏褰ч梻鍕瀵煡骞撻幒婵堝數闁荤姾娅g亸銊╁礉閻旀悶浜滈柡鍌涘閸ゅ洦鎱ㄦ繝鍐┿仢婵☆偄鍟埥澶嬫綇閵娿垺鐏侀梻鍌欑劍閹爼宕濆畝鈧竟鏇㈩敇閻樻彃鐏婇梺鍓插亞閸犲海娆㈤悙鐑樼厵闂侇叏绠戦獮姗€鏌涘Ο鍦煓婵﹪缂氶妵鎰板箳閹存粌鏋堥梻浣告憸婵敻銆冩繝鍌滄殾闁汇垻枪閻掑灚銇勯幒鎴濐仾闁抽攱鍨块弻鐔兼嚃閳轰椒绮堕梺閫炲苯鍘甸柛濠冪箓閻g兘骞庨懞銉︽珳闂佸憡渚楅崹鍗炩枔妤e啯鈷戦悹鎭掑妼閺嬫柨鈹戦纰卞殶缂侇喖鐗撳畷姗€顢欓悾灞藉箥缂傚倸鍊烽悞锕傛晪缂備焦銇涢弲婊堝Φ閸曨垰妫樻繛鍡欏亾閳诲牆鈹戦纭烽練婵炲拑绲块崚鎺戔枎閹寸偛纾梺闈浤涚仦鑺ユ毆缂傚倸鍊搁崐椋庣矆娓氣偓钘濋梺顒€绉寸粈鍌涗繆椤栨繃顏犻柡鍡閹叉悂鎮ч崼婵堢懆缂佺偓鍎抽崥瀣崲濞戙垹绠f繝闈涚墳缁辩偤姊哄ú璇插箺妞ゃ劌锕ら~蹇涙惞閻熸澘顕ч梺鍝勬川閸嬫盯鍩涙径濠庢富闁靛牆鍟俊濂告煙閾忣偄濮囨い鏇樺劜缁绘繈宕惰閺佹粌鈹戞幊閸婃捇鎳楅崼鏇炲偍濞寸姴顑嗛埛鎴︽⒒閸喓銆掔紒鐘靛仱閺屾稒绻濋崘顏勨吂闂佸疇妫勯ˇ鎶剿囪ぐ鎺撶厸鐎光偓鐎n剛袦闂佺硶鏅涚€氭澘鐣峰鈧、鏃堝川椤撶喓褰撮梻鍌氬€峰ù鍥敋閺嶎厼鐤い鎰剁畱閻愬﹦鎲搁弮鍫濊埞闁割偅娲橀埛鎴犵磽娴h偂鎴λ夐崼鐔翠簻闁靛闄勭亸鎵磼閸屾稑娴鐐叉喘閹囧醇閵忕姴绠洪梻浣侯攰閸嬫劗鎮伴妷鈺佺婵犻潧鐗婄€氬鏌ㄩ悢鍝勑i柣鎾存礋閹鏁愭惔鈾€鍋撶捄銊х=婵ǹ浜壕濂稿级閸碍娅呭ù鐘欏洦鐓冪憸婊堝礈閵娧呯闁糕剝绋戦悞鍨亜閹寸偛鍔ら柣蹇婃櫇缁辨挸顓奸崪鍐惈閻庢鍠栭…閿嬩繆濮濆矈妲烽梺绋款儐閹瑰洭寮幇顓熷劅婵☆垵妗ㄦ竟鏇烆渻閵堝棛澧﹂柛濠冪墱閳ь剚鐔幏锟�>>  闂傚倸鍊搁崐鎼佸磹瀹勬噴褰掑炊椤掑﹦绋忔繝銏f硾楗潙銆掓繝姘厱鐟滃酣銆冮崨鏉戠<闁靛ǹ鍎欓弮鍫熸櫜闁告侗鍘介悘鏇犵磽閸屾氨校闁绘顨堥幑銏犫攽鐎n偒妫冨┑鐐村灥瀹曨剟宕滈幍顔剧<缂備降鍨归獮鎰版煕鐎n偅宕屾慨濠勭帛閹峰懘宕ㄦ繝鍐ㄥ壍婵犵數鍋涢惇浼村礉瀹ュ绠為柕濞炬櫆閸婂鏌ら幁鎺戝姎闁告挸缍婇弻鐔煎礂閼测晜娈梺鍛婃煥缁夊綊骞冮敓鐘冲亹缁剧増锚娴滈箖鎮峰▎蹇擃仾缂佲偓閳ь剙鈹戦悙鑼勾闁稿﹥鐗滅划瀣箳濡や焦娅嗛梺鍛婃寙閸滃啰搴婃繝鐢靛仩閹活亞寰婃禒瀣婵犲﹤鐗嗙粻娲煟濡偐甯涢柣鎾寸懄閵囧嫰寮介妸褉濮囧銈冨劚閻楁捇寮婚埄鍐╁閻熸瑥瀚壕鎶芥⒑鏉炴壆鍔嶉柟鐟版喘瀵偊骞樼紒妯绘闂佽法鍣﹂幏锟�-婵犵數濮烽弫鍛婃叏閻戣棄鏋侀柟闂寸绾惧潡鏌熺€电ǹ孝缂佽翰鍊濋弻锕€螣娓氼垱楔闂佸搫妫撮梽鍕Φ閸曨垰绠抽柟瀛樼箥娴犲ジ姊哄ú璇插箺妞ゃ劌锕璇测槈閵忕姷鍔撮梺鍛婂姧缁辨洜妲愰弶娆炬富闁靛牆鍊瑰▍鍡涙煟閹垮嫮绡€鐎殿喛顕ч埥澶愬閻橀潧濮堕梻浣告啞閸旀牠宕曢崘娈嬫帡鍩€椤掑嫭鈷掑ù锝呮啞鐠愶繝鏌涙惔娑樷偓婵嬬嵁閹邦喚纾兼俊顖溾拡濞叉悂姊洪棃娑氬婵☆偅绋撶划缁樸偅閸愨晝鍘遍梺鏂ユ櫅閸欐劙骞嬮悩杈╁墾濡炪倕绻愰悧濠囨偂閸愵亝鍠愭繝濠傜墕缁€鍫熺箾閸℃ê鐏╅柣顓熸崌閺岀喓绱掗姀鐘崇彲缂傚倸绉甸悧鐘诲蓟閺囷紕鐤€閻庯綆浜栭崑鎾诲冀椤撶偟鏌ч梺鍝勮閸庢煡鎮¢弴鐔虹闁瑰瓨绻傞懜褰掓煛鐎e墎鐣甸柡灞剧☉椤繈鎮℃惔婵嗘瀳婵犳鍠栭敃銊モ枍閿濆绠栧ù鍏兼綑閻忔娊鏌涜箛鎾村櫣妞ゃ儲宀稿濠氬磼濞嗘劗銈伴悗瑙勬礈閺佽鐣锋导鏉戠疀妞ゆ帒顦遍崬闈涒攽閳藉棗鐏ラ柛瀣姉缁牊绻濋崒妯峰亾閹烘埈娼╅柨婵嗘噸婢规洟姊绘担鍛婃儓闁活剙銈稿畷浼村箻鐠囪尙鍔﹀銈嗗笂閼冲爼鍩婇弴銏$叆婵ǹ鍩栭悡鐔肩叓閸ャ儱鍔ょ紒瀣吹缁辨帞绱掑Ο鑲╃暫缂備胶绮换鍫濈暦濮椻偓婵℃瓕顦辨繛锝庡枟娣囧﹪鎮欓鍕ㄥ亾閺嶎灐娲煛閸愵亞顦繛鎾村焹閸嬫挾鈧娲樺浠嬪春閳ь剚銇勯幒宥夋濞存粍绮撻弻鐔兼倻濡櫣浠撮梺閫炲苯澧柛銏$叀閸┿垺绂掔€e灚鏅滈梺鍓插亞閸犳捇宕㈤幖浣光拺闁硅偐鍋涢崝妤呮煛閸涱喚娲存い銏℃尵娴狅箓宕滆椤旀洟姊洪崗鑲┿偞闁哄懏鐩崺銏ゅ醇閵夛妇鍘靛銈嗘⒒閻℃柨鈻撻弮鍫熺厓闁芥ê顦藉Ο鈧悗瑙勬礃閿氭い鏂跨箻椤㈡瑩鎸婃径瀣悍闂傚倸鍊搁崐鐑芥嚄閸撲礁鍨濇い鏍仦閸嬪鏌i幇顓犮偞闁哄绉归弻銊モ攽閸℃ɑ鎮欓梺鎼炲妽缁诲啴骞堥妸銉庣喖骞愭惔锝冣偓鎰磽娴f彃浜鹃梺鍓插亝缁剁柉銇愰幒鎾存珳闂佸憡渚楅崰娑氭兜閳ь剟姊绘担鍛婃儓婵☆偅绋掔换娑㈠焵椤掍焦鍙忓┑鐘插暞閵囨繈鏌熼鎯у幋妤犵偛绉归、娆愮節濮橆兛绮i梻鍌氬€烽懗鑸电仚濡炪倖鍨靛Λ婵嬬嵁閹达箑鐐婃い鎺嗗亾闁藉啰鍠栭弻銊╂偄閸濆嫅銏ゆ⒑閸楃偞澶勯柕鍥у楠炴帒顓奸崶鑸敌滄俊鐐€曟蹇涘箯閿燂拷>>
闂傚倸鍊搁崐鎼佸磹瀹勬噴褰掑炊椤掑﹦绋忔繝銏f硾楗潙銆掓繝姘厱鐟滃酣銆冮崨鏉戠<闁靛ǹ鍎欓弮鍫熸櫜闁告侗鍘介悘鏇犵磽閸屾氨校闁绘顨堥幑銏犫攽鐎n偒妫冨┑鐐村灥瀹曨剟宕滈幍顔剧<缂備降鍨归獮鎰版煕鐎n偅宕屾慨濠勭帛閹峰懘宕ㄦ繝鍐ㄥ壍婵犵數鍋涢惇浼村礉瀹ュ绠為柕濞炬櫆閸婂鏌ら幁鎺戝姎闁告挸缍婇弻鐔煎礂閼测晜娈梺鍛婃煥缁夊綊骞冮敓鐘冲亹缁剧増锚娴滈箖鎮峰▎蹇擃仾缂佲偓閳ь剙鈹戦悙鑼勾闁稿﹥鐗滅划瀣箳濡や焦娅嗛梺鍛婃寙閸滃啰搴婃繝鐢靛仩閹活亞寰婃禒瀣婵犲﹤鐗嗙粻娲煟濡偐甯涢柣鎾寸懄閵囧嫰寮介妸褉濮囧銈冨劚閻楁捇寮婚埄鍐╁閻熸瑥瀚壕鎶芥⒑鏉炴壆鍔嶉柟鐟版喘瀵偊骞樼紒妯绘闂佽法鍣﹂幏锟�-婵犵數濮烽弫鍛婃叏閻戣棄鏋侀柟闂寸绾惧潡鏌熺€电ǹ孝缂佽翰鍊濋弻锕€螣娓氼垱楔闂佸搫妫撮梽鍕Φ閸曨垰绠抽柟瀛樼箥娴犲ジ姊哄ú璇插箺妞ゃ劌锕璇测槈閵忕姷鍔撮梺鍛婂姧缁辨洜妲愰弶娆炬富闁靛牆鍊瑰▍鍡涙煟閹垮嫮绡€鐎殿喛顕ч埥澶愬閻橀潧濮堕梻浣告啞閸旀牠宕曢崘娈嬫帡鍩€椤掑嫭鈷掑ù锝呮啞鐠愶繝鏌涙惔娑樷偓婵嬬嵁閹邦喚纾兼俊顖溾拡濞叉悂姊洪棃娑氬婵☆偅绋撶划缁樸偅閸愨晝鍘遍梺鏂ユ櫅閸欐劙骞嬮悩杈╁墾濡炪倕绻愰悧濠囨偂閸愵亝鍠愭繝濠傜墕缁€鍫熺箾閸℃ê鐏╅柣顓熸崌閺岀喓绱掗姀鐘崇彲缂傚倸绉甸悧鐘诲蓟閺囷紕鐤€閻庯綆浜栭崑鎾诲冀椤撶偟鏌ч梺鍝勮閸庢煡鎮¢弴鐔虹闁瑰瓨绻傞懜褰掓煛鐎e墎鐣甸柡灞剧☉椤繈鎮℃惔婵嗘瀳婵犳鍠栭敃銊モ枍閿濆绠栧ù鍏兼綑閻忔娊鏌涜箛鎾村櫣妞ゃ儲宀稿濠氬磼濞嗘劗銈伴悗瑙勬礈閺佽鐣锋导鏉戠疀妞ゆ帒顦遍崬闈涒攽閳藉棗鐏ラ柛瀣姉缁牊绻濋崒妯峰亾閹烘埈娼╅柨婵嗘噸婢规洟姊绘担鍛婃儓闁活剙銈稿畷浼村箻鐠囪尙鍔﹀銈嗗笂閼冲爼鍩婇弴銏$叆婵ǹ鍩栭悡鐔肩叓閸ャ儱鍔ょ紒瀣吹缁辨帞绱掑Ο鑲╃暫缂備胶绮换鍫濈暦濮椻偓婵℃瓕顦辨繛锝庡枟娣囧﹪鎮欓鍕ㄥ亾閺嶎灐娲煛閸愵亞顦繛鎾村焹閸嬫挾鈧娲樺浠嬪春閳ь剚銇勯幒宥夋濞存粍绮撻弻鐔兼倻濡櫣浠撮梺閫炲苯澧柛銏$叀閸┿垺绂掔€e灚鏅滈梺鍓插亞閸犳捇宕㈤幖浣光拺闁硅偐鍋涢崝妤呮煛閸涱喚娲存い銏℃尵娴狅箓宕滆椤旀洟姊洪崗鑲┿偞闁哄懏鐩崺銏ゅ醇閵夛妇鍘靛銈嗘⒒閻℃柨鈻撻弮鍫熺厓闁芥ê顦藉Ο鈧悗瑙勬礃閿氭い鏂跨箻椤㈡瑩鎸婃径瀣悍闂傚倸鍊搁崐鐑芥嚄閸撲礁鍨濇い鏍仦閸嬪鏌i幇顓犮偞闁哄绉归弻銊モ攽閸℃ɑ鎮欓梺鎼炲妽缁诲啴骞堥妸銉庣喖骞愭惔锝冣偓鎰磽娴f彃浜鹃梺鍓插亝缁剁柉銇愰幒鎾存珳闂佸憡渚楅崰娑氭兜閳ь剟姊绘担鍛婃儓婵☆偅绋掔换娑㈠焵椤掍焦鍙忓┑鐘插暞閵囨繈鏌熼鎯у幋妤犵偛绉归、娆愮節濮橆兛绮i梻鍌氬€烽懗鑸电仚濡炪倖鍨靛Λ婵嬬嵁閹达箑鐐婃い鎺嗗亾闁藉啰鍠栭弻銊╂偄閸濆嫅銏ゆ⒑閸楃偞澶勯柕鍥у楠炴帒顓奸崶鑸敌滄俊鐐€曟蹇涘箯閿燂拷>>  濠电姷鏁告慨鐑藉极閹间礁纾婚柣鎰惈閸ㄥ倿鏌涢锝嗙缂佺姵婢橀埞鎴︽偐瀹曞浂鏆¢梺绋款儏椤戝棛鎹㈠┑鍥╃瘈闁稿本绮岄。娲⒑濮瑰洤鈧宕戦幘璇参﹂柛鏇ㄥ灠缁犳盯鏌涢锝嗙妞ゅ骸绉电换婵嗏枔閸喚浠╅梺鍛婅壘椤戝棛绮氭潏銊х瘈闁搞儺鐏涜閺屾稓浠﹂崜褏鍙濇繝銏n潐濞茬喎顫忕紒妯诲缂佹稑顑呭▓鎰版⒑閸濄儱校妞ゃ劌鎳庡畵鍕⒑閸濆嫬顏柣蹇撳厫mo Fisher闂傚倸鍊搁崐宄懊归崶褏鏆﹂柛顭戝亝閸欏繒鈧箍鍎遍ˇ顖滅矆鐎n偁浜滈柟鎹愭硾閺嬪酣鏌涢妸銊ゅ惈缂佽鲸鎹囧畷鎺戔枎閹达絿鐛ラ梻渚€娼荤紞鍡涘闯閿濆懐鏆︾憸鐗堝笚閻掕偐鈧鎸堕崕鍗灻洪敂閿亾娴e啫浜归柍褜鍓氱粙鎺楁晪闂侀€炲苯澧伴柛蹇旓耿瀵鎮㈢亸浣圭亖闂佸壊鐓堥崰妤呮倶閹剧粯鈷戠痪顓炴噺閻濐亪鏌涢弮鈧悷鈺侇嚕婵犳碍鏅查柛顐犲灮閺夋悂姊虹憴鍕姢濠⒀冮叄椤㈡瑦寰勬繛鐐杸濡炪倖姊婚妴瀣啅閵夛负浜滄い鎾跺Т閸樻挳鏌℃担鐟板闁诡喗鐟╁畷顐﹀礋椤愩垺鏆忓┑锛勫亼閸婃牠骞愭ィ鍐ㄧ;闁绘梻鈷堥弫濠囨煕濞戞ḿ鎽犻柍閿嬪灴濮婃椽顢曢妶鍛捕闂佸吋妞块崹閬嶅疾閸撲讲鍋撳☉娆欎緵婵炲牅绮欓弻锝夊箛椤栨氨姣㈢紓浣哄С閸楁娊寮诲澶嬪癄濠㈣埖蓱绗戞俊銈嗩殢娴滄瑩宕¢幎钘夋槬闁逞屽墯閵囧嫰骞掗幋婵冨亾閹间礁鍨傛繝闈涙储娴滄粍銇勮箛鎾愁伌闁告碍鐛攍d Application Scientist闂傚倸鍊搁崐鎼佸磹妞嬪孩顐芥慨姗嗗厳缂傛氨鎲稿鍫罕闂備礁鎼崯鐘诲磻閹剧粯鐓欐い鏍ㄧ⊕閻撱儵鏌曢崱妯虹瑲缂佸锕﹂懞杈ㄧ▕閻氱彻ng Develop缂傚倸鍊搁崐鎼佸磹閹间礁纾归柣鎴eГ閸婂潡鏌ㄩ弬鍨挃闁活厽鐟╅弻鐔封枎闄囬褍煤椤撱垹绠圭憸鐗堝俯閺佸啴鏌曢崼婵嗩劉闂佽¥鍊濆铏规嫚閹绘帩鍔夌紓浣割儐鐢喖骞楅锝囩瘈婵炲牆鐏濋悘鐘炽亜閺囥劌寮柛鈹惧亾濡炪倖宸婚崑鎾剁磼閻樿尙效鐎规洘娲樺ḿ蹇涘煛閸屾艾绨ラ梻浣告贡閸庛倕顫忔繝姘剹闁糕剝顨忛悢鍡涙煠閹间焦娑у┑顔肩墦閺屾稓鈧絽澧庣粔顕€鏌$仦鍓ф创濠碉紕鏌夐ˇ鏌ユ煕濡櫣鎽犲ǎ鍥э功缁辨帡濮€閻樺磭褰庨梻浣告惈閺堫剛绮欓幒妤€绠氶柡鍐ㄧ墛閺咁剟鏌涢弴銊ュ季闁哥偞妞藉缁樻媴閸濄儳楔濡炪們鍎查幐鑽ゆ崲濞戙垹鐒垫い鎺戝閻撴盯鎮橀悙棰濆殭濠碘€虫健閺屽秷顧侀柛鎾卞妿缁辩偤宕卞☉妯碱槶濠电偛妫楀ù姘跺吹閺囥垺鐓忓┑鐐靛亾濞呭棝鏌嶉柨瀣仸缂佺粯鐩幊鐘筹紣濠靛棙鏆紓鍌欓檷閸斿海鍒掗鐐参﹂柛鏇ㄥ灠缁狅絾绻濋棃娑欐悙闁哄濞€閹鈻撻崹顔界彯闂佺ǹ顑呴敃顏堟偘椤斿槈鐔兼嚃閳哄喛绱叉繝纰樻閸ㄩ潧顩奸妸褏纾鹃柡鍥ュ灪閳锋帒霉閿濆毥褰掑汲闁秵鐓欑痪鏉垮船娴滅増顨ラ悙璇ф敾鐎垫澘瀚伴獮鍥敆閸岋妇骞㈤梻鍌欑濠€閬嶅磻閹捐绀堟慨姗嗗厳缂傛岸鏌嶉崫鍕偓鑸电濠婂牊鐓欓柡澶婄仢椤f娊鏌熼鐓庢倯缂佺粯绻嗛ˇ鏌ユ倵濮橆厽绶叉い顐㈢箲閵堬妇鎲楅妶鍕潖闂備礁婀遍崕銈夊箰婵犳碍鐓ユい鎾跺Х绾捐棄霉閿濆懎顥忔俊鎻掓啞閵囧嫰寮撮妸銉ョ闂佸憡甯楃敮锟犲春閿熺姴宸濇い鎾卞灩閺佸綊姊绘担鍛婃儓婵炲眰鍔戝畷鎴︽倷閼碱剚娈奸悗骞垮劚椤︿即鍩涢幋鐘电=濞达絽顫栭鍫熷€堕柨鏇楀亾闁伙絾绻堥弫鎰板川椤旈棿娣柣搴ゎ潐濞叉粓宕曢妶鍜佸殫闁告洦鍨扮粻娑欍亜閹捐泛孝妤犵偞顨婂缁樻媴缁嬫寧姣愰梺鍦拡閸嬪﹪寮崘顔嘉ч柛娑变簼閻庡搫鈹戦悙鍙夘棡闁搞劌婀辨竟鏇熺附閸涘﹦鍘甸梺鍦帛鐢晠宕曢幇鐗堝€垫慨妯煎亾鐎氾拷>>
濠电姷鏁告慨鐑藉极閹间礁纾婚柣鎰惈閸ㄥ倿鏌涢锝嗙缂佺姵婢橀埞鎴︽偐瀹曞浂鏆¢梺绋款儏椤戝棛鎹㈠┑鍥╃瘈闁稿本绮岄。娲⒑濮瑰洤鈧宕戦幘璇参﹂柛鏇ㄥ灠缁犳盯鏌涢锝嗙妞ゅ骸绉电换婵嗏枔閸喚浠╅梺鍛婅壘椤戝棛绮氭潏銊х瘈闁搞儺鐏涜閺屾稓浠﹂崜褏鍙濇繝銏n潐濞茬喎顫忕紒妯诲缂佹稑顑呭▓鎰版⒑閸濄儱校妞ゃ劌鎳庡畵鍕⒑閸濆嫬顏柣蹇撳厫mo Fisher闂傚倸鍊搁崐宄懊归崶褏鏆﹂柛顭戝亝閸欏繒鈧箍鍎遍ˇ顖滅矆鐎n偁浜滈柟鎹愭硾閺嬪酣鏌涢妸銊ゅ惈缂佽鲸鎹囧畷鎺戔枎閹达絿鐛ラ梻渚€娼荤紞鍡涘闯閿濆懐鏆︾憸鐗堝笚閻掕偐鈧鎸堕崕鍗灻洪敂閿亾娴e啫浜归柍褜鍓氱粙鎺楁晪闂侀€炲苯澧伴柛蹇旓耿瀵鎮㈢亸浣圭亖闂佸壊鐓堥崰妤呮倶閹剧粯鈷戠痪顓炴噺閻濐亪鏌涢弮鈧悷鈺侇嚕婵犳碍鏅查柛顐犲灮閺夋悂姊虹憴鍕姢濠⒀冮叄椤㈡瑦寰勬繛鐐杸濡炪倖姊婚妴瀣啅閵夛负浜滄い鎾跺Т閸樻挳鏌℃担鐟板闁诡喗鐟╁畷顐﹀礋椤愩垺鏆忓┑锛勫亼閸婃牠骞愭ィ鍐ㄧ;闁绘梻鈷堥弫濠囨煕濞戞ḿ鎽犻柍閿嬪灴濮婃椽顢曢妶鍛捕闂佸吋妞块崹閬嶅疾閸撲讲鍋撳☉娆欎緵婵炲牅绮欓弻锝夊箛椤栨氨姣㈢紓浣哄С閸楁娊寮诲澶嬪癄濠㈣埖蓱绗戞俊銈嗩殢娴滄瑩宕¢幎钘夋槬闁逞屽墯閵囧嫰骞掗幋婵冨亾閹间礁鍨傛繝闈涙储娴滄粍銇勮箛鎾愁伌闁告碍鐛攍d Application Scientist闂傚倸鍊搁崐鎼佸磹妞嬪孩顐芥慨姗嗗厳缂傛氨鎲稿鍫罕闂備礁鎼崯鐘诲磻閹剧粯鐓欐い鏍ㄧ⊕閻撱儵鏌曢崱妯虹瑲缂佸锕﹂懞杈ㄧ▕閻氱彻ng Develop缂傚倸鍊搁崐鎼佸磹閹间礁纾归柣鎴eГ閸婂潡鏌ㄩ弬鍨挃闁活厽鐟╅弻鐔封枎闄囬褍煤椤撱垹绠圭憸鐗堝俯閺佸啴鏌曢崼婵嗩劉闂佽¥鍊濆铏规嫚閹绘帩鍔夌紓浣割儐鐢喖骞楅锝囩瘈婵炲牆鐏濋悘鐘炽亜閺囥劌寮柛鈹惧亾濡炪倖宸婚崑鎾剁磼閻樿尙效鐎规洘娲樺ḿ蹇涘煛閸屾艾绨ラ梻浣告贡閸庛倕顫忔繝姘剹闁糕剝顨忛悢鍡涙煠閹间焦娑у┑顔肩墦閺屾稓鈧絽澧庣粔顕€鏌$仦鍓ф创濠碉紕鏌夐ˇ鏌ユ煕濡櫣鎽犲ǎ鍥э功缁辨帡濮€閻樺磭褰庨梻浣告惈閺堫剛绮欓幒妤€绠氶柡鍐ㄧ墛閺咁剟鏌涢弴銊ュ季闁哥偞妞藉缁樻媴閸濄儳楔濡炪們鍎查幐鑽ゆ崲濞戙垹鐒垫い鎺戝閻撴盯鎮橀悙棰濆殭濠碘€虫健閺屽秷顧侀柛鎾卞妿缁辩偤宕卞☉妯碱槶濠电偛妫楀ù姘跺吹閺囥垺鐓忓┑鐐靛亾濞呭棝鏌嶉柨瀣仸缂佺粯鐩幊鐘筹紣濠靛棙鏆紓鍌欓檷閸斿海鍒掗鐐参﹂柛鏇ㄥ灠缁狅絾绻濋棃娑欐悙闁哄濞€閹鈻撻崹顔界彯闂佺ǹ顑呴敃顏堟偘椤斿槈鐔兼嚃閳哄喛绱叉繝纰樻閸ㄩ潧顩奸妸褏纾鹃柡鍥ュ灪閳锋帒霉閿濆毥褰掑汲闁秵鐓欑痪鏉垮船娴滅増顨ラ悙璇ф敾鐎垫澘瀚伴獮鍥敆閸岋妇骞㈤梻鍌欑濠€閬嶅磻閹捐绀堟慨姗嗗厳缂傛岸鏌嶉崫鍕偓鑸电濠婂牊鐓欓柡澶婄仢椤f娊鏌熼鐓庢倯缂佺粯绻嗛ˇ鏌ユ倵濮橆厽绶叉い顐㈢箲閵堬妇鎲楅妶鍕潖闂備礁婀遍崕銈夊箰婵犳碍鐓ユい鎾跺Х绾捐棄霉閿濆懎顥忔俊鎻掓啞閵囧嫰寮撮妸銉ョ闂佸憡甯楃敮锟犲春閿熺姴宸濇い鎾卞灩閺佸綊姊绘担鍛婃儓婵炲眰鍔戝畷鎴︽倷閼碱剚娈奸悗骞垮劚椤︿即鍩涢幋鐘电=濞达絽顫栭鍫熷€堕柨鏇楀亾闁伙絾绻堥弫鎰板川椤旈棿娣柣搴ゎ潐濞叉粓宕曢妶鍜佸殫闁告洦鍨扮粻娑欍亜閹捐泛孝妤犵偞顨婂缁樻媴缁嬫寧姣愰梺鍦拡閸嬪﹪寮崘顔嘉ч柛娑变簼閻庡搫鈹戦悙鍙夘棡闁搞劌婀辨竟鏇熺附閸涘﹦鍘甸梺鍦帛鐢晠宕曢幇鐗堝€垫慨妯煎亾鐎氾拷>>  闂傚倸鍊搁崐鎼佸磹妞嬪海鐭嗗〒姘e亾妤犵偛顦甸弫鎾绘偐閼碱剦妲遍柣鐔哥矌婢ф鏁幒鏃傜焼闁割偆鍠撶弧鈧梻鍌氱墛娓氭宕曞☉銏$厸濞达絽澹婇崕鏃堟煛鐏炵晫效鐎规洦鍋婂畷鐔碱敃閻旇渹澹曢柣鐔哥懃鐎氼噣銆呴弻銉︾厪闁割偅绻嶅Σ褰掓煟閹惧瓨绀嬮柡灞炬礃瀵板嫮鈧綆浜炴禒鎾煟鎼淬垹鍤柛鎾存皑缁顓兼径瀣姸閻庡箍鍎卞Λ宀勫箯濞差亝鈷戦柛锔诲帎閻熸噴褰掓倻閽樺)銉╂煙閻戞﹩娈曢柣鎾存礋閺岋絽螣閹稿海褰х紓浣插亾闁割偁鍨荤壕鍏笺亜閺冨洤袚闁抽攱甯¢弻宥堫檨闁告挻姘ㄧ划娆撳箳閺囩喐鍣锋繝鐢靛仜閻°劑宕垫惔銊ョ9婵犻潧顑呴拑鐔兼煏婵炵偓娅嗛柛瀣閺屾稓浠﹂崜褉妲堝銈呴獜閹凤拷14濠电姷鏁告慨鐑藉极閸涘﹥鍙忓ù鍏兼綑閸ㄥ倻鎲搁悧鍫濈瑲闁稿﹤鐖奸弻娑㈩敃閻樻彃濮庨梺姹囧€楅崑鎾舵崲濞戙垹绠f繛鍡楃箳娴犻箖姊虹粙娆惧剾濞存粠浜璇测槈閵忕姴宓嗛梺闈浨归崕閬嶅煕閹烘垟鏀介柣鎰皺婢с垽鏌¢崪浣镐喊闁糕斁鍋撳銈嗗坊閸嬫捇鏌涘Ο鑽ょ煉鐎规洘鍨块獮妯肩磼濡厧甯楅柣鐔哥矋缁挸鐣峰⿰鍫熷亜闁绘挸娴烽悾鐑樼箾閺夋垵鎮戞繛鍏肩懃閺侇噣姊绘担鍝ユ瀮婵℃ぜ鍔戦幊妤呭醇閺囩喎浜楅梺纭呮彧闂勫嫰鍩涢幋锔界厵缂佸瀵ч幑锝囩磼閻樿櫕灏扮紒缁樼〒閹风姾顦撮柣锝囨暬閺岀喖顢氶埀顒傜不閺嶎厼钃熼柛鈩冾殢閸氬鏌涢埄鍐噧妤犵偞锕㈠缁樻媴閸涘﹤鏆堥梺鑽ゅ枂閸庝絻妫熼柡澶婄墐閺呮繃绋夊鍡樺弿婵☆垰鐏濋悡鎰版煟閹惧瓨绀嬮柡宀€鍠栭幃娆擃敆娴h櫣鈻忔俊鐐€戦崕閬嶎敄閸モ晜顫曢柟鐑樻尰缂嶅洭鏌曟繛鍨姕閻犲洨鍋ら幃妤冩喆閸曨剛顦ラ悗瑙勬处閸撶喖鏁愰悙娴嬫斀閻庯絽鐏氶弲銏ゆ⒑闁偛鑻晶顖炴煙娓氬灝濮傜€规洘锕㈤、娆戞喆閿濆棗顏归梻鍌欑濠€杈ㄧ仚婵°倗濮甸幃鍌氱暦娴兼潙鍗抽柕蹇ョ磿閸樼敻姊洪崨濠傜仧闁稿﹥鐗滈埀顒佺啲閹凤拷>>
闂傚倸鍊搁崐鎼佸磹妞嬪海鐭嗗〒姘e亾妤犵偛顦甸弫鎾绘偐閼碱剦妲遍柣鐔哥矌婢ф鏁幒鏃傜焼闁割偆鍠撶弧鈧梻鍌氱墛娓氭宕曞☉銏$厸濞达絽澹婇崕鏃堟煛鐏炵晫效鐎规洦鍋婂畷鐔碱敃閻旇渹澹曢柣鐔哥懃鐎氼噣銆呴弻銉︾厪闁割偅绻嶅Σ褰掓煟閹惧瓨绀嬮柡灞炬礃瀵板嫮鈧綆浜炴禒鎾煟鎼淬垹鍤柛鎾存皑缁顓兼径瀣姸閻庡箍鍎卞Λ宀勫箯濞差亝鈷戦柛锔诲帎閻熸噴褰掓倻閽樺)銉╂煙閻戞﹩娈曢柣鎾存礋閺岋絽螣閹稿海褰х紓浣插亾闁割偁鍨荤壕鍏笺亜閺冨洤袚闁抽攱甯¢弻宥堫檨闁告挻姘ㄧ划娆撳箳閺囩喐鍣锋繝鐢靛仜閻°劑宕垫惔銊ョ9婵犻潧顑呴拑鐔兼煏婵炵偓娅嗛柛瀣閺屾稓浠﹂崜褉妲堝銈呴獜閹凤拷14濠电姷鏁告慨鐑藉极閸涘﹥鍙忓ù鍏兼綑閸ㄥ倻鎲搁悧鍫濈瑲闁稿﹤鐖奸弻娑㈩敃閻樻彃濮庨梺姹囧€楅崑鎾舵崲濞戙垹绠f繛鍡楃箳娴犻箖姊虹粙娆惧剾濞存粠浜璇测槈閵忕姴宓嗛梺闈浨归崕閬嶅煕閹烘垟鏀介柣鎰皺婢с垽鏌¢崪浣镐喊闁糕斁鍋撳銈嗗坊閸嬫捇鏌涘Ο鑽ょ煉鐎规洘鍨块獮妯肩磼濡厧甯楅柣鐔哥矋缁挸鐣峰⿰鍫熷亜闁绘挸娴烽悾鐑樼箾閺夋垵鎮戞繛鍏肩懃閺侇噣姊绘担鍝ユ瀮婵℃ぜ鍔戦幊妤呭醇閺囩喎浜楅梺纭呮彧闂勫嫰鍩涢幋锔界厵缂佸瀵ч幑锝囩磼閻樿櫕灏扮紒缁樼〒閹风姾顦撮柣锝囨暬閺岀喖顢氶埀顒傜不閺嶎厼钃熼柛鈩冾殢閸氬鏌涢埄鍐噧妤犵偞锕㈠缁樻媴閸涘﹤鏆堥梺鑽ゅ枂閸庝絻妫熼柡澶婄墐閺呮繃绋夊鍡樺弿婵☆垰鐏濋悡鎰版煟閹惧瓨绀嬮柡宀€鍠栭幃娆擃敆娴h櫣鈻忔俊鐐€戦崕閬嶎敄閸モ晜顫曢柟鐑樻尰缂嶅洭鏌曟繛鍨姕閻犲洨鍋ら幃妤冩喆閸曨剛顦ラ悗瑙勬处閸撶喖鏁愰悙娴嬫斀閻庯絽鐏氶弲銏ゆ⒑闁偛鑻晶顖炴煙娓氬灝濮傜€规洘锕㈤、娆戞喆閿濆棗顏归梻鍌欑濠€杈ㄧ仚婵°倗濮甸幃鍌氱暦娴兼潙鍗抽柕蹇ョ磿閸樼敻姊洪崨濠傜仧闁稿﹥鐗滈埀顒佺啲閹凤拷>>  生物通微信公众号
生物通微信公众号
知名企业招聘
今日动态 | 人才市场 | 新技术专栏 | 中国科学人 | 云展台 | BioHot | 云讲堂直播 | 会展中心 | 特价专栏 | 技术快讯 | 免费试用
版权所有 生物通
Copyright© eBiotrade.com, All Rights Reserved
联系信箱:
粤ICP备09063491号
